Существуют два метода составления окислительно - восстановительных реакций - метод электронного баланса и метод полуреакций. Здесь мы рассмотрим метод электронного баланса.
В этом методе сравнивают степени окисления атомов в исходных веществах и в продуктах реакции, приэтом руководствуемся правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединённых окислителем.
Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции. Рассмотрим этот метод на примере.
| Расставить коэффициенты в реакции, схема которой: HCl + MnO2 |
| Алгоритм расстановки коэффициентов |
| 1.Указываем степени окисления химических элементов.
Подчёркнуты химические элементы, в которых изменились степени окисления. |
| 2.Составляем электронные уравнения, в которых указываем число отданных и принятых электронов.
За вертикальной чертой ставим число электронов, перешедших при окислительном и восстановительном процессах. Находим наименьшее общее кратное ( взято в красный кружок). Делим это число на число перемещённых электронов и получаем коэффициенты (взяты в синий кружок). Значит перед марганцем будет стоять коэффициент-1, который мы не пишем, и перед Cl2 тоже -1. Перед HCl коэффициент 2 не ставим, а считаем число атомов хлора в продуктах реакции. Оно равно - 4.Следовательно и перед HCl ставим - 4,уравниваем число атомов водорода и кислорода справа, поставив перед H2O коэффициент - 2. В результате получится химическое уравнение:
|
| Рассмотрим более сложное уравнение: |
| H2S + KMnO4 + H2SO4 |
| Расставляем степени окисления химических элементов:
|
| Электронные уравнения примут следующий вид
Перед серой со степенями окисления -2 и 0 ставим коэффициент 5, перед соединениями марганца -2, уравниваем число атомов других химических элементов и получаем окончательное уравнение реакции |
|
|
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://www.alhimikov.net
ВЛИЯНИЕ СРЕДЫ НА ХАРАКТЕР РЕАКЦИЙ.
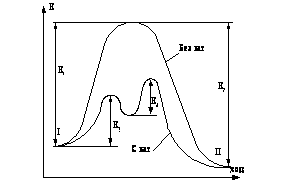
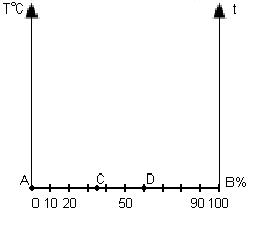
Реакции окисления - восстановления могут протекать в различных средах: в кислой, нейтральной и щелочной. В зависимости от среды может изменяться характер протекания реакции между одними и теми же веществами. Среда влияет на изменение степеней окисления. Рассмотрим пример влияния среды на восстановление перманганат-иона MnO4-:
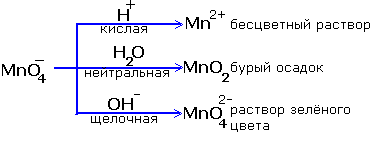
Обычно для создания в растворе кислой среды используют серную кислоту. Для создания щелочной среды применяются растворы гидроксидов калия или натрия.
Рассмотрим примеры протекания реакции между сульфитом натрия Na2SO4 (восстановитель) c перманганатом калия KMnO4(окислитель).
| Реакция в кислой среде |
|
|
| Реакция в нейтральной среде |
|
|
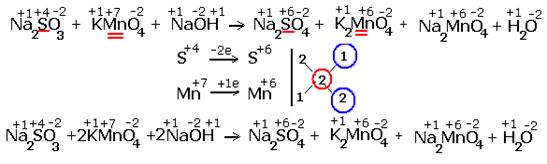
| Реакция в щелочной среде |
|
|
Похожие работы
... Для составления уравнений окислительно-восстановительных реакций обычно используют два метода: 1) метод электронного баланса, 2) электронно-ионный метод. При расчете коэффициентов в окислительно-восстановительных реакциях пользуются правилом электронного баланса: суммарное число электронов, теряемых восстановителем, должно быть равно суммарному числу электронов, приобретаемых окислителем. ...
... , а в нейтральных и щелочных растворах ионы О реагируют с образованием гидроксид-ионов НОН + О = 2ОН . Применяются в основном два метода составления уравнений окислительно-восстановительных реакций: 1) электронного баланса – основан на определении общего количества электронов, перемещающихся от восстановителя к окислителю; 2) ионно-электронный – предусматривает раздельное ...
... HСlO3 Хлораты Хлористая НClO2 Хлориты Хлорноватистая HClO Гипохлориты Хромовая H2CrO4 Хроматы Циановодородная (синильная кислота) слота) HCN Цианиды Основные типы химических реакций Среди разнообразных химических реакций можно выделить два типа, существенно отличающихся друг от друга. К первому типу реакций относятся те, в ходе которых степень окисления ...
... с кислородом, восстановлением - отнятие кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций было распространено на реакции, в которых кислород не участвует. В неорганической химии окислительно-восстановительные реакции (ОВР) формально могут рассматриваться как перемещение электронов от атома одного реагента (восстановителя) к атому другого ( ...
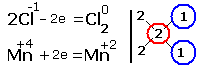
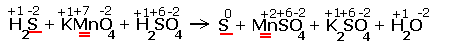
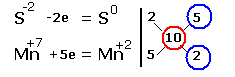
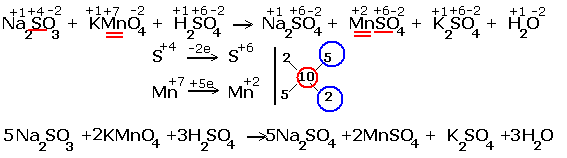
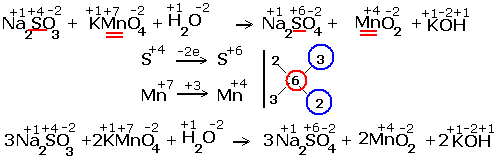
0 комментариев