Навигация
Общая и неорганическая химия
Теория строения атома основана на законах, описывающих движение микрочастиц (электронов, атомов, молекул) и их систем (например, кристаллов). Массы и размеры микрочастиц чрезвычайно малы по сравнению с массами и размерами макроскопических тел. Поэтому свойства и закономерности движения отдельных микрочастиц отличаются от свойств и закономерностей движения макроскопических тел, изучаемых классической физикой. Движение и взаимодействие микрочастиц описывает квантовая механика, которая основывается на представлении о квантовании энергии, волновом характере движения микрочастиц и вероятностном (статистическом) методе описания микрообъектов.
Примерно в начале XX в. исследования явлений (фотоэффект, атомные спектры) привели к выводу, что энергия распространяется и передаётся, поглощается и испускается не непрерывно, а дискретно, отдельными порциями – квантами. Энергия системы микрочастиц также может принимать определённые значения, которые являются кратными частицами квантов.
Предположение
о квантовании
энергии впервые
было высказано
М. Планком в
1900 г. и было обосновано
Эйнштейном
в 1905 г.: энергия
кванта ![]() зависит от
частоты излучения
зависит от
частоты излучения
![]() :
:
![]() ,
,
где (1)
![]() – постоянная
Планка (
– постоянная
Планка (![]() )
)
Частота
колебаний ![]() и длина волны
и длина волны
![]() связаны соотношением:
связаны соотношением:
![]() ,
,
где ![]() – скорость
света.
– скорость
света.
Согласно
соотношению
(1), чем меньше
![]() ,
тем больше
энергия кванта
,
тем больше
энергия кванта
![]() и наоборот.
Таким образом,
ультрафиолетовые
и рентгеновские
лучи обладают
большей энергией,
чем скажем
радиоволны
и инфракрасные
лучи. Для описания
электромагнитного
излучения
привлекают
как волновые,
так и корпускулярные
представления:
с одной стороны
монохроматическое
излучение
распространяется
как волна и
характеризуется
длиной волны
и наоборот.
Таким образом,
ультрафиолетовые
и рентгеновские
лучи обладают
большей энергией,
чем скажем
радиоволны
и инфракрасные
лучи. Для описания
электромагнитного
излучения
привлекают
как волновые,
так и корпускулярные
представления:
с одной стороны
монохроматическое
излучение
распространяется
как волна и
характеризуется
длиной волны
![]() ,
с другой стороны
оно состоит
из микрочастиц
– фотонов,
переносящих
кванты энергии.
,
с другой стороны
оно состоит
из микрочастиц
– фотонов,
переносящих
кванты энергии.
Явление
дифракции
электромагнитного
излучения
доказывает
его волновую
природу. В то
же время электромагнитное
излучение
обладает энергией,
массой, производит
давление. Так,
вычислено, что
за 1 год масса
Солнца уменьшается
за счёт излучения
на ![]() .
.
В 1924 г. Луи де
Бройль предложил
распространить
корпускулярно-волновые
представления
на все микрочастицы,
т.е. движение
любой микрочастицы
рассматривать
как волновой
процесс. Математически
это выражается
соотношением
де Бройля, согласно
которому частице
массой ![]() ,
движущейся
со скоростью
,
движущейся
со скоростью
![]() ,
соответствует
волна длиной
,
соответствует
волна длиной
![]() :
:
![]() ,
(2)
,
(2)
![]() – импульс
частицы.
– импульс
частицы.
Гипотеза де Бройля была экспериментально подтверждена обнаружением дифракционного и интерферентного эффектов потока электронов.
Согласно
соотношению
(2) движению
электрона (![]() ,
,
![]() )
отвечает волна
длиной
)
отвечает волна
длиной ![]() ,
т.е. её длина
соизмерима
с размерами
атомов.
,
т.е. её длина
соизмерима
с размерами
атомов.
В 1925 г. Шрёдингер
предположил,
что состояние
движения электрона
в атоме должно
описываться
уравнением
стоячей электромагнитной
волны. Он получил
уравнение,
которое энергию
электрона
связывает с
пространством
Декартовых
координат и
так называемой
волновой функцией
![]() ,
которая соответствует
амплитуде 3-х
мерного волнового
процесса:
,
которая соответствует
амплитуде 3-х
мерного волнового
процесса:
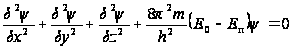 ,
где
,
где
![]() – полная
энергия электрона
– полная
энергия электрона
![]() – потенциальная
энергия электрона
– потенциальная
энергия электрона
![]() – вторая
частная производная
– вторая
частная производная
![]()
Уравнение
Шредингера
позволяет найти
волновую функцию
![]() как функцию
координат.
Физический
смысл волновой
функции в том,
что квадрат
её модуля определяет
вероятность
нахождения
электрона в
элементарном
объёме
как функцию
координат.
Физический
смысл волновой
функции в том,
что квадрат
её модуля определяет
вероятность
нахождения
электрона в
элементарном
объёме ![]() ,
т.е. характеризует
электронную
плотность.Т.
к. электрон
обладает свойствами
волны и частицы,
мы не можем
определить
его положение
в пространстве
в определённый
момент времени.
Электрон размазан,
т.е. делокализирован
в пространстве
атома. В этом
заключается
принцип Гейзенберга.
,
т.е. характеризует
электронную
плотность.Т.
к. электрон
обладает свойствами
волны и частицы,
мы не можем
определить
его положение
в пространстве
в определённый
момент времени.
Электрон размазан,
т.е. делокализирован
в пространстве
атома. В этом
заключается
принцип Гейзенберга.
Микрочастица, так же как и волна не имеет одновременно точных значений координат и импульса. Это проявляется в том, что чем точнее определяется координаты частицы, тем неопределеннее её импульс, и наоборот. Поэтому мы говорим о максимально вероятном нахождении электрона в данном месте в определённый момент времени. Та область пространства, где >90% находится электрон называется атомной орбиталью. Уравнение Шредингера имеет множество решений, но физически осмысленное решение только в определённых условиях.
Для описания
стоячей волны,
образованной
в атоме движущимся
электроном,
т.е. для нахождения
волновой функции
![]() необходимы
квантовые
числа.
необходимы
квантовые
числа.
В 3-х мерном пространстве 4-мя квантовыми числами описывается состояние электрона:
Главное
квантовое число
![]() характеризует
удалённость
электрона от
ядра и определяет
его энергию
(чем больше
характеризует
удалённость
электрона от
ядра и определяет
его энергию
(чем больше ![]() ,
тем больше
энергия электрона
и тем меньше
энергия связи
с ядром).
,
тем больше
энергия электрона
и тем меньше
энергия связи
с ядром). ![]() принимает
целочисленные
значения от
1 до Ґ.
принимает
целочисленные
значения от
1 до Ґ.
Состояние
электрона
характеризующееся
различными
значениями
главного квантового
числа ![]() ,
называется
электронным
слоем (электронной
оболочкой,
энергетическим
уровнем). Они
обозначаются
цифрами 1, 2, 3, 4, 5, …
или соответственно
буквами K,
L, M, N,
O ….
,
называется
электронным
слоем (электронной
оболочкой,
энергетическим
уровнем). Они
обозначаются
цифрами 1, 2, 3, 4, 5, …
или соответственно
буквами K,
L, M, N,
O ….
Квантовое
состояние атома
с наименьшей
энергией –
основное состояние,
а с более высокой
– возбуждённое
состояние.
Переход электрона
с одного уровня
на другой
сопровождается
либо поглощением,
либо выделением
энергии: ![]() .
.
Побочное
квантовое
(орбитальное,
азимутальное)
число ![]() (принимает все
целочисленные
значения от
0 до (n-1)).
(принимает все
целочисленные
значения от
0 до (n-1)).
|
|
| Орбиталь |
| 1 | 0 | 1s |
| 2 | 0,1 | 2s,2p |
| 3 | 0,1,2 | 3s,3p,3d |
Состояние
электрона
характеризующееся
различными
значениями
побочного
квантового
числа ![]() называется
энергетическим
подуровнем.
В пределах
каждого уровня
с увеличением
называется
энергетическим
подуровнем.
В пределах
каждого уровня
с увеличением ![]() ,
растёт энергия
орбитали.
,
растёт энергия
орбитали.
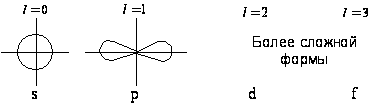
Каждому
значению ![]() соответствует
определённая
форма орбитали
(например, при
соответствует
определённая
форма орбитали
(например, при ![]() – это сфера,
центр которой
совпадает с
ядром).
– это сфера,
центр которой
совпадает с
ядром).
Магнитное
квантовое число ![]() характеризует
ориентацию
орбитали в
пространстве
(принимает все
целочисленные
значения от
-
характеризует
ориентацию
орбитали в
пространстве
(принимает все
целочисленные
значения от
- ![]() до +
до +![]() ).
).
Например,
для ![]()
![]() .
В пределах
каждого подуровня
орбиталь имеет
одинаковую
энергию.
.
В пределах
каждого подуровня
орбиталь имеет
одинаковую
энергию.
Спиновое
квантовое число ![]() характеризует
вращательный
момент, который
приобретает
электрон в
результате
собственного
вращения вокруг
своей оси (принимает
два значения:
характеризует
вращательный
момент, который
приобретает
электрон в
результате
собственного
вращения вокруг
своей оси (принимает
два значения: ![]() – вращение по
часовой стрелке,
– вращение по
часовой стрелке, ![]() – вращение
против часовой
стрелки).
– вращение
против часовой
стрелки).
Атомные орбитали заполняются электронами в соответствии с 3-мя принципами:
Принцип устойчивости (принцип min энергии): Каждая новая орбиталь заполняется только после того, как будут заполнены все предыдущие, т.е. более устойчивые (с min энергией) орбитали.
Энергия атомных орбиталей возрастает следующим образом:
![]()
Правило
Клечковского:
заполнение
электронами
атомных орбиталей
происходит
в соответствии
с увеличением
суммы главного ![]() и побочного
и побочного ![]() квантовых
чисел; если
квантовых
чисел; если ![]() одинакова, то
атомная орбиталь
заполняется
от больших
одинакова, то
атомная орбиталь
заполняется
от больших ![]() и меньших
и меньших ![]() к меньшим
к меньшим ![]() и большим
и большим ![]() .
.
| | | | Орбиталь |
| 1 | 0 | 1 | 1s |
| 2 | 0 | 2 | 2s |
| 1 | 3 | 2p | |
| 3 | 0 | 3 | 3s |
| 1 | 4 | 3p | |
| 2 | 5 | 3d | |
| 4 | 0 | 4 | 4s |
| 1 | 5 | 4p | |
| 2 | 6 | 4d | |
| 3 | 7 | 4f | |
| 5 | 0 | 5 | 5s |
| 1 | 6 | 5p | |
| 2 | 7 | 5d | |
| 3 | 8 | 5f | |
| 4 | 9 | 5g | |
| 6 | 0 | 6 | 6s |
Принцип Паули:
в атоме не может
быть 2 электрона,
у которых 4
одинаковых
квантовых
числа. Следовательно,
на 1-ой орбитали
могут находиться
не более 2-х
электронов,
отличающихся
друг от друга
значением
спинового
квантового
числа. Отсюда
следует, что
максимальное
количество
электронов
на энергетическом
уровне ![]() ,
на энергетическом
подуровне
,
на энергетическом
подуровне ![]() .
.
Пример:
![]()
![]()
![]()
Правило Хунда: электроны располагаются на орбиталях равной энергии таким образом, чтобы их суммарный спин был максимальный. Это означает, что первоначально электроны заполняют все свободные орбитали данного подуровня по 1-му, имея при этом параллельные спины, и только потом происходит заполнение этих орбиталей 2-ми электронами.
Пример:
![]()
![]() Px Py Pz
Px Py Pz
| ↑ | ↑ |
| ↑ | ↑ | ↑ |
| ↑↓ | ↑ | ↑ |
| K | L | M | ||||||||
|
| 1 | 2 | 3 | |||||||
|
| 0 | 0 | 1 | 0 | 1 | 2 | ||||
|
| 0 | 0 | -1 | 0 | +1 | 0 | -1 | 0 | +1 | |
|
| ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | ↓↑ | |
|
|
|
|
|
|
|
|
|
| ||
Количество неспаренных электронов на внешнем уровне определяет валентность элемента, т.е. способность образовывать химические связи с другими атомами. В большинстве случаев, но не всегда.
![]() 5
5 ![]()
![]() 4
4 ![]()
4 ![]() 3
3 ![]()
3 ![]() 2
2 ![]()
2 ![]() 1
1 ![]()
1 ![]()
Периодический закон (1869 г): свойства простых тел, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
До появления сведений о сложном строении атома основной характеристикой элемента служил атомный вес (относительная атомная масса). Развитие теории строения атома привело к установлению того факта, что главной характеристикой атома является положительный заряд ядра.
В современной формулировке периодический закон звучит: свойства химических элементов, а также формулы и свойства образуемых ими соединений находятся в периодической зависимости от величины заряда ядер их атомов.
Физической основой структуры периодической системы элементов служит определённая последовательность формирования электронных конфигураций атомов по мере роста порядкового номера элемента.
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают 4 типа элементов:
![]() – элементы
(последним
заполняется
– элементы
(последним
заполняется ![]() -подуровень
внешнего
энергетического
уровня)
-подуровень
внешнего
энергетического
уровня)
![]() – элементы
(последним
заполняется
– элементы
(последним
заполняется
![]() -подуровень
внешнего
энергетического
уровня)
-подуровень
внешнего
энергетического
уровня)
![]() – элементы
(последним
заполняется
– элементы
(последним
заполняется
![]() -подуровень
предпоследнего
энергетического
уровня)
-подуровень
предпоследнего
энергетического
уровня)
![]() – элементы
(последним
заполняется
– элементы
(последним
заполняется
![]() -подуровень
3-го снаружи
энергетического
уровня).
-подуровень
3-го снаружи
энергетического
уровня).
Горизонтально
располагаются
периоды –
последовательный
ряд элементов,
электронная
конфигурация
внешнего
энергетического
уровня которых
изменяется
от ![]() до
до ![]() .
Номер периода
совпадает со
значением
главного квантового
числа
.
Номер периода
совпадает со
значением
главного квантового
числа ![]() внешнего
энергетического
уровня.
внешнего
энергетического
уровня.
Вертикально
располагаются
группы – элементы
имеющие сходное
электронное
строение. У
элементов
главной подгруппы
последним
заполняется ![]() и
и ![]() подуровни
внешнего
энергетического
уровня, у элементов
побочной подгруппы
происходит
заполнение
внутренних
подуровни
внешнего
энергетического
уровня, у элементов
побочной подгруппы
происходит
заполнение
внутренних
![]() и
и ![]() подуровней.
Одинаковый
номер группы,
как правило,
определяет
число электронов,
которое может
участвовать
в образовании
химических
связей.
подуровней.
Одинаковый
номер группы,
как правило,
определяет
число электронов,
которое может
участвовать
в образовании
химических
связей.
Строение многоэлектронных атомов. Принцип наименьшей энергии, принцип Паули, правило Гунда, правило Клечковского. Электронные формулы
Число электронов, которые могут находиться на одном энергетическом уровне, определяется формулой 2n2, где n – номер уровня. Максимальное заполнение первых четырех энергетических уровней: для первого уровня – 2 электрона, для второго – 8, для третьего – 18, для четвертого – 32 электрона. Максимально возможное заполнение электронами более высоких энергетических уровней, в атомах известных элементов не достигнуто.
Квантово-механические расчеты показывают, что в многоэлектронных энергия электронов одного уровня неодинакова; электроны заполняют атомные орбитали разных видов и имеют разную энергию. Каждый энергетический уровень, кроме первого, расщепляется на такое число энергетических подуровней, сколько видов орбиталей включает этот уровень. Второй энергетический уровень расщепляется на два подуровня (2s – и 2p-подуровни), третий энергетический уровень – на три подуровня (3s-, 3p- и 3d-подуровни).
Каждый s-подуровень содержит одну s орбиталь, каждый р-подуровень – три р-орбитали, каждый d-подуровень семь f-орбиталей.
Закономерность заполнения электронных оболочек атомов определяется принципом запрета, установленным в 1925 г швейцарским физиком Паули (принцип Паули):
В атоме не могут одновременно находиться два электрона с одинаковым набором четырех квантовых квантовых чисел (заполнение электронами орбиталей происходит следующим образом: сначала на каждой орбитали располагается по одному электрону, затем, после заполнения всех орбиталей происходит распределение вторых электронов с противоположным спином).
Используя понятия квантовые числа можно сказать, что:
Каждый электрон в атоме однозначно характеризуется своим набором четырех квантовых чисел - главного n, орбитальногоl, магнитного ml, и спинового ms.
Заселение электронами энергетических уровней, подуровней и атомных орбиталей подчиняется следующему правилу:
В невозбужденном атоме все электроны обладают наименьшей энергией (принцип наименьшей энергии).
Это означает, что каждый из электронов, заполняющих оболочку атома, занимает такую орбиталь, чтобы атом в целом имел минимальную энергию. Последовательно квантовое возрастание энергии подуровней происходит в следующем порядке: 1s - 2s -2р - 3s – 3р - 4s –3d - 4р - 5s -….
Такой порядок увеличения энергии подуровней определяет расположение эле Ментов в Периодической системе.
Заполнение атомных орбиталей внутри одного энергетического подуровня происходит в соответствии с правилом, сформулированным немецким физиком Ф. Хундом (1927г) (правило Хунда):
При данном значении квантового числа l (т.е. в пределах одного подуровня) в основном состоянии электроны располагаются таким образом, что значение суммарного спина атома максимально. Это означает, что на подуровне должно быть максимально возможное число неспаренных электронов.
Порядок возрастания энергии атомной орбитали в сложных атомах описывается правилом Клечковского: энергия атомной орбитали возрастает в соответствии с увеличением n +l главного и орбитального квантовых чисел. При одинаковом значении суммы энергия меньше у атомной орбитали с меньшим значением главного квантового числа.
Распределение электронов по различным атомным орбиталям называют электронной конфигурацией атома. Электронная конфигурация с наименьшей энергией соответствует основному состоянию атома, остальные конфигурации относятся к возбужденным состояниям.
Электронную конфигурацию атома изображают двумя способами – в виде электронных формул и электронно-графических диаграмм. При написании электронных формул используют главное и орбитальное квантовые числа. Подуровень обозначают с помощью главного квантового числа (цифрой) и орбитального квантового числа (соответствующей буквой). Число электронов на подуровне характеризует верхний индекс. Например. Для основного состоянии атома водорода электронная формула: 1s1.
Более полно строение электронных подуровней можно описать с помощью электронографических диаграмм, где распределение электронов по подуровням представляют в виде квантовых ячеек. Орбиталь в этом случае принято условно изображать квадратом, около которого проставлено обозначение подуровня. Подуровни на каждом уровне должны быть немного смещены по высоте, так как их энергия несколько различается. Электроны обозначают стрелками или Ї в зависимости от знака спинового квантового числа.
С учетом структуры электронных конфигураций атомов все известные элементы в соответствии со значением орбитального квантового числа последнего заполняемого подуровня можно разбить на четыре группы: s –элементы, р-элементы, d-элементы, f-элементы.
Основные типы химической связи. Характеристики химической связи. Энергия связи. Длина связи
При образовании химической связи происходит перераспределение в пространстве электронных плотностей, первоначально принадлежавших разным атомам. Поскольку наименее прочно связаны с ядром электроны внешнего уровня, то этим электронам принадлежит главная роль в образовании химической связи. Количество химических связей, образованных данным атомом в соединении, называют валентностью. Электроны, принимающие участие в образовании химической связи, называются валентными: у s- и р элементов — это внешние электроны, у d- элементов — внешние (последние) s-электроны и предпоследние d-электроны. С энергетической точки зрения наиболее устойчивым является атом, на внешнем уровне которого содержится максимальное число электронов (2 и 8 электронов). Такой уровень называют завершенным. Завершенные уровни отличаются большой прочностью и характерны для атомов благородных газов, поэтому при обычных условиях они находятся в состоянии химически инертного одноатомного газа.
У атомов других элементов внешние энергетические уровни незавершенные. В процессе хим реакции осуществляется завершение внешних уровней, что достигается либо присоединением, либо отдачей электронов, а также образованием общих электронных пар. Эти способы приводят к образованию двух основных типов связи: ковалентной и ионной. Таким образом, при образовании молекулы каждый атом стремится приобрести устойчивую внешнюю электронную оболочку: либо двухэлектронную (дублет), либо восьми-злектромную (октет). Эта закономерность положена в основу теории образования химической связи. Образование химической связи за счет завершения внешних уровней в образующих связь атомах сопровождается выделением большого количества энергии, то есть возникновение химической связи всегда протекает экзотермически, поскольку оно приводит к появлению новых частиц (молекул), обладающих при обычных условиях большей устойчивостью, а следовательно, они меньшей энергией, чем у исходных. Одним из существенных показателей, определяющих какая связь образуется между атомами, является электроотрицательность, то есть способность атомом притягивать к себе электроны от других атомов. Электроотрицательность атомов элементов изменяется постепенно: в периодах периодической системы слева направо ее значение возрастает а в группах сверху вниз — уменьшается.
Химическая связь, осуществляемая за счет образования общих (связывающих) электронных пар, называется ковалентной.1) Разберем пример образования химической связи между атомами с одинаковой электроотрицательностью, например, молекулы водорода Н2 Образование химической связи в молекуле водорода можно представить в виде двух точек: Н- + -Н -> Н : Н или черточкой, которая символизирует пару электронов: H-H Ковалентная связь, образованная атомами с одинаковой электроотрицательностью называется неполярной. Такую связь образуют двухатомные молекулы, состоящие из атомов одного химического элемента: H 2, Cl 2 и др.2) Образование ковалентной связи между атомами, электроотрицательность которых различается незначительно. Ковалентная связь, образованная атомами с различной электроотрицательностью, называется полярной. При ковалентной полярной связи электронная плотность от общей пары электронов смещена к атому с большей электроотрицательностью. Примерами могут служить молекулы Н2О, NH3, H2S, CH3Cl. Ковалентная (полярная и неполярная) связь в наших примерах образовалась за счет неспаренных электронов связывающихся атомов. Такой механизм образования ковалентной связи называется обменным. Другой механизм образования ковалентной связи — донорно-акцепторный. В этом случае связь возникает за счет двух спаренных электронов одного атома (донора) и свободной орбитали другого атома (акцептор). Хорошо известный пример — образование иона аммония: Н++:NH 3 -> [ Н : NH3 | + <=====> NH4+ акцептор донор ион аммония электронов. При образовании иона аммония электронная пара азота становится общей для атомов N и Н, то есть возникает четвертая связь, которая не отличается от остальных трех. Их изображают одинаково:
Н+
H-N-H
Н
Ионная связь возникает между атомами, электроотрицательность которых резко различается Рассмотрим способ образования на примере хлорида натрия NaCl. Электронную конфигурацию атомов натрия и хлора можно представить: 11 Na ls2 2s2 2p 6 3s1; 17 Cl ls2 2p 6 Зs2 3р5 Как это атомы с незавершенными энергетическими уровнями. Очевидно, для их завершения атому натрия легче отдать один электрон, чем присоединить семь, а атому хлора легче присоединить один электрон, чем отдать семь. При химическом взаимодействии атом натрия полностью отдает один электрон, а атом хлора принимает его. Схематично это можно записать так: Na. — l е —> Na+ ион натрия, устойчивая восьмиэлектронная 1s2 2s2 2p6 оболочка за счет второго энергетического уровня. :Cl + 1е -->.Cl - ион хлора, устойчивая восьмиэлектронная оболочка. Между ионами Na+ и Cl- возникают силы электростатического притяжения, в результате чего образуется соединение.
Химическая связь, осуществляемая за счет электростатического притяжения между ионами, называется ионной связью. Соединения, образованные путем притяжения ионов называются ионными. Ионные соединения состоят из отдельных молекул только в парообразном состоянии. В твердом (кристаллическом) состоянии ионные соединения состоят из закономерно расположенных положительных и отрицательных ионов. Молекулы в этом случае отсутствуют. Ионные соединения образуют резко различные по величине электроотрицательности элементы главных подгрупп I и II групп и главных подгрупп VI и VII групп. Ионных соединений сравнительно немного. Например неорганические соли: NH4Cl (ион аммония NH4 + и ион хлора Cl-), а также солеобразные органические соединения: алкоголяты соли карбоновых кислот, соли аминов Неполярная ковалентная связь и ионная связь — два предельных случая распределения электронной плотности. Неполярной связи отвечает равномерное распределение связующего двух электронного облака между одинаковыми атомами. Наоборот, при ионной связи связующие электронное облако практически полностью принадлежит одному из атомов. В большинстве же соединений химические связи оказывают промежуточными между этими видами связи, то есть в них осуществляется полярная ковалентная связь.
Металлическая связь существует в металлах в твердом в жидком состоянии. В соответствии с положением в периодической системе атомы металлов имеют небольшое число валентных электронов (1-3 электрона) и низкую энергию ионизации (отрыва электрона). Поэтому валентные электроны слабо удерживаются в атоме, легко отрываются и имеют возможность перемещаться по всему кристаллу. В узлах кристаллической решетки металлов находятся свободные атомы, положительно заряженные коны, а часть валентных электронов, свободно перемещаясь в объеме кристаллической решетки, образует «электронный газ», обеспечивающий связь между атомами металла. Связь, которую осуществляют относительно свободные электроны между ионами металлов в кристаллической решетке, называется металлической связью. Металлическая связь возникает за счет обобществления атомами валентных электронов. Однако между этими видами связи есть существенное различие. Электроны, осуществляющие ковалентную связь, в основном пребывают в непосредственной близости от двух соединенных атомов. В случае металлической связи электроны, осуществляющие связь, перемещаются по всему куску металла. Этим определяются общие признаки металлов: металлический блеск, хорошая проводимость теплоты и электричества, ковкость, пластичность и т. д. Общим химическим свойством металлов является их относительно высокая восстановительная способность.
Водородные связи могут образовываться между атомом водорода, связанным с атомом электроотрицательного элемента, и электроотрицательным элементом, имеющим свободную пару электронов(О,F,N). Водородная связь обусловлена электростатическим притяжением, которому способствуют малые размеры атома водорода, и отчасти, донорно-акцепторным взаимодействием. Водородная связь может быть межмолекулярной и внутримолекулярной. Связи 0-Н имеют выраженный полярный характер: Водородная связь гораздо более слабая, чем ионная или ковалентная, но более сильная, чем межмолекулярное взаимодействие. Водородные связи обуславливают некоторые физические свойства веществ (например, высокие температуры кипения). Особенно распространены водородные связи в молекулах белков, нуклеиновых кислот и других биологически важных соединений, обеспечивая им определенную пространственную структуру (организацию).
Энергия связи(Eсв). Кол-во энергии, выделяющейся при образовании химической связи, называется энергией химической связи[кДж/моль]. Для многоатомных соединений принимают среднее её значение. Чем больше Eсв тем устойчивее молекула.
Длина связи(lсв). Расстояние между ядрами в соединении. Чем больше длина связи — тем меньше энергия связи.
Метод валентных связей.
А) химическая связь между двумя атомами возникает как результат перекрытия АО с образованием электронных пар.
Б) атомы вступающие в химическую связь, обмениваются между собой электронами, которые образуют связывающие пары. Энергия обмена электронами между атомами(энергия притяжения атомов) вносит основной вклад в энергию химической связи. Дополнительный вклад в энергию связи дают кулоновские силы взаимодействия частиц.
В) в соответствии с принципом Паули химическая связь образуется лишь при взаимодействии электронов с разными спинами.
Г)характеристики химической связи(энергия, длина, полярность) определяются типом перекрывающихся АО.
Метод валентных связей. Ковалентная связь направлена в сторону максимального перекрывания АО реагирующих атомов.
Валентность. Способность атома присоединять или замещать определённое число других атомов с образованием химических связей.
При переходе в возбуждённое состояние, один из спаренных электронов переходит в свободную орбиталь той же оболочки.
Донорно-акцепторный механизм: образуется общая электронная пара за счёт неподелённой пары электронов одного атома и вакантной орбитали другого атома.
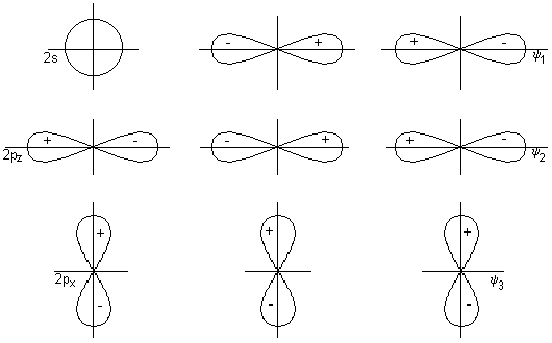
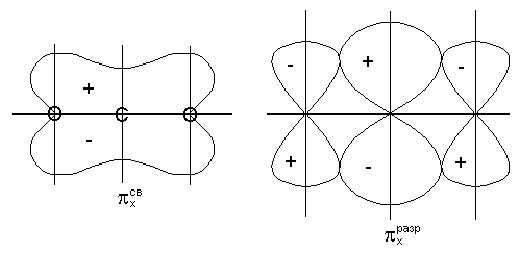
Метод молекулярных орбиталей. Электроны в молекуле распределены по МО, которые подобно АО характеризуются определённой энергией и формой. МО охватывают всю молекулу. Молекула рассматривается как единая система.
1. Число МО равно общему числу АО, из которых комбинируется МО.
2. Энергия одних МО оказывается выше, других — ниже энергии исходных АО. Средняя энергия МО, полученная из набора АО, приблизительно совпадает с средней энергией этих АО.
3. Электроны заполняют МО, как и АО, в порядке возрастания энергии, при это соблюдается принцип запрета Паули и правило Гунда.
4. Наиболее эффективно комбинируются АО с теми АО которые характеризуются сопоставимыми энергиями и соответствующей симметрией.
5. Как и в методе ВС, прочность связи в методе МО пропорциональна степени перекрывания атомных орбиталей.
Порядок и энергия связи. Порядок связи n=(Nсв-Nр)/2. Nсв — число e на связывающих молекулярных орбиталях, Nр — число e на разрыхляющих молекулярных орбиталях.
Если Nсв = Nр, то n=0 и молекула не образуется. С увеличением n в однотипных молекулах растёт энергия связи. В отличии от метода АО, в методе МО допускается, что связь может быть образована одним электроном.
Комплексные соеденения. Сложные соединения у которых имеются ковалентные связи, образованные по донорно акцепторному механизму
Похожие работы
... подкрепляет своим одобрением неправильный или не вполне точный ответ ученика. 1.2 Совершенствование школьного химического эксперимента при проблемном обучении 1.2.1 Принципы разработки методической системы и содержания опытов по химии в системе проблемного обучения Характерной особенностью развивающего обучения является широкое использование проблемного подхода, который включает создание ...
ависимо от способа получения и места нахождения. 2. Строение внешнего электронного уровня атома калия и кальция. 1 правило Клечковского. Строение внешнего электронного уровня атома скандия. 2правило Клечковского У атома аргона остаются незанятыми все орбитали 3d-подуровня. Однако у следующих за аргоном элементов – калия и кальция – заполнение 3-го электронного слоя временно прекращается, и ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... учреждение страны, а в ее задачи входило усовершенствование наук, просвещение, а также усовершенствование мануфактур, ремесел и фабрик. В то же время в начале XIX столетия, особенно после Отечественной войны 1812 г., в развитии химии в России появились новые черты. Смена мануфактурного производства фабрично-заводским выдвинула перед учеными множество практических задач, связанных с рациональной ...
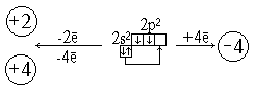
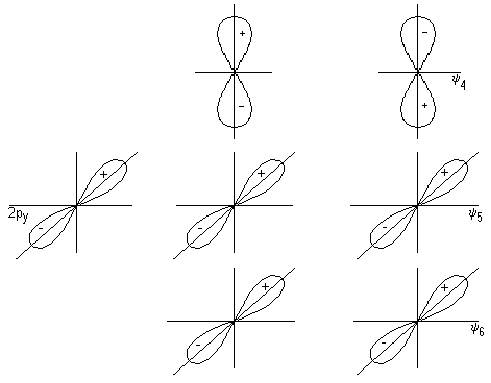
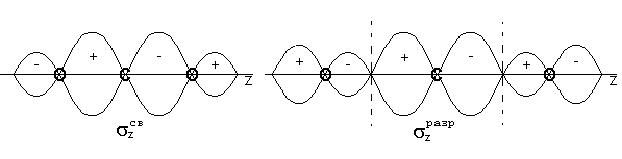
0 комментариев