Навигация
Адсорбция и адсорбционные равновесия
Понятие адсорбции. Автоадсорбция. Адсорбент и адсорбат. Абсолютная и Гиббсовская адсорбция. Единицы измерения адсорбции. Зависимость величины адсорбции от концентрации, давления и температуры. Изотерма, изобара, изопикна, изостера адсорбции
Адсорбция - процесс самопроизвольного перераспределения компонентов системы между поверхностным слоем и объемом фазы.
Адсорбция может наблюдаться в многокомпонентных системах и при перераспределении в поверхностный слой уходит тот компонент, который сильнее понижает поверхностное натяжение. В однокомпонентной системе при формировании поверхностного слоя происходит изменение его структуры - уплотнение, которое называется автоадсорбцией.
В общем случае адсорбция может происходить не только благодаря стремлению поверхностной энергии к уменьшению, но и за счет химической реакции компонентов с поверхностью вещества. В этом случае поверхностная энергия может даже увеличиваться на фоне снижения энергии всей системы.
Вещество, на поверхности которого происходит адсорбция, называется адсорбентом, а вещество, которое перераспределяется – адсорбатом.
Обратный процесс перехода вещества с поверхности в объем фазы - десорбция.
В зависимости от агрегатного состояния фаз различают адсорбцию газа на твердых адсорбентах, твердое тело – жидкость, жидкость - жидкость, жидкость - газ. Для количественного описания адсорбции применяют две величины: первая измеряется числом молей или граммами, приходящимися на единицу поверхности или массы адсорбента:
А = m1/m2- абсолютная адсорбция, А = ni/S.
Величина, определяемая избытком вещества в поверхностном слое, также отнесенным к единице площади поверхности или массы адсорбента, называется Гиббсовской или относительной адсорбцией (Г).
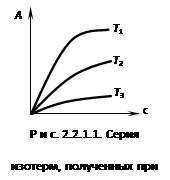
Адсорбция зависит от концентрации компонентов и температуры.
А = f(c,T)- жидкость;
А = f(P,T)- газ
Различают следующие виды зависимостей:
| 1. Изотерма (рис. 8) | 2. Изобара | 3. Изостера |
| А=fT(c) | А=fP(T) | c=fA(T) |
| A=fT(P) | A=fC(T) | P=fA(T) |
Считаем Vповерхности раздела = 0.
dU = TdS +s dS + ![]()
Проинтегрировав, получим: U = TS + sS + ![]()
Полный дифференциал от этого уравнения:
dU = TdS + SdT + sdS + ![]() + Sds +
+ Sds + ![]() .
.
Подставляя значение dU из (6) в (7) и сократив одинаковые члены правой и левой части, получим:
SdT + Sds + ![]() = 0.
= 0.
Предположим, что T = const: ![]()
Разделив правую и левую часть на поверхность S, получим фундаментальное адсорбционное уравнение Гиббса:
![]() ;
; ![]() ;
;
![]() .
.
Определение зависимости поверхностного натяжения от адсорбции одного компонента, при постоянстве химических потенциалов других компонентов.
![]() .
.
Известно, что ![]() ,
, ![]() , (где
, (где ![]() ,
, ![]() - равновесный и стандартный химический потенциал компонента i; ln ai- логарифм активности i –го компонента). Тогда уравнение Гиббса будет выглядеть так
- равновесный и стандартный химический потенциал компонента i; ln ai- логарифм активности i –го компонента). Тогда уравнение Гиббса будет выглядеть так
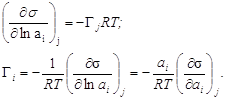
Активность связана с концентрацией: с = ×а. Предположим, что = 1 (при с ® 0). Тогда
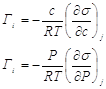 - для жидкости и газа
- для жидкости и газа
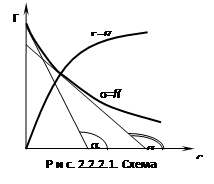
Обычно уравнение Гиббса применяют для растворов. Растворителем может быть не только индивидуальное вещество, но и смесь. В разбавленных растворах гиббсовская адсорбция очень мала, а его химический потенциал меняется очень мало с изменением концентрации растворенного вещества, т.е. dm= 0. Поэтому для разбавленного раствора фундаментальное уравнение Гиббса выглядит так:
![]()
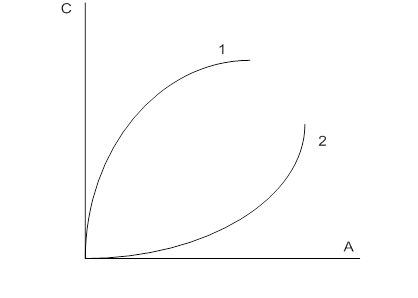
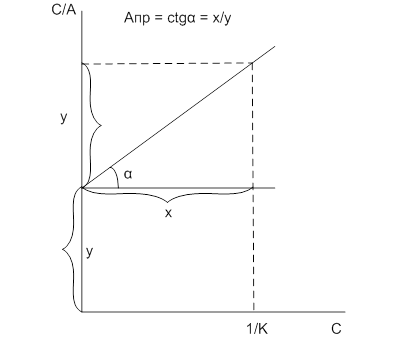
Из этих уравнений следует, что зная зависимость ![]() = f(С) (где С - концентрация растворенного вещества), можно рассчитать изотерму адсорбции, пользуясь адсорбционным уравнением Гиббса. Схема графического расчета показана на рис. 2.2.2.1: Тангенс угла наклона соответствует значениям производных
= f(С) (где С - концентрация растворенного вещества), можно рассчитать изотерму адсорбции, пользуясь адсорбционным уравнением Гиббса. Схема графического расчета показана на рис. 2.2.2.1: Тангенс угла наклона соответствует значениям производных ![]() в этих точках.
в этих точках.
Зная эти производные уравнения Гиббса, можно рассчитать значение Г, что позволяет построить зависимость Г = f(С). Уравнение Гиббса показывает, что единица измерения гиббсовской адсорбции не зависит от единицы измерений концентрации, а зависит от размерности величины R. Так как величина R отнесена к молю вещества, а s - к единице площади, то Г = [моль/ единица площади]. Если s выразить в [Дж/м2], то R нужно подставлять: R = 8,314 Дж/моль×К.
Поверхностная активность. Поверхностно-активные и поверхностно-инактивные вещества. Анализ уравнения Гиббса. ПАВ. Эффект Ребиндера. Правило Дюкло-ТраубеВ уравнении Гиббса влияние природы вещества на адсорбцию отражается производной![]() . Эта производная определяет и знак гиббсовской адсорбции, и может служить характеристикой вещества при адсорбции. Чтобы исключить влияние концентрации на производную берут ее предельные значения, т.е. при стремлении концентрации к нулю. Эту величину Ребиндер назвал поверхностной активностью.
. Эта производная определяет и знак гиббсовской адсорбции, и может служить характеристикой вещества при адсорбции. Чтобы исключить влияние концентрации на производную берут ее предельные значения, т.е. при стремлении концентрации к нулю. Эту величину Ребиндер назвал поверхностной активностью.
![]() ;
;
g = [Дж×м/моль] = [Н×м2/моль]; [эрг см/моль] = [Гиббс].
Уравнение показывает, что чем сильнее снижается ![]() = f(c) с увеличением концентрации, тем больше поверхностная активность этого вещества.
= f(c) с увеличением концентрации, тем больше поверхностная активность этого вещества.
Физический смысл поверхностной активности состоит в том, что она представляет силу, удерживающую вещество на поверхности и отнесенную к единице гиббсовской адсорбции.
Поверхностную активность можно представить как отрицательный тангенс угла наклона к касательной, проведенной к кривой Г = f(C) в точке пересечения с осью ординат. Поверхностная активность может быть положительной и отрицательной. Значение и знак ее зависят от природы растворенного вещества и растворителя.
1. ![]() 2<
2<![]() 1, тогда
1, тогда ![]() <0 и Г>0: g>0 Þ с увеличением концентрации поверхностное натяжение на границе раздела фаз убывает и вещество поверхностно-активно.
<0 и Г>0: g>0 Þ с увеличением концентрации поверхностное натяжение на границе раздела фаз убывает и вещество поверхностно-активно.
1. ![]() 2<
2<![]() 1, то g<0: Г <0 Þ вещество поверхностно-инактивно.
1, то g<0: Г <0 Þ вещество поверхностно-инактивно.
Похожие работы
... слое и объемной фазе: ; ; , где - химический потенциал вещества в адсорбционном слое; - химический потенциал вещества в объемной фазе. При равновесии потенциалы равны: . Преобразуем: ; – адсорбция; аi= c. , , где D - коэффициент распределения. Выражение - константа Генри. Она не зависит от концентрации, определяется при постоянной температуре, A/a=Kг, А=а×Кг – закон Генри, ...
... промышленных сточных вод. Цель регенерации – с одной стороны, десорбция адсорбированных молекул (при регенеративной очистке воды) или деструктивное их разрушение и, с другой стороны, восстановление адсорбционной способности активного угля. Для удаления органических веществ с поверхности активного угля используют вытеснительную десорбцию, смещение равновесного состояния системы с помощью изменения ...
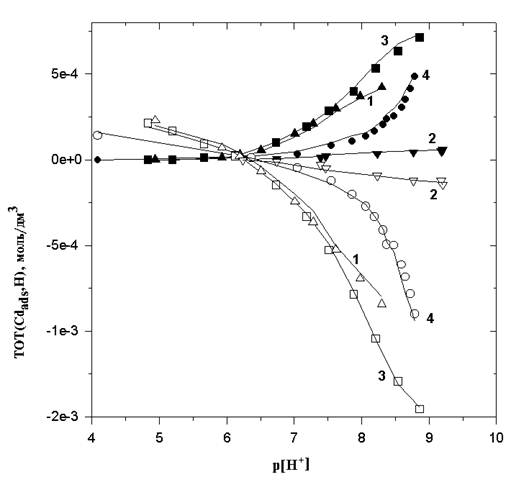
... , где уже произошло насыщение адсорбционных центров, и наблюдается дальнейшее снижение концентрации кадмия в растворе. В работах Мореля с сотрудниками [8,15] впервые предложена модель поверхностного осаждения, удовлетворительно описывающая сорбцию, включая переходную область между адсорбцией (поверхностным комплексообразованием) и объемным осаждением гидроксида металла. При рассмотрении процесса ...
... . Адсорбция полимера на пористой породе является причиной снижения концентрации полимера в водной фазе и, следовательно, снижение вязкости. 1. Теоретическая часть 1.1 Адсорбция полимеров на неорганических носителях 1.1.1 Теории адсорбции полимеров В 1953 году Фриш, Сима и Ирих одними из первых исследовали изменение в конформациях при соприкосновении Гауссовских цепей с поверхностью и ...
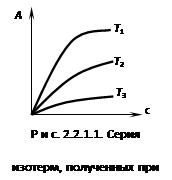







0 комментариев