Навигация
Адсорбционная хроматография. Уравнения изотермы адсорбции, их анализ и области применения
77. Адсорбционная хроматография. Уравнения изотермы адсорбции, их анализ и области применения.
Адсорбция – процесс самопроизвольного поглощения вещества (адсорбтива) поверхностью адсорбента. Уравнение Гиббса устанавливает взаимосвязь величины адсорбции (Г, кмоль/кг или кмоль/м 2) с изменением поверхностного натяжения (Дж/м2 от концентрации раствора (С, кмоль/л). ![]() ,
,
где С – концентрация раствора, кмоль/л;
R – универсальная газовая постоянная;
T – температура;
d/dС – производная, являющаяся мерой поверхностной активности; может быть определена графически по зависимости поверхностного натяжения от концентрации (при 0).
Физические процессы молекулярной адсорбции на твердой поверхности описываются уравнениями Ленгмюра и Фрейндлиха.
Уравнение Ленгмюра:
![]() ,
,
где Г – величина адсорбции, кмоль/кг или кмоль/м2;
Гmax – величина предельной адсорбции, кмоль/кг (кмоль/м2);
С – концентрация раствора, кмоль/л;
а – константа равновесия адсорбции.
Это уравнение хорошо описывает адсорбцию для малых и больших концентраций растворов (или давлений газа).
Эмпирическое уравнение Фрейндлиха:
![]() ,
,
где Г – величина адсорбции, кмоль/кг (кмоль/м2);
n – количество вещества-адсорбтива, кмоль;
m – масса адсорбента, кг;
К – константа (при С = 1 моль/л К = Г);
1/а – константа (адсорбционный показатель); зависит от природы адсорбента и температуры. 1/а = 0,1–1.
Уравнение (2.11) хорошо описывает адсорбцию для интервала средних концентраций растворов (или давлений газа).
Адсорбция на жидкой поверхности может приводить как к уменьшению поверхностного натяжения (например, при адсорбции малорастворимых, дифильных поверхностно-активных веществ), так и к его увеличению (в частности, при адсорбции поверхностно-инактивных веществ, т. е. хорошо растворимых в воде неорганических электролитов) или не изменять его (растворы сахаров в воде). В последнем случае вещество распределяется равномерно между поверхностным слоем и объемом раствора.
Адсорбция кислорода на поверхности мелких порошков и аэрозолей в ряде случаев может приводить к резкому ускорению процесса окисления дисперсной фазы, что может стать причиной самовозгорания и даже взрыва, например, мелкодисперсной муки, мучной, сахарной пыли и т. п. Ионная адсорбция может быть обратимой или необратимой. Обратимая адсорбция является основой ионообменной хроматографии.
Газовая хроматография может быть разделена на газо-адсорбционную (газо-твердую) и газо-жидкостную. В первом случае неподвижной фазой служит твердое вещество — адсорбент, во втором — жидкость, распределенная тонким слоем по поверхности какого-либо твердого носителя (зерненого материала, стенок колонки).
82. В каком объемном соотношении следует смешать 0,029 %-ный раствор NaCl и 0,001 н раствор AgNO3, чтобы получить незаряженные частицы золя AgCl? Плотность раствора NaCl равна 1 г/мл.
Решение. Запишем уравнение реакции:
NaCl + AgNO3 = AgCl + NaNO3
0,029 0,001 н.
Запишем формулу мицеллы: [m (AgСl) n Cl– · (n-1) Ag+]1– x Ag+
Для того, чтобы ее получить, следует взять в избытке раствор NaCl.
Исходя из формулы %-ной концентрации вещества можно записать, что:
![]()
Для того, чтобы определить массу растворенного нитрата серебра, воспользуемся формулой:
![]()
Откуда масса вещества AgNO3 равна:
![]()
По уравнению масса хлорида натрия:
х_-------------------------107 г.
58 г/моль------------------107г/моль
х=58 г
Объем раствора хлорида натрия:
![]()
Объем раствора нитрата серебра
2000, 42 мл----------------------------х мл
58 г/моль 107 г/моль
х = 2000, 42*107 /58 = 3690,43 мл
Соотношение объемов веществ:![]()
98. Коагуляция дисперсной системы. Скорость коагуляции. Причины, вызывающие процесс самопроизвольной коагуляции.
Коагуляция – процесс самопроизвольного укрупнения (слипания) дисперсных частиц, который может происходить при действии на дисперсную систему различных факторов: при интенсивном перемешивании или встряхивании, нагреве или охлаждении, облучении светом или пропускании электрического тока, при добавлении к системе электролитов или неэлектролитов и др. При разных способах воздействия на систему происходит уменьшение энергии связи диспергированных частиц с окружающей их дисперсионной средой. Так, добавление электролита вызывает сжатие диффузного слоя в коллоидной частице, следовательно, понижение величины электрокинетического потенциала. Это приводит к уменьшению электростатического отталкивания коллоидных частиц и, как следствие, к большей вероятности их слипания.
Минимальная концентрация электролита, добавляемого к дисперсной системе, при которой наступает явная коагуляция за определенный промежуток времени, носит название порога коагуляции ![]() . Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
. Порог коагуляции определяется температурой, природой добавленного электролита, знаком заряда добавляемого иона (действует прежде всего ион, имеющий заряд, противоположный заряду коллоидных частиц) и величиной заряда этого иона. Так, для трех-, двух- и однозарядных ионов явная коагуляция наступает при концентрации электролитов в соотношении 1:10 - 50: 500-1000 (приближенное правило Шульце-Гарди).
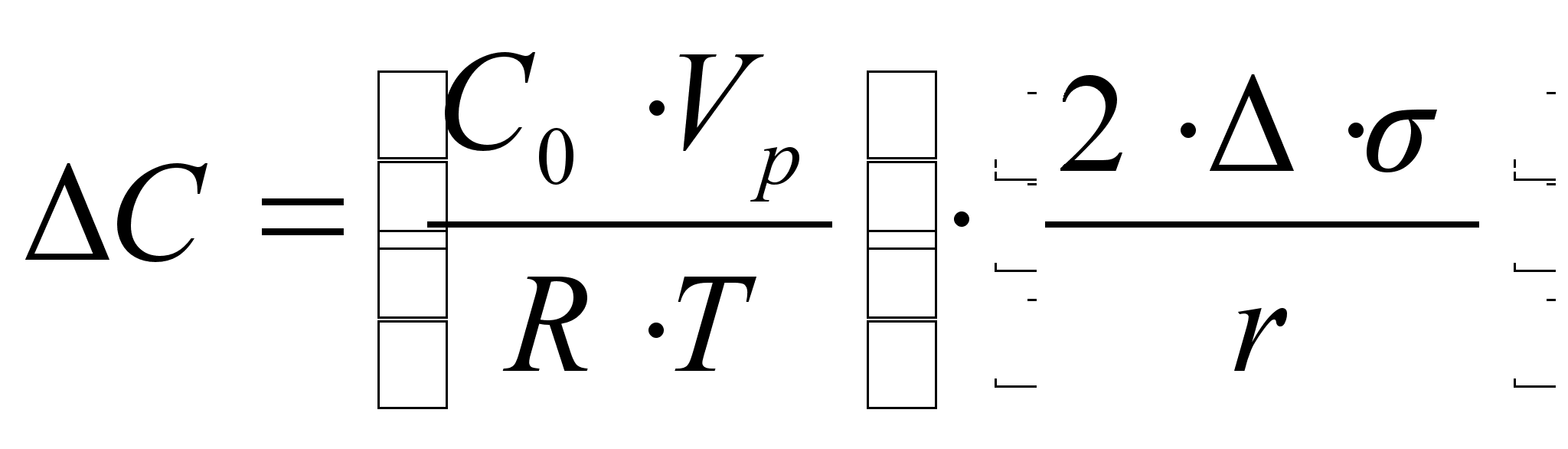
Порог коагуляции рассчитывается следующим образом:
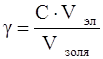 , (1)
, (1)
где порог коагуляции, кмоль/м3;
С – молярная концентрация раствора электролита, кмоль/м3;
Vэл – объем раствора электролита, м3;
Vзоля – объем золя, м3.
Теорию быстрой скорости коагуляции разработал Смолуховский. Он автор уравнения для расчета константы скорости коагуляции K:
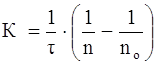 , (2)
, (2)
где n0 и n – число частиц в единице объема системы до начала коагуляции и к моменту времени ![]() соответственно
соответственно
время коагуляции, с.
Константа скорости коагуляции зависит от коэффициента диффузии для частиц и их радиуса следующим образом:
К = 8 · ·D · r. (3)
Учитывая уравнение (2) и уравнение Эйнштейна, окончательное уравнение для константы скорости коагуляции принимает вид:
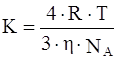 , (4)
, (4)
где К – константа скорости коагуляции, м3/с;
![]() – вязкость среды, Па·с;
– вязкость среды, Па·с;
NA – число Авогадро.
Смолуховский ввел также понятие о времени половинной коагуляции, согласно которому время, необходимое для уменьшения первоначального числа частиц в 2 раза, связано с их исходным числом следующим образом:
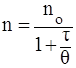 , (5)
, (5)
где – время половинной коагуляции, с;
– время от начала коагуляции, с.
Из уравнения, преобразованного к виду:
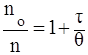 , (6)
, (6)
следует, что если построенный в координатах nо/n = f ( график представляет собой прямую линию, то это служит показателем соответствия экспериментальных данных теории Смолуховского.
Похожие работы
... , чтобы подчеркнуть, что дисперсной средой является жидкость. Если дисперсной средой является вода, то такие золи называют гидрозолями, а если органическая жидкость – органозолями. Дисперсные системы могут быть свободнодисперсными и связнодисперсными в зависимости от отсутствия или наличия взаимодействия между частицами дисперсной фазы. К свободнодисперсным системам относятся аэрозоли, ...
... , а -потенциал уменьшается, постепенно приближаясь к нулю. При разбавлении системы, наоборот, диффузный слой расширяется и -потенциал возрастает. II.Электрокинетический потенциал Протекание электрокинетических явлений в дисперсных системах возможно при наличии на границе раздела фаз двойного электрического слоя, имеющего диффузное строение. При относительном смещении фаз происходит разрыв ...
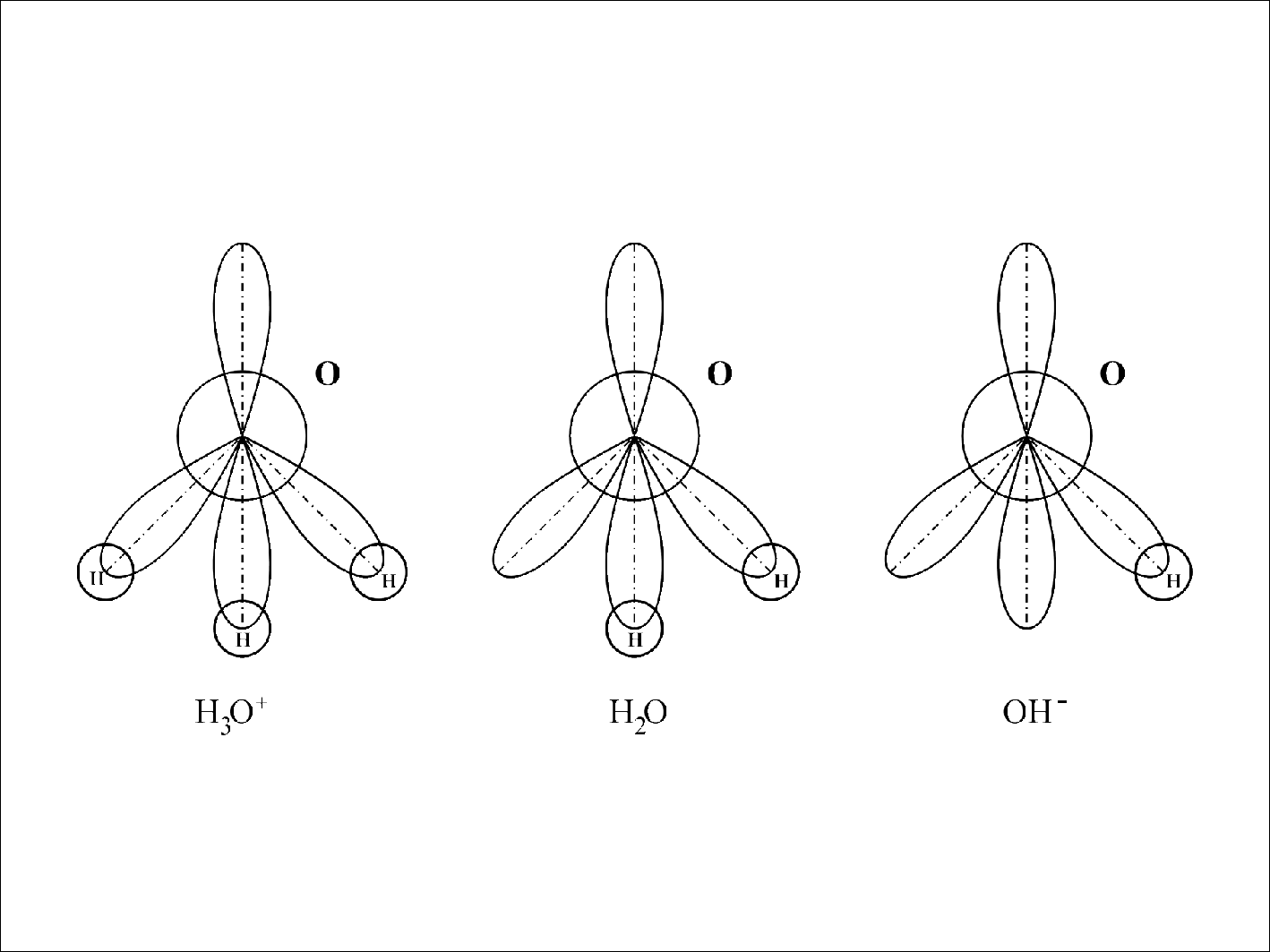
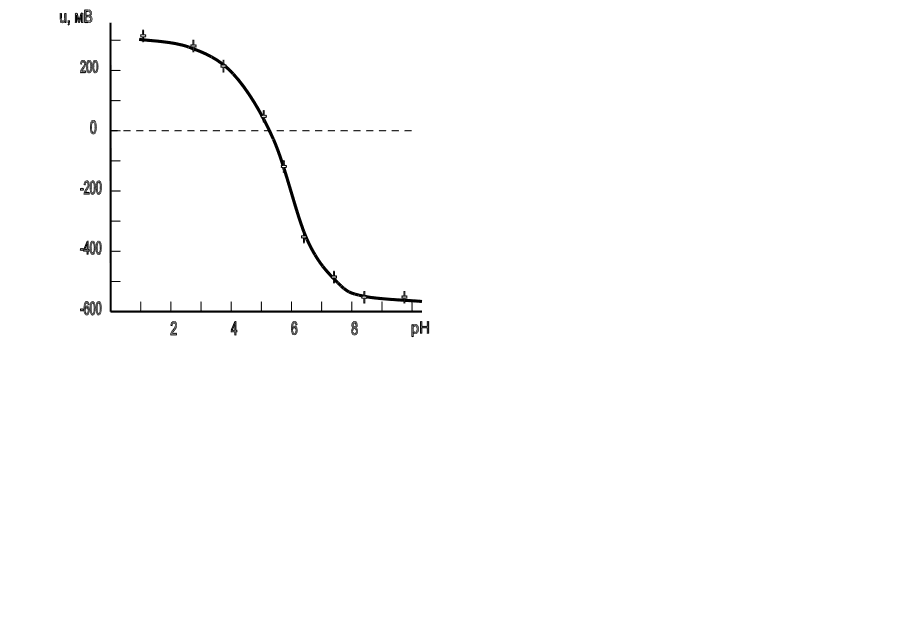
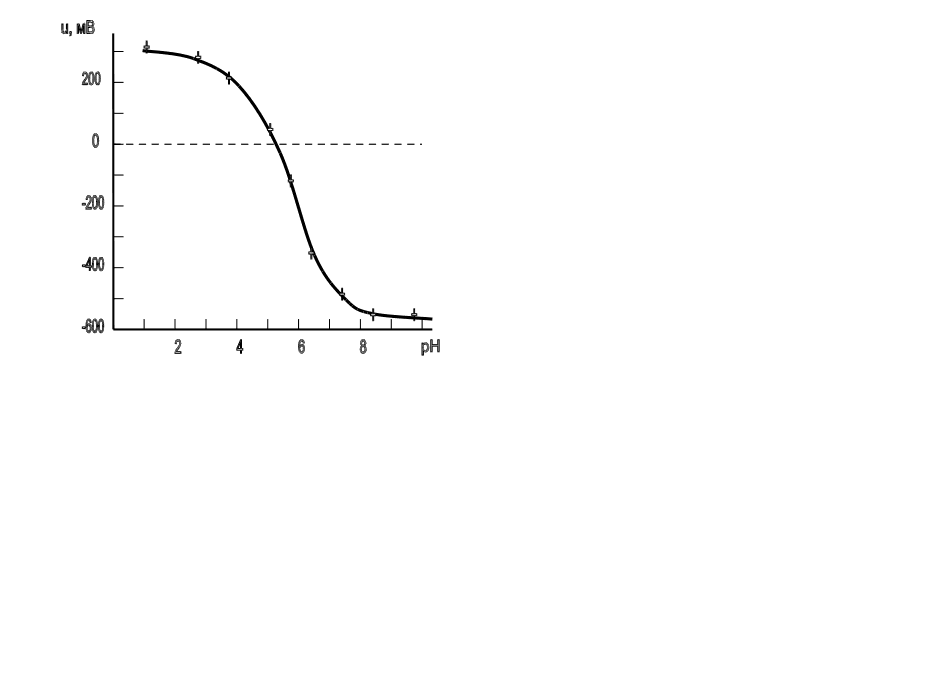
... на поверхность. Величины адсорбции ионов Н3О+ и OH- обусловлены особенностям химического состава, кристаллической структуры и состояния поверхности частиц дисперсной фазы. Свойства межфазных границ «вода – дисперсная фаза» зависят также от поверхностного потенциала воды. Известно, что в нейтральной среде поверхность воды имеет отрицательный потенциал -450 мВ, несмотря на то, что концентрация ионов ...
... и многое другое, без чего немыслима сама жизнь. Все человеческое тело – это мир частиц, находящихся в постоянном движении строго по определенным правилам, подчиняющимся физиологии человека. Коллоидные системы организмов обладают рядом биологических свойств, характеризующих то или иное коллоидное состояние: 2.2 Коллоидная система клеток. С точки зрения коллоидно-химической физиологии ...
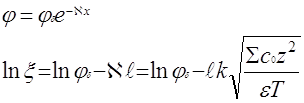
0 комментариев