Навигация
Исследование кинетики набухания в различных средах
2.3 Исследование кинетики набухания в различных средах
Определение кинетики набухания в воде
В результате исследований кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в воде получили следующие данные Приложение А (таблица 2). По полученным данным построили график кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в воде Приложение А (рис. 2).
Коэффициента набухания для гидрогелей АА - АК - ПЭИ в воде.
Для чистого гидрогеля, а = 20,23.
Для гидрогеля с никелем, а = 37,21.
Время равновесного набухания одинаково для обоих гидрогелей, и оно составляет 72 часа.
Определение коэффициента набухания в 0,1 н растворе гидроксида натрия.
В результате исследований кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в NaOH 0.1н. получили следующие данные Приложение Б (таблица 3). По полученным данным построили график кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в NaOH 0.1н. Приложение Б (рис. 3).
Время равновесного набухания для гидрогеля АА - АК - ПЭИ чистого составляет 4 часа, а для гидрогеля с «вшитым» металлом никелем оно составляет 2 часа.
Определение коэффициента набухания в 0,1 н растворе соляной кислоты.
В результате исследований кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в HCl 0.1 н воде получили следующие данные Приложение В (таблица 4). По полученным данным построили график кинетики набухания гидрогеля АА – АК - ПЭИ чистого и с «вшитым» металлом никелем в HCl 0.1 н Приложение В (рис. 4).
Время равновесного набухания одинаково для обоих гидрогелей, и оно составляет 48 часов.
Определение коэффициента набухания в 5% растворе гидроксида аммония.
В результате исследований кинетики набухания гидрогеля АА - АК - ПЭИ чистого и с «вшитым» металлом никелем в NH4OH 5% получили следующие данные Приложение Г (таблица 5). По полученным данным построили график кинетики набухания гидрогеля АА – АК - ПЭИ чистого и с «вшитым» металлом никелем в NH4OH 5% Приложение Г (рис. 5).
Время равновесного набухания одинаково для обоих гидрогелей, и оно составляет 2 часа.
2.4 Исследование влияния растворителей, ионной силы и pH
Определение влияния ионной силы раствора (раствор хлорида калия).
В результате исследований влияния ионной силы раствора (раствор хлорида калия) на гидрогель АА - АК - ПЭИ чистый и с «вшитым» металлом никелем получили следующие данные Приложение Д (таблица 6). По полученным данным построили график. Приложение Д (рис. 6).
Определение влияния растворителя вода – этанол.
В результате исследований влияния растворителя вода – спирт на гидрогель АА - АК - ПЭИ чистый и с «вшитым» металлом никелем получили следующие данные Приложение Е (таблица 7). По полученным данным построили график. Приложение Е (рис. 7).
Определение влияния растворителя вода – ацетон.
В результате исследований влияния растворителя вода – ацетон на гидрогель АА – АК - ПЭИ чистый и с «вшитым» металлом никелем получили следующие данные Приложение Ж (таблица 8). По полученным данным построили график. Приложение Ж (рис. 8).
Определение влияния pH.
В результате исследования влияния pH на гидрогель АА - АК - ПЭИ чистый и с «вшитым» металлом никелем получили следующие данные Приложение З (таблица 9). По полученным данным построили график. Приложение З (рис. 9).
3 Обсуждение результатов и выводы
В результате проведенных экспериментов были получены результаты:
1. Коэффициент набухания АА – АК - ПЭИ чистого и с «вшитым» металлом никелем соответственно составляет, а = 20,33; а = 37,21.
2. Время равновесного набухания в воде - 72 часа, в 0,1 н. растворе соляной кислоты - 48 часов, в 5% растворе гидроксида аммония – 2 часа; причем время в одной среде одинаково для обоих гидрогелей. Время равновесного набухания в 0,1 н растворе гидроксида натрия различно, оно составляет 4 часа для гидрогеля АА - АК - ПЭИ чистого и 2 часа для гидрогеля АА - АК - ПЭИ с «вшитым» металлом никелем.
3. Исследованы кинетики набухания в различных средах гель- иммобилизованных полиметаллических комплексов на основе полиакриламид акриловая кислота полиэтиленимина (чистого и с «вшитым» металлом никелем).
4. Исследовано влияние растворителей, ионной силы и pH на гель- иммобилизованные полиметаллические комплексы на основе полиакриламид акриловая кислота полиэтиленимина (чистого и с «вшитым» металлом никелем).
Полученные нами результаты позволяют в данное время сделать следующие выводы:
1. Полимерметаллический комплекс с «вшитым» в него никелем ведет себя более активней в воде; в других средах он проявляет себя менее активно по сравнению с аналогичным полимером (чистым). Возможно, это указывает на то, что металл никель придает большую устойчивость полимерметаллическому комплексу по сравнению с аналогичным гидрогелем, но без иммобилизованного металла.
2. Под действием ионной силы и молекул растворителя (этанол, ацетон) сетка гидрогеля акрил амид акриловая кислота сжимается, т.е. происходит коллапс, что указывает на адекватность гидрогеля на изменение среды, в которой он находится. Влияние pH среды обуславливается ее кислотно - основностью, что уже оговаривалось выше, в связи с исследованиями кинетики набухания исследуемого гидрогеля. Возможно, предположить, что у гидрогеля АА - АК - ПЭИ с иммобилизованным металлом никелем, константа устойчивости комплекса больше, чем у гидрогеля АА - АК - ПЭИ без иммобилизованного металла.
Список использованной литературы
1. Бектуров Е.А. // Полимерные электролиты, гидрогели, комплексы и катализаторы Алматы 2007г.С.140-143
2. Мамбетказиев Е.А., Лобанов Ф.И., Мамбетказиева Р.А. // Вестник КазНУ имени Аль-Фараби 2002 г. № 3.С.166
3. Кульдашева Ш.А., Агзамходжаев А.А. //Узб. Хим. Ж. 2000 г.№5.С.73
4. Пописов И.М. Матричная полимиризация и другие матричные и псевдоматричные процессы как путь получения композиционных материалов. //Высокомалек. Соед. 1979 Т. А21. С. 243
5. Литманский А.А., Пописов И.Н //Высокомалек. Соед. 1997. Т. Б 39 С. 323
6. Литманович О.Е., Литманович А.А., Пописов И.М. Высокомалек. Соед. 1997 С.1608
7. Хамзамурина Р.Е., Бектуров Е.А., Бимендина Л.А. 1994 С. 943
8. Мусабеков К.Б., Адильбеков А.О., Абилов Ж.А. // Вестн. КазГУ. Сер. Хим. 1998 №10. С. 49
9. Измаилова В.Н., Левачев С.М., Ямпольская Г. П., Грецкова И.А. //Коллоидные растворы. Ж. 2000. Т. 62 С.70
10. Бектуров Е.А. // Полимерные электролиты, гидрогели, комплексы и катализаторы Алматы 2007г.С.77-81
11. Сперлинг Л.Х. Взаимопроникающие Полимерные Сетки и Связывающие Материалы. Нью-Йорк, 1981 г.
12. Гупта Н., Сривастава А. К. Взаимопроникающие Полимерные Сетки: обзор синтеза и свойств. Полим. Инт. 1994 г., 35(2), 109-118.
13. Миллар Ж.Р. //Взаимопроникающие сетки. 1960 г.
14. Сперлинг Л.Х. /Многофазные макромолекулярные системы. Современные темы в Полимерной науке. Под редакцией Кулбертсона Б.М. Нью-Йорк, 1989 г., 6-е издание.
15.Шилов В.В., Липатов Ю.С., Карабанова Л., Сергеева Л. Фазовое разделение во взаимопроникающих полимерных сетках на базе полиуретана и полистирена. 1979 г.
16. Кудайбергенов С. Е., Бимендина Л. А., Жумадилова Ж. Т. // Полимеры 2000. Т. 11
17. Кудайбергенов С., Сигитов В., Тастанов К., Тенху Х., Асеев В. Анализ качества подземных вод Аральского региона и методы их очистки// Материалы 6 – го Международного конгресса и технической выставки «Вода: экология и технология» ЭКВАТЕК - 2004. – Ч.1. – С.174 – 175.
18. Кудайбергенов С.Е., Бимендина Л.А., Яшкарова М.Г., Оразжанова Л.К., Сигитов В.Б. Синтез, свойства и применение новых полимерных бетаинов на основе аминокротонатов. Науч. Изд. СГУ им. Шакарима, Семипалатинск 2006.
19. Гросберг А.Ю., Хохлов А.Р. Физика в мире полимеров. М., 1989.
20. Хохлов А.Р., Дормидонтова Е.Е. // Успехи физ. наук. 1997. Т.167. 2. С.113-128.
21. Хохлов А.Р. // Соросовский образовательный журнал. 1998. 11. С.138-142.
22. Филиппова О.Е. // Высокомолек. соед., серия С. 2000. Т.42. 12. С.2328-2352.
23. Галаев Ю.В. // Успехи химии. 1995. Т.64. 5. С.505-524.
24. Ергожин Е.Е., Уткелов Б.А. Хелатные полимерные реагенты.- Алматы, Гылым, 1998. – 247 с.
25. Аширов А. Ионообменная очистка сточных вод, ратсворов и газов. – Л., 1983. – 295 с.
26. Бектуров Е.А., Бимендина Л.А., Кудайбергенов С.Е. Полимерные комплексы и катализаторы. Алма – Ата. 1982. – 191 с.
27. Бектуров Е.А., Кудайбергенов С.Е. Катализ полимерами. – Алма – Ата, Наука, 1988. – 184 с.
28. Гембицкий П.А., Жук Д.С., Каргин В.А. // Полиэтиленимин Изд. Наука Москва 1991г С. 97-99
29. Филиппова О.Е. ««Умные» полимерные гидрогели» Публикация физфак МГУ.
30. Гросберг А.Ю., Хохлов А.Р. //Физика в мире полимеров. М., 1989.
31. Матвеева Н.Г. //Координационные полимеры. Энциклопедия полимеров. – М., 1972. Т.1. С. 1110.
Приложение А
| Время (ч) | масса (мг) гидрогеля с Ni | Масса (мг) гидрогеля |
| 0 | 48 | 45 |
| 0,08 | 469 | 357 |
| 0,166 | 656 | 390 |
| 0,25 | 914 | 459 |
| 0,5 | 1305 | 602 |
| 1 | 1510 | 903 |
| 2 | 1759 | 1059 |
| 4 | 1872 | 1228 |
| 24 | 1880 | 1228 |
| 48 | 3355 | 1721 |
| 72 | 3514 | 1784 |
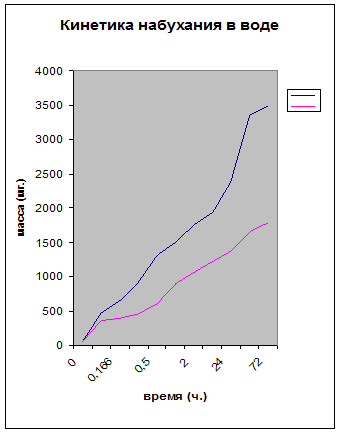
Рис.2 Кинетика набухания гидрогеля АА - АК - ПЭИ чистый и с «вшитым» металлом никелем в воде
Приложение Б
| время (ч) | Масса (мг) гидрогеля с Ni | масса (мг) гидрогеля |
| 0 | 747 | 867 |
| 0,08 | 894 | 1132 |
| 0,166 | 1020 | 1272 |
| 0,25 | 1198 | 1441 |
| 0,5 | 1230 | 1634 |
| 1 | 1185 | 1902 |
| 2 | 1184 | 1923 |
| 4 | 1010 | 2124 |
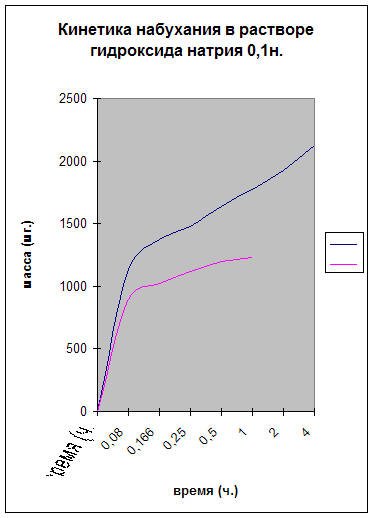
Рис.3 Кинетика набухания гидрогеля АА - АК - ПЭИ чистый и с «вшитым» металлом никелем в растворе NaOH 0.1н
Приложение В
| время (ч) | масса (мг) гидрогеля с Ni | масса (мг) гидрогеля |
| 0 | 969 | 1213 |
| 0,08 | 610 | 1069 |
| 0,166 | 548 | 873 |
| 0,25 | 459 | 766 |
| 0,5 | 414 | 661 |
| 1 | 363 | 575 |
| 2 | 298 | 482 |
| 4 | 218 | 368 |
| 24 | 35 | 97 |
| 48 | 22 | 87 |
| 72 | 27 | 106 |
Рис.4 Кинетика набухания гидрогеля АА - АК - ПЭИ чистый и с «вшитым» металлом никелем в растворе HCl 0.1 н.
Приложение Г
| время (ч) | масса (мг) для гидрогеля с Ni | масса (мг) гидрогеля |
| 0 | 636 | 453 |
| 0,08 | 773 | 670 |
| 0,166 | 840 | 763 |
| 0,25 | 879 | 833 |
| 0,5 | 954 | 997 |
| 1 | 957 | 1149 |
| 2 | 978 | 1152 |
| 4 | 870 | 1034 |
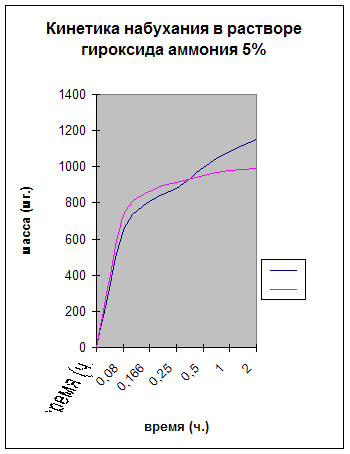
Рис.5 Кинетика набухания гидрогеля АА - АК - ПЭИ чистый и с «вшитым» металлом никелем в NH4OH 5%
Приложение Д
| Концентрация р-ра KCl (н.) | m/ m0 гидрогеля с Ni | m/ m0 гидрогеля |
| 1 | 0,101 | 0,128 |
| 0.1 | 0,194 | 0,158 |
| 0,01 | 0,528 | 0,360 |
| 0,001 | 0,870 | 0,694 |
|
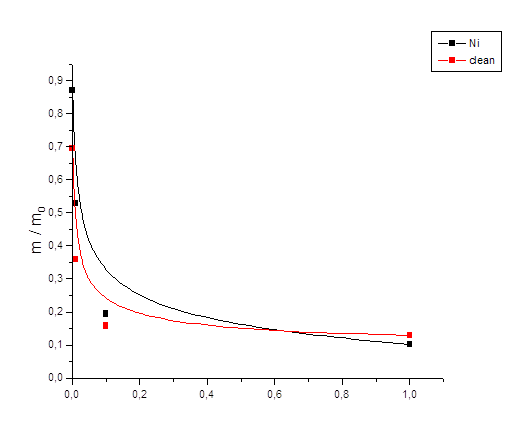
Рис. 6 Кривые ионная сила – отношение m/m0 гидрогелей АА - АК - ПЭИ чистый и с «вшитым» металлом никелем
Приложение Е
| Соотношение вода – спирт | m/ m0 гидрогеля с Ni | m/ m0 гидрогеля |
| 10: 0 | 1,000 | 1,000 |
| 9: 1 | 0,970 | 0,745 |
| 8: 2 | 0,945 | 0,710 |
| 7: 3 | 0,749 | 0,675 |
| 6: 4 | 0,660 | 0,591 |
| 5: 5 | 0,551 | 0,478 |
| 4: 6 | 0,473 | 0,393 |
| 3: 7 | 0,431 | 0,176 |
| 2: 8 | 0,397 | 0,095 |
| 1: 9 | 0,185 | 0,084 |
| 0: 10 | 0,082 | 0,051 |
|
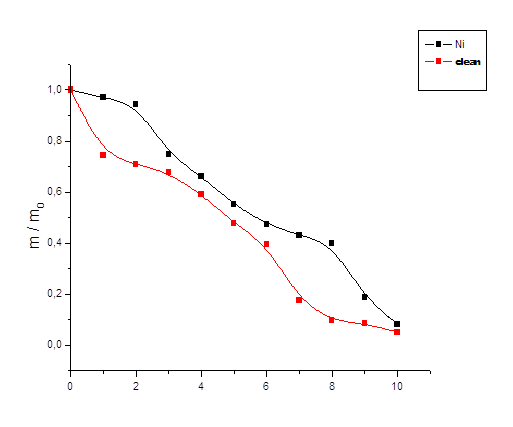
Рис. 7 Кривые вода–этанол – отношение m/m0 гидрогелей АА - АК - ПЭИ чистый и с «вшитым» металлом никелем
Приложение Ж
| Соотношение вода – ацетон | m/ m0 гидрогеля с Ni | m/ m0 гидрогеля |
| 10: 0 | 1,000 | 1,000 |
| 9: 1 | 0,980 | 0,930 |
| 8: 2 | 0,876 | 0,710 |
| 7: 3 | 0,693 | 0,672 |
| 6: 4 | 0,656 | 0,518 |
| 5: 5 | 0,601 | 0,437 |
| 4: 6 | 0,534 | 0,391 |
| 3: 7 | 0,345 | 0,266 |
| 2: 8 | 0,256 | 0,196 |
| 1: 9 | 0,169 | 0,124 |
| 0: 10 | 0,092 | 0,101 |
|
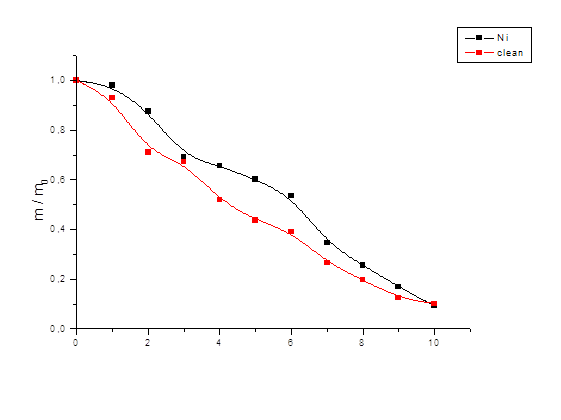
Рис. 8 Кривые вода–ацетон – отношение m/m0 гидрогелей АА - АК - ПЭИ чистый с «вшитым» металлом никелем
Приложение З
| pH – среда | m/ m0 гидрогеля с Ni | m/ m0 гидрогеля |
| 1,65 | 0,063 | 0,041 |
| 4,01 | 0,213 | 0,108 |
| 6,86 | 0,618 | 0,401 |
| 9,18 | 1,010 | 0,896 |
|
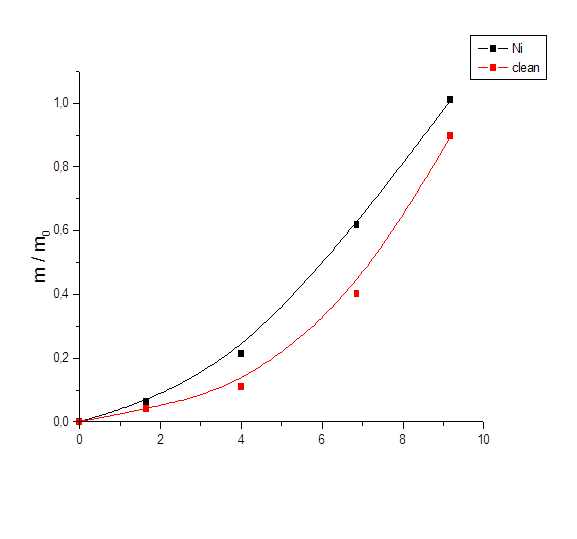
Рис. 9 Кривые pH-среда – отношение m/m0 гидрогелей АА - АК - ПЭИ чистый и с «вшитым» металлом никелем
0 комментариев