Навигация
ТЕХНИКО-ЭКОНОМИЧЕСКИЕ ПОКАЗАТЕЛИ
5. ТЕХНИКО-ЭКОНОМИЧЕСКИЕ ПОКАЗАТЕЛИ
В разделе 3 дана характеристика энергетических ресурсов используемых в производстве кальцинированной соды. В таблице 5.1 приведены нормы расхода этих ресурсов на 1 тонну выпускаемой соды [1–3]:
Таблица 5.1 – Усредненные энергетические затраты на 1 тонну 100 %–ой кальцинированной соды
| Затраты | Расходный коэффициент |
| Электроэнергия, МДж (кВт·ч) | 220 (61) |
| Пар на технологические нужды, ГДж (Гкал) | 5,36 (1,28) |
| Вода (оборотная), м3 | 150 |
| Топливо (в пересчете на условное топливо), кг: для кальцинации гидрокарбоната натрия для обжига карбонатного сырья | 130 95 |
При этом необходимо отметить, что в окружающую среду отводится около 1 МВт тепловой энергии на 1 тонну кальцинированной соды.
Ниже приведены обобщенные нормы расхода для производства кальцинированной соды аммиачным методом [2]:
Таблица 5.2 – Расходные нормы по сырью для производства 1 т соды
| Затраты | Расходный коэффициент |
| Рассол очищенный (310 г/л NaCl), м3 | 5,1 |
| Известняк (в пересчете на 100 % СаСО3), кг | 1280 |
| Кальцинированная сода на очистку сырого рассола от солей кальция, кг | 22 |
| Аммиачная вода (25,5 % NH3), кг | 9 |
| Гидросульфит натрия (в пересчете на 22,0 % NaHS), кг | 5 |
6. ОТХОДЫ В ПРОИЗВОДСТВЕ СОДЫ И МЕТОДЫ ИХ ПЕРЕРАБОТКИ
В традиционной технологии кальцинированной соды на 1 тонну продукта приходятся следующие отходы:
хлоридные стоки, содержащие около 115–125 г/л СаС12, 55–58 г/л NaCl и 20–25 г/л взвеси Са(ОН)2, СаСО3 и CaSO4 – около 9,1 м3;
шлам от очистки рассола, содержащий 250–300 г/л взвеси Са(ОН)2 и Mg(OH)2 – 0,l м3, шлам дистилляции;
недопал при обжиге мела или известняка, отделяемый в процессе получения известковой суспензии и содержащий СаСО3, СаО и золу топлива, около 55 кг.
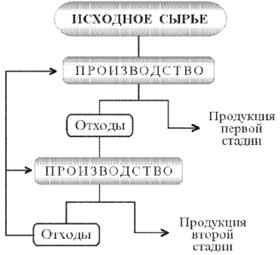
В так называемые производственные отходы переходит весь содержащийся в сырье кальций, хлор и около 1/3 натрия. В пересчете на твердое состояние при производстве 1 т кальцинированной соды в отходах содержится около 1 т СаСl2, 0,5 т NaCl, 200 кг шлама и 55 кг недопала [1–3, 5]. На рис. 6.1 изображена простая схема цикла.

Рис. 6.1 – Простая схема цикла производства кальцинированной соды
6.1 ПЕРЕРАБОТКА ЖИДКИХ ОТХОДОВ
Для фильтровой жидкости предлагается получение хлористого аммония.
При производстве хлорида аммония часть или весь поток фильтровой жидкости после барабанных вакуум-фильтров направляется на дегазацию (узел XII), которая осуществляется паром (раздел 3 рис. 3.2). Десорбированные из жидкости в парогазовый поток аммиак и диоксида углерода поступают на абсорбцию II.
На абсорбцию в отделение II дополнительно подается газообразный аммиак от аммиачно-испарительной установки для восполнения убыли аммиака, который выводится из цикла хлоридом аммония, растворенным в дегазированной фильтровой жидкости. Дегазированная фильтровальная жидкость направляется на выпарку (отделение XIII), после которой образующаяся соляная пульпа проходит стадию отстаивания и центрифугирования (XIV), сушки и прокалки поваренной соли (XV).
Соляной маточный раствор подается на вакуум-кристаллизацию (XVI); пульпа хлорида аммония поступает далее на отстаивание и центрифугирование (XVII); хлорид аммония проходит сушку, зернение (XVIII) и направляется на склад готовой продукции.
Существует и предлагается несколько способов утилизации дистиллерной жидкости: первое – переработка осветленной дистиллерной жидкости, которая заключается в получении хлорида кальция, второе – после соответствующей подготовки закачивание дистиллерной жидкости в нефтяные скважины, третье – получение из дистиллерной жидкости химически осажденного карбоната кальция [8].
При производстве СаСl2 весь поток дистиллерной суспензии (рис. 3.2) или его часть подвергается предварительной карбонизации и далее поступает на отстаивание от взвешенных частиц (XIX). Шлам из отстойника направляется для дальнейшей переработки (стадия XXIV), а осветленный раствор сливается в ёмкость (XX), в которую подают затравку из активного сульфат кальция для предотвращения инкрустирования выпарной трёхкорпусной прямоточной батареи. Дистиллерная жидкость упаривается до достижения концентрации хлорида кальция 18 % масс. Во второй трёхкорпусной прямоточной батарее (стадия XXI) дистиллерная жидкость упаривается до концентрации хлорида кальция 38 % масс, с выделением основной массы поваренной соли. Осветленный 38 %-ый раствор раствор хлорида кальция подается на вакуум-кристаллизатор (стадия XXII), в котором происходит образование 40 %-го раствора хлорида кальция и выделение хлорида натрия. Далее раствор подается в аппарат XXIII, где упаривается с образованием плава, содержащего 72 % хлорида кальция. После чего плав чешуируется, закаливается, сушится, охлаждается и направляется на склад готовой продукции.
Способ подготовки дистиллерной жидкости, используемой для закачки в нефтяные скважины, включает следующие стадии:
– отстой суспензии в накопителе – “белое море”;
– разбавление ответвленной дистиллерной жидкости водой с целью снятия пересыщения по гипсу;
– карбонизация разбавленной дистиллерной жидкости газом известковых печей в присутствии ретурного шлама;
– отстаивание и транспортирование прокарбонизарованной дистиллерной жидкости.
Описанный способ подготовки позволяет получать для заводнения нефтяных пластов дистиллерную жидкость следующего качества:
· Отсутствие OH––ионов, которые с Fe2+ и Mg2+ вместе с образуют нерастворимые осадки, способные кальматировать пласты;
· Отсутствие взвешенных и емханических примесей в количествах, превышающих предельно допустимую концентрацию;
· Отсутствие пересыщения по гипсу.
Автором работы [8] предложена и описана принципиальная аппаратурно-технологическая схема производства осажденного CaCO3.
Согласно предлагаемой схеме дистиллерная жидкость (содержание твердой фазы 22,75 г/дм3) с производства кальцинированной соды поступает в отстойник при температуре 363–368 К. Сгущенная твердая фаза (шлам) с соотношением Т:Ж = 1:2 откачивается в шламонакопитель, а осветленная часть поступает в соответствующий сборник.
Избыточный маточный раствор производства очищенного карбоната натрия с температурой 333–348 К подается в соответствующий сборник. Ответвленная часть дистиллерной жидкости и избыточный маточный раствор смешиваются в реакторе–осадителе в течение 3 минут при их одновременном смешивании при температуре 353–358 К.
Полученная суспензия CaCO3 подается на фильтрование, а диоксид углерода, полученный после разложения кислой соли кальция выводится из реактора в производство соды. Полученный осадок CaCO3 отмывается от ионов хлора и фильтруется на камерных фильтрпрессах. После чего полученный фильтрат и промывные воды откачиваются на розсоломпромысел.
Промытый осадок CaCO3 высушивается в ленточной сушилке при помощи топочных газов, а затем направляется на измельчение в дезинтегратор, откуда на рассев. Затаривание готового продукта осуществляется в шнековой розфасовочной машине. Полученный продукт CaCO3 соответствует требованиям ГОСТ 8253–79 [9].
Имеются в литературе данные по переработке дистиллерной жидкости в пероксид кальция CaO2 , который имею широкую область применения [10].
В области охраны окружающей среды его можно использовать при очистке воды от катионов железа, мышьяка, марганца, цинка, хрома и меди [11].
Также пероксид кальция можно использовать в катализаторе для очистки промышленных и бытовых сточных вод от нефтепродуктов и для очистки сточных вод содержащих органические красители [12, 13]. Очистка вредных газовых выбросов химической промышленности от диоксида серы и оксидов азота может быть обеспечена суспензией содержащей смесь пероксида и гидроксида кальция в соотношении 1:1. Также можно осуществить и очистку газовой смеси от формальдегида [11]. Пероксид кальция применяют в обезвреживании радиоактивных отходов переменного состава [13]. Его используют и для обеззараживания ила бытовых городских стоков [11].
В органическом синтезе пероксид кальция используется как катализатор для окисления изопропилбензола до α-кумулгидроперекиси и для получения полисульфидов этилена, пропилена, бутилена. Он также используется в качестве промотора оксида серебра, употребляемого в качестве катализатора в процессе окисления этана до оксида этилена, диоксида углерода и воды. Также предложено использовать пероксид кальция для стабилизации вулканизированных сополимеров изобутилена и наряду с пероксидом стронция в процессе вулканизации бутилкаучука.
Пероксид кальция используют как источник кислорода в алюмотермических и других металлургических процессах. Его также используют при рафинировании металлов шлаки, содержащие сульфиды и для дефосфоризации стали.
6.2 ПЕРЕРАБОТКА ТВЕРДЫХ ОТХОДОВК твердым отходам содового производства относятся:
– шлам рассолоочистки;
– шлам дистилляции;
– отходы гашения извести и известковой пыли производства извести и гидратированной извести.
Рассмотрим вкратце по порядку предлагаемые технологии [2–3].
Технология утилизации шламов рассолоочисткиДля уменьшения количества шлама предлагается рассолоочистку проводить с поэтапным осаждением из раствора Mg(OH)2, CaCO3, 5CaSO4·Na2SO4·H2O. Отмечается, что указанные продукты выделяются в достаточно чистом виде и могут быть переработаны в целевые продукты.
При классической рассолоочистке тожу можно выделить из шлама компоненты. При этом процесс переработки шлама можно разделить на несколько стадий:
· Частичная нейтрализация шлама;
· Карбонизация частично нейтрализованного шлама;
· Фильтрование карбонизованной суспензии и промывка осадка мела;
· Получение основного карбоната магния.
В результате этой технология на й тонну соды можно получать 2,2·10–3 т основного карбоната магния, 0,6 м3 очищенного рассола NaCl, 1,3·10–3 т химически осажденного мела.
Технологии утилизации шлама дистилляцииКоличество твердых отходов на стадии дистилляции оставляет 200–250 кг на 1 т выпускаемой соды.
В течение ряда лет одним из основных направлений по утилизации твердых отходов дистилляции являлась технология переработки шламов на мелиорант для химической мелиорации почв, кормовой добавки для кормления сельскохозяйственной птицы, комплексной добавки для сельскохозяйственных животных, использование в производстве вяжущих и цементного клинкера.
Технологии утилизации отходов гашения извести и известковой пыли производства извести и гидратированной известиНа эту тему существует много патентов и публикаций. Однако несмотря на положительный эффект, эти практические предложения не нашли применения в промышленной практике, по крайней мере на заводах СНГ. Это объясняется, по-видимому, тем, что затраты на вывод мелких отходов гашения из цикла, а так же улавливание пыли, превышает доход от применения при производстве строительных материалов. Поэтому на большинстве содовых заводов мелкие отходы гашения подвергают мокрому помолу и сбрасывают в шламонакопители. Фактически в отвалы и шламонакопители отводится улавливаемые известкова пыль и пыль улавливаемая мокрым способом при очистке газа известковых печей.
7. РАСЧЕТНАЯ ЧАСТЬ
Процесс производства соды можно отобразить в виде суммарных реакций:
![]() (1)
(1)
![]() (2)
(2)
Задание №1: Рассчитаем материальный баланс по реакции (1) на 1000 кг NaHCO3 при a1=1 двумя способами.
Первый способ
Рассчитаем массу NaCl, NH3, CO2, H2O необходимую для получения 1000 кг NaHCO3.
Расчет будем вести по пропорции, где слева – реагент, справа – продукт.
![]()
M(NaCl)=23+35,5=58,5 кг/кмоль; M(NaHCO3)=23+1+12+16·3=84 кг/кмоль; M(NH3)=14 +1·3=17 кг/кмоль; M(CO2)=12 +16·2=44 кг/кмоль;
M(H2O)=16 +1·2=18 кг/кмоль, M(NH4Cl)=14 +1·4+35,5=53,5 кг/кмоль.
Масса NaCl, необходимая на взаимодействие: ![]()
![]()
Масса NH3, необходимая на взаимодействие: ![]()
![]()
Масса CO2, необходимая на взаимодействие: ![]()
![]()
Масса H2O, необходимая на взаимодействие: ![]()
Тогда масса образовавшегося хлорида аммония равна:
![]()
Второй способ
Рассчитаем число кмоль NaHCO3, которое соответствует 1000 кг.
![]()
Из уравнения реакции (1) число моль каждого из реагентов равно числу молей NaHCO3 и равно 11,905 кмоль.
Тогда массы реагентов и продуктов равны:
![]()
![]()
![]()
![]()
![]()
Задание №2: Рассчитаем материальный баланс по реакциям (1–2) на 1000 кг Na2CO3 при a1=a2=95 %.
![]() (2)
(2)
Найдем число молей Na2CO3, которое соответствует 1000 кг:
![]()
Из уравнения реакции (2) число моль каждого продуктов равно числу молей Na2CO3 и равно 9,434 кмоль при a2= 100%, но у нас 95 %
Тогда массы продуктов и продуктов по уравнению (2) равны:
![]()
![]()
![]()
Масса непрореагировавшего NaHCO3: ![]()
Результаты промежуточных расчетов по реакции (2) сведем в таблицу:
| Вещество | Приход, кг | Расход, кг |
| NaHCO3 | 1668,3 | 83,4 |
| Na2CO3 | – | 1000 |
| CO2 | – | 415,1 |
| H2O | – | 169,8 |
| Итого: | 1668,3 | 1668,3 |
Полученные данные используем для расчетов по реакции (1):
![]() (1)
(1)
Из предыдущих расчетов получена масса NaHCO3 равная 1668,3 кг и используем её для дальнейших расчетов.
Число кмоль NaHCO3 содержащееся в 1668,3 кг:
![]()
Из уравнения реакции (1) число моль каждого продуктов равно числу молей NaHCO3 и равно 19,861 кмоль при a1= 100%, но у нас 95 %.
Тогда массы реагентов и продуктов равны:
![]()
![]()
![]()
![]()
![]()
Масса непрореагировавших веществ:
![]()
![]()
![]()
![]()
Результаты расчетов по реакциям (1–2) сведем в общую таблицу.
| Вещество | Приход, кг | Расход (сумма по двум реакциям), кг |
| NaCl | 1223 | 61,15 |
| NH3 | 355,4 | 17,77 |
| CO2 | 919,9 | 46+415,1=461,1 |
| H2O | 376,3 | 169,8+18,8=188,6 |
| Na2CO3 | – | 1000 |
| NaHCO3 | – | 83,4 |
| NH4Cl | – | 1062,6 |
| Итого: | 2874,6 | 2874,6 |
Вывод: Для обеспечения работоспособности цикла, а это главный элемент безотходности технологии необходимо стремиться к степени превращения теоретической, т.е. 100 %. Для этого нужны новые конструкции аппаратов и новые технологические приемы.
СПИСОК ЛИТЕРАТУРЫ
1. Шокин И.Н., Крашенинников С.А., Технология соды: Учебное пособие для вузов. – М.: Химия, 1975. – 287 с.
2. Производство соды по малоотходной технологии: Монография/Ткач Г.А., Шапорев В.П., Титов В.М. – Х.: ХГПУ, 1998. – 429 с.
3. Зайцев И.Д., ткач Г.А., Стоев Н.Д. Производство соды. – М.: Химия, 1986. – 312 с.
4. ГОСТ 5100–85 Сода кальцинированная техническая. Технические условия. Дата введения 01.01.86.
5. Мельников Е.Я., Салтанова В.П., Наумова А.М., Блинова Ж.С. Технология неорганических веществ и минеральных удобрений: Учебник для техникумов. – М.: Химия, 1983. – 432 с.
6. Федотьев П.П. Сборник Исследовательских работ. – Л.: 1936.
7. Панасенко В.А. Физико-химические основы получения кальцинированной соды с использованием диэтиламина: Дис. … канд. техн. наук: 05.17.01 – Харьков, 1992. – 203 с.
8. Михайлова Є.О. Одержання хімічно осадженого карбонату кальцію з відходів алмазного виробництва: Автореф. дис. на здобуття наукового ступеня кандидата технічних наук . – Харків. – 2006. – 20 с.
9. ГОСТ 8253–79 Мел химически осажденный. Технические условия.
10. Бикбулатов И.Х., Насыров Р.Р., Даминев Р.Р., Бакиев А.Ю. Способ утилизации основного отхода производства кальцинированной соды // Нефтегазовае дело, 2007. – С. 1–9.
11. Вольнов И.И. Перекисные соединения щелочноземельных металлов. – М.: Наука, 1983.
12. Пат. RU2189949, Россия, 2002.
13. Пат. RU2031858, Россия, 1995.
14. Пат. RU2065216, Россия, 1996.
Похожие работы
... в воде и рассоле. При этом плотность раствора понижается, а объем его увеличивается. Растворимость аммиака увеличивается с понижением температуры и повышением давления. 2.Топливо. В производстве кальцинированной соды топливо применяют в известковых печах при получении извести и в содовых печах при кальцинации бикарбоната натрия. Основным видом топлива обжига известняка или мела следует ...
... материалов синтетической химии лежит технология переработки ТПО производства резины и резинотехнических изделий. Итак, к ТПО резины следует отнести собственно отходы производства резины и отходы резино-технических изделий в процессе производства. Предварительно остановимся на видах резины. В зависимости от содержания серы в резине ее называют мягкой (2-8% S); полутвердой (12-20% S); твердой или ...
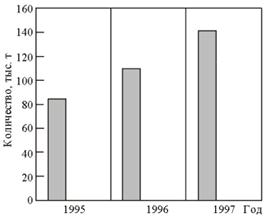
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...
... на предприятиях сырья, а также особенностями технологических процессов, высоким диапазоном использования в народном хозяйстве, АПК и в быту его готовой продукции и полуфабрикатов. Химический комплекс Украины играет исключительно важную роль в развитии производительных сил, обеспечении жизненных потребностей населения. На химических и электрохимических процессах основана выплавка чугуна и стали, ...
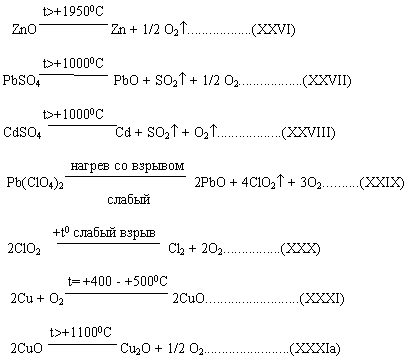
0 комментариев