Навигация
2. Силилирование сахаров.
2.1. Способ с использованием трифторуксусной кислоты. В подготовленную навеску образца приливают 1,0 см3 пиридина (нуклеофильный катализатор), 0,9 см3 гексаметилдисилазана, 0,1 см3 трифторуксусной кислоты (облегчающий алкилирование), плотно закрывают и энергично встряхивают в течение 30 секунд. Вначале наблюдают расслоение жидкости на 2 фазы, при этом нижний слой незначителен. По мере стояния раствора в течение 20...30 минут это расслоение исчезает и начинает выделяться аммиак, что указывает на успешное протекание реакции силилирования:
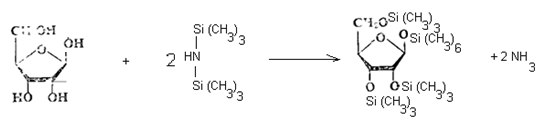
После прекращения выделения аммиака раствор выдерживают 12 часов при комнатной температуре или 1 час при 60 "С. Длительно сохраняющееся расслоение, исчезающее только при нагревании, говорит о том, что реакция силилирования прошла не полностью из-за высокого содержания влаги (более 40%) или повышенного содержания углеводов. В этом случае подготовку пробы повторяют, уменьшив при этом навеску или увеличив время высушивания на роторном испарителе.
![]()
![]() 2.2. Способ с использованием триметилхлорсилана. В подготовленную навеску образца приливают точно 1,0 см3 пиридина, 0,2 см3 гексаметилдисилазана и 0,1 см3 триметилхлорсилана, встряхивают в течение 1 минуты и нагревают в термостате 45 минут при 60 °С:
2.2. Способ с использованием триметилхлорсилана. В подготовленную навеску образца приливают точно 1,0 см3 пиридина, 0,2 см3 гексаметилдисилазана и 0,1 см3 триметилхлорсилана, встряхивают в течение 1 минуты и нагревают в термостате 45 минут при 60 °С:
Затем хроматографируют.
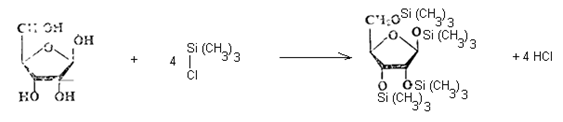
Для упрощения идентификации и количественных расчетов (если не требуется знания аномерного состава сахаров) определение сахаров производят в виде ТМС-производных сахаров. В подготовленную пробу образца добавляют 100 г гидроксиламина солянокислого, приливают 10 см3 пиридина и выдерживают в термостате при 80 °С в течение 2 часов:
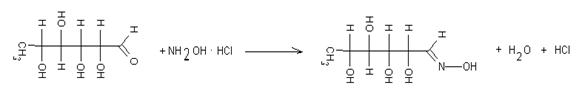
Охлаждают и далее приливают силилирующие агенты.
3. Газохроматографический анализ.
3.1.Подготовка хроматографической колонки. Стеклянную колонку, заполненную готовым сорбентом (количество неподвижной фазы 3...5% от массы носителя) длиной 2 м и внутренним диаметром З мм устанавливают в термостате хроматографа и проводят термокондиционирование при продувании потоком газа-носителя (гелий, азот, водород) 2 ч при 100°С, 2 ч при 150°С, 4 ч при 200°С и 8 ч при 250"С. Затем устанавливают рабочий режим: температуру колонки профаммируют от 125 до 270°С со скоростью 4 °С в 1 мин, температуру испарителя 250 °С, расход газа-носителя 40см3/мин, температура пламенно-ионизационного детектора 250 °С, продолжают кондиционировать в течение рабочего дня.
3.2.Газохроматографическое определение. 1 мкл пиридинового раствора триметилсилильных производных углеводов вводят в испаритель и элюируют из колонки газом-носителем. Идентификацию индивидуальных триметилсилильных производных проводят по времени удерживания триметилсилильных производных сахаров-метчиков и методом добавок.
3.3. Приготовление стандартных растворов сахаров.
3.3.1. Сахара, имеющие аномеры . Навеску ксилита и навеску определяемого сахара, взятую с точностью 0,0001 г, помещают в коническую колбу и заливают дистиллированной водой до полного растворения углеводов. Раствор выдерживают в течение суток. Аликвотную часть раствора отбирают пипеткой, помещают в круглодонную колбу и упаривают досуха, после чего проводят силилирование.
3.3.2. Сахара, не имеющие аномеров. Силилируются без предварительного растворения.
Массовую долю отдельных сахаров (в %) в навеске продукта определяют по формуле:
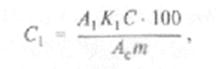
где С, — содержание отдельного сахара в навеске, %; К1 — поправочный коэффициент данного сахара; С — масса навески стандарта, мг; m — масса навески образца; Ас — площадь пика стандарта в относительных единицах; Лс— площадь пика данного сахара в относительных единицах.
Ввиду того, что альфа-лактоза и сахароза выходят на хроматограмме одним пиком, площадь пика альфа-лактозы определяют, исходя из соотношения площадей альфа- и бета-лактозы в модельном соединении лактозы. За основу берется площадь пика бета-лактозы. Площадь пика сахарозы определяют вычитанием от суммарного пика сахарозы пика альфа-лактозы, из пика бета-лактозы. За окончательный результат принимают среднеарифметическое результатов двух параллельных определений и округляют до трехзначной цифры.
Количественное определение сахаров по реакции с пикриновой кислотой (по Крезелиус – Зейферт)
При взаимодействии редуцирующих сахаров с пикриновой кислотой они окисляются до соответствующих кислот, а пикриновая кислота восстанавливается в пикраминовую, обладающую красной или буровато-красной окраской:
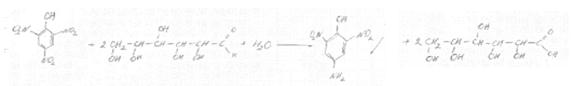
Метод пригоден для количественного определения глюкозы, галактозы, арабинозы, фруктозы, рамнозы, ксилозы, мальтозы, лактозы и крахмала. Метод быстр, но не очень точен. Ошибка может превышать 10-20%. В связи с этим указанный метод имеет ориентировочное значение;
Реактивы и приборы: а) пикриновая кислота, насыщенный раствор; б) углекислый натрий, 20%-ный раствор; в) спектрофотометр.
Ход работы: К 1 мл испытуемого раствора (в котором должно содержаться ее более 3 мг редуцирующих сахаров) прибавляют 2 мл насыщенного водного раствора пикриновой кислоты и 1 мл раствора углекислого натрия, после чего пробирку переносят на 30 мин. в кипящую водяную баню. Охлаждают до комнатной температуры и доводят дистиллированной водой до объема 10 мл. Оптическую плотность раствора определяют при 455 нм (синий светофильтр). Содержание редуцирующих сахаров рассчитывают по калибровочной кривой, составленной по стандартным растворам глюкозы как в работе «Количественное определение сахаров по антроновому методу».
Определение редуцирующего общего сахара по реакции с 3,5-дииитросалицнловой кислотой
При взаимодействии сахаров с 3,5-динитросалициловой кислотой она восстанавливается в З-амино-5-нитросалицнловую:
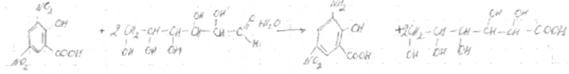
В остальном реакция протекает так же, как и с пикриновой кислотой.
Реактивы и приборы: а) динитросалициловый реактив:
В мерной колбе на 1 л растворяют в дистиллированной воде 10 г 3,5-динитросалициловой кислоты, 300 г сегнетовой соли, 16 г едкого натра и доводят водой до метки. Раствор выдерживают два дня в темном месте, затем фильтруют в склянку оранжевого стекла и хранят в темноте;
б) спектроколориметр «Спекол» (ГДР).
Ход работы: К 1 мл испытуемого раствора (где не более 2 мг редуцирующих сахаров) прибавляют 2 мл динитросалицилового реактива, нагревают 5 мин. в кипящей водяной бане, охлаждают до комнатной температуры, после чего доводят до объема 25 мл. Оптическую плотность раствора определяют при 530 нм (зеленый светофильтр).
Антроновый метод определения сахаров (по Моррису-Роэ)
Антроновый реактив образует зеленое окрашивание со всеми растворимыми углеводами, которые в одинаковой концентрации дают окрашенные растворы практически одной и той же оптической плотности.
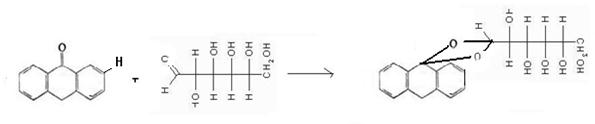
Это позволяет при определении углеводов использовать калибровочную кривую, составленную по глюкозе, для определения других сахаров в небольших концентрациях (до 0,2 мг в пробе). Точные результаты могут быть получены при наличии высокоочищенных химических реактивов и соблюдении постоянной температуры.
Реактивы и материалы: а) Антроновый реактив
200 мг антрона растворяют в 100 см3 концентрированной серной кислоты (плотность 1,84).
б) 0,5%-ный раствор H2SO4
2,8 см3 серной кислоты, плотностью 1,84 растворяют в 1 дм3 дистиллированной воды.
в) 30 %-ный раствор сернокислого цинка г)15 %-ный раствор желтой кровяной соли 3-водной.
Ход работы. 1 г измельченного материала (корнеплодов, плодов и др.) помещают в 2 мерные колбы на 100 см3. Проводят извлечение сахаров в течение часа с 80 см3 воды при периодическом перемешивании. После этого экстракт осветляют, прибавляя по 1 см3 растворов сернокислого цинка и желтой кровяной соли. Берут 2 пробирки и приливают по 3 см3 антронового реактива, а затем отбирают 1 см3 опытной вытяжки. В качестве контроля используют пробирки, в которых вместо вытяжки добавляют 1 см3 воды. Все пробирки быстро взбалтывают и помещают в кипящую водяную баню на 7 минут. После кипячения пробирки с растворами охлаждают до комнатной температуры, определяют оптическую плот![]()
![]()
![]()
![]() ность при 610 нм против контрольной пробы. По калибровочной кривой рассчитывают содержание сахаров. Расчет производят по формуле:
ность при 610 нм против контрольной пробы. По калибровочной кривой рассчитывают содержание сахаров. Расчет производят по формуле:
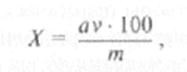
где а — количество сахаров, найденное по калибровочной кривой; v — объем экстракта (см3); т — масса навески, взятой на определение.
Определение содержания общего сахара в продуктах кондитерского производства
Считается экспресс-методом, основанным на окислении сахаров дихроматом калия в сильнокислой среде по общей схеме:
![]()
Соединения хрома (Ш) окрашены в сине-зеленый цвет, их количество пропорционально содержанию общего сахара в анализируемом продукте.
Реактивы и материалы:
а) Раствор сахарозы — 0,004 г/см3 (стандартный раствор сахарозы).
1,0000 г сахарозы взвешивают с точностью до 0,0002 г и растворяют в мерной колбе вместимостью 250 см3. Объем раствора доводят до метки дистиллированной водой.
б) 1 %-ный раствор дихромата калия (основной реактив).
49 г дихромата калия растворяют при нагревании в 300см3 воды, отдельно в 300 см воды медленно при перемешивании вводят 300 см3 концентрированной H2SO4 и охлаждают. В мерную колбу вместимостью 1000 см3 сначала помещают раствор дихромата калия, затем — серную кислоту, объем раствора доводят водой до метки, осторожно перемешивают.
в) Серная кислота — плотность 1,84 г/см3. г) 0,5 М раствор сульфата цинка. д) 1 М раствор гидроксида натрия.
Ход работы.
Похожие работы
... присутствует сахар различных производителей и различных марок (сахар-песок, сахарная пудра, сахар-рафинад), а также различной фасовки. Предметом исследования послужили характеристики сахара-песка (фасовкой по 800 грамм) трех производителей: -"Русский сахар" Никифоровского завода, -"Услад" Добринского завода, -"Кристалл-Бел" Чернянского завода. Нами были отобранные пробы в соответствии с ...
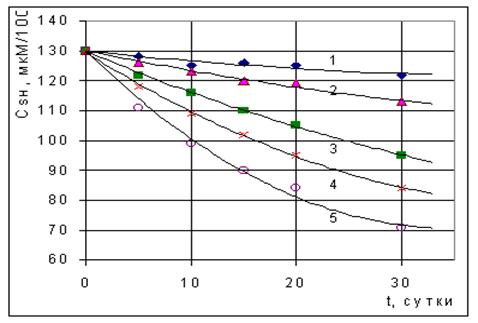
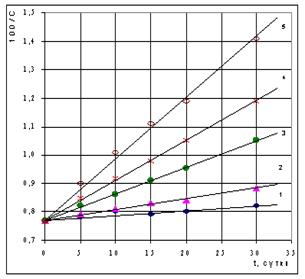
... воде, а зная концентрацию SH-групп в тканях рыб и их возраст можно оценить "интегральное биологическое воздействие" нефтяного загрязнения природных вод на гидробионты. Кинетический метод определения йода в пищевых продуктах и продовольственном сырье Среди каталитических методов получил применение рода-нидно-нитритный метод. Он основан на реакции окисления роданид-иона смесью нитрат- и нитрит- ...
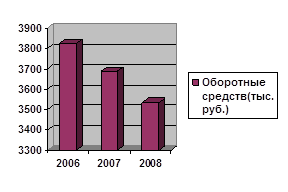
... приносит прибыль. Это все переменные составляющие предприятия от сырья и до денежных средств, которыми располагает предприятие. Из этого напрямую следует, что от эффективности использования оборотных средств зависит размер прибыли и само существование предприятия, потому что в реалиях современного рыночного механизма, когда оно перестанет оборачиваться – оно перестанет существовать. 1.2 ...
... биохимических, бактериологических показателей мясо используют на пищевые цели после санитарной обработки (зачистки измененных мест и обезвреживание проваркой) или направляют на техническую утилизацию. 3. МЕТОДЫ ОПРЕДЕЛЕНИЯ СВЕЖЕСТИ МЯСА 3.1 Органолептический метод Большое значение при оценке степени свежести мяса придается органолептическому методу. Однако этот метод субъективен и бывает, ...


0 комментариев