Навигация
Химический элемент № 30
4.Электронное строение атома.
4.2. Дайте объяснение физического смысла всех индексов у данного химического элемента в системе Д.И. Менделеева (порядковый номер, номер периода, номер группы, принадлежность к группе «А» или «Б»). Определите возможность «Эффекта провала электрона».
Решение.
Порядковый номер химического элемента в периодический системе – 30. молярная масса элемента равна 65.39 г/моль.
![]() . Это значит, что в нейтральном атоме цинка содержится 30 электронов, заряд ядра атома цинка также равен 30. Цинк расположен в четвертом периоде системы. Это значит, что в атоме цинка есть четыре электронных слоя, на которых расположены электроны. Цинк расположен во второй группе периодической системы. В атоме цинка полностью заполняется 3d-подуровень на котором теперь находится 10 электронов. Цинк принадлежит к побочной подгруппе, или группе «Б».
. Это значит, что в нейтральном атоме цинка содержится 30 электронов, заряд ядра атома цинка также равен 30. Цинк расположен в четвертом периоде системы. Это значит, что в атоме цинка есть четыре электронных слоя, на которых расположены электроны. Цинк расположен во второй группе периодической системы. В атоме цинка полностью заполняется 3d-подуровень на котором теперь находится 10 электронов. Цинк принадлежит к побочной подгруппе, или группе «Б».
Провал или проскок электрона для цинка невозможен, поскольку у него полностью заполнен 3d-подуровень. Провал электрона характерен для меди, серебра, у них количество d-электронов также равно 10, но s-электрон только один. Это можно объяснить повышенной энергетической стойкостью электронных структур, отвечающих полностью заполненным энергетическим подуровням. Переход электрона в атоме меди с 4s на 3d-подуровень приводит к образованию полностью заполненного 3d-подуровня и это энергетически выгодно. У цинка 3d – под уровень заполнен и электрону некуда переходить.
4.3. Выделите валентные подуровни в электронной формуле атома химического элемента, определите принадлежность химического элемента к типу s-, p-, d-, f-элементов.
Решение.
Покажем расположение валентных электронов в атоме цинка. Как видно из электронной формулы цинк относится к d-элементам, поскольку у него заполняется 3d-подуровень.
![]()
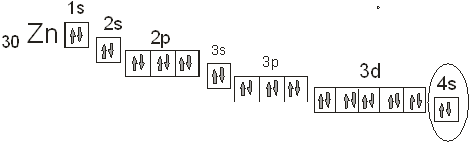
На приведенном рисунке эллипсом выделено расположение валентных электронов.
4.4. Напишите наборы квантовых чисел для всех валентных электронов.
Решение.
У атома цинка будет два валентных электрона. Запишем наборы квантовых чисел для этих электронов. Главное квантовое число равно 4 и химический элемент находится в 4 периоде периодической системы химических элементов. Поскольку в цинка валентные электроны расположены только на s-подуровне то его орбитальное квантовое число имеет значение равное 0. Поскольку этих электронов будет 2 то они имеют противоположные спины ms = ±1/2. Поскольку ml = 0 то у элемента не будет других подуровней кроме s-подуровня.
Наборы квантовых чисел будут иметь вид:
n = 5; l = 0; ml = 0; ms = +1/2.
n = 5; l = 0; ml = 0; ms = -1/2.
4.5. Определите принадлежность химического элемента к металлам или неметаллам, спрогнозируйте величины степени окисления.
Решение.
Поскольку цинк расположен во второй группе периодической системы, то он относится к металлам. В химических реакциях он будет проявлять металлические свойства. для металлов более приемлема отдача электронов. Поэтому цинк может отдавать два электрона с ![]() - подуровня. Поэтому цинк будет проявлять степень окисления +2. В связи с экранированием 3d – подуровня и его заполненостью, электроны с него не будут брать участие в химических процессах и поэтому цинк будет проявлять только степень окисления равную +2.
- подуровня. Поэтому цинк будет проявлять степень окисления +2. В связи с экранированием 3d – подуровня и его заполненостью, электроны с него не будут брать участие в химических процессах и поэтому цинк будет проявлять только степень окисления равную +2.
4.6. Распределите валентные электроны атома химического элемента по энергетическим ячейкам в соответствии с принципом наименьшей энергии и правилом Гунда.
Решение.
В соответствии с принципом наименьшей энергии два валентных электрона атома цинка расположатся на 4s-подуровне, поскольку он располагает меньшей энергией чем любой другой подуровень. Правило Хунда гласит, что устойчивому состоянию атома отвечает такое расположение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. Поэтому мы моглы бы считать. Что в одной ячейке будут электроны с одинаково направлеными спинами. Но это противоречит принципу Паули. И поэтому расположение электронов для цинка будет таково как на приведенном нами рисунке:
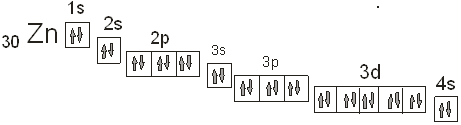
4.7. Прогнозируйте тип гибридизация валентных атомных орбиталей при образовании бинарных соединений (фторидов, хлоридов и др.).
Решение.
Рассмотрим получение ![]() :
:
![]()
Каждый атом фтора, входящий в состав данной молекулы, обладает одним неспаренным электроном, который и берет участие в создании ковалентной связи. Атом цинка в не возбужденном состоянии неспаренных электронов не имеет вообще:
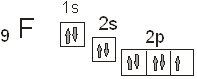
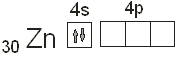
Поэтому для участия в химическом соединении атом цинка должен перейти в возбужденное состояние: ![]() .
.
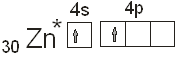
Образовавшийся возбужденный атом цинка владеет двумя не спаренными электронами, электронное облако одного электрона соответствует состоянию 4s, а другого состоянию 4p. При затрате некоторой энергии вместо исходных орбита лей могут образовываться две равноценные гибридные орбитали (sp – орбитали). У атома цинка в бинарных соединениях будет наблюдаться sp –гибридизация. Гибридные sp –орбитали будут вытянуты в противоположных направлениях, как это показано на рисунке.
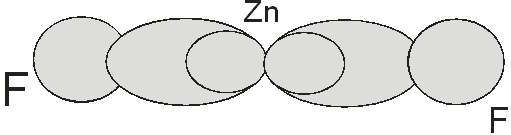
Рис. 1. Строение молекулы ZnF2.
5. Соединение данного химического элемента с неметаллами.
5.2. С галогенами.
Решение.
Газообразные фтор, бром, хлор, иод не реагируют с цинком на холоду. Но в присутствии паров воды реакция может проходить с воспламенение металла и выделением большого количества теплоты (для фтора 172 ккал, для хлора 95,6 ккал на моль цинка)
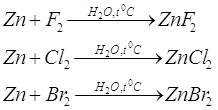
В реакции с галогенами получаем галоген производные цинка: фториды, хлориды, броматы.
5.4. С азотом.
Решение.
С азотом, даже в парах цинк не реагирует, но довольно легко реагирует при температуре красного каления с аммиаком с выделением нитрида цинка ![]() .
.
![]()
5.5. С углеродом.
Решение.
Цинк непосредственно не реагирует с углеродом и карбид цинка мы можем получить только через промежуточные реакции. Карбид цинка мы можем получить при нагревании цинка в токе ацетилена при температурах около 200 – 300 С.
![]()
Карбид цинка ![]() довольно нестойкое соединение, которое легко разлагается водой и кислотами.
довольно нестойкое соединение, которое легко разлагается водой и кислотами.
6. Оксиды и гидроксиды данного химического элемента.
6.1. Запишите ряд оксидов данного химического элемента (прогноз по электронной формуле и ковалентности).
Решение.
Для цинка характерна степень окисления +2. поэтому цинк имеет только один оксид: ZnO. Другие оксиды цинка неизвестны. Возможно существование пер оксида цинка ZnO2. ковалентность цинка в пер оксиде равна двум, строение его молекулы приведено на рисунке.

Ковалентность цинка в оксиде ZnO равна двум.
Запишем электронную формулу для ZnO:

Похожие работы
... а и b очень близки. В отражённом свете хлорофилл, кажется вишнёво-красным, так как он излучает поглощённый свет с изменением длины его волны. Это свойство хлорофилла называется флюоресценцией. Биосинтез хлорофилла Исходными для синтеза хлорофилла субстратами являются очень простые органические соединения – ацетат и глицин. Процесс синтеза хлорофилла принято подразделять на три этапа. ...
... ртутью он дает амальгаму, которая при небольшом содержании свинца жидкая. 2.Химические свойства По химическим свойствам свинец – малоактивный металл: в электрохимическом ряду напряжений он стоит непосредственно перед водородом. Поэтому свинец легко вытесняется другими металлами из растворов его солей. Если опустить в подкисленный раствор ацетата свинца цинковую палочку, свинец выделяется на ...
... 500 °C), достигая чистоты 98,7 %. Применяющаяся иногда более сложная и дорогая очистка ректификацией дает металл чистотой 99,995 % и позволяет извлекать кадмий. Основной способ получения цинка — электролитический (гидрометаллургический). Обожженные концентраты обрабатывают серной кислотой; получаемый сульфатный раствор очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу в ...
... из цинка. Значительна роль этого элемента в полиграфии. Из цинка делают клише, позволяющие воспроизвести в печати рисунки и фотографии. Специально приготовленный и обработанный типографский цинк воспринимает фотоизображение. Это изображение в нужных местах защищают краской, и будущее клише протравливают кислотой. Изображение приобретает рельефность, опытные граверы подчищают его, делают ...


0 комментариев