Навигация
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Химическая кинетика - это наука о скоростях и механизмах химических превращений, о явлениях, сопровождающих эти превращения, и о факторах, влияющих на них.
Механизм реакции - это последовательность стадий, предлагаемая на основании экспериментально установленных данных о скорости реакции и на экспериментально обнаруженных интер-медиатах реакции (промежуточных продуктах).
Кинетика по способу описания химических реакции делится на два раздела. В формальной или феноменологической кинетике сформулированы закономерности, позволяющие описывать химическую реакцию макроскопически на основе экспериментальных данных. Молекулярная кинетика изучает превращение на основе молекулярных данных о свойствах частиц.
Теоретическую основу химической кинетики составляют теории столкновений и переходного состояния.
Теория столкновений позволяет объяснить влияние концентрации и температуры на скорости реакций.
Теория переходного состояния рассматривает изменение в геометрическом расположении атомов реагирующих молекул как единой системы.
Переходным состоянием или активированным комплексом называется критическая конфигурация, которой соответствует максимум потенциальной энергии вдоль координаты реакции.
Реагирующие молекулы, которые достигают этой критической конфигурации, образуют молекулы продуктов.
Кинетические исследования позволяют определить порядок и константу скорости реакции, число и характер промежуточных продуктов, энергию активации реакции, выяснить влияние природы растворителя, установить характер и число связей, разрываемых в ходе реакции и т.п.
Рассмотрим основные понятия химической кинетики.
1.1 Скорость, константа скорости, порядок и молекулярность химической реакции
С течением времени в процессе химической реакции происходит изменение количеств исходных веществ и продуктов реакции. Эти изменения могут быть различными из-за разных стехиометрических коэффициентов у веществ, принимающих участие в химической реакции. Поэтому, при рассмотрении скорости реакции введены два понятия: скорость реакции по данному веществу и скорость реакции в целом (просто скорость реакции).
Скоростью реакции называется изменение количества i-того вещества (в молях) в единицу времени в единице реакционного пространства R:
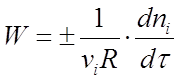 (1)
(1)
где ni - число молей i-го вещества, израсходованное или полученное в ходе реакции.
Это определение скорости является наиболее общим. Оно справедливо для любых условий, в том числе и для неизотермических.
Если реакция гетерогенная и протекает на границе раздела фаз, то реакционным пространством является поверхность (R = S), и изменение количества вещества относится к единице поверхности. Если реакция гомогенная и протекает в объеме, то реакционным пространством является объем (R = V). Изменение количества вещества рассматривается в единице объема. При условии V = const выражение (1) принимает вид 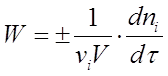 (2)
(2)
Если учесть, что ni /V = Сi, тогда вместо (2) получим
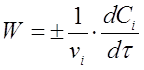 (3)
(3)
где vi - стехиометрический коэффициент перед i-тым веществом в уравнении химической реакции;
Сi - концентрация i-того вещества, моль/л;
τ - время реакции, с.
В данном случае скорость химической реакции численно равна изменению концентрации одного из реагирующих веществ в единицу времени.
Из уравнения (3) следует, что скорость реакции всегда положительна. Производная d Сi /d τ характеризует скорость реакции по данному веществу. Она имеет отрицательное значение для исходных веществ веществ, так как их концентрация в ходе реакции уменьшается, и положительное для продуктов реакции. Их количество в течение времени возрастает.
Основным законом химической кинетики является закон действующих масс, выражающий зависимость скорости химической реакции от концентрации реагирующих (исходных) веществ, который записывают в виде
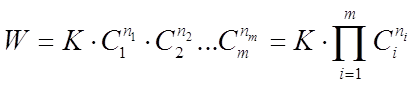 (3)
(3)
где К - коэффициент пропорциональности или константа скорости химической реакции, численно равная скорости данной реакции при равенстве единице концентраций всех исходных веществ;
n1, n2, .... nm - показатели степени - порядки реакции по индивидуальным веществам;
C1 , С2,....Сm - концентрации веществ, принимающих участие в данной реакции;
П - произведение.
Константа скорости химической реакции зависит от природы реагирующих веществ, температуры и факторов, влияющих на протекание реакции.
Сумму
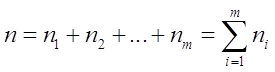
называют порядком химической реакции, т.е. порядок химической реакции равен сумме показателей степени концентраций реагентов в кинетическом уравнении реакции и является экспериментальной величиной.
Порядок по данному веществу (частный порядок) определяется как показатель степени концентрации этого вещества в уравнении для скорости реакции.
Мoлекулярность химической реакции равна числу исходных молекул (или других частиц), принимающих участие в элементарном акте этой реакции. При этом число молекул продуктов реакции не имеет значения. В зависимости от числа исходных молекул различают мономолекулярные, бимолекулярные и тримолекулярные реакции. Молекулярность реакции - понятие теоретическое.
Порядок и молекулярностъ реакции совпадают только для простых реакций, протекающих в полном соответствии с их стехиометрическим равнением и законом действующих масс.
Порядок и молекулярностъ реакции не совпадают, если:
- один из компонентов находится в большом избытке;
- реакция имеет сложный механизм;
- на ее протекание оказывают воздействие катализаторы или ингибиторы.
Похожие работы
... основные закономерностей активации LiAl, LixC6 и С8С3 электродов путем механических, физико-химических и электрохимических воздействий, а также изучние обратимой работа модифицированных электродов, работающих по "принципу электрохимического внедрения, в макетах литиевых аккумуляторов. Задачи исследования. Для достижения поставленной цели потребовалось: -провести комплексное систематическое ...
... можно судить с тех же позиций, которые применяются в координационной химии для связи металл-лиганд, для характеристики изменений свойств лиганда (т.е. его активации). Основные понятия координационной химии В основе современных представлении о природе комплексов лежит координационная теория Вернера (1893 г.). Основные положения теории А. Вернер вывел, рассматривая соединения, которые либо ...
... или кислот; так получают, например, золь гидроксида железа(III), имеющий следующее строение: {[Fe(OH)3]m n FeO+ · (n–x)Cl–}x+ x Cl– 4.2.2 Агрегативная устойчивость лиофобных коллоидов. Строение коллоидной мицеллы Лиофобные коллоиды обладают очень высокой поверхностной энергией и являются поэтому термодинамически неустойчивыми; это делает возможным самопроизвольный процесс уменьшения ...
... : ,(2.8) где фотопроводимость; — константа для данного образца; — термическая энергия активации проводимости (обычно 0,1—0,3 эв). Знак световых носителей тока у большинства органических полупроводников дырочный. Некоторые адсорбированные пары и газы существенно изменяют фотоэлектрическую чувствительность органических полупроводников. Зависимость фототока от освещенности выражается ...

0 комментариев