Навигация
Аппаратурно-технологическая схема
4.1.2.9. Аппаратурно-технологическая схема.
Схема 2. Аппаратурно-технологическая схема переработки сплава карбидов окислительным обжигом в печи кипящего слоя.
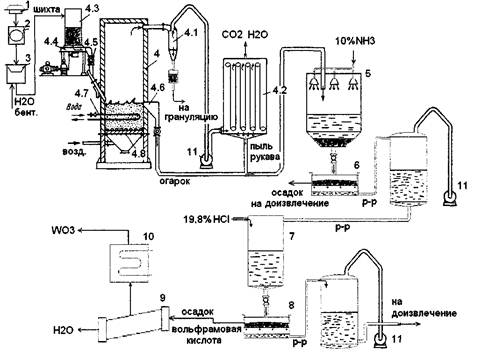
Щековая дробилка
Печь кипящего слоя
Чашевой гранулятор
Дисковая мельница 4.1-Циклон
Рукавный фильтр
Бункер
Тарельчатый питатель
Шлюзовый питатель
Порог выгрузки
Система водяного охлаждения
Подина
Реактор выщелачивания (с распыляющимся с верху реагентом)
ПУТЧ фильтр
Шахтная емкость осаждения (колонна осаждения)
НУТЧ фильтр.
Сушильные аппараты с вращающимися барабанами.
10-Индукционная печь 11-Насос
4.2. Состав исходного сырья
Таблица 2. Состав исходного сырья.
| WC | TiC | Со | Zn | Си | Fe | всего | |
| кг/ч | 130,000 | 25,000 | 10,000 | 0,500 | 1,000 | 0,167 | 166,667 |
| % | 78,000 | 15,000 | 6,000 | 0,300 | 0,600 | 0,100 | 100 |
Молекулярная масса: 195,86
Получаются прокаливанием смеси W и С при 1400-1500°С.
Физические и химические свойства, tnn WC свыше 3000°С; плотность WC 15,6 г/см3.
Нерастворимы без разложения ни в одном из известных растворителей.
Применение: в производстве твердых сплавов.
Внешний вид: серые кристаллы
4.3.2. WO3 - Оксид вольфрама (VI) [12].Парамагнитные желтые (оранжевые при нагревании) ромбические мелкие кристаллы (плотность равна 7,16-7,22 г/смЗ), которые плавятся при 1473°С, превращаясь в зеленую жидкость, кипящую при 1750°С. Они сублимируются, начиная от 1357°С. Мало растворимы в воде и кислотах. Растворяется в расплавах и растворах щелочей с образованием вольфраматов или поливольфраматов. Получают нагреванием металлического вольфрама при 900°С на воздухе или в токе кислорода, а также прокаливанием вольфрамовой кислоты H2WO4. Применяют в химической, стекольной и керамической промышленности для получения металлического вольфрама и его сплавов.
4.3.3.TiC - Карбид титана [12]tun свыше 3000 °С. Карбид титана, обладающий высокой твердостью и тугоплавкостью, является компонентом жаропрочных и твердых инструментальных сплавов, абразивный материал, его используют для нанесения износостойких покрытий, для изготовления различных керамических изделий, в т. ч. тиглей и чехлов термопар, стойких к расплавленным металлам, для футеровки вакуумных высокотемпературных печей.
4.3.4. ТЮ2 - Оксид титана (IV) [12]Встречается в природе в виде минерала рутила, анатаза (тетрагональные кристаллы) и брукита (ромбические кристаллы). Белый порошок. tra=1870°C, tKtni=30000C, плотность равна 3,6-3,95 г/см3 (анатаз), плотность равна 4,1-4,2 г/см3 [2] (брукит), плотность равна 4,2-4,3 г/см3 [2] (рутил). Разлагается выше 2927°С. Мало растворим в воде, разбавленных кислотах или растворах щелочей. Растворяется в концентрированной серной кислоте при нагревании, в расплавах гидроксидов или карбонатов щелочных металлов. Получают сжиганием металлического титана в избытке кислорода. Применяют в качестве пигмента для пластических масс, масляных красок, при производстве молочного стекла, тугоплавких стекол, фарфора, огнеупорного кирпича, в производстве эмалей, глазурей. В реакциях органической химии служит в качестве катализатора.
4.3.5.Со-Кобальт [12]Электронная формула KL3s23p63d74s2, еион (Ме<=>Ме++е) =7,86 эВ.
Степень окисления: (+1), +2, (+3, +4); валентность: (1), 2, (3,4)
Физические свойства: серебристо-серый с розоватым оттенком металл, tra=1494°C,
1кип=2960°С, плотность кобальта 8,90 г/см3
Распространенность в природе: содержание в земной коре 410"3%(масс)
Основной минерал: кобальтин CoAsS (кобальтовый блеск).
Получение: из руд пиро - и гидрометаллургическими методами. В частности на конечной стадии смесь оксидов кобальта восстанавливается углеродом в электропечах.
Химические свойства: малоактивный металл. Устойчив к действию сухого и влажного воздуха. Растворяется в разбавленных кислотах. При нагревании реагирует с кислородом, галогенами, азотом, серой и другими неметаллами.
4.3.6.СоО - Оксид кобальта (П) [12]Серовато-зеленый кристаллический порошок с решеткой типа NaCl.1ПЛ=1935°С, плотность равна 6,45 г/см. Устойчив до 2860°С. Мало растворим в воде и других растворителях. Проявляет основные свойства. Восстанавливается до металлического кобальта водородом, углеродом, серой, алюминием. Получают действием кислорода или паров воды на металлический кобальт при температуре выше 940°С, разложением СозСч или СоаОз, прокаливанием гидроксида, сульфата, нитрата кобальта (П). Применяют для изготовления отрицательных электродов аккумуляторов, для получения окрашенных стекол, фарфора и эмалей, в качестве катализатора.
4.3.7.Со2О3 - Оксид кобальта (Ш) [12]Черные гексагональные мелкие кристаллы. Плотность равна 5,34 г/см3. Устойчив в виде моногидрата. Превращается в СозСч при 265°С, в СоО при 940°С с выделением кислорода. Окисляет хлороводородную кислоту с выделением хлора. Восстанавливается водородом или метаном. Получают дегидратацией Со20з nt^O или прокаливанием нитрата кобальта (П) при 180°С. Применяют как пигмент для эмалей и глазурей.
4.3.8. Zn - Цинк [12]Электронная формула KLM4s2, Еион(Ме=>Ме++е) =9,39 эВ
Степень окисления: +2; валентность: 2
Физические свойства: серебристо-белый с голубоватым оттенком мягкий металл,
U =1809°C, tjonr^OOCfC, плотность равна 7,13 г/см3
Распространенность в природе: содержание в земной коре 8,010"3%(масс)
Основные минералы: сфалерит (цинковая обманка) ZnS
Получение: из руды пирометаллургическим и гидрометаллургическим способом
Химические свойства: малоактивный металл, проявляет амфотерные свойства. Реагирует с неметаллами, водой, кислотами, щелочами.
4.3.9.ZnO - Оксид цинка [12]Встречается в природе в виде минерала цинкита. Диамагнитные кристаллы со структурой вюртцита белого цвета. tnn=1969°C, плотность равна 5,70 г/см3. Мало растворим в воде. Растворяется в кислотах и щелочах. Обладает люминесцентными и фотохимическими свойствами. При нагревании восстанавливается углеродом, монооксидом углерода, водородом. В лаборатории может быть получен сжиганием металлического цинка или прокаливанием гидроксида, карбоната или нитрата цинка. Применяют для приготовления масляных красок, для получения некоторых препаратов, используемых в медицине и косметике, в резиновой и керамической промышленности, а также в качестве катализатора при синтезе метанола.
4.3.10. Си - Медь [12]Электронная формула KLM4S1, Еи0н(Ме<=>Ме++е) =7,72 эВ
Степень окисления: +1, +2, (+3); валентность: 1,2, (3)
Физические свойства: мягкий блестящий металл красноватого цвета, 1Ш =1085°С,
1кип=2540°С, плотность меди 8,94 г/см3
Распространенность в природе: содержание в земной коре 4,710"3%(масс)
Основные минералы: халькопирит CuFeSi, халькозин (медный блеск) CuiS, малахит Си2(ОН) 2СОз, встречается также в свободном состоянии (самородная медь).
Получение: из руд пирометаллургическим и гидрометаллургическим способом. В пирометаллургическом способе медь получается при нагревании смеси оксида и сульфида меди(1). В гидрометаллургическом - восстановлением железом (металлическим ломом) из раствора медного купороса.
4.3.11. Си2О - Оксид меди (I) [12]Встречается в природе в виде минерала куприта. Диамагнитные кубические кристаллы, цвет которых меняется от коричневого до карминово-красного. tnn=1238°C. Мало растворим в воде. Растворяется в аммиаке или галогеноводородах. При 1025°С превращается в СиО, выше 1050°С - термически диссоциирует на элементы. Можно получить обработкой солей меди (II) щелочами или карбонатами щелочных металлов в присутствии восстановителя. Применяют в керамической промышленности в качестве пигмента.
4.3.12. СиО - Оксид меди (П) [12]Встречается в природе и называется черной медью, мелаконитом или теноритом. Парамагнитный черный порошок (или черные кубические кристаллы). tnn=1335°C, 1пл=1026°С, плотность равна 6,45 г/см3. Мало растворим в воде. Растворяется в концентрированных кислотах, при нагревании или в иодиде аммония. Растворяется в стекле, эмалях, придавая им зеленовато-синюю окраску. Восстанавливается до меди водородом, монооксидом углерода, металлами. Получают нагреванием меди выше 80°С, водной суспензии гидроксида меди (П), прокаливанием нитрата или основного карбоната меди. Применяется в производстве стекла и эмалей в качестве пигмента, в микроанализе для определения углерода, водорода и азота в органических соединениях.
4.3.13. Fe-Железо [12]Электронная формула KL3s23p63d64s2, ЕиОН(М<=>Ме++е) =7,90 эВ.
Степень окисления: +2, +3, (+4, +6, +8);
валентность: 2,3, (4,6, 8).
Физические свойства: серебристо-серый твердый металл, tim=1539°C, 1кип=3200°С, плотность железа 7,87 г/см3.
Распространенность в природе: четвертый (после О, Si, A1) по распространенности в земной коре элемент (4,65%(масс))
Основные минералы: магнетит РезО4, гематит Рб20з, лимонит Рв2Оз хН2О
Получение: восстановлением железной руды коксом или оксидом углерода (II).
Химические свойства: металл средней химической активности. Окисляется при обычной температуре во влажном воздухе. Растворяется в разбавленных кислотах. При нагревании реагирует с неметаллами.
4.3.14. ГеО - Оксид железа (II) [12]Диамагнитный черный неустойчивый кристаллический порошок. Решетка типа NaCl. tm=13680C. Превращается в при нагревании на воздухе. Мало растворим в воде и щелочах. Растворяется в кислотах. Разлагает при нагревании воду. Получают окислением металлического железа, восстановлением оксида железа (Ш) СО или водородом, прокаливанием смеси Рб2Оз и порошка железа.
4.3.15. Fe2O3 - Оксид железа (Ш) [12]Самое устойчивое природное кислородсодержащее соединение железа, которое встречается в виде минералов гематита или красного железняка. Существует три модификации: a-Fe2O3 (парамагнитна), у-Ре2Оз (ферромагнитна), 8-Ре2Оз (ферромагнитна). а-Ре2Оз представляет собой красный порошок. tra=1562°C [1], плотность равна 5,24 г/см3. Мало растворим в воде. Растворимость в кислотах зависит от температуры и продолжительности прокаливания оксида перед растворением. Получают прокаливанием гидроксида или нитрата железа (III), карбоната, сульфата железа (П) или пирита на воздухе. Применяется как пигмент для изготовления красок.
4.3.16. Бентонит [13]Бентониты представляют собой монтмориллонитовую породу общей формулы:
(Cao,5Na) oj(Al,Mg,Fe) 4(Si,Al) 802o(OH) 4nH2
и являются разновидностью белых или сукновальных глин. Характеризуются рядом ценных свойств, таких, как высокая набухаемость в воде, способность сохранять приданную форму, тонкая дисперсность, обладают моющей, эмульгирующей, клеящей, загущающей способностями, что обусловливается свойствами ведущего минерала этих глин - монтмориллонита; последний подразделяют на щелочной - с высоким содержанием Na2O и щелочноземельный - содержащий преимущественно CaO, MgO.
Известно о применении бентонитовых глин в качестве загустителей печатных красок при набивке шелковых тканей активными и кубовыми красителями.
Таблица 3. Типовой химический состав бентонита.
4.4. Термодинамические данные компонентов сырьяТаблица 4. Термодинамические данные компонентов сырья [5].
| Со203 | 159 | - | 19,3 | 8Д | -2,4 |
| Си | 0 | 1085 | 5,41 | 1,5 | _ |
| СиО | 39,5 | 1026 | 9,27 | 4,8 | - |
| Си20 | 40,76 | 1238 | 14,9 | 5,7 | - |
| Zn | 0 | 1809 | 5,43 | 2,4 | - |
| ZnO | 83,4 | 1969 | 11,71 | 1,22 | -2,18 |
| Fe | 0 | 1539 | 9,0 | - | - |
| FeO | 63 | 1368 | 12,38 | 1,62 | -0,38 |
| Fe203 | 197,51 | 1562 | 31 | 1,76 | - |
| C02 | 94,05 | . | 10,55 | 2,16 | -2,84 |
| H20 | 57,795 | - | 7,17 | 2,56 | -2,84 |
| 02 | 0 | - | 7,52 | 0,81 | -0,9 |
| N2 | 0 | . | 6,66 | 1,02 | _ |
4.4.1.1.Основные реакции протекающие при обжиге.
WC + 2,5О2 = WO3 + СО2
TiC + 2О2 = ТЮ2 + СО2 3) Со + 0,5О2=СоО 4) Zn + 0,5O2= ZnO 5) 2Cu+0,5O2 = Cu2O 6) Ре+1,5О2 = Ре2Оз
0,5Cu2O +%О2 = CuO
2СоО + 0,5О2 = Со2О3
Fe + 0,5О2 = FeO
4.4.1.2. Расчет термодинамических величин протекания реакций окисления [5]ДН7з=ЛН298+298Р173*ЛСр*с1Т
AHi173=AH298+ а*(1173-298) +1/2* Ь*10'3*(1173-298) 2 - с*105*1/Т
1) WC + 2,502 = W03 + СО2
ДН298=-20146-94,05+9,67= - 285840 кал/моль
АСр=(17,58+10,55-2,5*7,52-12,27) +(6,79+2,16-2,5*0,81-2,06) *10-3*Т+(0-2,04 + 0,9 *2,5+ 2,68) *105/Т2=-2,94+4,86*10"3*Т+2,89*107Т2
AHii73=-285840-2,94*875+4,86*10'3*1287125/2-2,89*105*(-0,0025) = - 284553,8= - 1190,5кДж/моль
2) TiC + 2О2 = TiO2 + СО2 ДН298=-225,8-94,05+43,9= - 245950 кал/моль
АСр=(17,97+10,55-2*7,52-13,296) +(0,28+2,16-2*0,81+1,944) *10-3*Т+(-4,35+2,04+4,212+0,912) *105/Т2=0,184+2,764*10-3*Т+2,35*105/Т2 АНц7з=-245950+0,184*875+2,764*10-3*1287125/2-2,35*105*(-0,0025) = - 243423,0= - 1018,5кДж/моль
3) Со + 0,5О2=СоО
АН298==-57100 кал/моль
АСр= (11,54-3,3-7,52/2) +(2,04-5,86-0,81/2) *10'3*Т+(0,4+0,9/2) *105/Т2= 4,48-4,22*
10-**Т+0,85*105/Т2
АНП7з= - 57100 +4,48*875-4,22*10'3*1287125/2-0,85*105*(-0,0025) =
-55683,3= - 232,9кДж/моль
4) Zn + 0,5O2 = ZnO
AH298=-83400 кал/моль
ДСр=(11,71-5,43-7,52/2) +(1,22-0,81/2-2,4) *10-3*Т+(-2Д8+0,9/2) *105/Т2= 2,52-1,58*
1(Г*Т-1,73*105/Т2
ЛНц7з= - 83400 +2,52*875-1,58*10-3*1287125/2+1,73 *105*(-0,0025) =
-82644= - 345,8кДж/моль
5) 2Cu+0,502 = Cu20
ДН298=-40760 кал/моль
АСр(14,9-2*5,41-7,52/2) +(5,7-2,15-0,81/2) *10-3*Т+(0+0,9/2) *105/Т2= 0,32+2,29*
1(И*Т+0,45*105/Т2
ДН„73= - 40760 +0,32*875+2,29*10-3*1287125/2-0,45*105*(-0,0025) =
-38893,7= - 162,7кДж/моль
6) Ре+1,5О2 = Ре2Оз
АН298=-197510 кал/моль
АСр=(31/2-9-1,5/2*7,52) +(1,76/2-1,5/2*0,81) *10'3*Т+(0+0,9*1,5/2) *105/Т2= 0,86+0,272*
10^*Т+0,675*105/Т2
АНц7з= - 197510 +0,86*875+0,272*10-3*1287125/2-0,675*105*(-0,0025) =-821,787кДж/моль
7) 0,5Си20 + У4О2 = СиО АН298=-18620 кал/моль
ACp(9,27-14,9/2-7,54/4) +(4,80-5,7/2-0,81/4) *10'3*T+(0+0,9/4) *105/T2=-0,06+1,75* 10-з*т+052о*ю5АГ2
АНц7з= - 18620 - 0,06*875+1,75*10-3*1287125/2-0, 20*105*(-0,0025) = - 17496,26= - 73,2кДж/моль
8) 2СоО + 0,5О2 = Со2О3 АН298=-22400 кал/моль
АСр (19,3/2-11,54-7,52/4) +(8,1/2-2,04-0,81/4) *10'3*Т+(-2,4/2-0,4+0,9/2) *105/Т2= - 3,77+1,807*
10'% -1,15*105Я2
АНц7з=-22400-3,77*875+1,807*10"3*1287125/2+1,15*105*(-0,0025) =
-24248,332= - 101,455кДж/моль
9) Fe + 0,5О2 = FeO ДНаэв^-бЗООО кал/моль
ACp=(12,38-4,18-7,52/2) +(l,62-5,92-0,81/2) *10'3*T+(-0,38+0,9/2) *105/T2= 4,44-4,7* 10'3*Т+0,07*105/Т2 AHii73=-63000+4,44*875-4,7*10'3*1287125/2-0,07*105*(-050025) =
-62122= - 259,9кДж/моль
5. Материальный балансСхему переработки можно разбить на 5 блоков:
Дробление и измельчение.
Грануляция и окисление в печи кипящего слоя.
Выщелачивание и фильтрация.
Осаждение и фильтрация.
Прокалка и сушка.
Схема 3. Блок схема процесса переработки карбида.
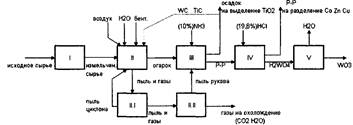
Производительность по поступающему сырью - 4т. в сутки, т.е.166,667 кг. в час. В блок 1 поступает исходное сырье, где дробится и измельчается.
5.1. Блок 2. Грануляция и окисление в печи кипящего слояВ блок 2 поступает измельченное сырье не более 1 мм., где смешивается с не прореагировавшими карбидами и гранулируется. Крупность гранул - до 2мм.; распределение по крупности,% (масс) [3].:
(2-Й,5 мм) - 15(1,0+0,5 мм) - 35(1,5-1,0 мм) - 350,5 мм. -15
Продуктами обжига являются огарок 65%, циклонная пыль20%, пыль рукавного фильтра 15%. В огарок переходит 65% карбида, в циклонную пыль20% карбида, в пыль рукавного фильтра 15% карбида.
Степень окисления карбида в циклонной пыли 90%, в пыли рукавного фильтра 99%, необходима степень окисления в огарке 98%. Металлы Со, Zn, Cu, Fe окисляются нацело. Пыль рукавного фильтра и огарок поступают на выщелачивание, а пыль циклона идет на грануляцию. Не прореагировавший карбид также возвращается на грануляцию, т. к. при дальнейшем разделении присутствует как балласт.
Для расчета материального баланса нам необходимо знать состав исходной шихты для обжига.Т. к. после первого блока сырье гранулируется и смешивается с возвратным карбидом и пылью циклона, его состав и количество изменяются.
Таблица 5. Обозначение потоков.
| Наименование потока | Обозначение | Значение кг/ч |
| Первичное сырье | ХО | 166,667 |
| Шихта для обжига | Х1 | 273,638 |
| Возвратный карбид ог. | Х21 | 2,082 |
| Возвратный карбид рук. | Х211 | 3, 202 |
| Пыль циклона карбид | Хк221 | 0,24 |
| Пыль циклона оксид | Хо221 | 30,992 |
| Связующая вода | ХН20 | 38,36 |
| Связующий бентонит | Хбент. | 13,152 |
Схема 4. Потоковая схема процесса окисления карбидов.
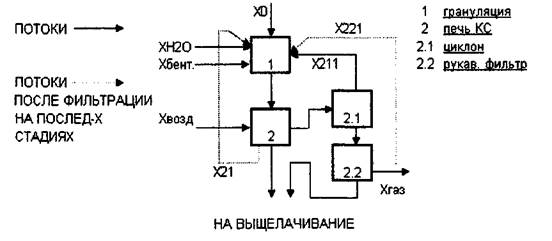
Xi=Xo+XK2i i+XO2l 1+X21+X221
Хо=166,67
Хк211=0,2*0,1 *(0,78+0,15) *Xi
X2i=0,65*0,02*(0,78+0,15) *X1
X22i=0,15*0,01*(0,78+0,15) *Xi
0,1 - доля не окислившегося карбида в циклоне
0,02 - доля не окислившегося карбида в огарке
0,01 - доля не окислившегося карбида в рукаве
Получим:
Хк211=0,019*Xi
X2i=0,012*X!
Х221=0,001*Х!
Решение:
X1-0,019*Xi-0,012*X1-0,001*X1=166,67
0,968*Х1=166,67
Ху=172Л8 (без оксидов и связующих компонентов)
5.1.2Расчет потоков:
Поток Хк2ц равен:
Хи„=3, 202
Найдем количества веществ в этом потоке:
Xk2ii(WC): 0,2*0,78*0,1*172,18=2,686
ХииСТЮ): 0,2*0,15*0,1*172,18=0,516
Поток X2i равен:
Х2] =2,082
Найдем количества веществ в этом потоке:
X2i(WC): 0,65*0,02*0,78*172,18=1,746 X2i(TiC): 0,65*0,02*0,15*172,18=0,336
Поток X22i равен:
X22i(WC): 0,15*0,01*0,78*172,18=0, 201
X22i(TiC): 0,15*0,01*0,15*172,18=0,039
5.1.3. Расчет циклонной пылиКоличество карбида окисляемого в циклоне в виде металлов (Со, Zn, Cu, Fe), (кг/ч): 3, 202*(0,06+0,006+0,003+0,001) /(0,78+0,15) = 0,241
Количество оксидов в циклоне без учета оксидов поступающих из шихты:
X'o22i = 0,2 *0,9*Xi=30,992
Количества оксидов, (кг/ч):
По реакции (1) WO3: 0,78*30,992*231,82/195,86=28,612
По реакции (2) ТЮ2: 0,15*30,992*79,88/59,84=6, 206
По реакции (3) СоО: (0,06*(30,992+0,241)) *74,93/58,93=2,383
По реакции (4) ZnO: (0,06*(30,992+0,241)) *81,39/65,39=0,233
По реакции (5) Си2О: (0,06*(30,992+0,241)) *143,1/2*63,55=0,105
По реакции (6) Fe2O3: (0,06*(30,992+0,241)) *231,55/2*55,85=0,065
Суммарное количество оксидов, (кг/ч): 37,604
Таблица 6. Количество оксидов в циклоне без учета оксидов поступающих из шихты.
| W03 | ТЮ2 | СоО | ZnO | Cu2O | Fe203 | всего | |
| кг/ч | 28,612 | 6, 206 | 2,383 | 0,233 | 0,105 | 0,065 | 37,604 |
| % | 76,088 | 16,504 | 6,337 | 0,620 | 0,279 | 0,173 | 100 |
Итоговое количество оксида в шихте:
Хо2ц=37,604+0,2*Хо2ц
0,8*Х211=37,604
Xo2i 1=47,005 кг/ч
Количество оксида приходящее из шихты в циклон:
0,2*Xo2i 1=9,401 кг/ч
Состав и количество приходящих в циклон оксидов их шихты, (кг/ч):
WO3: 9,401*0,761=7,154
ТЮ2: 9,401*0,165=1,551
СоО: 9,401*0,063=0,592
ZnO: 9,401*0,006=0,056
Cu20: 9,401*0,003=0,028
Fe2O3: 9,401*0,003=0,019
Итоговое суммарное состав и количество оксидов, (кг/ч):
WO3: 7,154 + 28,612=35,766
ТЮ2: 1,551+6, 206=7,757
СоО: 0,592+2,383=2,975
Си20: 0,028+0,105=0,133
ZnO: 0,056+0,233=0,289
Fe2O3: 0,019+0,065=0,084
5.1.4. Количество связующих веществ в исходной шихтеКоличество WC в шихте, (кг/ч): 166,67*0,76+1,746+2,686+0, 201=134,636 Количество ТЮ в шихте, (кг/ч): 166,67*0,15+0,516+0,336+0,039=25,531 Количество шихты без связующих веществ, (кг/ч): 166,67+47,005+0,24+2,082,3, 202=219, 199
Количество связующих веществ 219, 199*(14%+6%) /80%:
Н2О: 219, 199*0,14/0,8=38,360 кг/ч Хшо=3 8,360 кг/ч
Бентонита: 219, 199*0,06/0,8=16,440кг/ч Распределение бентонита, (кг/ч):
огарок: 16,440*0,65=10,686
пыль циклона: 16,440*0, 20=3,288
пыль рукавного фильтра: 16,440*0,15=2,466 Хбент. =16,440 - 3,288=13,152
Таблица 7. Состав шихты поступающей на обжиг.
| WC | ТЮ | Со | Zn | Си | Fe | W03 | ТЮ2 | СоО | ZnO | Си2О | Fe2O3 | Н2О | бенг | всего |
| кг/ч 134,636% 49, 202 | 25,531 9,330 | 10,000 3,654 | 1,000 0,365 | 0,500 0,183 | ОД 67 0,061 | 35,766 13,071 | 7,757 2,835 | 2,975 1,087 | 0,289 0,106 | 0,133 0,049 | 0,084 0,031 | 38,360 14,019 | 16,440 6,008 | 273,638 100,000 |
Распределение компонента, (кг/ч):
огарок: 134,636*0,65=87,513
пыль циклона: 134,636*0, 20=26,927
пыль рукавного фильтра: 134,636*0,15=20, 195
Основная реакция: WC + 2.5О? = WCb + ССЬ
М=195,86 М=16 М=231,82 М=44,01 (г/моль)
1) в огарке окислится: 26,927*0,9= 85,763 кг/ч Расходуется кислорода, (кг/ч):
02: 85,763*2,5*2*16/195,86=17,515
Образуется веществ, (кг/ч):
С02: 85,763*44,01/195,86=19,272
WO3: 85,763*231,82/195,86=101,509
Оксида WO3 в исходной шихте, (кг/ч): 47,005*0,65*0,761=23,251
Суммарное количество WOs, (кг/ч): 124,76
2) в циклоне окислится: 26,927*0,9=24,234 кг/ч Расходуется кислорода, (кг/ч):
О2: 24,334 * 2,5*2*1,6/195,86 = 4,949 Образуется веществ, (кг/ч): СО2: 24,334*44,01/195,86=5,445
WO3: 28,612
Оксида WO3 в исходной шихте, (кг/ч): 47,005*0,2*0,761=7,154
Суммарное количество WO3, (кг/ч): 35,76
3) в рукаве окислится: 20, 195*0,99=19,993 кг/ч
Расходуется кислорода, (кг/ч):
О2: 19,993*2,5*2*16/195,86=4,083
Образуется веществ, (кг/ч):
СО2: 19,993*44,01/195,86=4,492
W03: 19,993*231,82/195,86=23,664
Оксида WO3 в исходной шихте, (кг/ч): 47,005*0,15*0,761=5,366
Суммарное количество WO3, (кг/ч): 29,03
5.2.2. Окисление TiC:Распределение компонента, (кг/ч):
огарок: 25,531*0,65=16,595
пыль циклона: 25,531*0, 20=5,106
пыль рукавного фильтра: 25,531*0,15=3,830
Основная реакция: TiC + 2OZ = TIP? + СО?
M=59,84 M=16 М=79,88 М=44,01 (г/моль)
1) в огарке окислится: 16,595* 0,98=10,787 кг/ч Расходуется кислорода, (кг/ч):
02: 10,787*2*2* 16/59,84=5,768 кг/ч
Образуется веществ, (кг/ч):
ТЮ2: 10,787*79,88/59,84=14,399
СО2: 10,787*44,01/59,84=7,933
Оксида ТЮ2 в исходной шихте, (кг/ч): 47,005*0,65*0,165=5,042
Суммарное количество ТЮ2, (кг/ч): 12,975
2) в циклоне окислится: 5,106*0,9 =3,319 кг/ч Расходуется кислорода, (кг/ч):
О2: 3,319*2*2*16/59,84=1,331
Образуется веществ, (кг/ч):
СО2: 3,319*44,01/59,84=2,441
ТЮ2: 6, 206
Оксида ТЮ2 в исходной шихте, (кг/ч): 47,005*0, 20*0,165=1,551
Суммарное количество ТЮ2, (кг/ч): 12,975
3) в рукаве окислится: 3,830*0,99=2,498 кг/ч Расходуется кислорода, (кг/ч):
02: 2,489*2*2*16/59,84=1,331
Образуется веществ, (кг/ч):
ТЮ2: 2,489*79,88/59,84=3,322
С02: 2,489*44,01/59,84=1,831
Оксида ТЮ2 в исходной шихте, (кг/ч): 47,005*0,15*0,165=1,163
Суммарное количество ТЮ2, (кг/ч): 4,485
5.2.3. Окисление Со:Распределение компонента, (кг/ч):
огарок: 10*0,65=6,5
пыль циклона: 10*0,2=2,0
пыль рукавного фильтра: 10*0,15=1,5
Реакции: а) Со + 0.5От= СоО
М=58,93 М=16 М=74,93 (г/моль)
б) 2СоО + 0.5О7 = CozCb М=74,93 М=16 М=165,86 (г/моль)
Весь СоО оседает в циклоне, а Со2Оз образуется в огарке и пыли рукавного фильтра. СоО приходящий с исходной шихтой (оборотный) окисляется до Со2Оз нацело.
1) в огарке окислится: 6,5кг/ч По реакции (а):
Расходуется кислорода, (кг/ч):
О2: 6,5* 16/58,93=1,765 Образуется веществ, (кг/ч):
Считаем, что СоО из шихты образуется 100% -98%=2%: 6,5* 2%=0,13
Из этого СоО по реакции (б) не будет доокисляться: 0,13*74,94/58,93=0,165
СоО: 6,5*74,93/58,93=8,265
По реакции (б):
Расходуется кислорода, (кг/ч):
О2: 8,965*16/165,86=0,865 Образуется веществ, (кг/ч):
СогО3: (8,265-0,165) * 165; 86/2*7,493=8; 965
Оксида СоО в исходной шихте, (кг/ч): 47,005*0,65*0,063=1,934 Со203: 1,934*165,86/2*7,493=2,140 Суммарное количество Со2Оз, (кг/ч): 11,105
2) в огарке окислится: 2,0 кг/ч
В циклоне окисление идет до СоО.
Расходуется кислорода, (кг/ч):
О2: 2,0*16/58,93=0,543
Образуется веществ, (кг/ч):
СоО: 2,383
Оксида СоО в исходной шихте, (кг/ч): 47,005*0, 20*0,0,063=0,592
Суммарное количество СоО, (кг/ч): 2,975
3) в рукаве окислится: 1,5 кг/ч По реакции (а):
Расходуется кислорода, (кг/ч):
О2: 1,5*16/58,93=0,407 Образуется веществ, (кг/ч):
Считаем, что СоО из шихты образуется 100% -99%=1%: 1,5* 1%=0,015
Из этого СоО по реакции (б) не будет доокисляться: 0,015*74,94/58,93=0,019
СоО: 1,5*74,93/58,93=1,907
По реакции (б):
Расходуется кислорода, (кг/ч):
О2: (1,907 - 0,019) * 16/165,86=0,182
Образуется веществ, (кг/ч):
Со2О3: (1,907-0,019) * 165,86/2*74,93=2,091
Оксида СоО в исходной шихте, (кг/ч): 47,005*0,15*0,063=0,444
Со203: 0,444*165,86/2*74,93=0,492
Суммарное количество Со2Оз, (кг/ч): 2,583
5.2.4. Окисление Zn:Распределение компонента, (кг/ч):
огарок: 1,0*0,65=0,65
пыль циклона: 1,0*0, 20=0, 20
пыль рукавного фильтра: 1,0*0,15=0,15
Основная реакция: Zn + 0,50? = ZnO
М=65,39 М=16 М=81,39 (г/моль)
1) в огарке окислится: 0,65 кг/ч Расходуется кислорода, (кг/ч):
О2: 0,65*16/65,39=0,159 Образуется веществ, (кг/ч):
ZnO: 0,65*81,39/65,39=0,809
Оксида ZnO в исходной шихте, (кг/ч): 47,005*0,65*0,006=0,188 Суммарное количество ZnO, (кг/ч): 0,997
2) в циклоне окислится: 0,2 кг/ч Расходуется кислорода, (кг/ч):
02: 0,2*16/65,39=0,049 Образуется веществ, (кг/ч):
ZnO: 0,233
Оксида ZnO в исходной шихте, (кг/ч): 47,005*0, 20*0,006=0,056 Суммарное количество ZnO, (кг/ч): 0,289
3) в рукаве окислится: 0,15кг/ч Расходуется кислорода, (кг/ч):
02: 0,15*16/65,39=0,037 Образуется веществ, (кг/ч):
ZnO: 0,15*81,39/65,39=0,187
Оксида ZnO в исходной шихте, (кг/ч): 47,005*0,15*0,006=0,043 Суммарное количество ZnO, (кг/ч): 0,230
5.2.5. Окисление Си:Распределение компонента, (кг/ч):
огарок: 0,5*0,65=0,325
пыль циклона: 0,5 *0, 20=0,1
пыль рукавного фильтра: 0,5*0,15=0,075
Реакции: а) 2Си + 0.5О2 = СшО
М=63,552 М=16 М=143,1 (г/моль)
![]()
По реакции (а): Расходуется кислорода, (кг/ч): О2: 0,325*16/63,552*2=0,041 Образуется веществ, (кг/ч): Си2О: 0,325*143,1/63,55*2=0,366
Оксида Си2О в исходной шихте, (кг/ч): 47,005*0,65*0,003=0,086
Из исходной шихты Си2О окисляется до СиО нацело. Из окислившегося Си2О по реакциям не будет окисляться до СиО 100% -98%=2%: 0,366*2%=0,007кг/ч Отношение распределения образования оксидов: Cu20/CuO = 2/1 0,366*0,98=0,359 кг/ч следовательно образуется: Си2О=0,244 кг/ч и 0,122 кг/ч идет на доокисление до СиО Суммарное количество Си2О, (кг/ч): 0,007+0,244=0,251
По реакции (б):
Расходуется кислорода, (кг/ч):
О2: 0,232*1/4*32/79,56=0,023
Образуется веществ, (кг/ч):
СиО: (0,122+0,086) *79,55/143,1* 1/2=0,232
2) в циклоне окислится: 0,1 кг/ч
Будем считать, что реакция идет до образования Си2О.
Расходуется кислорода, (кг/ч):
02: 0,1*16/2*63,55=0,013
Образуется веществ, (кг/ч):
Си20: =0,105
Оксида Си2О в исходной шихте, (кг/ч): 47,005*0, 20*0,003=0,028
Суммарное количество Си2О, (кг/ч): 0,133
3) в рукаве окислится: 0,075кг/ч По реакции (а):
Расходуется кислорода, (кг/ч):
О2: 0,075*169/2*63,55=0,009 Образуется веществ, (кг/ч):
Си2О: 0,075*143,1/63,55*2=0,084
Оксида Си2О в исходной шихте, (кг/ч): 47,005*0,15*0,003=0,002
Из исходной шихты Си2О окисляется до СиО нацело. Из окислившегося Си2О по реакциям
не будет окисляться до СиО 100% -99%=2%: 0,084*1%=0,001кг/ч
Отношение распределения образования оксидов: Cu20/CuO = 2/1
0,084*0,99=0,083 кг/ч следовательно образуется:
Си2О=0,056 кг/ч и 0,028 кг/ч идет на доокисление до СиО
Суммарное количество Си2О, (кг/ч): 0,001+0,056=0,057
По реакции (б):
Расходуется кислорода, (кг/ч):
О2: 0,053*1/4*32/79,55=0,005
Образуется веществ, (кг/ч):
СиО: (0,028+0,133*0,15) *79,55=0,005
5.2.6. Окисление Ге:Распределение компонента, (кг/ч):
огарок: 0,167*0,65=0,108
пыль циклона: 0,167*0,2=0,033
пыль рукавного фильтра: 0,167*0,15=0,025
Реакции: a) Fe + 0.50? = FeO
М=55,85 М=16 М=71,85 (г/моль)
![]()
1) в огарке окислится: 0,108 кг/ч
Отношение распределения образования оксидов: РеаОз/ FeO =3/1=0,081/0,027
По реакции (а):
Расходуется кислорода, (кг/ч):
О2: 0,027*16/55,85=0,008
Образуется веществ, (кг/ч):
FeO: 0,027*71,85/55,85=0,035
По реакции (б):
Расходуется кислорода, (кг/ч):
02: 0,081*1,5*32/55,85*2=0,04
Образуется веществ, (кг/ч):
FeiOs: 0,081*159,7/2*55,85=0,116
Оксида FeiOs в исходной шихте, (кг/ч): 47,005*0,65*0,002=0,065
Суммарное количество Ре2Оз, (кг/ч): 0,181
2) в циклоне окислится: 0,033кг/ч
В циклоне окисление идет до РеаОз.
Расходуется кислорода, (кг/ч):
О2: 0,033*1,5*32/55,85*2=0,014
Образуется веществ, (кг/ч):
РегОз =0,065
Оксида Ре2Оз в исходной шихте, (кг/ч): 47,005*0, 20*0,002=0,019
Суммарное количество Ре2Оз, (кг/ч): 0,084
1) в огарке окислится: 0,025 кг/ч
Отношение распределения образования оксидов: РезОз/ FeO =3/1=0,019/0,006
По реакции (а):
Расходуется кислорода, (кг/ч):
О2: 0,006*16/55,85=0,002
Образуется веществ, (кг/ч):
FeO: 0,006*71,85/55,85=0,008
По реакции (б):
Расходуется кислорода, (кг/ч):
О2: 0,019*1,5*32/55,85*2=0,008
Образуется веществ, (кг/ч):
FeiOs: 0,019*159,7/2*55,85=0,027
Оксида Ре2Оз в исходной шихте, (кг/ч): 47,005*0,15*0,002=0,013
Суммарное количество Ре2Оз, (кг/ч): 0,04
5.2.7. Теоретическое количество воздухаСуммарное количество кислорода, (кг/ч): 35,03 + 9,939 + 11,563 + 3,55 + 2,662 + 1,765 + 0,865 + 0,543 + 0,407 + 0,182 + 0,159 + 0,049 + 0,037+0,023+0,013+0,009+0,005+0,003+ 0,008+ 0,014+0,002+0,008=75,043
Теоретический расход воздуха (из расчета. Оа - 23% по массе)
75,043*0,23=326,274 кг/ч
Количество азота: 326,274 - 75,043= 251,231 кг/ч
Количество влаги, вносимое с воздухом при Т=20°С и относительной влажности 80%
(содержание влаги "0,012 кг. на 1кг. сухого воздуха):
326,274* 0,012 = 3,915 кг/ч
Теоретический расход влажного воздуха (кг/ч)
326,274 + 3,915 = 330,189 кг/ч.
Таблица 8. Состав огарка.
| Со203 |
| 11,105 |
| 6,793 |
| WC | ТЮ | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe203 | H20 | Бент. всего | ||
| кг/ч | 1,746 | 0,336 | 0 | 0 | 0 | 0 | 124,760 | 12,975 | 0,165 | 0,997 | 0,251 | 0,181 | 0 | 10,686 163,469 | |
| % | 1,068 | 0, 206 | 0 | 0 | 0 | 0 | 76,320 | 7,937 | 0,101 | 0,610 | 0,154 | 0,111 | 0 | 6,537 100,000 | |
| СиО FeO |
| ||||||||||||||
| 0,232 0,035 |
| ||||||||||||||
| 0,142 0,021 |
| ||||||||||||||
Таблица 9. Состав циклонной пыли.
| WC | TiC | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe2O3 | Н2О | Бент. | всего | |
| кг/ч | 2,686 | 0,516 | 0 | 0 | 0 | 0 | 35,766 | 7,757 | 2,925 | 0,289 | 0,133 | 0,084 | 0 | 3,288 | 53,444 |
| % | 5,026 | 0,965 | 0 | 0 | 0 | 0 | 66,922 | 14,514 | 5,473 | 0,541 | 0,249 | 0,157 | 0 | 6,152 | 100,000 |
Таблица 10. Состав пыли рукавного фильтра.
| Со2ОЗ |
| 2,583 |
| 6,587 |
| WC | TiC | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe2O3 | H2O | Бент. | всего | |||
| кг/ч | 0, 201 | 0,039 | 0 | 0 | 0 | 0 | 29,030 | 4,485 | 0,019 | 0,230 | 0,057 | 0,040 | 0 | 2,466 | 39,211 | ||
| % | 0,513 | 0,099 | 0 | 0 | 0 | 0 | 74,035 | 11,438 | 0,048 | 0,587 | 0,145 | 0,102 | 0 | 6,289 | 100,000 | ||
| СиО | FeO |
| |||||||||||||||
| 0,053 | 0,008 |
| |||||||||||||||
| 0,135 | 0,020 |
| |||||||||||||||
Таблица 11. Состав газов.
| N2 кг/ч 251,231 | Н2О 42,275 | СО2 41,414 | всего 334,920 |
| % 75,012 | 12,622 | 12,365 | 100,000 |
Таблица 12. Материальный баланс обжига.
| Г | Приход | Об | разуется | ||
| Вещество | кг/ч | % | Вещество | кг/ч | % |
| WC | 134,636 | 22,366 | WC | 4,633 | 0,786 |
| TiC | 25,531 | 4,241 | TiC | 0,891 | 0,151 |
| Со | 10,000 | 1,661 | |||
| Zn | 1,000 | 0,166 | WO3 | 189,556 | 32,172 |
| Си | 0,500 | 0,083 | ТЮ2 | 25,217 | 4,280 |
| Fe | 0,167 | 0,028 | СоО | 3,109 | 0,528 |
| Со203 | 13,688 | 2,323 | |||
| W03 | 35,766 | 5,941 | ZnO | 1,516 | 0,257 |
| ТЮ2 | 7,757 | 1,289 | Си20 | 0,441 | 0,075 |
| СоО | 2,975 | 0,494 | СиО | 0,285 | 0,048 |
| ZnO | 0,289 | 0,048 | Fe203 | 0,305 | 0,052 |
| Си2О | 0,133 | 0,022 | FeO | 0,043 | 0,007 |
| Fe203 | 0,084 | 0,014 | |||
| бент | 16,440 | 2,790 | |||
| бент | 16,440 | 2,731 | |||
| H20 | 40,424 | 6,715 | H20 | 40,424 | 6,861 |
| N2 | 251,231 | 42,640 | |||
| 02 | 75,043 | 12,466 | C02 | 41,414 | 7,029 |
| N2 | 251,231 | 41,734 | |||
| Всего | 601,976 | 100 | Всего | 589, 193 | 100 |
| Нее пр | язка от ихода | 12,783 | 2,124 |
тшо: 3,036*МШо/201,38=0,270
тшо: 0,594*МШо/165,54=0,065
тшо: 0,178*МШо/165,54=0,019 Остаток воды: 547,236-21,251=525,985 кг.
Количество NH3 пошедшее на реакции, (кг/ч):
тотв: 201,227*2*MNH3 (17) 7303,3=22,557
тшз: 0,520* 6*МШЗ /211,93=0,250
тшз: 34,980*12* Мню /211,93=33,670
ткш: 3,036* 6*МШЗ /201,38=1,537
тшз: 0,594*4* Мынз /165,54=0,240
6) тщз: ОД78* 4*МШЗ /165,54=0,078 Остаток NH3: 60,804-58,324=2,480 кг.
Таблица 13. Материальный баланс выщелачивания.
| Приход | Образуется | ||||||
| Вещество WC | кг/ч 1,947 | % 0,236 | Вещество (NH4) 2WO4 | кг/ч 201,227 | % 25,084 |
| |
| TiC | 0,375 | 0,046 | [Co(NH3) 6] (OH) 3 | 35,500 | 4,425 |
| |
| WO3 | 153,790 | 18,662 | [Zn (NH3) 6] (OH) 2 [Cu (NH3) 6j (OH) 2 | 3,036 0,774 | 0,378 0,096 |
| |
Продолжение таблицы.
| ТЮ2 | 17,460 | 2,119 | |||
| СоО | 0,184 | 0,022 | WC | 1,947 | 0,243 |
| Со203 | 13,688 | 1,661 | TiC | 0,375 | 0,047 |
| ZnO | 1,227 | 0,149 | |||
| Cu20 | 13,688 | 1,661 | ТЮ2 | 17,460 | 2,177 |
| CuO | 0,285 | 0,035 | Fe203 | 0,221 | 0,028 |
| Fe2O3 | 0,221 | 0,027 | FeO | 0,043 | 0,005 |
| FeO | 0,043 | 0,005 | |||
| бент | 13,152 | 1,639 | |||
| бент | 13,152 | 1,596 | |||
| NH3 | 60,804 | 7,378 | NH3 | 2,480 | 0,309 |
| H20 | 547,236 | 66,404 | H20 | 525,985 | 65,568 |
| Всего | 824,100 | 100 | Всего | 802,2 | 100 |
| Невязка от прихода | 21,900 | 2,657 |
mCu(H20) 4ci2: (0,594+0,178) Mcu(mo) 4 012 206,44/165,54 = 0,963
mcocn: 7,756 M 7,756 Mc0ci2129,83/165,25= 6,093
Количество МНЦ С1, (кг/ч):
(165,765*2*53,5/249,85) +(7,756*6*53,5/165,28) +(3,683*6*53,5/244,28) +(0,963* 4*53,5/
206,44) =91,891
Количество поглощаемой реакциями H2O, (кг/ч):
(3,683*4*18/244,28) +(0,963*2*18/206,44) +(6,093*0,5*18/129,83) =1,676
Количество образующейся Н2О, (кг/ч):
7,756*3*18/165,765=2,527
Количество Н2О, приходящее с кислотой, (кг/ч):
Состав кислоты 19,8% НС1 80,2% Н2О
Количество требуемого НС1, (кг/ч):
(165,765*2*36,45/249,85) + (7,756 * 9 * 36,45 / 165,28) + (3,683 * 8 * 36,45/244,28) +(0,963*6*36,45/206,44) =69,177
Приходящей с кислотой Н2О, (кг/ч):
69,177*0,802/0, 198= 280, 202
Суммарное количество приходящей Н2О, (кг/ч):
280, 202+525,985=806,187
Суммарное количество уходящей Н2О, (кг/ч):
806,187+2,527-1,676=807,03 8
Таблица 14. Материальный баланс осаждения.
| Приход | Образуется | ||||||
| |||||||
| Вещество | кг/ч | % | Вещество | кг/ч | % |
| |
| (NH4) 2 WO4 | 201,227 | 18,033 | H2W04 | 165,765 | 15,414 |
| |
| [Co(NH3) 6] (OH) 3 | 35,500 | 3,181 | Zn(H2O) 6Cl2 | 3,683 | 0,342 |
| |
| [Zn (NH3) 6] (OH) 2 | 3,036 | 0,272 | Си(Н2О) 4С12 | 0,963 | 0,090 |
| |
| [Си (NH3) 6] (OH) 2 | 0,774 | 0,069 | СоС12 | 6,093 | 0,567 |
| |
| NH4C1 | 91,891 | 8,545 |
| ||||
| НС1 | 69,177 | 6, 199 |
| ||||
| Н2О | 806,187 | 72,245 | Н20 | 807,038 | 75,043 |
| |
| Всего | 1115,901 | 100 | Всего | 1075,433 | 100 |
| |
| Невя: | ка от прихода | 40,468 | 3,626 |
| |||
WOs получают термическим разложением H2WC4 при 750-800 °С
При прокалке идет следующая реакция:
H2WO4^WO3+H2O
Количество продуктов, (кг/ч):
Масса WO3 =153,79 (кг/ч)
Масса Н2О = 165,765-153,76= 11,075 (кг/ч)
Вывод: полученная нарастающая с каждой стадией невязка до 3,626% вызвана погрешностью расчетов.
6. Тепловой баланс 6.1 Зона кипящего слоя 6.1.1. Приход тепла зоны кипящего слоя
Похожие работы
... они брали ту самую "чистую" медь, почему соединили ее именно с оловом, а не с каким-нибудь другим металлом, в каких месторождениях встречается в природе медь, в каких именно химических соединениях, где эти месторождения расположены и насколько легко было древним людям ее вырабатывать и переплавлять? Очень странно, что кабинетные историки совершенно не утруждают себя подобными вопросами. А, ведь, ...




0 комментариев