Навигация
Опишите процесс электрохимической коррозии при контакте металла и изделия из Mg во влажной среде (Без аэрации и при аэрации). PH=10
10.4. Опишите процесс электрохимической коррозии при контакте металла и изделия из Mg во влажной среде (Без аэрации и при аэрации). PH=10
Очевидно, что образуется гальванический элемент. В полученном гальваническом элементе один из металлов, а именно более активный, будет окислятся, а на менее активном будет восстанавливаться ион ОН-, или какой то другой ион.
Имеем короткозамкнутый элемент, где магний является анодом, а молибден – катодом. Как видно из условия РН раствора щелочной, РН=10.
В разбавленных щелочах цинк реагирует по уравнению:
![]() , поскольку в растворе есть большое количество ионов ОН- то это будет несколько тормозить реакцию окисления магния, равновесие реакции сдвинется влево.
, поскольку в растворе есть большое количество ионов ОН- то это будет несколько тормозить реакцию окисления магния, равновесие реакции сдвинется влево.
Поскольку молибден находится в контакте с магнием и оба эти металла окружены раствором электролита, гальванический элемент оказывается «включенным». Магний в виде иона Mg2+ переходит в раствор щелочи, а оставшиеся от каждого атома два электрона перетекают на более электроположительный металл – молибден :
Mg = Mg2+ + 2e–
К молибденовому катоду подходят ионы водорода, принимают электроны и превращаются в атомы водорода, а затем и в молекулы водорода:
Н+ + е- = Н; 2Н = H2
Таким образом, потоки движения ионов разделены и при избытке щелочи процесс протекает до тех пор, пока не растворится весь магний. Мы рассмотрели процесс электрохимической коррозии при отсутствии поступления воздуха.
В присутствии воздуха в растворе протекают следующие реакции:
Mg + H2O + 1/2O2 = Mg(OH)2
![]()
При наличии в растворе газообразного кислорода и невозможности протекания процесса коррозии с водородной деполяризацией основную роль деполяризатора исполняет кислород. Коррозионные процессы, у которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют процессами коррозии металлов с кислородной деполяризацией. Это наиболее распространенный тип коррозии металла в воде.
Общая схема кислородной деполяризации сводится к восстановлению молекулярного кислорода до иона гидроокисла:
O2 +2H2O + 4e- = 4OH-
Суммарно на аноде будет проходить растворение магния, на катоде – выделение гидроксид-ионов. Процесс будет протекать до полного растворения магния и перехода его в гидроксид.
10.5. Опишите процесс электролиза с учетом перенапряжения.
Электролит – раствор ![]() PH= 4, 5
PH= 4, 5
Электроды: катод – Сu,
анод – Zn.
В растворе хлорид молибдена будет диссоциировать на ионы согласно уравнения:
![]()
Рассмотрим процессы, которые будут происходить на аноде.
Анод цинковый. На цинковом аноде могут происходить несколько процесов:

Запишем потенциалы прохождения указанных процессов:

Перенапряжение выделения кислорода на цинковом электроде при плотности тока 1мА/см2 равно 1,75 В. Это значит, что кислород в данной реакции выделятся не будет и на аноде возможны только две электрохимические реакции:
![]()
Как видно из значений электродных потенциалов на аноде будет происходить реакция окисления цинка: ![]() , потенциал которой будет ниже чем потенциал восстановления хлора. Мы будем иметь дело с электрорафинированием цинка.
, потенциал которой будет ниже чем потенциал восстановления хлора. Мы будем иметь дело с электрорафинированием цинка.
Рассмотрим электродные процессы на катоде. Материал катода – медь, катод довольно инертен и не будет брать участия в электрохимических процессах. Конечно мы только допускаем это, медь содержит некоторые примеси, которые и будут брать участие в электродных реакциях, но мы считаем, что эти процессы не повлияют существенно на суммарную реакцию. На катоде также возможны несколько реакций, рассмотрим их.
РН среды равно 4,5, среда кислая. На меди при температуре 20ºС перенапряжение выделения водорода при плотности тока 1 А/см2 равно 1,2 В, а при плотности тока 1 мА/см2 всего лишь 0,6 В. За уравнением Нернста мы можем вычислить значение потенциала перенапряжения водорода при РН=4,5. Потенциал водородного электрода находится в линейной зависимости от РН среды.
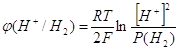
При давлении водорода 1 атмосфера ![]() , и при РН=4,5 мы получим перенапряжение равное:
, и при РН=4,5 мы получим перенапряжение равное: ![]()
При плотности тока равной 1 А/см2 перенапряжение равно: ![]() а при плотности тока 1 мА/см2
а при плотности тока 1 мА/см2 ![]() .
.
Ионы же цинка восстанавливаются при потенциале равном - 0,763 В, ионы молибдена восстанавливаются при потенциале равном -0,2 В. Перенапряжением восстановления ионов цинка и молибдена на медном электроде можно пренебречь, поскольку оно довольно мало по значению. Из полученных расчетов видно что при малых плотностях тока на медном электроде возможны три конкурирующие реакции:
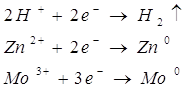
При плотности тока ![]() на катоде будет выделятся молибден по уравнению
на катоде будет выделятся молибден по уравнению ![]() , поскольку потенциал восстановления молибдена будет равен
, поскольку потенциал восстановления молибдена будет равен ![]() , что больше потенциала восстановления цинка и водорода в данном растворе.
, что больше потенциала восстановления цинка и водорода в данном растворе.
При этих условиях потенциал восстановления водорода равен около ![]() . При плотности тока равной 1 А/см2 перенапряжение равно:
. При плотности тока равной 1 А/см2 перенапряжение равно: ![]() , при этих условиях мы можем вести выделение молибдена из раствора по уравнению:
, при этих условиях мы можем вести выделение молибдена из раствора по уравнению: ![]() . Тогда водород на электродах выделяться не будет. Выделение молибдена из раствора будет происходить до тех пор пока не выделится он весь, или же его в растворе будет содержаться ничтожно мало. Тогда будет происходить восстановление цинка, потенциал восстановления которого равен - 0,76 В, тогда как потенциал выделения водорода выше – 0,83 В:
. Тогда водород на электродах выделяться не будет. Выделение молибдена из раствора будет происходить до тех пор пока не выделится он весь, или же его в растворе будет содержаться ничтожно мало. Тогда будет происходить восстановление цинка, потенциал восстановления которого равен - 0,76 В, тогда как потенциал выделения водорода выше – 0,83 В: ![]() . По нашим данным выделение водорода не будет происходить, реакции восстановления металлов будут более энергетически выгодно.
. По нашим данным выделение водорода не будет происходить, реакции восстановления металлов будут более энергетически выгодно.
При проведении электролиза надо учитывать повешение температуры, при повышении температуры на 1ºС перенапряжение уменьшается на 2 – 3 мВ. Оно также зависит от вида поверхности электрода и от наличия некоторых органических добавок в электролите.
11. Применение.
Молибден имеет большое значение в современной технике. Из всего его количества, потребляемого промышленностью, до 80% используется в черной металлургии для производства жаропрочных, жаростойких антикоррозионных, инструментальных, быстрорежущих, магнитных, конструкционных сталей, жаропрочных и жаростойких чугунов. Молибден повышает прочность сталей на холоду и содействует ее сохранению при высокой температуре, повышает жаростойкость сталей и чугуна, улучшает способность принимать закалку, 1 вес. ч. Мо повышает прочность стали эквивалентно 2 - 2,5 вес. ч. вольфрама.
Молибден в стали входит в состав как свободных выделений карбидов, так и твердого раствора. Присадка его в сталь способствует созданию мелкозернистой структуры. Вследствие этих причин и повышается прочность стали на холоду, при повышенной температуре, кратковременной и длительной нагрузке. Молибден также повышает способность стали к цементации. В магнитных сталях и сплавах он увеличивает магнитную проницаемость. Придает жаропрочность и жаростойкость ряду сплавов на основе цветных металлов.
В жаропрочных сплавах с цветными металлами потребляется около 4 – 5% вырабатываемого молибдена. Также около 5 – 6,5 % Мо выпускают в виде проволоки, прутков, листа для электро- и радиотехнической промышленности и других назначений. Для реактивов, красок и других химикатов используется 4 – 5% Мо. Возрастает и его применение в сельском хозяйстве.
Молибден вводят в стали в виде сплава с железом - ферромолибдена. Молибдена в ферросплавах не менее 50%.
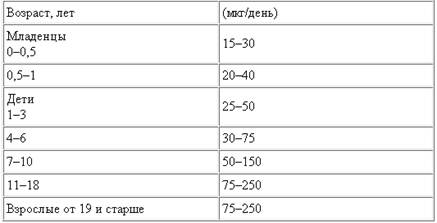
Проволока и прутки из чистого молибдена применяются для холоднокатаной арматуры, вводов, анодов радио- и электроламп, элементов сопротивления высокотемпературных печей с защитной атмосферой, высокотемпературных термопар. Листовой молибден применяется в машиностроении как жаропрочный материал, а в радиоэлектронике – для анодов мощных радиоламп, защитных экранов высокотемпературных электропечей и для других целей. Из молибденового порошка получают «псевдосплавы» (сплавы-смеси) с серебром для электротехнических контактов, карбид молибдена применяется в твердых сплавах, силицид молибдена MoSi2 – в жаростойких изделиях. Последний, как указывалось, применяется в элементах сопротивления электропечей, работающих до 1600°С без защитной атмосферы. Соединения молибдена применяются как катализаторы в органическом синтезе и как реактивы в аналитической химии (парамолибдат аммония и комплексные соединения молибдена), в производстве лаков и красок для шерсти и шелка. В сельском хозяйстве используются соединения молибдена в виде слабых растворов: он облегчает усвояемость растениями питательных веществ из почвы. Но в то же время большие дозы молибдена оказывают токсическое действие на растительные и животные организмы.
Из MoS2 готовят сухую смазку для деталей механизмов, работающих при повышенной температуре. Его смазывающее действие эффективнее, чем графита.
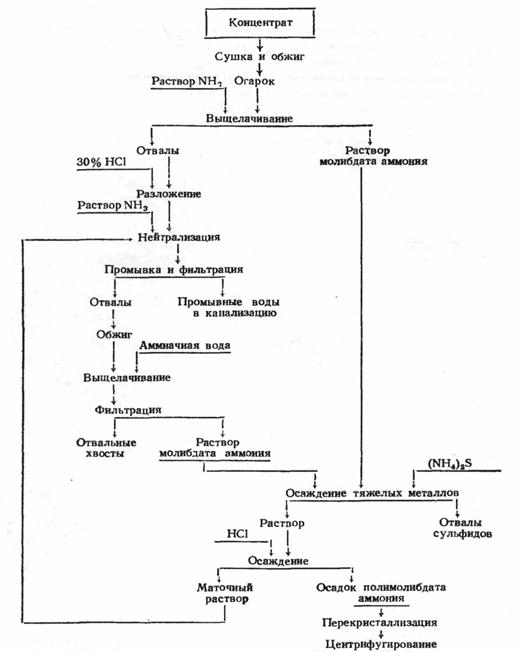
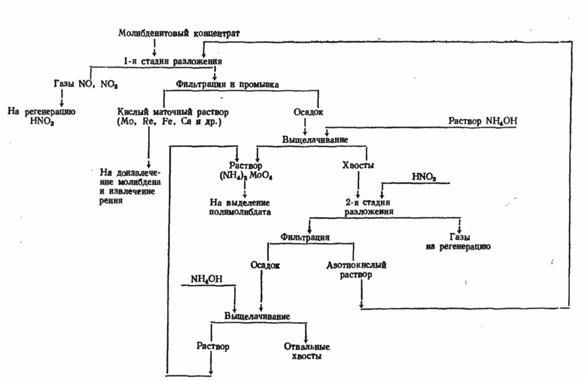
Молибденовые рудные концентраты перерабатывают на ферромолибден, молибдат кальция, МоО3, парамолибдат аммония, MoS2. Первые два – полуфабрикаты для производства молибденсодержащих сталей, парамолибдат аммония – полуфабрикат для производства чистых соединений молибдена и самого молибдена.
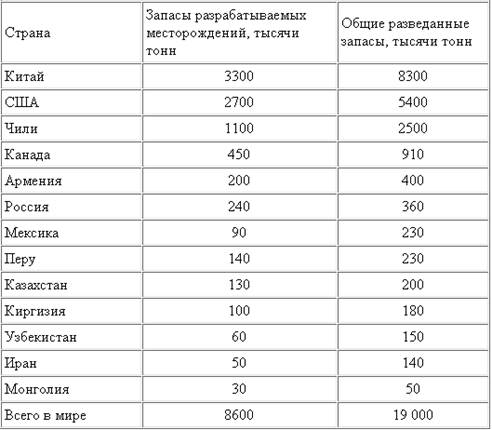
В последние годы значительно увеличился выпуск молибденовых концентратов в Канаде и Чили, которые в мире вышли в этой области соответственно на второе и третье места. Значительные залежи молибденовых руд есть в России, которая также производит довольно большие количества его как для собственной металлургической промышленности так и на экспорт. Товарная продукция молибдена в США выпускается в виде трехокиси, порошка молибдена, молибдатов аммония и натрия, ферромолибдена, сульфида молибдена MoS2 и др.
Список использованной литературы.
1. Глинка Н. Л. Общая химия. – Л.: Химия, 1988. – 702 с.
2. Полеес М. Э. Аналитическая химия. – М.: Медицина, 1981. – 286 с.
3. Крешков А. П., Ярославцев А. А. Курс аналитической химии. – М.: Химия, 1964. – 430 с.
4. Мороз А. С., Ковальова А. Г. Физическая и коллоидная химия. – Л. : Мир, 1994. – 278 с.
5. Физическая химия. Практическое и теоретическое руководство. Под ред. Б. П. Никольского, Л.: Химия, 1987. – 875 с.
6. Скуг Д., Уэст Д. Основы аналитической химии. В 2 т. Пер с англ. М.: Мир, 1979, - 438 с.
7. Бусев А. И. Аналитическая химия молибдена. М.: Издательство АН СССР, 1962, - 300с.
8. Химия и технология редких и рассеянных элементов. Ч. ІІІ. М.: Высшая школа, 1976, 320 с.
Похожие работы
... месторождений перерабатывается Сорским и Жирекенским горно-обогатительными комбинатами, оба они являются собственностью ОАО "Группа Сибирский алюминий". 3. Физико-химические свойства молибдена МОЛИБДЕН - (Molybdenum), Mo - химический элемент 6 (VI Б) группы периодической системы, атомный номер 42, атомная масса 95,94. Известен 31 изотоп молибдена с 83Мо по 113Мо. Из них стабильные: 92Мо, ...
... C5H12CO, циклогексаноном (СН2)5СО и ацетофеноном СН3СОС6Н5. Экстрагирование молибдена дорганическими веществами с целью его выделения из отходов молибденового производства является наиболее рациональным способом получения молибдена. Глава 2. Свойства молибдена и его соединений Рассмотрим основные физические и химические свойства молибдена, что поможет в дальнейшем объяснить его способы ...
... из отработанных катализаторов и химических остатков [16]. 3.3 Молибден из колошниковой пыли плавильных печей Этот процесс, разработанный X. Кастанья, предназначен для выделения молибдена в виде молибденовой кислоты из отходов, в частности, из отработанных катализаторов, содержащих носитель - у-оксид алюминия и молибден в виде оксида или сульфида. Процесс включает обработку отходов ...
... породы складируются в отвалы вскрышных пород. Отвалы вскрышных пород. Отвалы вскрышных пород (смотреть приложение № 12, экспликация) формируются при разработке карьера медно - молибденового месторождения Шорское. Отходы горнодобывающего производства в виде вскрышных пород, не содержащих молибден, медь и сопутствующие полезные компоненты образуются при отборе крупнотоннажной технологической ...

0 комментариев