Навигация
Аналитическое определение ионов алюминия(III) и меди(II)
1.3 Аналитическое определение ионов алюминия(III) и меди(II)
По Шварценбаху, алюминий можно определить как прямым, так и косвенным титрованием[6]. При прямом определении со смешанным индикатором CuY – ПАН, к кислому анализируемому раствору добавляют аммиак до рН между 0 и 1. Затем приливают каплю бромфенолового синего и, добавляя ацетат аммония, доводят окраску раствора до сине-серой, после чего быстро приливают концентрированную уксусную кислоту; рН раствора должен составлять приблизительно 3, если необходимо, его корректируют с помощью уксусной кислоты или ацетата аммония. После приливания нескольких капель комплексона меди и индикатора ПАН (до появления глубокой фиолетовой окраски) раствор нагревают до кипения. Далее проводят титрование, причем раствор все время поддерживают в состоянии, близкому к кипению. Около точки эквивалентности окраска переходит в желтую, так как ЭДТА быстрее реагирует с CuY – ПАН быстрее чем с алюминием, однако фиолетовая окраска быстро возвращается. Восстановление окраски индикатора замедляется около точки эквивалентности, поэтому необходимо прибавлять титрант по каплям. Точку эквивалентности считают достигнутой, когда желтая окраска раствора остается неизменной после кипячения в течении полминуты. Для предосторожности кипятят еще одну минуту, причем иногда появляется слабый красный оттенок, который исчезает при добавлении последней капли ЭДТА.
При обратном титровании Al(III) раствором железа (III) с салициловой кислотой осадок алюминия растворяют в небольшом объеме соляной кислоты и приливают в небольшом избытке ЭДТА[6]. В смеси устанавливают значение рН=6 прибавлением по каплям раствора аммиака. Затем раствор быстро кипятят, по охлаждении доводят объем раствора дистиллированной водой до 100 мл и прибавляют раствора ацетата натрия до рН смеси, равного 6 - 6,5. Далее добавляют кристаллический индикатор, и титруют смесь стандартным раствором FeCl3 до появления красно – коричневой окраски, устойчивой в течение короткого времени. В ходе титрования значение рН раствора должно быть не ниже 5. Чтобы избежать понижения рН, необходимо к раствору прибавить несколько капель аммиака[6].
Среди методов определения ионов алюминия (III) одним из важнейших является колориметрическое определение экстракцией оксихинолята алюминия[8]. Метод основан на том, что оксихинолят алюминия количественно экстрагируется хлороформом в слабокислой среде (рН = 4,35 — 4,5), окрашивая хлороформный слой в желто-зеленый цвет. По интенсивности этой окраски определяют содержание алюминия колориметрическим титрованием или методом стандартной шкалы. Мешающее определению железо предварительно окисляют до трехвалентного и извлекают хлороформом в более кислой среде (рН = 1,7 — 2,0).
К аликвоте добавляют ацетатного буферного раствора, приливая по каплям ледяную уксусную кислоту до рН = 3. Раствор нагревают до кипения. К кипящему раствору добавляют комплексонат меди и индикатор АН, причем раствор окрашивается в красно-фиолетовый цвет. Горячий раствор титруют стандартным раствором комплексона III до желтого цвета[9].
Также для определения ионов алюминия (III) используют метод колориметрического определения с применением эриохромцианина R[9]. Ионы алюминия образуют с эриохромцианином R при рН = = 5,4 комплексное соединение, имеющее фиолетовую окраску. Светопоглощение измеряют при λ - 530 нм, молярный коэффициент светопоглощения равен 40∙103.
Мешающее определению железо(III) восстанавливают до железа(II) гидрохлоридом гидроксиламина. Мешают также фториды, фосфаты и большие количества органических веществ. Органические вещества и фтор можно удалить выпариванием пробы с хлористоводородной кислотой досуха и прокаливанием остатка.
По Шварценбаху[6], медь можно определить как прямым, так и косвенным титрованием. При прямом определении меди с ПАНом к анализируемому раствору добавляют ацетатный буферный раствор и индикатор. Тотчас доводят раствор до кипения и тируют раствором ЭДТА до очень резкого перехода темно-фиолетовой окраски в капарсечно – желтую.
По Васильеву[7], медь можно определить амперометрическим титрованием. Для этого анализируемый раствор помещают в мерную колбу вместимостью 100мл, добавляют 2М серной кислоты, доводят до метки водой и тщательно перемешивают. Аликвоту помещают в электролизер, добавляют KI и титруют раствором тиосульфата натрия, погружая платиновый электрод, соединяя цепь мостиком из фильтровальной бумаги, при этом во время титрования должна работать магнитная мешалка.
Также медь можно определить методом внутреннего электролиза. Он позволяет выделить медь, отделяя ее от бериллия, цинка, марганца, кобальта, никеля, олова (IV), железа, алюминия, лантана, хрома, галлия, индия, таллия (I), циркония, тория, теллура (IV), ванадия, щелочноземельных металлов, магния, кадмия, свинца, арсенатов, титана, уранил- и вольфрамат-ионов, прибавляя перед электролизом 10%-ный раствор ЭДТА в количестве, по крайней мере в 10 раз превышающем содержание этих ионов, разбавляя раствор и приводя его рН к 9,0. Электролиз надо проводить с цинковым анодом. Вместе с медью в этих условиях выделяются только серебро и висмут. Если предполагается присутствие этих двух элементов, то рекомендуется их выделить сначала в тех же условиях, но с добавлением 10%-ного раствора цианида калия для связывания меди [8].
При относительно большом содержании меди в сточной воде определение ее может быть сделано с большей точностью йодометрическим методом. Один из его вариантов, в котором мешающее влияние солей железа(III) устраняется путем добавления к раствору бифторида аммония[8].
Также медь можно определить пиридин - роданидным методом. При прибавлении к раствору соли меди роданида аммония и пиридина образуется комплекс [Cu(C5H5N2)](NCS)2, который при взбалтывании раствора с хлороформом переходит в органический слой, окрашивая его в зеленый цвет.
Определению мешают извлекаемые хлороформом (и при этом его окрашивающие) органические вещества. Если они присутствуют, то их извлекают хлороформом до образования меднороданового комплекса[9].
Однин из точных методов определения меди(II) это метод с применением диэтилдитиокарбамата натрия [9]. Ионы меди реагируют с диэтилдитиокарбаматом натрия (C2H5)2NCS2Na с образованием коричневого внутрикомплексного соединения, которое растворяется в четыреххлористом углероде, окрашивая его в желто-коричневый цвет. Оптическая плотность получаемых растворов в широких пределах пропорциональна концентрации меди. Четыреххлористым углеродом можно экстрагировать как из слабокислой, так и аммиачной среды, но при использовании последней и добавления цитрата аммония и ЭДТА полнее устраняется мешающее влияние других катионов. В этих условиях в реакцию с диэтилдитиокарбаматом помимо меди вступают лишь висмут, серебро и ртуть. Однако комплексы серебра и ртути практически бесцветны и на определение меди не влияют. Комплекс висмута окрашивает ССl4 в желтый цвет, но окраска эта по своей интенсивности в 15 раз слабее окраски, получаемой от раствора комплекса меди той же концентрации. В большинстве случаев этим мешающим влиянием висмута можно пренебречь, если же последнего много - рассчитать поправку и ввести ее в результат определения меди.
Если присутствуют цианиды или большие количества органических веществ, надо провести предварительную обработку пробы для их разрушения[10].
Глава 2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Похожие работы
... при реагентном способе очистки, по предлагаемой технологии извлекаются в виде элюатов и направляются на повторное использование. Таблица 3.1. Показатели очистки хромсодержащих сточных вод по предлагаемой технологической схеме Наименование Единицы Показатели Показатели ГОСТ Степень ингредиентов измерения до очистки после ...
... алюминия. 6. ГОСТ Р 51211-98 Вода питьевая. Методы определения содержания ПАВ. 7. ГОСТ Р 51210-98 Вода питьевая. Метод определения содержания бора. 8. ПНД Ф 14.1:2:4.24-95 Методика выполнения измерений массовых концентраций алюминия в пробах природной, питьевой и сточной воды на анализаторе "ФЛЮОРАТ-02". 9. ПНД Ф 14.1:2:4.26-95 Методика выполнения измерений массовых концентраций нитрит ...
... илом. При этом происходит образование комплексов ионов с белком активного ила, следствием чего является, с одной стороны, накопление соединений металлов в осадках, а с другой - снижение качества очистки сточных вод, так как сорбированные металлы концентрируются в активном иле и с возвратным илом неоднократно попадают в аэротенк, где значительная часть подаваемого кислорода воздуха затрачивается не ...
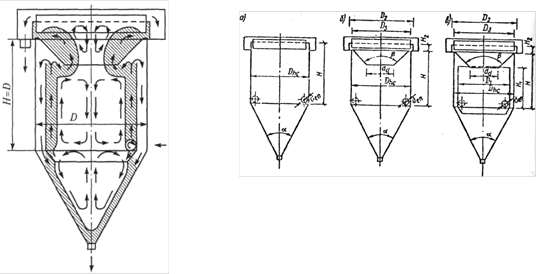
... , а тяжелые примеси вдоль конической части перемещаются вниз и выводятся через патрубок шлама. Промышленность выпускает напорные гидроциклоны нескольких типоразмеров. Для грубой очистки применяют гидроциклоны больших диаметров. При целесообразности глубокой очистки сточной воды используют схему последовательного соединения различных типоразмеров гидроциклонов. При такой сложной схеме соединения ...





0 комментариев