Навигация
Выбор объектов исследования
2.1 Выбор объектов исследования
В настоящее время человек оказывает большое влияние на природу. Из-за этого окружающая среда подвергается большему загрязнению, возрастает необходимость исследования водных ресурсов на пригодность к употреблению. Именно поэтому, нами выбрана в качестве объекта исследования сточная вода для определения в ней общего содержания алюминия(III) и меди (II), так как соединения этих элементов, попадая в природные водоемы, нарушают общий состав воды, и влияют на экосистему водоемов в целом.
2.2 Оборудование и реактивы, используемые в работе
Штатив с лапкой;
Конические колбы для титрования – 3 шт;
Мерная колба вместимостью 100мл;
Градуированная пипетка вместимостью 10мл;
Химические стаканы на 100 мл – 2 шт;
Фильтровальная бумага;
Тиосульфат натрия(![]() ), 0,03N раствор;
), 0,03N раствор;
Иодид калия(KI), 20%-ый раствор;
Серная кислота(H2SO4), 2N раствор;
Крахмал(![]() )
)![]() раствор;
раствор;
Комплексон III, 0,1N раствор;
Сульфат меди(![]() ·5 H2O), 0,02М раствор;
·5 H2O), 0,02М раствор;
Индикатор ПАН раствор;
Ацетат аммония(CH3COONH4) раствор.
2.3 Методики, используемые в работе
2.3.1 Определение меди (II) йодометрическим методом
В колбу для титрования наливают 15 мл 20%-ного раствора KI, 2 мл 2 н. раствора H2SO4 и аликвотную часть (10,0 мл) исследуемого раствора. Оставляют смесь в темноте на пять минут, после чего оттитровывают раствором тиосульфата натрия, прибавляя 5 мл раствора крахмала в самом конце титрования, когда раствор со взмученным в нем осадком будет иметь светло-желтую окраску. Синяя окраска жидкости должна исчезнуть от одной капли титранта и вновь не появляться несколько минут. Взмученный осадок CuI после окончания титрования должен иметь цвет «слоновой кости». Титрование повторяют несколько раз и по сходящимся отсчетам по бюретке рассчитывают средний объем титранта, и вычисляют содержание меди.
2.3.2 Определение алюминия(III) комплексонометрическим методом
В колбу для титрования наливают аликвотную часть (10,0 мл) исследуемого раствора. Затем вводят избыток стандартного раствора ЭДТА (50 мл) и разбавляют раствор до объема 100 мл. Раствор нагревают до кипения и кипятят 10 мин; затем охлаждают, вводят 10 мл ацетата аммония, прибавляют 10 капель индикатора ПАН и титруют 0,02 М раствором сульфата меди до перехода зеленой окраски в фиолетовую, устойчивую в течение 30 сек. Затем вычисляют содержание алюминия.
2.4 Обсуждение результатов
В данной работе нами было определено общее содержание алюминия и меди.
В мерную колбу вместимостью 250,0 мл помещали 25,0 мл сточной воды, доводили до метки дистиллированной водой и перемешивали. Проба имела бесцветную окраску, не имела запаха, значение рН равнялось 1.
При титровании меди по сходящимся отсчетам по бюретке находим объемы V1 = 1,2 мл, V2 = 1,3 мл, V3 = 1,2 мл. По формуле определяем концентрацию N ,моль/л:
N1 = (0,03 · 1,2) / 10 = 0,0036 моль·экв/л, (5)
N2 = (0,03 · 1,3) / 10 = 0,0039 моль·экв/л, (6)
N3 = (0,03 · 1,2) / 10 = 0,0036 моль·экв/л. (7)
Найдем среднюю концентрацию Nср = (0,0036 + 0,0039 + 0,0036) / 3 = 0,0037 моль·экв/л. Проверяем концентрацию по 3Sn –критерию:
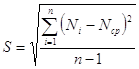 , (8)
, (8)
![]() (9)
(9)
3S3 = 1,7· 10-4 · 3 = 5,1 · 10-4. (10)
Рассчитаем доверительный интервал, при t=4,303, n=3:
![]() . (11)
. (11)
Из этого следует, что в нашей работе нет промахов и Nср = (0,0037±0,0004) моль·экв/л. Рассчитаем концентрацию меди в исследуемом растворе, в мг/л:
![]() мг/л. (12)
мг/л. (12)
При титровании алюминия по сходящимся отсчетам по бюретке находим объемы V1 = 23,1 мл, V2 = 23,0 мл, V3 = 22,9 мл.
По формуле определяем объем затраченного на титрование раствора ЭДТА:
![]() =(0,02·23,1)/0,1=4,62 мл, (13)
=(0,02·23,1)/0,1=4,62 мл, (13)
![]() =(0,02·23,0)/0,1=4,60 мл, (14)
=(0,02·23,0)/0,1=4,60 мл, (14)
![]() =(0,02·22,9)/0,1=4,58 мл. (15)
=(0,02·22,9)/0,1=4,58 мл. (15)
Рассчитает объем титранта, который пошел на титрование раствора:
![]() , (16)
, (16)
![]() мл , (17)
мл , (17)
![]() мл . (18)
мл . (18)
Затем рассчитываем концентрация алюминия в растворе:
![]() =(0,02·18,48)/20=0,01848 моль·экв/л, (19)
=(0,02·18,48)/20=0,01848 моль·экв/л, (19)
![]() =(0,02·18,40)/20=0,01840 моль·экв/л, (20)
=(0,02·18,40)/20=0,01840 моль·экв/л, (20)
![]() =(0,02·18,32)/20=0,01832 моль·экв/л. (21)
=(0,02·18,32)/20=0,01832 моль·экв/л. (21)
Найдем среднюю концентрацию Nср = (0,01848 + 0,01840 + 0,01832) / 3 = 0,01840 моль·экв/л.
Проверяем концентрацию по 3Sn –критерию, по формуле (8):
![]() , (22)
, (22)
3S3 = 0,7· 10-4 · 3 = 2,1 · 10-4. (23)
Рассчитаем доверительный интервал:
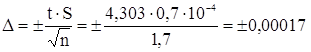 . (24)
. (24)
Из этого следует, что в нашей работе нет промахов и Nср = (0,01840±0,00017) моль·экв/л.
Рассчитываем концентрацию алюминия в исследуемом растворе:
![]() мг/л. (25)
мг/л. (25)
В ходе эксперимента нами были установлены содержания меди и алюминия в сточной воде, они составляют N = (118,4±0,0004) мг/л и N = (496,8±0,00017) мг/л соответственно. Норма ПДК для меди составляет 0,3 мг/л, для алюминия 0,2 мг/л. Можно сделать вывод, что концентрации меди и алюминия превышает предельно допустимую концентрацию, и эта вода должна подвергнуться дополнительной очистке.
ВЫВОДЫ
1. Полученный раствор сточной воды содержал ионы алюминия и меди(II).
2. Йодометрическим методом определили содержание меди (II) в сточной воде N = (118,4±0,0004) мг/л.
3. Комплексонометрическим методом определили содержание алюминия в сточной воде N = (496,8±0,00017) мг/л.
4. Полученные концентрации были сравнены с ПДК, они значительно превышают предельно допустимые концентрации данных ионов в сточной воде.
СПИСОК ЛИТЕРАТУРЫ
1. Ахметов, Н.С. Общая и неорганическая химия / Н.П.Ахметов. – М.: Высшая школа, 2001. – С488-502.
2. Реми, Г. Курс неорганической химии Т.1 / Г.Реми. – М.: Мир, 1966. –С381-386.
3. Некрасов, Б. В. Основы общей химии Т.2/ Б. В. Некрасов. – М.: Химия, 1973. – С32-34.
4. Реми, Г. Курс неорганической химии Т.2 / Г.Реми. – М.: Мир, 1966. –С394-410.
5. Угай, Н. П. Общая и неорганическая химия / Н.П.Угай. - М.: Высшая школа, 2000. – С. 310-315.
6. Шварценбах, Г. Комплексонометрическое титрование / Г. Шварценбах, Г. Флашка. – М.: Химия, 1970 – С183-192, 251-257.
7. Васильев, В. П. Аналитическая химия. Лабораторный практикум / В.П.Васильев, Р.П.Морозова, Л.А. Кочергина. – М.: Дрофа, 2004.-С329-331.
8. Лурье, Ю.Ю. Аналитическая химия промышленных сточных вод/Ю. Ю.Лурье. – М.: Химия, 1984. – 447 с.
9. Лурье, Ю.Ю. Химический анализ производственных сточных вод/Ю.Ю.Лурье, А.И.Рыбникова. – М.: Химия, 1974. – 335 с.
10. Голосницкая, В.А. Анализ природных и сточных вод/В.А.Голосницкая. – Новочеркасск: Химия, 1979. – 84 с.
Похожие работы
... при реагентном способе очистки, по предлагаемой технологии извлекаются в виде элюатов и направляются на повторное использование. Таблица 3.1. Показатели очистки хромсодержащих сточных вод по предлагаемой технологической схеме Наименование Единицы Показатели Показатели ГОСТ Степень ингредиентов измерения до очистки после ...
... алюминия. 6. ГОСТ Р 51211-98 Вода питьевая. Методы определения содержания ПАВ. 7. ГОСТ Р 51210-98 Вода питьевая. Метод определения содержания бора. 8. ПНД Ф 14.1:2:4.24-95 Методика выполнения измерений массовых концентраций алюминия в пробах природной, питьевой и сточной воды на анализаторе "ФЛЮОРАТ-02". 9. ПНД Ф 14.1:2:4.26-95 Методика выполнения измерений массовых концентраций нитрит ...
... илом. При этом происходит образование комплексов ионов с белком активного ила, следствием чего является, с одной стороны, накопление соединений металлов в осадках, а с другой - снижение качества очистки сточных вод, так как сорбированные металлы концентрируются в активном иле и с возвратным илом неоднократно попадают в аэротенк, где значительная часть подаваемого кислорода воздуха затрачивается не ...
... , а тяжелые примеси вдоль конической части перемещаются вниз и выводятся через патрубок шлама. Промышленность выпускает напорные гидроциклоны нескольких типоразмеров. Для грубой очистки применяют гидроциклоны больших диаметров. При целесообразности глубокой очистки сточной воды используют схему последовательного соединения различных типоразмеров гидроциклонов. При такой сложной схеме соединения ...





0 комментариев