Навигация
Можливість судово-медичної діагностики раптової серцевої смерті за результатами лабораторних досліджень
Можливість судово-медичної діагностики раптової серцевої смерті за результатами лабораторних досліджень
14.01.25 – судова медицина
Авторефератдисертації на здобуття наукового ступеня
кандидата медичних наук
Київ – 2008Дисертацією є рукопис
Робота виконана в Луганському державному медичному університеті МОЗ України
Науковий керівник: доктор медичних наук, професор
Мішалов Володимир Дем’янович, Національна
медична академія післядипломної освіти імені
П.Л. Шупика, завідувач кафедри судової медицини
Офіційні опоненти: доктор медичних наук, професор
Кривда Григорій Федорович,
Одеський державний медичний університет,
завідувач кафедри судової медицини з
післядипломною підготовкою;
доктор медичних наук, професор
Ольховський Василь Олексійович,
Харківський державний медичний університет, завідувач кафедри судової медицини та основ права.
Захист відбудеться “_18__” __квітня__2008 року о _12_ годині на засіданні спеціалізованої вченої ради Д 26.613.03 при Національній медичній академії післядипломної освіти імені П.Л. Шупика МОЗ України за адресою: 04112, м. Київ, вул. Оранжерейна, 9.
З дисертацією можна ознайомитись у бібліотеці Національної медичної академії післядипломної освіти імені П.Л. Шупика за адресою: 04112, м. Київ, вул. Дорогожицька, 9.
Автореферат розісланий 17.03.2008 р.
Вчений секретар спеціалізованої вченої ради,
кандидат медичних наук, доцент Гуріна О.О.
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИ
Актуальність роботи. Виходячи з надзвичайної розповсюдженості серед населення України і переважного ураження осіб працездатного віку, однією з найважливіших медико-соціальних і економічних проблем сьогодення є смертність внаслідок захворювань системи кровообігу (В.Ф. Москаленко, Г.В. Дзяк, 2001; Г.Ф. Кривда, 2007). При цьому, найбільш поширеною і важко діагностованою серед них, є раптова серцева смерть (РСС), викликана гострою ішемічною хворобою серця (ГІХС), зокрема, такою її формою, як гостра коронарна недостатність (ГКН). За визначенням ВООЗ, раптова серцева (кардіальна) смерть – це смерть практично здорових людей у перші шість годин після появи симптомів захворювання. У 95% випадків вона настає протягом однієї години, з них – у 73% випадків у провдовж 10 хвилин (M. Papanicolaon et al, 1986).
За останні часи проблемі судово-медичної діагностики раптової серцевої смерті присвячена значна кількість публікацій, серед яких левова частина присвячена морфологічним (гістологічним) змінам скорочувального міокарда (О.І. Герасименко і співавт, 2000; В.В. Войченко, 2002; О.Р. Малик, 2006). Однак, гістологічне дослідження не завжди може підтвердити гострі ішемічні порушення в міокарді (В.О. Ольховський і співавт. 2006), оскільки для розвитку виразних морфологічних змін у серці необхідно не менше 12 годин (Л.А. Зимина, Ю.С. Исаев, 2005; Л.А. Зимина, Т.Д. Лелюх, Л.С. Маслаускайте, 2006). Тому, у разі раптової смерті внаслідок гострої ішемічної хвороби серця, особливо, якщо смерть настала зразу після серцевого нападу або на його висоті, виявлення будь-яких мікроскопічних змін серцевого м’яза для судово-медичного гістолога являє складне завдання.
Інша частина робіт висвітлює зміни кількісного вмісту хімічних елементів серця за результатами полум’яної фотометрії (К.М. Сулоєв, 2005), атомно-абсорбційного дослідження (Є.П. Федорчук-Незнакомцева, С.М. Федорчук, 2006). Однак, наведені методи дослідження не набули широкого використання у практиці бюро судово-медичної експертизи України.
Найбільш інформативнішими і найчутливішими методами у подібних випадках можуть бути біохімічні дослідження, оскільки період альтерації навіть при невеликих (до 1 г) некрозах міокарда можна визначити за змінами біохімічних характеристик (А. Хехт, 1975; Т.А. Дежинова, 2003; Н.В. Дзик Н.В., В.С. Берестовская, 2003; Л.Л. Сидорова, 2006). Тому, окрім морфологічних, актуальним є пошук біохімічних критеріїв ішемії і некрозу м¢язових волокон шлуночків у разі смерті внаслідок ГІХС. Однак, наявні відомості про них носять суперечливий характер, вони фрагментарні, не систематизовані.
Наслідками ішемії серцевого м’язу при ГІХС є зміни його енергетичного метаболізму, зниження рівня енергозабезпечення міокарда. Тому доцільним буде вивчення мітохондріального апарату та змін енергетичного метаболізму шлуночків у разі смерті внаслідок гострої ішемічної хвороби серця.
Судово-медична практика потребує об’єктивізації надійності оцінки критеріїв причини раптової смерті. Тому пошук ранніх ознак ушкодження м¢язових волокон шлуночків серця як за змінами гістологічних структур міокарда, так і за змінами його біохімічних показників у разі смерті внаслідок ГІХС, є предметом перспективних досліджень.
За останній час мають місце роботи, в яких висвітлені дані, отримані шляхом використання лазерів в оптиці світлорозсіяння біологічних тканин (О.В. Пішак, В.П. Пішак, 2000), зокрема, при встановленні давності настання смерті (О.Я. Ванчуляк, 2007). В основу такого підходу покладено сукупність методів лазерної поляриметрії, які поєднують розвиток традиційних методів еліпсометрії та стоксполяриметрії з розробкою нових методів поляризаційної корелометрії когерентних зображень біологічних тканин (Ushenko A.G., 2000). З огляду на розвиток нового напрямку досліджень у судово-медичній практиці - лазерної поляриметрії біологічних тканин, яка спрямована на дослідження особливостей структури їх зображень, було б доцільним провести вивчення особливостей поляризації зображень серця, для визначення його патологічних змін у разі смерті внаслідок гострої коронарної недостатності.
Все вищесказане свідчить про недостатню вирішеність даної проблеми, підкреслює її актуальність і зумовлює необхідність подальшого вивчення.
Зв¢язок роботи з науковими програмами, планами, темами.
Дисертація є самостійною роботою (№ держреєстрації 0106U011205).
Мета і завдання дослідження. Визначення морфологічних, біофізичних та деяких біохімічних критеріїв діагностики раптової смерті внаслідок гострої ішемічної хвороби серця.
Для досягнення поставленої мети необхідно вирішити завдання:
1. Провести аналіз показників смертності від хвороб системи кровообігу серед населення м. Луганська та Луганської області за останні 5 років (2003 – 2007 р.р.).
2. Визначити особливості локалізації ішемії та гістологічних змін та кровопостачання міокарда шлуночків у разі раптової смерті внаслідок гострої ішемічної хвороби серця.
3. Визначити морфологічні особливості змін ендокарда та субендокардіального простору шлуночків у разі раптової смерті внаслідок гострої ішемічної хвороби серця.
4. Визначити особливості змін мітохондріального апарату та енергетичного метаболізму міокарда шлуночків у разі раптової смерті внаслідок гострої гострої коронарної недостатності.
5. Дослідити можливість виявлення ознак некрозу міокарда у разі раптової коронарної смерті за даними мікроспектрофотометрії.
6. Провести імунохроматографічне дослідження та визначення серцевого тропоніна І в крові осіб, що померли раптово внаслідок гострої ішемічної хвороби серця.
7. Виявити особливості архітектоніки міокарда шлуночків у разі раптової серцевої смерті за змінами його лазерних поляриметричних характеристик.
Об¢єкт дослідження: патологічні зміни міокарда шлуночків серця, цільної крові осіб чоловічої та жіночої статі віком від 18 до 45 років, що померли раптово, внаслідок гострої ішемічної хвороби серця.
Предмет дослідження: морфологічні, біохімічні критерії та лазерні поляриметричні зміни міокарда у разі раптової смерті внаслідок гострої ішемічної хвороби серця.
Методи дослідження: макроскопічні, морфометричні, гістологічні методи, світлова та електронна міскроскопія, біохімічні методи, мікрофотоспектрометрія, лазерно-поляриметричні досліди, методи математичної статистики.
Наукова новизна дослідження. Визначені та узагальнені особливості динаміки раптової смерті внаслідок гострої ішемічної хвороби серця серед населення м. Луганська та Луганської області за останні 5 років. Показано, що основну масу померлих внаслідок ГІХС складали особи від 40 до 60 років переважно чоловічої статі.
Визначені макро- та мікроскопічні ознаки патоморфологічних змін міокарда шлуночків серця, їх мітохондріального апарату та енергетичного метаболізму кардіоміоцитів у разі раптової смерті внаслідок гострої коронарної недостатності.
Вперше виявлені прояви морфо-функціональних розладів ендокарда та субендокардіального простору лівого шлуночка у разі смерті внаслідок гострої ішемічної хвороби серця.
Вперше показано, що імунохроматографічне дослідження пізнього маркеру некроза міокарда – серцевого тропініна І у цільній крові трупів та виміри світлооптичної щільності кардіоміоцитів шлуночків серця померлих раптово внаслідок гострої ішемічної хвороби серця комплексно підвищують точність верифікації раптової кардіальної смерті.
Вперше, шляхом вивчення лазерно-поляриметричечних зображень, були виявлені дистрофічні зміни міокарда шлуночків у разі раптової смерті внаслідок гострої ішемічної хвороби серця, що може бути одним із критеріїв її веріфікації.
Практичне значення одержаних результатів. Шляхом статистичних досліджень доведена необхідність посилення уваги до підвищення тенденції смертності внаслідок гострої ішемічної хвороби серця серед осіб працездатного віку населення м. Луганська та Луганської області та пошуку нових організаційно-тактичних форм їх ранньої діагностики, впровадження нових стратегічних змін в управлінні суспільного здоров¢я.
Результати вивчення макро- та мікроскопічних змін міокарда та ендокарда шлуночків серця і їх мікроциркуляторного русла у випадках раптової серцевої смерті поглиблюють розуміння розвитку патоморфологічних процесів, можуть бути діагностичними критеріями, здатними підвищити точність і об’єктивність секційної діагностики причин раптової смерті.
Встановлена можливість післясмертного виявлення патологічних змін міокарда у випадках раптової смерті за зміною серцевого тропоніна І у цільній крові трупа, тест на визначення якого є швидким експрес-аналізом при проведенні диференційної діагностики раптової смерті внаслідок гострої ішемічної хвороби серця.
Розроблений спосіб визначення патологічних змін біологічних тканин, оснований на їх лазерній поляриметрії (патент України на корисну модель №26357 u МПК А61К 49/00, G01 33/00, заявлено 18.06. 2007, опубліковано 10.09 2007.- Бюл. №14), дозволяє без суттєвих матеріальних затрат поліпшити проведення діагностики раптової смерті внаслідок гострої ішемічної хвороби серця у практиці судово-медичної експертизи.
Результати вивчення гістологічних, біохімічних і біофізичних змін міокарда шлуночків та цільної крові померлих внаслідок гострої ішемічної хвороби серця комплексно підвищують точність і об¢єктивність секційної діагностики причин раптової смерті за результатами лабораторних досліджень.
Одержані результати діагностики раптової смерті внаслідок гострої ішемічної хвороби серця впроваджені у практичну роботу Луганського, Дніпропетровського, Харківського та Запорізького обласних бюро судово-медичної експертизи, у навчальну роботу кафедри патоморфології, судової медицини та медичного законодавства Луганського державного медичного університету.
Особистий внесок автора. Дослідження проведено на базі Луганського обласного бюро судово-медичної експертизи. Автором особисто вивчалися дані вітчизняної та закордонної літератури (258 джерел), проведений патентно-ліцензійний пошук, визначені мета й завдання дослідження, проводився збір матеріалу з 110 трупів людей молодого і зрілого віку, 12 експериментальних тварин (білих безпородних щурів), що утримувалися у віварію ЦНДЛ Луганського державного медичного університету, опис макро-мікропрепаратів, морфометрія, гістологічні, біохімічні та біофізичні дослідження, документування і математична обробка даних. Автором особисто проаналізовано одержані дані, порівняно окремі групи спостережень, співставлено дані власних досліджень з літературними джерелами, узагальнено результати та сформульовано висновки.
Апробація результатів дисертації. Результати дослідження докладені на науково-практичних конференціях “Сучасні методичні підходи до аналізу стану здоров’я” (Луганськ, 2007), “Актуальні питання експериментальної та клінічної медицини” (Суми, 2007), на сумісному засіданні кафедри патоморфології, судової медицини і медичного законодавства Луганського державного медичного університету, кафедри судової медицини Національної медичної академії післядипломної освіти імені П.Л. Шупика, кафедри патологічної анатомії та судової медицини Дніпропетровської державної медичної академії та Луганського обласного бюро судово-медичної експертизи 10 грудня 2007 року.
Публікації. За матеріалами дисертації опубліковано 9 праць: статті в журналах (затверджених переліком ВАК) – 6; тези конференцій - 2; 1 деклараційний патент на винахід України. 3 статті написані без співавторів, решта робіт - у співавторстві.
Структура та обсяг дисертації. Дисертацію викладено державною мовою на 151 сторінці, з яких 123 сторінках залікового принтерного тексту. Робота складається зі вступу, огляду літератури, загальної методики і основних методів долідження, 4 розділів власних досліджень, аналізу та узагальнення результатів дослідження, висновків, практичних рекомендацій та списку літературних джерел. Робота має 26 ілюстрацій, 13 таблиць та 9 графіків. Список використаної літератури містить 258 джерел, з них українською – 31, російською – 152, англійською – 68, французькою – 8 мовами.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Матеріал і методи дослідження. Для судово-медичного визначення походження судинної недостатності у випадках раптової смерті внаслідок ГІХС лабораторними методами були вивчені серця та цільна кров від 110 трупів людей зрілого віку (20-45 років). Із загальної кількості були взяті серця від 48 трупів здорових людей (контрольна група), які загинули внаслідок механічної травми, несумісної з життям без алкогольного фону.
З метою вивчення патоморфологічних, біохімічних та біофізичних змін міокарда та цільної крові були досліджені 62 сердець людей, які померли раптово внаслідок ГІХС без алкогольного фону. Усі зазначені об’єкти підлягали комплексному дослідженню: судово-медичному, гістологічному біохімічному та біофізичному - лазерній поляризаційній мікроскопії міокарда шлуночків.
Розтин трупів та їх судово-медичне дослідження проводили за загальновизнаним методом з евентерацією внутрішніх органів за Г.В. Шором. Вилучення матеріалу для дослідження проводилось у морзі бюро судово-медичної експертизи управління охорони здоров`я Луганської обласної державної адміністрації. Верифікація причин смерті проводилась у відповідності до МКХ-10.З метою єдиного уніфікованого підходу, що виключав явища аутолізу тканин, судово-медичне дослідження (експертиза) трупів і взяття секційного матеріалу та крові проводилось у терміни не пізніше чим 24 години після настання смерті. Причина смерті визначалась на підставі даних зовнішнього та внутрішнього дослідження органів і тканин, даних судово-токсикологічного, судово-гістологічного і судово-біохмічного досліджень.
З метою дослідження змін стану мітохондріального апарату скорочувальних кардіоміоцитів шлуночків при гострій ішемії міокарда було проведене експериментальне дослідження на 12 білих, безпородних щурах, які утримувались в умовах віварію ЦНДЛ Луганського державного медичного університету. В основу моделювання гострої ішемії міокарда були покладені рекомендації Н.О. Горчакової, І.С. Чекмана, А.І. Солов`йова (2001), за якими шляхом внутрішньоочеревинного введення щурам 1 ОД вазопресину або пітуїтрину (під контролем ЕКГ) створювався пітуїтриновий (вазопресиновий) коронароспазм.
Статистичний аналіз демографічних змін та смертності серед мешканців м. Луганська й Луганської області був проведений шляхом аналізу звітних документів бюро судово-медичної експертизи управління охорони здоров`я Луганської обласної державної адміністрації за термін 2002-2006 р.р. Всього було вивчено 7185 актів і висновків судово-медичних експертиз (досліджень) щодо вивчення причин смертності серед мешканців м. Луганська та 35085 актів і висновків судово-медичних експертиз (досліджень) щодо вивчення причин смертності серед мешканців Луганської області. Також були досліджені звіти статистичного відділу управління міського та обласного відділів охорони здоров’я за термін 2002-2006 роки. В зв¢язку з відсутністю необхідного об’єму кількісної і якісної інформації із зазначеної офіційної доповідно-облікової документації, на основі рекомендацій Г.Г. Автандилова, Т.А. Гевондяна (1983), були використані вибіркові дослідження показників смертності внаслідок ІХС.
Враховуючи складність розподілу кількості матеріалу за наведеними нижче методиками дослідження та морфометрії, яка включала вивчення на одному і тому ж серці таких різнорідних структурних тканин як епікард, міокард і ендокард, були використані принципи набору матеріалу дослідження з урахуванням всієї повноти вибірки (які відображали контроль, патологію – ГІХС), репрезентативних по відношенню до органа в цілому згідно рекомендацій А.Ю. Сопільника і співавт. (1982). Необхідний об¢єм вибірки був розрахований із 95% рівня безпомилкового судження (Р=0,95). Розподіл матеріалу за віком був проведений згідно класифікації, запропоновоної Л.К. Семеновою (1978).
Для більш адекватного та повного вирішення поставлених задач, був використаний широкий вибір морфологічних та лабораторних методик з обробкою отриманих результатів методами математичного аналізу.
Препарування було використане для відділення епікарда, ендокарда, вилучення субепікардіального жиру, для забору матеріалу із різних шарів шлуночків серця з наступним його вивченням гістологічними, біохімічними та біфізичними методами.
З метою виявлення особливостей ангіоархітектоніки термінальних відділів судинної системи серця при гострій ішемії міокарда, була застосована ін¢єкція кровоносного русла серця туш-желатиновою масою згідно з рекомендаціями Н.А. Джавахішвілі, М.Е. Комахідзе (1967). З метою виявлення архітектоніки внутрішньоорганної і субендокардіальної кровоносної системи (у тому числі і венозного субендокардіального сплетіння – так званих судин В`єссена-Тебезія), проводилась згідно з рекомендаціями А.А. Сушка , Л.В. Чернишенко (1963). Для одномоментного виявлення судин ГМЦР та ендотеліальних клітин ендокарда була використана методика внутрішньоорганної імпрегнації Ю.Є. Виренкова і співавт. (1982).
Для гістометричного вивчення тканин шлуночків серця використовували фарбування гістологічних зрізів гематоксилін-еозином по загальновизнаній методиці. Матеріал фіксували у 10% розчині нейтрального формаліну, розчинах Буена, Карнуа, обезводжувались у спиртах висхідної концентрації, після дегідратації заключали в парафін. На санному мікротомі МС-2 виготовляли зрізи тканин товщиною до 7 мкм і фарбували гематоксиліном та еозином, а також за Малорі за загальновизнаними методиками, залізним гематоксиліном за Ван-Гізон у поєднанні з резорцин-фуксином за Вейгертом, комбіноване забарвлення шляхом поєднання ШИК-реакції, колоїдним залізом за Хейлом та гематоксилін-оранжем. Поряд з цим, зрізи забарвлювались за методиками імпрегнації нітратом срібла по В.В. Купріянову (1969) та за методикою Н.З. Слінченка (1964).
Морфологічне дослідження мітохондріального апарата серця включало ультраструктурне вивчення й гістохімічне вивчення міокарда лівого шлуночка. Електронно-мікроскопічне дослідження проводили за схемою, запропонованою В.Я. Карупу, на електронному мікроскопі ЕМВ-100Б при прискорюючій напрузі 75 кВ і первинних збільшеннях від 2000 до 25000.
З метою встановлення особливостей патологічних змін ендокарда та субендокардіального простору шлуночків серця були застосовані скануюча електронна мікроскопія нативних та корозійних препаратів (СЕМНП і СЕМКП) згідно з рекомендаціями Караганова Я.Л. і співавт. (1983). Отримання сканограм з нативних препаратів міокарда проводилось після їх обезводнення, напилення йонами металу, вивчення під скануючим електронним мікроскопом (СЕМ) “Jeol-35”.
Загальний судово-токсикологічний аналіз проводився з метою визначення вмісту алкоголю у всіх трупів брали кров і сечу. Вивчались 5 мл крові і 5 мл сечі методом газо-рідинної хроматографії на хроматографах типу “Л-6”і “ХМ-8МД”. Особливості судово-медичної діагностики смертельних отруєнь етиловим алкоголем на основі визначення кількісного вмісту спиртів в крові і сечі оцінювались згідно з методичними рекомендаціями „Судово-медична діагностика смертельних отруєнь етиловим алкоголем” (2005).
Для пошуку непрямих доказів змін компонентів стінки шлуночків, отриманих при вивченні кровоносного русла серця в зв¢язку з порушенням обміну речовин при раптовій смерті внаслідок ГІХС, була проведена мікроспектрофотометрія, а саме - порівняльне кількісне вивчення вмісту нуклеїнових кислот (НК) в кардіоміоцитах (КМЦ) як в нормі, так і при ГІХС. Для цього був застосований метод фарбування НК в гістологічних препаратах при товщині зрізів 5 мкм галлоцианін-хромовими квасцями по Ейнарсону. Кількісні показники вмісту НК отримували за допомогою методу мікроспектрофотометрії цитоплазми і ядер КМЦ. Даний метод дозволяв проводити порівняльне дослідження на основі даних про світлооптичну щільність цитоплазми і ядер КМЦ при стандартних умовах гістохімічних реакцій та одинакової тощини зрізів. Мікроспектрофотометрію проводили на однопроменевому скануючому інтегруючому мікроспектрофотометрі (СИМ-2) при оптичному збільшенні 600х та довжині хвилі монохроматичного променя 560 мм. У кожному препараті визначали світлооптичну щільність цитоплазми і ядер 30 КМЦ. Площа вимірюваних ділянок складала 25 кв. мкм.
Виходячи з того, що гістологічне дослідження не завжди може підтвердити гострі ішемічні порушення в міокарді, оскільки для розвитку виразних морфологічних змін в серці необхідно не менше 6-12 годин, з метою об’єктивізації судово-медичного дослідження та встановлення реальної можливості післясмертного виявлення патологічних змін в міокарді у випадках раптової смерті внаслідок ГІХС було проведене вивчення маркеру некрозу – серцевого Тропоніна І в цільній крові. В основу принципу дії тесту на визначення сТn І покладено принцип хроматографії, при якій відбувається міграція нанесених антитіл до сТn І вздовж мембрани, реакція вказаних компонентів із реагентом, який заздалегідь нанесений на тестову ділянку мембрани і захоплює для селективного визначення сТn І в цільній крові, сироватці чи плазмі. В результаті реакції утворюється кольорова лінія, наявність якої свідчить про позитивний результат, в той час як відсутність лінії вказує на негативний результат тесту. Пороговий рівень визначення сТn І становить 0,5 нг/мл. Кількісний вміст сТn І чи ступінь його підвищення в крові, плазмі чи сироватці – тест не визначає. Тому він не може бути єдиним критерієм ГІХС, ІМ, а в сукупності з іншими лабораторними (перш за все – гістологічним) методами дослідження. Матеріалом дослідження була кров, узята із порожнин шлуночків серця 11 трупів осіб молодого та зрілого віку, що померли раптово, без наявних ознак насильницької смерті. Дослідження проводилося в умовах моргу Луганського обласного бюро судово-медичної експертизи.
З метою встановлення додаткових критеріїв диференціальної діагностики патологічних станів серця на основі власного способу визначення патологічних змін біологічних тканин (патент України на корисну модель №26357, 2007), було проведене дослідження лазерних поляриметричних зображень міокарда шлуночків серця осіб, загиблих внаслідок механічної травми (контрольна група - 7 осіб), та раптово померлих внаслідок гострої ішемічної хвороби серця ( 9 осіб).
Отримані дані опрацьовувались методами математичного аналізу для об¢єктивізації і кількісного описання властивостей як органа в цілому, так і його структурних компонентів: біометричний аналіз, варіаційна статистика. Розбіжності між груповими середніми величинами вважались вірогідними за умови довірчої імовірності безпомилкового судження не менш 0,95 (Р< 0,05) (Г.Г. Автандилов, 1984; Г.Ф. Лакін, 1990).
Результати дослідження та їх обговорення. За даними бюро судово-медичної експертизи управління охорони здоров'я Луганської обласної державної адміністрації за 5 років (2002-2006 р.р.) у м. Луганську серед померлих від причин, зумовлених ненасильницькою смертю, у 2250 (72,25%) випадках смерть наставала від ішемічної хвороби серця (ІХС), та інших захворювань системи кровообігу - 368 випадків (16,35%). Із них 1524 (67,7%) були чоловіки, 726 (32,3%) - жінки. Кількість померлих внаслідок захворювань системи кровообігу та, зокрема, від ІХС, збільшилась у 1,5 рази. Внаслідок гострої ішемічної хвороби серця (ГІХС) померло 164 (7,2%) осіб. Серед них - 134 (81%) чоловіків і 30 (19%) жінок. В основному, при розтинах, у померлих мали місце такі форми, як гостра коронарна недостатність з розвитком раптової коронарної смерті, гострий і повторний інфаркти міокарда різної локалізації, об'єму і площі поразнення серцевого м'яза. Основну масу (81%) померлих внаслідок гострої ішемічної хвороби серця складали особи чоловічої статі працездатного віку (рис. 1).
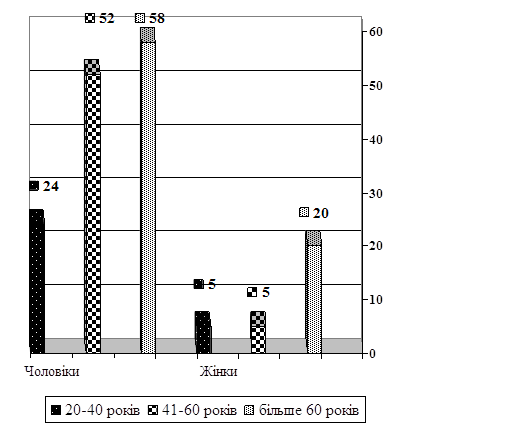
Рис. 1. Розподіл померлих мешканців м. Луганська у термін 2002-2006 р.р. внаслідок ГІХС за віком та статтю
Вивчення показників смертності внаслідок захворювань системи кровообігу серед населення Луганської області за останні 5 років (2002-2006 р.р.) дозволило встановити такі ж самі тенденції демографічних зрушень, як і серед мешканців м. Луганська. Серед померлих від причин ненасильницької смерті у 11161 (79,98%) випадків смерть настала від ІХС, та інших форм захворювань системи кровообігу. Із них 8527 (76,39%) були чоловіки, 2634 (23,61%) - жінки. Кількість померлих від захворювань системи кровообігу, та зокрема від ІХС - збільшилась у 1,5 рази. Загальна кількість померлих від ХІХС - 8028 (71,92%). З них 6149 (76,59%) чоловіків і 1879 (23,41%) жінок. У разі смерті внаслідок гострої ішемічної хвороби серця (ГІХС) померло 1116 (9,55%) осіб. Серед них: 917 (82%) чоловіків і 199 (18%) жінок. За віковими групами серед чоловіків померлі особи були розподілені таким чином: віком до 20 років - 22 випадки; 21-40 років – 360 випадків; від 41-60 років – 422 випадки; від 60 років і більше – 113 випадків. Серед жінок: віком до 20 років – 12 випадків; 21-40 років – 65 випадків; від 41-60 років – 97 випадків; від 60 років і більше – 25 випадків (рис. 2).
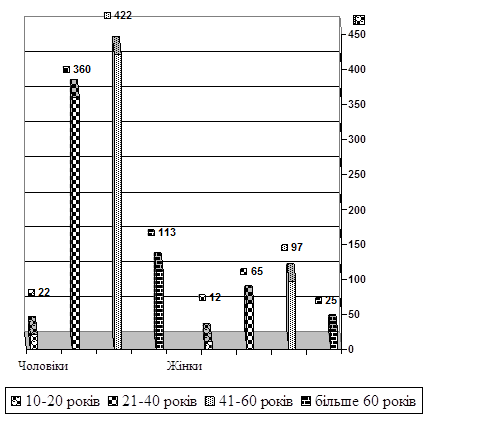
Рис. 2. Розподіл померлих мешканців Луганської області у термін 2002-2006 р.р. внаслідок ГІХС за віком та статтю
Таким чином, в структурі ненасильницької смерті серед померлих осіб м. Луганська та Луганської області значне місце належить різним формам ішемічної хвороби серця, зокрема гострій ішемічній хворобі серця. Серцево-судинні захворювання, у тому числі і ГІХС, суттєво "помолодшали". Основна маса померлих від ГІХС - це люди працездатного віку і домінуючим серед них були особи чоловічої статі, що ставить проблему захворювань системи кровообігу на перший план у вирішенні соціальних питань серед населення Луганської області.
З огляду на те, що однозначної думки відносно гістологічної оцінки уражень кардіоміоцитів при ГІХС, як ознак гострої коронарної недостатності, немає, нами й були дослідження особливостей гістологічних змін міокарда лівого шлуночка у разі раптової смерті внаслідок гострої коронарної недостатності. Так, в ділянках ішемії у разі раптової смерті внаслідок ГІХС безпосереднім об’єктом патологічних змін міокарда були кардіоміоцити (КМЦ) субендокардіального шару та ділянок ішемії і некрозу інтрамуральної локалізації. Для вказаних ділянок характерними були набряк, мікронекрози м’язових волокон. В останніх визначались гіперхромія та збільшення розмірів ядер, хвилеподібна деформація, ділянки міолізу та фрагментація м’язових волокон. Кардіоміоцити були потоншеними до 11,16±1,89 мкм, вони розділялись на повздовжні пучки міофібрил зі слабо виразною сарколемою, між якими знаходились брилки порушених м’язових волокон, що створювало передумови для фуксинофільної дегенерації та вакуольної дистрофії КМЦ. В м¢язових клітинах визначались ділянки атрофії міофібрил з брилками ліпофусцину у цитоплазмі. Також для карідоміоцитів вказаних ділянок лівого шлуночка виразною ознакою патологічних змін була втрата ними поперекової смугасті, яка добре виявлялась при імпрегнації гістологічних зрізів нітратом срібла. Для ділянок ішемії та некрозу міокарда характерним було нерівномірне його кровонаповнення. У переважній більшості досліджуваних випадків це явище спостерігалось на передній стінці лівого шлуночка, частіше субендокардіально. Такі особливості кровопостачання були зумовлені станом спазму артерій та дистонічно кровонаповнених вен. Так, при мікроскопічному вивченні виявлялись крупні артерії та їх гілки зі звивистістю та зменшенням просвіту внаслідок спазму та облітерації, зумовленої наявністю склеротичних змін та тромбоутворення. Зменшення ширини просвіту, спазм і плазматичне просякання стінки були визначені серед артеріол, прекапілярних артеріол міокарда. В ділянці ішемії міокарда мало місце достовірне зменшення до 0,06±0,002% питомої щільності артерій і збільшення до 0,17±0,06% питомої щільності вен; повнокров’я та стаз еритроцитів в артеріолах і гемокапілярах, спазм та плазматичне просякання їх стінок. Одним із проявів патологічних змін в ділянках ішемії і некрозу міокарда було збільшення у 2 рази числа гемокапілярів, ширина простору яких не перевершувала 2,0 мкм. Враховуючи відсутність у них еритроцитів та наявніть тільки компонентів плазми – вони були віднесені до плазматичних. Плазматичні ГК у полях зору відрізнялись підвищеною звивистістю, та довжиною, яка сягала 200,0-230,0 мкм й була зумовлена зменшеним числом поперечних міжкапілярних сполучень, що надавало капілярній сітці розріджений вигляд, що є проявом розвитку ішемії міокарда та створює передумови до його некротичних змін.
При дослідженні поверхні ендокарда шлуночків серця за допомогою скануючого електронного мікроскопа, було встановлено, що їх ендокардіальна поверхня представлена хвилястими складками у вигляді валикоподібних підвищень і заглиблень між ними, що в цілому, забезпечує “шорсткість” рел’єфу, призначеного для створення турбулентності кровотоку в порожнинах серця. У випадках смерті внаслідок ГКН, характерними були вогнищеві зміни рел’єфу ендокарда лівого шлуночка з ознаками погрубішання, фрагментарності та збільшення товщини складок, втрати ними хвилястості й придбанням лінійності напрямку. При вивченні поверхні ендокарда лівого шлуночка на імпрегнованих 0,25% нітратом срібла гістологічних зрізах було встановлено, що у разі раптової смерті внаслідок ГКН ендотеліальні клітини відрізнялися поліморфністю і ступінь зв’язності їх із сусідніми клітинами змінювався і коливався в діапазоні 4-8, тоді як в нормі він становив 6. Встановлено, що у випадках смерті внаслідок ГКН у сполучній тканині ендокарда лівого шлуночка вогнищево мали місце виразні патологічні зміни, проявами яких були погрубішання, втрата фібрілярності, фрагментарність.Їм відповідали вогнищеві контрактурні зміни каріоміоцитів, локалізованих в субендокардіальному шарі міокарда лівого шлуночка. Наведеними морфологічними змінами шарів міокарда і можна пояснити вогнищеві зміни рел’єфу ендокарда лівого шлуночка з погрубішанням, фрагментарністю та збільшенням товщини складок, значною втратою ними хвилястості і придбанням лінійності напрямку у разі смерті внаслідок ГКН.
З метою отримання більш повного обсягу інформації про особливості патологічних змін ендокарду лівого шлуночка у разі раптової смерті внаслідок ГКН були вивчені кровоносні судини субендокарділаьного шару. Був використаний метод ін’єкції метилметакрилату через коронарні артерії з наступною його полімеризацією і дослідженням у скануючому електронному мікроскопі. Встановлено, що в субендокардіальному просторі шлуночків мають місце зліпки судин у вигляді приплющених прямокутників із закругленими краями, орієнтовані за повздовжньою віссю. Глибина їх розповсюдження від ендотеліального шару до компактного міокарду складала 300,0-500,0 мкм. Рел’єф цих судин був рівний, з вдавленнями від ядер ендотеліальних клітин. Форма і розміри судин дозволили вважати їх капіляроподібними синусоїдами. Вони розташовувались в декілька ярусів. Між судинами кожного ярусу визначались з’єднання короткими капіляроподібними синусоїдами. Особливістю капіляроподібних синусоїдів лівого шлуночку було те, що вони мали числені, безпосередні сполучення з судинами мікроциркуляторного русла компактного міокарда, переважно з гемокапілярами та венулами. У разі смерті внаслідок ГКН капіляроподібні синусоїди субендокардіального простору, що локалізувались вогнищево, відрізнялись меншою довжиною, фрагментарністю, порідшенням сітки за рахунок зменшення числа поперечних сполучень, наявністю мікродеформацій, сплощень стінки. Окрім цього, у разі смерті внаслідок ГКН, у субендокардіальному просторі лівого шлуночка поряд з капіляроподібними синусоїдами виявлялись спазмовані гемокапіляри, ширина простору яких не перевищувала 2 мкм, а також значно розширені судини венозного сплетіння.
З метою дослідження особливостей змін мітохондріального апарату міокарда шлуночків у разі раптової смерті внаслідок гострої коронарної недостатності було проведене експериментальне дослідження на 12 білих, безпородних щурах. Ультраструктурне дослідження змін мітохондріального апарату міокарда шлуночків у разі раптової смерті внаслідок гострої коронарної недостатності визначило, що в різних зонах міокарда шлуночків щурів у саркоплазмі скорочувальних кардіоміоцитів закономірно спостерігався значний гетерогенітет мітохондрій, що відрізнялися щільністю та кількістю крист, ступенем їх орієнтації. Кількісна оцінка співвідношення між трьома типами мітохондрій показала, що найбільша частка високоенергетичних мітохондрій була характерною для інтрамуральних зон лівого и правого шлуночків, сягаючи 73% і 71% відповідно. При моделюванні гострої коронарної недостатності в міокарді шлуночків серця щурів спостерігалися різноманітні патологічні зміни, які залежали від розташування ділянок міокарда відносно зон ішемічного ушкодження, а також виявлялися неоднаково в різних досліджуваних локалізаціях стінки шлуночків. Зокрема, у ділянках шлуночкового міокарда, що були наближеними до зон ішемічного ушкодження, загальна гістологічна будова в цілому зберігалася, апоптотичні зміни спостерігалися рідко, проте на ультраструктурному рівні виявлялися численні патологічні зміни мітохондріального апарата. Кількісне дослідження показало, що у субендокардіальній зоні міокарда лівого шлуночка найбільшою мірою зменшувались щільність і кількість мітохондріальних крист (-74,1% і -71,4% відповідно; р<0,05). Також різко зменшувались середній об’єм мітохондрій, площа поверхні зовнішньої і внутрішньої мембран. У ділянках міокарда в зоні ішемії були наявні групи апоптотично загиблих кардіоміоцитів з характерними ознаками деструкції ядер і більшості органел, причому ушкодження мітохондрій мали найбільш значний ступінь. У цитоплазмі серцевих міоцитів, що знаходилися на початкових етапах апоптотичної загибелі, були виявлені групи мітохондрій з ознаками фрагментації зовнішньої і внутрішньої мембран, деструкції мітохондріальних крист, вакуолізації матрикса. Виявлялися поодинокі органели з конденсованими мембранними фрагментами, що свідчить про різке зниження рівня енергетичного метаболізму скорочувальних кардіоміоцитів за рахунок тотальної деструкції мітохондрій, серед яких найбільш уразливими були високоенергетичні мітохондрії.
З метою визначення лабораторно-діагностичних паралелей отриманих порушень тканинних компонентів, кровоносної системи шлуночків серця при смерті внаслідок ГІХС, нами було проведені дослідження біофізичних змін вказаних об¢єктів. Мікроспектрофотометрія, проведена нами з метою пошуку непрямих доказів змін компонентів стінки лівого шлуночка, отриманих при вивченні кровоносного та лімфатичного русла серця в зв¢язку з порушенням обміну речовин при раптовій смерті від ГІХС. Було проведене порівняльне кількісне вивчення вмісту нуклеїнових кислот в кардіоміоцитах в нормі та при ГІХС. Аналіз мікроспектрохімічного дослідження змін вмісту нуклеїнових кислот показав, що їх вміст у складі кардіоміоцитів лівого шлуночка при раптовій смерті внаслідок гострої ішемічної хвороби серця та у осіб контрольної групи відрізняється. Так, показники світлооптичної щільності ядер та цитоплазми КМЦ ЛШ при смерті внаслідок ГІХС достовірно перевершували такі ж показники контрольної групи, сягаючи 106, 87 ± 4,32 у.о та 71,83 ± 3,83 у.о. відповідно. Ці особливості можуть бути зумовлені зближенням анізотропних дисків та скороченням ізотропних білків, утворенням анізотропних конгломератів внаслідок фрагментації міофібріл у порушених КМЦ.
Для встановлення можливості посмертного виявлення патологічних змін в міокарді у випадках раптової смерті внаслідок ГІХС було проведене вивчення маркеру некрозу – серцевого тропоніна І (сТn І) в крові. Результати тестування порівнювались із результатами гістологічного дослідження серця померлих раптово. Було встановлено, що у 10 із 11 випадків позитивні результати на визначення сТn І повністю співпадали з виявленими гістологічними порушеннями міокарда у разі раптової смерті внаслідок ГІХС, а саме – з дистрофічними змінам кардіоміоцитів та появою білка у крові осіб, що померли раптово. Таким чином, за зміною серцевого тропоніна І, встановлена можливість посмертного виявлення патологічного процесу в міокарді у випадках раптової смерті внаслідок ГІХС. Тест для визначення сТn І у цільній крові є швидким імунохроматографічним експрес-аналізом для диференційної діагностики раптової смерті внаслідок ГІХС, ІМ. Однак, оскільки кількісний вміст сТn І чи ступінь його підвищення в крові тест не визначає, він не може бути єдиним критерієм ГІХС, а застосуватися в сукупності з іншими лабораторними (перш за все – гістологічним) методами дослідження.
Аналіз лазерно-поляриметричного дослідження виявив, що статистична структура розподілів інтенсивності поляризаційно контрастованих (00 – 900) поляризаційних зображень двопроменезаломлюючої архітектоніки (міозинові фібрили) гістологічних зрізів тканини міокарда суттєво відрізняється для її різних станів. Зокрема, середнє значення і дисперсія розподілів інтенсивності зображень гістологічних зрізів тканини міокарда при раптовій смерті внаслідок гострої ішемічної хвороби серця на 53% були меншими від значень аналогічних статистичних моментів розподілів інтенсивності зображень контрольної групи тканин міокарда. Асиметрія та ексцес розподілів інтенсивності в зображенні гістологічних зрізів тканини міокарда у разі смерті внаслідок гострої ішемічної хвороби серця були у 3-3,5 рази більшими від значень аналогічних статистичних моментів розподілів інтенсивності зображень контрольної групи тканин міокарда. Одержані результати можна пов’язати з тим, що вплив патологічних (ішемічних, некротичних) змін виявлявся у розслабленні та дистрофічних змінах тканини міокарда. Такі процеси призводять до загального зменшення двопроменезаломлення міозинових фібрил. В результаті чого знижується загальний рівень просвітлення і поява вогнищ затемнення у зображеннях міокарда шлуночків, які були одержані для перехрещених поляризатора і аналізатора, що може бути одним із критеріїв верифікації раптової смерті внаслідок гострої ішемічної хвороби серця.
ВИСНОВКИ
1. Вивчення показників смертності населення м. Луганська і Луганської області за останні 5 років (2002 – 2006 р.р.) засвідчило, що в структурі ненасильницької смерті від 72,25% до 79,98% складали випадки смерті внаслідок ішемічної хвороби серця: хронічної (76,35% і 71,92%) та гострої ішемічної хвороби серця (7,2% та 9,55%). Основну масу (77,7%) померлих внаслідок гострої ішемічної хвороби серця складали особи чоловічої статі молодого та зрілого віку.
2. У випадках раптової смерті внаслідок гострої ішемічної хвороби серця найчастішою локалізацією ішемії міокарда лівого шлуночка були субендокардіальні та інтрамуральні ділянки його стінки, в яких визначалось достовірне зменшення до 11,16±1,89 мкм товщини кардіоміоцитів, їх хвилеподібна деформація, фрагментація, втрата ними поперечної смугастості, гіперхромія та збільшення розмірів ядер, зменшення ядерно-цитоплазматичного індекса. В ділянці ішемії міокарда мало місце достовірне зменшення до 0,06±0,002% питомої щільності артерій і збільшення до 0,17±0,06% питомої щільності вен; повнокров’я та стаз еритроцитів в артеріолах і гемокапілярах, спазм та плазматичне просякання їх стінок; збільшення у 2 рази числа плазматичних гемокапілярів, що є проявом розвитку ішемії міокарда та створює передумови до його некротичних змін.
3. За допомогою скануючої електронної мікроскопії нативних препаратів міокарда було виявлено, що у разі смерті внаслідок гострої ішемічної хвороби серця у лівому шлуночку мали місце: ділянкове потовщення, фрагментарність та збільшення товщини складок ендокарда, втрата ними хвилястості і набуття лінійності напрямку, виразні патологічні зміни клітинних і неклітинних компонентів сполучної тканини субендокардіального шару, яким відповідали ділянкові контрактурні зміни підлеглих м’язових волокон міокарда, що є проявами морфо-функціональних розладів ендокарда лівого шлуночка серця.
4. У випадках раптової смерті внаслідок гострої ішемічної хвороби серця в ділянках ішемії субендокардіального простору лівого шлуночка виявлялось зменшення довжини капіляроподібних синусоїдів, наявність мікродеформацій та сплощень їх стінки, наслідком чого могло стати погіршення кровопостачання як субендокардіального простору, так і ендокарда шлуночка.
5.При експериментальному моделюванні гострої коронарної недостатності у щурів в зоні ішемії міокарда шлуночків та в ділянках, наближених до неї, підтверджене різке зниження рівня енергетичного метаболізму скорочувальних кардіоміоцитів за рахунок тотальної деструкції мітохондрій, серед яких найбільш уразливими були високоенергетичні мітохондрії.
6. Показники світлооптичної щільності ядер (106,87±4,32 у.о.) та цитоплазми (71,83±3,83 у.о.) кардіоміоцитів лівого шлуночка у осіб, що померли раптово, внаслідок гострої ішемічної хвороби серця, достовірно перевершували аналогічні показники у осіб контрольної групи, що свідчить про можливість виявлення ознак некрозу міокарда за даними мікроспектрофотометрії.
7. Проведення імунохроматографічного тесту на визначення серцевого тропоніна І у крові трупів, у випадках раптової смерті внаслідок гострої ішемічної хвороби серця, виявило позитивну реакцію на наявність дистрофічних змін міокарда, що може вказувати на його значну лабільність та бути додатковим критерієм диференційної діагностики.
8. У разі раптової смерті внаслідок гострої ішемічної хвороби серця, асиметрія та ексцес розподілів інтенсивності у лазерних поляризаційних зображеннях гістологічних зрізів міокарда лівого шлуночка у 3-3,5 рази перевершували аналогічні показники у осіб контрольної групи, що свідчить про дистрофічні зміни міокарда і може бути одним із критеріїв верифікації раптової смерті внаслідок вказаної патології.
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ
1. Судово-медичне визначення причини раптової смерті внаслідок гострої ішемічної хвороби серця повинне здійснюватись шляхом комплексного використання патоморфологічних, біохімічних та біофізичних методів дослідження.
2. При гістологічному дослідженні сердець померлих раптово з підозрою на гостру коронарну недостатність, з метою виявлення ознак ГІХС, необхідно проводити комбіноване забарвлення гістологічних зрізів шляхом поєднання ШИК-реакції, гематоксилін-оранжем, що передбачає добре виявлення і диференціацію клітинних елементів: кислих мукополісахаридів, глікозаміно-гліканів, глікогену, базальних мембран, ретикулярних волокон, глікопротеїдів.
Похожие работы
... ії й алергології”. Київ-Миргород 19-23 листопада, 2007. - Миргород. – С.82. (Здобувачем зібрано фактичний матеріал лабораторних досліджень стану імунної системи при РКС й узагальнено результати). АНОТАЦІЯ Мішин М.Ю. Судово-медична діагностика раптової кардіальної смерті за допомогою комплексу лабораторних досліджень. – Рукопис. Дисертація на здобуття наукового ступеня кандидата медичних на
... лікувально-оздоровчих заходів і підвищення якості активних методів лікування; 3) запровадження у практику роботи сучасних методів профілактики, діагностики та лікування хворих на основі досягнень медичної науки і передового досвіду діяльності лікувально-профілактичних закладів; 4) зниження захворюваності з тимчасовою втратою працездатності серед працюючих; 5) оздоровлення осіб, які часто і ...
... хребта. Розглянуті технології, мережеві протоколи і програмне забезпечення можуть бути використані для вирішення проблем телемедицини і в інших клінічних областях. Експертна система "Лазерна рефлексотерапія" Застосування експертних систем, призначених для вирішення завдань діагностики і лікування захворювань, особливо ефективне в тих випадках, коли врахування дуже великого обсягу вхідної і ...
... , 1985. 3. Атлас для експериментального дослідження в психічній діяльності людини. /Під ред. И. А. Поліщука, А. Е. Видренко. – Київ, 1980. 4. Банщиків В. М., Гуськов В. С., Мягков И. Ф. Медична психологія. – М., 1967. 5. Банщиків В. М. і ін. Методичний посібник до практичного курсу психіатрії на лікувальному факультеті медичного інституту. – М., 1962. 6. Банщиків ...

0 комментариев