Навигация
Диазометан не пригоден, так как приводит к о-метиловому эфиру четвертичной соли, частично образующимся и при метилировании иодистым метилом
1. Диазометан не пригоден, так как приводит к о-метиловому эфиру четвертичной соли, частично образующимся и при метилировании иодистым метилом.
2. Лучше для этих целей использовать хлористый или бромистый метил, диметилсульфат или, лучше, метиловый эфир бензолсульфокислоты, так как в этом случае нет необходимости в поглощающих автоклавах (СН3Вr – 18 атм.; СН3Сl – 65 атм.).
Очистка получаемого антипирина обычно осуществляется 2-3 кратной перекристаллизацией из воды; может быть использована перегонка в вакууме (200-205 оС при 4-5 мм, 141-142 оС в вакууме катодного свечения).
Антипирин – кристаллы слабогорького вкуса, без запаха, хорошо растворим в воде (1:1), в спирте (1:1), в хлороформе (1:15) хуже в эфире (1:75). Дает все характерные качественные реакции на алкалоиды. С FeCl3 дает интенсивное красное окрашивание. Качественной реакцией на антипирин является изумрудная окраска нитрозоантипирина.
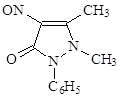
Жаропонижающее, обезболивающее, как местное кровеостанавливающее.
Изучена масса разнообразных производных антипирина.
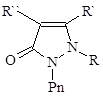
Из всех производных только амидопирин и анальгин оказались ценными анальгетиками, превосходящими по свойствам антипирин.
4 .Технология синтеза антипирина Описание основных стадий процесса.
В эмалированный реактор с масляным обогревом загружают фенилметилпиразолон и проводят его сушку в вакууме при 100 оС до полного удаления влаги. Затем повышают температуру до 127-130 оС и к раствору фенилметилпиразолона приливают метиловый эфир бензосульфокислоты. Температура реакции не выше 135-140 оС. По окончании процесса реакционную массу передавливают в кристаллизатор, куда загружают небольшое количество воды и охлаждают до 10 оС. Выпавший бензосульфонат антипирина отжимают и промывают на центрифуге. Для выделения антипирина, эту соль борабатывают водным раствором NaOH, полученный антипирин отделяют от раствора соли переосаждают в изопропиловом спирте, антипирин очищают перекристаллизацией из изопропилового спирта. Выпускается в порошках и таблетках по 0,25 г.
Амидопирин.
Если антипирин был открыт при изучении алкалоида хинина, то переход от антипирина к амидопирину связан с исследованием морфина.
Установление N-метильной группы в структуре морфина дало основание полагать, что обезболивающее действие антипирина может быть усилено введением в ядро еще одной третичной аминогруппы.
В 1893 г. был синтезирован – 4-диметиламиноантипирин – амидопирин, который по силе в 3-4 раза превосходит антипирин. В последние годы используется только в сочетании с другими препаратами, ввиду нежелательных явлений: аллергии, угнетения кроветворения.
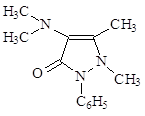
1-Фенил-2,3-диметил-4-диметиламинопиразолон-5 (в воде 1:11).
Качественная реакция с FeCl3 – сине-фиолетовое окрашивание. Получение амидопирина.
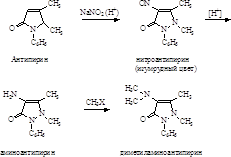
Разработано большое число методов проведения процессов восстановления и метилирования. В производственных условиях отдается предпочтение следующим:
1. Использование антипирина в виде бензолсульфокислоты:
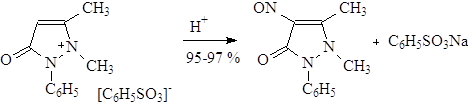
Необходимая для нитрования азотистая кислота образуемая в этом случае при взаимодействии NaNO2 с бензолсульфокислотой, связанной с антипирином.
Восстановление нитрозоантипирина в аминоантипирин (св.желтые кристаллы с Тпл.109°) проводится с высокими выходами при помощи сульфитно-бисульфитной смеси в водной среде:

Механизм реакции.
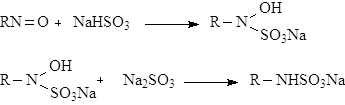
Имеются разработанные методы восстановления нитрозоантипирина сероводородом, цинком (пыль), в CH3COOH, и др.
Очистка аминоантипирина и выделение его из различных растворов осуществляется через бензилиденовое производное (светложелтые, блестящие кристаллы, tпл 172-173 оС), легко образуется при взаимодействии аминоантипирина с бензальдегидом:
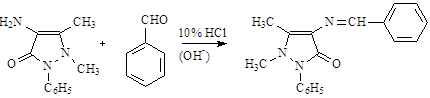
бензилиденаминоантипирин – является исходным продуктом в синтезе анальгина.
Метилирование аминоантипирина наиболее экономичным путем достигается при помощи смеси CH2O - HCOOH.
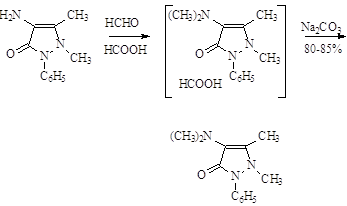
Механизм реакции метилирования:
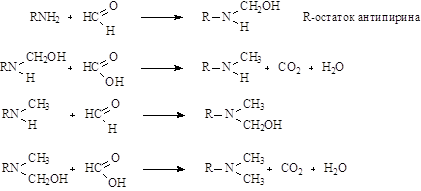
При таком способе метилирования, избегают образования четвертичных аммониевых соединений, образующихся при использовании в качестве метилирующего агента галоидозамещенного диметилсульфоната.
При использовании галоидамина, образующееся четвертичное соединение может быть превращено в автоклаве.
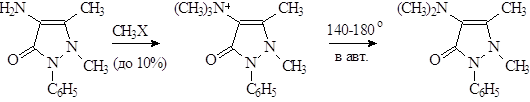
Для выделения и очистки амидопирина применяется многократная перекристаллизация из изопропилового или этилового спирта.
5. Технология синтеза антипирина
Химизм процесса

Описание основных стадий процесса.
Водную суспензию соли антипирина передавливают в нейтрализатор, охлаждают до 20 оС и постепенно приливают 20%-раствор NaNO2. Температура реакции не должна превышать 4-5 оС. Полученную суспензию изумрудно-зеленые кристаллы нитрозоантипирина и промывают холодной водой. Кристаллы загружают в реактор, куда добавляют бисульфитно-сульфатную смесь. Смесь сначала выдерживают 3 ч. при 22-285оС, затем 2-2,5 ч. при 80 оС. раствор натриевой соли передавливают в гидролизатор. Получают гидролизат аминоантипирина, который подвергают метилированию в реакторе смесью формальдегида и муравьиной кислоты. Выделяют амидопирин из муравьинокислой соли, обработкой раствора соли при 50 оС раствором соды. После нейтрализации амидопирин всплывает в виде масла. Отделяют масляный слой и переводят его в нейтрализатор, где перекристаллизовывают из изопропилового спирта.
Анальгин.
Структурная формула анальгина
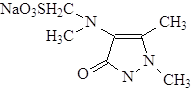
1-Фенил-2,3-диметилпиразолон-5-4-метиламинометиленсернокислый натрий.
Эмпирическая формула – C13H16O4N3SNa · H2O – белый, слегка желтоватый кристаллический порошок, легко растворим в воде (1:1,5), трудно в спирте. Водный раствор прозрачен и нейтрален на лакмус. При стоянии желтеет, не утрачивая активности.
Анальгин – лучший препарат среди соединений пиразолонового ряда. Превосходит все анальгетики пиразолонового ряда. Малотоксичен. Анальгин входит в состав многих препаратов
Его высшая разовая доза –1 г, суточная –3 г.
Промышленный синтез анальгина основан на двух химических схемах.
1).
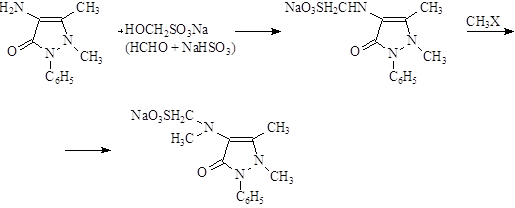
2). Производственный способ получения из бензилиденаминоантипирина.
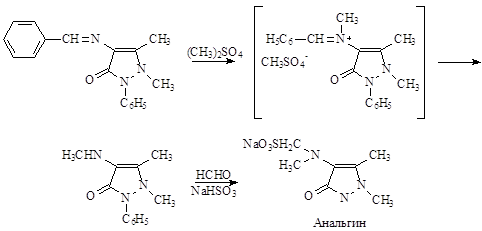
Эмпирическая формула – C13H16O4N3SNa · H2O – белый, слегка желтоватый кристаллический порошок, легко растворим в воде (1:15), трудно в спирте. Водный раствор прозрачен и нейтрален на лакмус.
Анальгин – лучший препарат среди соединений пиразолонового ряда. Превосходит все анальгетики пиразолонового ряда. Малотоксичен.
Описание технологического процесса.
В эмалированный реактор с масляным обогревом загружают фенилметилпиразолон и проводят сушку в вакууме при 100 оС до полного удаления влаги. Температуру поднимают до 127-130 оС и к раствору ФМП приливают метиловый эфир бензосульфокислоты. Температура реакции 135-140 оС. По окончании процесса реакционную массу передавливают в кристаллизатор, куда загружают небольшое количество воды и охлаждают до 10 оС. Выпавший бензолсульфонат антипирина промывают на фильтре и подают в следующий реактор для проведения реакции нитрозирования. Там смесь охлаждают до 20 оС и постепенно приливают 20%-ный раствор NaNO2. Температура реакции 4-5 оС. Полученную суспензию изумрудно-зеленых кристаллов фильтруют на вакуум-фильтре и промывают холодной водой. Кристаллы загружают в реактор, куда добавляют бисульфитно-сульфатнцю смесь, которую сначала выдерживают 3 часа при 22-25 оС, затем еще 2-2,5 часа при 80 оС. Образовавшуюся соль передавливают в реактор омыления, где обрабатывают раствором NaOH, в результате чего образуется динатриевая соль сульфоаминоантипирина.
Полученная соль передавливается в реактор для метилирования диметилсульфатом. ДМС подается в реактор из мерника. Реакция идет при 107-110 оС в течение 5 часов. По окончании реакции продукт реакции отделяют от Na2SO4 на фильтре 15. Раствор натриевой соли передавливают в реактор и гидролизуют серной кислотой при 85 оС в течение 3 часов. По окончании реакции к реакционной смеси добавляют NaOH для нейтрализации кислоты. Температура реакции не должна превышать 58-62 оС. Полученный монометиламиноантипирин отделяют от Na2SO4 на фильтре, и передают в реактор метилирования. Метилирование проводят смесью формальдегида и бисульфита натрия при 68-70 оС. В результате реакции получается анальгин, который затем очищают.
Раствор упаривают. Анальгин перекристаллизовывают из воды, промывают спиртом и сушат.
II спсоб – через бензилиденаминоантипирин..
Список использованных источников:
1. Лекарственные средства, применяемые в медицинской практике в СССР /Под ред. М.А. Клюева. – М.: Медицина, 1991. – 512с.
2. Лекарственные средства: в 2-х томах. Т.2. – 10 – изд. стер. - М.: Медицина, 1986. – 624 с.
3. Основные процессы и аппараты химической технологии: пособие по проектированию / Г.С. Борисов, В.П. Брыков, Ю.И. Дытнерский и др., 2-е изд., перераб. И дополн. М.: Химия, 1991. – 496 с.
Похожие работы
... . Арахидоновая кислота находится в мембране клетки, метаболизируеюся по двум путям: лейкотриеновый и эндотелиальный. На уровне эндотелия, действует фермент - циклооксигеназа, который угнетают ненаркотические анальгетики. По циклооксигеназному пути образуются простогландины, тромбоксаны, простациклины. Механизм анальгезии связа с угнетением циклооксигеназ и уменьшения образования простогландинов - ...
... . По анальгетической активности препарат не уступает морфину при меньших побочных эффектах и меньшей способности к развитию толерантности и физической зависимости.Производные пиперидина. Идея создания наркотических анальгетиков, производных пиперидола, возникла в результате исследования химического строения фенантренизохинолиновой структуры морфина и других алкалоидов, содержащихся в опии. Общая ...
... группы: 1) анальгетики наркотические — морфин, близкие к нему другие опиаты, а также опиоиды — синтетические соединения (промедол, фентанил, трамадол, бупренорфин, пентазоцин и др.); 2) анальгетики ненаркотические, в основном из группы противовоспалительных и жаропонижающих средств (амидопирин, анальгин, натрия салицилат, ацетилсалициловая кислота, фенацетин и др.). Анальгетики первой группы ...
... анальгетиков силой эффекта, с другой стороны ненаркотические анальгетики не вызывают лекарственной зависимости. В 1863 году английский фармацевт Сертюрер выделил морфин. Классификация наркотических анальгетиков: производные алкалоидов опия (морфин, омнопон, кодеин, этилморфина гидрохлорид). Производные дифенилпиперидина (промедол, фентанил). Производные дефинметана (дипидолор). Производные ...

0 комментариев