Навигация
Биохимические методы исследования сыворотки крови
2.2.5 Биохимические методы исследования сыворотки крови
Современная медицина располагает большими возможностями для детального изучения строения и функционирования органов и систем, быстрой и точной диагностики каких-либо отклонений от нормы или заболеваний. Методы лабораторной диагностики в большей степени отражают проблемы на клеточном и субклеточном уровне, но в то же время позволяют судить о «поломках» в конкретном органе. Чтобы увидеть, что происходит в данном органе, используют, в частности, инструментальные методы диагностики.
Кровь для биохимического анализа берут из вены. Затем определяют множество показателей, позволяющих контролировать состояние различных органов и систем, а также косвенно оценивать состояние организма в целом.
Биохимический анализ сыворотки крови проводили с помощью автоматического анализатора «SMARTLAB», Япония - этот аппарат позволяет выполнять биохимические исследования субстратов, ферментов, липидов с использованием следующих режимов измерений: конечная точка, кинетические измерения, двухточечная кинетика, бихроматические измерения. В комплект прилагается перечень кассет, для определения и мониторирования сердечно-сосудистых заболеваний (CHOLESTECH LDX).
«SMARTLAB» программируется для выполнения 48 методик, параметры которых постоянно хранятся в памяти прибора. Дополнительно можно создать 6 профилей (группа тестов), каждый из которых может содержать до 16 разных методик. В дальнейшем оператор лишь выбирает для данного пациента нужные тесты или профили, обозначает позиции для стандартов, контролей и пациентов и проводит подготовку реагентов.
«SMARTLAB» - свободно и легко настраивается на любые типы реагентов.
Приготовление реагентов и их хранение. Для работы рекомендуется использовать свежеприготовленные реагенты. Реагенты переливаются во флаконы, которые следует после каждого использования тщательно промывать дистиллированной водой и высушивать. Реагенты хранящиеся в холодильнике, следует выдерживать при комнатной температуре перед работой не менее 15 минут.
Обработка проб. Проверить все пробы после центрифугирования на наличие остатков фибрина.
Тип измерения: двухточечная кинетика. Концентрация или активность в пробе рассчитывается путем умножения изменения оптической плотности за фиксированный промежуток времени на фактор, заданный пользователем или рассчитанный по калибратору. Данный тип измерений применяется при определении креатинина, мочевины кинетической, кислой фосфатазы и др.
Кинетические методики (определение активности ферментов):
1) кинетика по фактору: активность в пробе рассчитывается путем умножения среднего значения изменения оптической плотности за 1 минуту на фактор, заданный пользователем. Таким образом исследуются все ферменты;
2) кинетика по стандарту - активность в пробе рассчитывается путем умножения среднего значения изменения оптической плотности за 1 минуту на фактор, рассчитанный по калибратору с известной активностью.
Конечная точка (определение содержания субстратов): по стандарту - концентрация в пробе рассчитывается путем умножения оптической плотности пробы на фактор, представляющий собой отношение концентрации стандарта к его оптической плотности; по фактору - фактор можно задать в параметрах теста и проводить измерения проб, рассчитывая результат по фактору.
Расчет концентрации по заданной калибровке. Концентрация в пробе рассчитывается по линейной калибровочной зависимости, которая хранится в памяти прибора.
Построение нелинейной калибровки. Построение калибровочной зависимости производится заранее при помощи 6-ти или менее стандартных растворов с возрастающими или убывающими значениями концентраций. Также поступают и при исследовании гормонов.
Измерение оптической плотности. Измерение оптической плотности проб в реакционных кюветах при длине волны, заданной пользователем в диапазоне от 0 до 2,5 ед. оптической плотности (ОП).
Конечная точка с бланком по пробе. Измерения с бланком по пробе рекомендуется использовать для уменьшения влияния интерферирующих веществ на результат анализа – пробы липемические, иктеричные, с гемолизом. Определение билирубина, железа и др. методики выполняются с бланком по пробе.
Измерение оптической плотности с бланком по пробе. Измерение оптической плотности проб в реакционных кюветах, имеющих бланк по пробе при длине волны, заданной пользователем в диапазоне от 0 до 2,5 ед. ОП. Результат получается путем вычисления ОП холостой пробы из величины ОП пробы [46].
2.2.6 Метод статистической обработки результатов
Для характеристики и оценки физиологических данных необходимо сравнение цифровых величин, получаемых при исследовании, с величинами, свойственными практически здоровому организму. Это сравнение позволяет решить вопрос: протекает данный процесс нормально или имеет отклонение от его обычного течения. Получаемые величины всегда имеют разброс параметров, поэтому после проведения эксперимента встает задача – на базе полученных числовых данных сделать обоснованные, надежные выводы относительно исследованного процесса в целом.
В своей работе мы использовали компьютерную обработку полученных данных, по программе «Биостатистика».
Выбирали нужный критерий, производили ввод данных в таблицу, для вычисления результата нажимали кнопку суммировать, после чего появлялись цифровые значения на экране.
Критические точки t-критерия Стьюдента при различных уровнях значимости сравнивали с таблицей Г.Ф. Лакина (1990) [47], полученные данные заносили в таблицы. Уровень значимости определяет ту вероятность ошибочного вывода о различии средних арифметических, которую исследователь считает допустимой, в условиях данного опыта.
Порядок пользования таблицей критических значений критерия Стьюдента состоит в следующем: вычисленное значение коэффициента достоверности сравнивают с табличными значениями, находящимися в строке, соответствующей данному числу степеней свободы. Если t-фактическое больше любого табличного, то вывод о достоверности разницы средних можно считать практически абсолютно надежным. Если значение t-фактического больше табличного, соответствующего уровню Р1, и меньше второго табличного значения, соответствующего уровню Р2, то достоверность различий можно считать установленной лишь с точностью Р1<0,05. Если найденное значение коэффициента Стьюдента меньше табличного, то вывод о различии средних для данного уровня Р неправомочен.
Обработанные таким образом данные позволяют сделать вывод о случайности или закономерности полученного экспериментального результата; сделать анализ на основании сопоставления средних арифметических изучаемой функции у опытной группы по сравнению с контрольной [47].
ГЛАВА 3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Артериальная гипертензия является одним из факторов, способствующих развитию сердечной недостаточности. Знание механизмов развития, методов диагностики и профилактики, выбор патогенетически обоснованной тактики лечения, безусловно, уменьшит количество больных с артериальной гипертензией, следовательно, и случаев возникновения сердечной недостаточности. И часто единственным способом узнать имеется ли повышенное артериальное давление, является его измерение [10, 48].
Фактором повышения артериального давления в начальном периоде гипертонической болезни (период становления), является возрастание активности симпатико-адреналовой системы. В этом периоде формируется гиперкинетический тип кровообращения, для которого характерно повышение сердечного выброса при малоизмененном общем периферическом сопротивлении. В то же время уже в начальном периоде гипертонической болезни иногда повышается сосудистое сопротивление в почках [8, 48].
Первым этапом нашей исследовательской работы явилось определение и оценка ИМТ у больных, страдающих артериальной гипертонией I, II степени и ишемической болезнью сердца (табл. 1).
Как видно из таблицы 1 у мужчин, имеющих в анамнезе АГ II степени и ИБС, ИМТ был выше физиологической нормы и контрольных величин (Р<0,05; Р<0,001).
Кроме того, анализ результатов таблицы 1 выявил достоверное (Р<0,001) повышение ИМТ у лиц, в анамнезе которых имеется ИБС, по сравнению с пациентами страдающими АГ І степени.
Таким образом, оценка ИМТ у больных мужчин выявила повышение данного параметра по мере тяжести течения заболевания.
Так у пациентов, имеющих ИБС, ИМТ выше, чем у страдающих АГ II степени, а у больных АГ II степени ИМТ выше, чем у страдающих АГ I степени.
Наше исследование подтвердило, что лишний вес вызывает метаболические сдвиги в организме и ведет к возникновению тяжелой патологии. При отсутствии контроля этих сдвигов может прогрессировать ожирение, артериальная гипертония, распространенный атеросклероз, ИБС.
Таблица 1
Индекс массы тела мужчин г. Катайска, больных артериальной гипертонией I, II степени и ишемической болезнью сердца, M±m
| Группы Показатель | Условно здоровые (n=20) | АГ I степени (n=20) | АГ II степени (n=28) | ИБС (n=20) |
| ИМТ N - 18,5-24,9 кг/м² | 24,41±0,41 | 24,63±0,69 | 26,08±0,61 * | 28,18±0,08 ***; ΔΔΔ |
Примечание: n - количество человек в выборке; N – норма [42]; ИМТ - индекс массы тела; АГ - артериальная гипертония; ИБС - ишемическая болезнь сердца; достоверность различий по сравнению с условно здоровыми лицами - * - Р<0,05; *** - Р<0,001; достоверность различий по сравнению с больными АГ I степени - ΔΔΔ - Р<0,001.
Наши данные согласуются с рядом исследований, в частности Фремингемского, которое показало, что более 70% пациентов с АГ имеют избыточную массу тела и более 45% лиц с избыточной массой страдают АГ, причем в 70% случаев АГ у мужчин определенно связано с ожирением. На каждый дополнительный килограмм массы тела риск развития АГ повышается на 5% [49]. Выше сказанное в определенной степени может объяснить достаточно быстрое прогрессирование заболевания. Если принять меры по снижению массы тела на 5-10%, то это приведет к клинически значимому уменьшению выраженности метаболических факторов риска развития АГ и ИБС [50].
Развитию ожирения может способствовать ряд факторов, включая генетическую предрасположенность, эндокринные факторы, психологический тип и уровень физической активности пациента. Прирост массы тела становится неизбежным, когда организм получает с пищей больше энергии, чем расходует; данный механизм имеет наибольшее значение.
Наличие генетической предрасположенности к ожирению подтверждает тот постулат, что это - болезнь. Поскольку данное заболевание длится всю жизнь, оно требует продолжительного лечения, которое должно начинаться с немедикаментозных методов - таких, как диета, физические упражнения и изменения в образе жизни [4].
Ожирение следует отличать от избыточной массы тела. Его можно классифицировать несколькими способами, например, по фенотипу (на основании расположения избыточного жира), или по тяжести - с помощью индекса массы тела; последний из этих двух методов классификации пропагандирует Всемирная Организация Здравоохранения [51].
Для того чтобы адекватно распоряжаться жировыми запасами и поддерживать постоянство массы тела, жировая ткань и гипоталамус обмениваются сложными гормональными сигналами, от которых зависят аппетит, усвоение пищи, расход энергии и вес. Жировая ткань, составляющая в норме 15-20% от массы тела у мужчин и 20-25% у женщин, это не инертный складской отсек организма, а метаболически активное образование, где постоянно протекают балансовые процессы липогенеза и липолиза, контролируемые нейроэндокринной системой. Правильное взаимодействие жировой ткани и гипоталамуса обеспечивает эффект липостата (система, контролирующая постоянство веса тела), то есть гомеостаз массы тела. Тучность как болезнь не сводится к причинению косметического, психологического и физического дискомфорта. Она сокращает продолжительность жизни, увеличивая смертность, которая среди лиц с повышенным индексом массы тела, в среднем, возрастает на 50%.
Минимальная смертность наблюдается при значениях индекса массы тела от 23 до 25 кг/м².
Увеличение ИМТ > 25 кг/м² - это пациенты, предрасположенные к ожирению. Под ожирением понимают нарушение обмена веществ, характеризующееся избыточным объемом жировой ткани, которое обладает тенденцией к прогрессированию в отсутствии специфической терапии.
Процессы в жировой ткани энергозатратны, это приводит к увеличению потребности тканей в кислороде и повышению артериовенозной разницы парциального давления кислорода. В дальнейшем развивается увеличение диастолического давления в левом желудочке, что ведет к развитию артериальной гипертонии.
Дальнейшим этапом нашей исследовательской работы была оценка распределения больных по индексу массы тела, в зависимости от вида патологии (рис. 2 - а, б, в, г).
Среди контрольной группы мужчин было выявлено, что 65% имели нормальную массу тела (ИМТ от 18,5 до 24,9 кг/м²), а 35% - избыточную массу тела (ИМТ от 25 до 29,9 кг/м²).
Среди мужчин, больных артериальной гипертонией I степени, 65% имели нормальную массу тела, 25% - избыточную массу тела и 10% - I степень ожирения (ИМТ от 30 до 34,9 кг/м2).
Далее было определено, что у пациентов, страдающих артериальной гипертонией II степени, нормальный вес имели 29% больных, избыточную массу тела и ожирение I степени соответственно - 60% и 11% мужчин.
Как видно из рисунка 1 у мужчин, страдающих ИБС, распределение по ИМТ было следующее: 80% пациентов имели избыточную массу тела и 20% - ожирение I степени.
а)
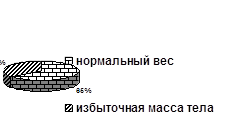
б)

в)
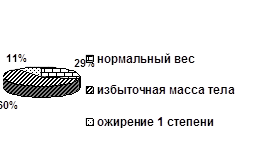
г)

Рис. 2. Оценка индекса массы тела мужчин, имеющих различные сердечно-сосудистые заболевания.
Примечание: а - условно здоровые лица; б - пациенты с гипертонией I степени; в - пациенты с гипертонией II степени. г - пациенты с ишемической болезнью сердца.
В заключение данного этапа исследований можно сделать следующий вывод: по мере тяжести течения сердечно-сосудистой патологии среди пациентов увеличивается количество лиц имеющих избыточную массу тела и ожирение I степени, это косвенно подтверждает тот факт, что избыточная масса тела является предиктором сердечно-сосудистой патологии.
Следующим этапом исследовательской работы было определение талиево-бедренного коэффициента у мужчин, больных гипертонией I, II степени и ИБС. Известно, что периферический тип ожирения (нижнее ожирение), «женский тип» ожирения, развивается с детства и характеризуется преимущественным отложением жира на бедрах, ягодицах, при этом на верхней половине туловища жира не много.
Туловищный тип ожирения (верхнее ожирение), «мужской тип» ожирения, обычно развивается во взрослом состоянии и характеризуется избыточным отложением жира на животе, спине, лице, при этом на ягодицах и конечностях жира мало [51].
Таким образом, как видно из таблицы 2, ТБК у мужчин возрастал по мере тяжести течения заболевания. У мужчин, имеющих АГ I, II степени, был выявлен периферический (гиноидный) тип ожирения, а лица, имеющие ИБС, имели - туловищный (андроидный) тип.
Кроме того, ТБК у пациентов с АГ II степени и ИБС был достоверно (Р<0,001) повышен по сравнению с контрольными цифрами и больными, имеющими АГ I степени.
Как было показано выше, больший процент обследованных пациентов имели избыточную массу тела и ожирение I степени. Известно, что для риска сердечно-сосудистых заболеваний более важен характер распределения жира, чем содержание общего жира [52]. Установлено, что именно андроидное распределение жира связано с повышенным риском заболеваний коронарных артерий. Соотношение андроидного жира положительно связано с уровнем триглицеридов в плазме и отрицательно с уровнем ЛПВП и ЛПНП [49, 52].
Таблица 2
Талиево-бедренный коэффициент мужчин г. Катайска, больных артериальной гипертонией I, II степени и ишемической болезнью сердца, M±m
| Группы | Мужчины ОТ/ОБ > 1 - андроидальный тип ожирения; ОТ/ОБ < 1 - гиноидальный тип ожирения |
| Условно здоровые (n=20) | 0,860±0,004 |
| АГ I степени (n=20) | 0,870±0,004 |
| АГ II степени (n=28) | 0,950±0,002 ***; DDD |
| ИБС (n=20) | 1,013±0,002 ***; ΔΔΔ |
Примечание: n – количество человек в выборке; ИБС – ишемическая болезнь сердца; АГ - артериальная гипертония; достоверность различий по сравнению с условно здоровыми людьми - *** - Р<0,001; достоверность различий по сравнению с больными АГ І степени - ∆∆∆ - Р<0,001.
Следующим этапом нашей исследовательской работы явилось определение и оценка гемодинамических показателей сердечно-сосудистой системы (ЧСС, САД, ДАД, ПД) у мужчин, страдающих артериальной гипертонией I, II степени и ишемической болезнью сердца.
Как видно из таблицы 3, у мужчин контрольной группы все показатели системы кровообращения были в пределах физиологических нормативов, а у пациентов с АГ I, II степени и ИБС - на уровне верхней границы нормы или превышали ее. Результаты наших исследований также выявили достоверное (Р<0,01; Р<0,001) повышение уровня артериального давления (САД, ДАД), ЧСС и ПД у лиц, имеющих в анамнезе АГ I степени, АГ II степени и ИБС, по сравненению с параметрами контрольной группы. Исключение составили больные с АГ I степени, у которых увеличение ЧСС не имело достоверного характера.
Таким образом, постоянно повышенное кровяное давление вынуждает сердце работать с перегрузкой, что в дальнейшем приведет к развитию артериальной гипертонии II степени (период стабилизации и стойкого повышения АД), гипертрофии миокарда (увеличению толщины стенки левого желудочка и расширению его объема), а также может привести к развитию сердечной недостаточности [25, 45].
Артериальная гипертония II степени, характеризуется более высоким и стойким повышением цифр АД. Основное значение здесь имеют неврогенные стимулы, которые благодаря высокой чувствительности почечных артериол и констрикторным воздействиям вызывают ишимизацию почек и различную по продолжительности и степени выраженности гиперпродукцию прессорно-активных гуморальных веществ: ренина, ангиотензина II, альдостерона и других [7, 9].
Как показали наши исследования, фактические показатели ЧСС, САД и ПД у всех мужчин, страдающих артериальной гипертонией I, II степени и ИБС, были достоверно (Р<0,001) выше должных величин, исключение составили мужчины с ИБС у которых САД было достоверно (Р<0,001) ниже должного параметра. ДАД же у больных с АГ II степени и ИБС было ниже, а у пациентов с АГ I степени выше должных величин, но только у мужчин, страдающих ИБС, эти различия имели достоверный характер (Р<0,001).
Кроме того, мужчины, страдающие АГ II степени и ИБС, имели достоверно (Р<0,05; Р<0,001) более высокие цифры САД и ДАД чем мужчины, страдающие АГ I степени; а ПД было достоверно (Р<0,001) выше у больных артериальной гипертонией II степени, по сравнению с лицами имеющими АГ I степени.
Дальнейший анализ показателей таблицы 3 показал, что ЧСС у пациентов с ИБС была достоверно (Р<0,001) выше по сравнению с аналогичным параметром у лиц, имеющих АГ I степени.
Наши данные согласуются с результатами ряда популяционных исследований, показавших, что САД и ДАД постепенно повышаются с возрастом и в зависимости от степени артериальной гипертензии, однако ДАД достигает пика приблизительно к 60-ти годам, затем прогрессивно снижается, тогда как САД продолжает повышаться. Таким образом, пульсовое давление (ПД, разница между САД и ДАД) неуклонно повышается в группе пожилых людей. В настоящее время известно, что риск осложнений артериальной гипертензии, в частности, инсульта (как ишемического, так и геморрагического), ИБС, сердечной недостаточности и прогрессивного нарушения функции почек находится в линейной зависимости, как от систолического, так и от диастолического давления. При этом возраст является единственным, наиболее значимым фактором риска инсульта. Существует, в частности, сильная взаимосвязь между высоким САД и возрастом, что определяет в значительной степени более высокий риск цереброваскулярных болезней среди пожилых пациентов [26, 48].
Нарушение адаптационной способности коронарного кровообращения к изменяющимся потребностям миокарда в крови приводит к состоянию его ишемии, а это лежит в основе возникновения ИБС [18].
Таким образом, сравнительный анализ параметров ССС у мужчин, страдающих АГ I, II степени и ИБС со здоровыми, показал, что САД, ДАД и ПД были достоверно выше у больных мужчин, нежели у здоровых.
Наши данные совпадают с анализом баз данных Фремингемского исследования и исследования SHEP, которые определили большое прогностическое значение повышенного ПД [2]. Так, у лиц страдающих артериальной гипертензией и у людей с нормальным АД, ПД является более значимым прогностическим индикатором сердечно-сосудистого риска, чем САД или ДАД. В частности, Фремингемское исследование показало, что снижение ДАД у пожилых пациентов приводит к повышению риска сердечно-сосудистых осложнений и что, изолированная систолическая артериальная гипертензия, ассоциированная с высоким ПД, является, в частности, злокачественным (неблагоприятным) патологическим изменением гемодинамики. Участники Фремингемского исследования сделали вывод, что у лиц среднего и пожилого возраста риск развития ИБС повышается при снижении ДАД и при любом уровне САД > 120 мм рт. ст. Ни САД, ни ДАД не имеют преимущества перед ПД в предсказании риска ИБС [49].
Таким образом, польза лечения изолированной систолической артериальной гипертензии (даже умеренного снижения АД) представляется значительной, в частности, среди пожилых пациентов, получающих низкие дозы диуретиков. В настоящее время при лечении любого сердечно-сосудистого заболевания, клиницисты в большей степени думают более о снижении абсолютного, нежели относительного риска. Антигипертензивное лечение, в общем, ассоциировано со снижением относительного риска инсульта на 40%, и снижением риска ИБС на 15-20%, но конечная польза лечения зависит от индивидуального абсолютного риска сердечно-сосудистых осложнений у конкретного пациента. У имеющих несколько факторов риска, включая пожилой возраст и абсолютный риск сердечно-сосудистых осложнений, польза снижения АД, соответственно, значительно большая.
Таблица 3
Некоторые показатели системы кровообращения мужчин г. Катайска, больных артериальной гипертонией I, II степени и ишемической болезнью сердца, M±m
| Показатели Группы | ЧСС, уд/мин N – 60-80 | дЧСС, уд/мин | САД, мм рт. ст. N - 100-139 | дСАД, мм рт. ст. | ДАД, мм рт. ст. N – 60-90 | дДАД, мм рт. ст. | ПД, мм рт. ст. N – 30-40 |
| Условно здоровые (n=20) | 69,60±0,39 | 64,19±0,43 | 117,25±1,23 | 126,36±1,36 | 77,25±0,99 | 83,30±1,14 | 40,00±0,73 |
| АГ I степени (n=20) | 71,00±0,62 | 63,58±0,53 | 132,60±0,62 ***; | 125,16±1,00 | 84,25±0,58 *** | 82,30±0,83 | 48,35±0,70 ***; |
| АГ II степени (n=28) | 72,11±0,69 **; | 63,02±0,48 | 151,68±1,17 ***; DDD; | 139,35±1,01 | 92,57±0,70 ***; DDD | 94,13±0,84 | 59,11±1,05 ***; DDD; |
| ИБС (n=20) | 87,55±0,31 ***; ΔΔΔ; | 60,75±0,08 | 136,50±0,58 ***; ΔΔΔ; | 139,29±0,22 | 85,75±0,39 ***; Δ; | 94,08±0,19 | 48,95±0,45 ***; |
Примечание: n - количество человек в выборке; N – норма [44, 45]; ЧСС - частота сердечных сокращений; дЧСС - должная частота сердечных сокращений; САД – систолическое артериальное давление; дСАД – должное систолическое артериальное давление; ДАД – диастолическое артериальное давление; дДАД - должное диастолическое артериальное давление; ПД – пульсовое давление; дПД – должное пульсовое давление; АГ – артериальная гипертония; ИБС – ишемическая болезнь сердца; достоверность различий по сравнению с условно здоровыми людьми - ** - Р<0,01; *** - Р<0,001; достоверность различий по сравнению с больными артериальной гипертонией I степени - Δ - Р<0,05; DDD - Р<0,001; достоверность различий по сравнению с должными величинами - - Р<0,001.
Так, даже умеренное снижение САД (например, на 10 мм рт. ст.) имеет значительные преимущества в сокращении частоты фатальных и нефатальных инсультов, ИБС и общей сердечно-сосудистой смертности [8].
Заключительным этапом исследовательской работы стало изучение некоторых биохимических показателей сыворотки крови у обледуемых больных (концентрации общего холестерина, триглицеридов, ЛПВП, ЛПНП, ЛПОНП, общего билирубина; индекса атерогенности; активности аланинаминотрансферазы, аспартатаминотрансферазы, криатинфосфокиназы и лактатдегидрогеназы).
Как видно из таблицы 4, показатели липидного спектра сыворотки крови у практически здоровых мужчин, не выходили за границы физиологической нормы, принятой в практическом здравоохранении. У больных мужчин данные параметры были на уровне верхней границы нормы или превышали ее. Хотя, если оценивать лабораторные критерии нарушений липидного обмена, риск развития и прогрессирования атеросклероза у обследованных нами лиц существует: идеальное содержание общего холестерина в крови < 4 ммоль/л; желательное < 5,2 ммоль/л; пограничное 5,2-6,5 ммоль/л и аномальное > 6,5 ммоль/л [31, 33, 36, 51].
Группа экспертов Европейского атеросклеротического общества [37] на основании проспективных эпидемиологических исследований установила: для лиц обоих полов старше 20 лет уровень холестерина в крови меньше 5,2 ммоль/л (200 мг/дл) следует считать оптимальным; 5,2-6,5 ммоль/л (200-250 мг/дл) – умеренной гиперхолестеринемией, причем средней и тяжелой формами гиперхолестеринемии предлагается считать концентрации в пределах 6,5-7,8 и более 7,8 ммоль/л соответственно [20, 23, 33, 37].
Если придерживаться этих данных, то в нашем исследовании, даже в контрольной группе, идеального содержания общего холестерина в сыворотке крови не было выявлено. При умеренном повышении концентрации общего холестерина в сыворотке крови у здоровых мужчин имелась тенденция к снижению содержания ЛПВП и повышению - ЛПНП. Нарушение соотношения между концентрациями ЛПВП, ЛПНП и ЛПОНП в сыворотке крови у этих мужчин, вероятно, связано с наследственными нарушениями обмена веществ и с преобладанием в пище жиров.
Как известно, состояние липидного обмена зависит от возраста и от интегрирующей роли центральной нервной системы (ЦНС) [53].
Ряд факторов внешней среды может вызвать дискоординацию работы высших систем регуляции липидного обмена и возникновение эндогенной гиперхолестеринемии и гиперлипопротеидемии. Одним из наиболее распространенных факторов, способных нарушить высшие механизмы регуляции липидного обмена, может быть длительное, функциональное напряжение и перенапряжение ЦНС – фактор, постоянно присутствующий в жизни современного человека [50, 53, 54].
По данным В.С. Камышникова (2002) [55], норма холестерина сыворотки крови человека находится в пределах от 4,33 до 6,28 ммоль/л, хотя большинство авторов придерживаются мнения, что наименьший риск развития атеросклероза будет наблюдаться, если уровень холестерина крови не будет превышать 5,2 ммоль/л [22, 34, 35, 36, 52].
Если следовать выводам этих авторов, то в нашем исследовании наблюдалось достоверное (Р<0,001) повышение уровня холестерина свыше 5,2 ммоль/л у мужчин, страдающих АГ II степени и ИБС, по сравнению с условно здоровыми лицами и пациентами, имеющих АГ I степени.
Проводя биохимический анализ крови мужчин, страдающих АГ I степени, нами не было выявлено у них достоверных различий по содержанию в сыворотке крови общего холестерина, по сравнению с аналогичным показателем у здоровых мужчин.
Как видно из таблицы 4, зарегистрировано достоверное (Р<0,001) повышение концентрации триглицеридов у пациентов с АГ I степени, по сравнению со здоровыми мужчинами. Так же было отмечено достоверное (Р<0,001) снижение уровня ЛПВП в сыворотке крови у пациентов с АГ I степени, по сравнению с этим же показателем у здоровых лиц.
Дальнейшие исследования показали, что у мужчин с АГ I степени содержание ЛПНП и ЛПОНП в сыворотке крови, а также коэффициент атерогенности были достоверно (Р<0,001) выше, чем у практически здоровых мужчин. Коэффициент атерогенности у пациентов с АГ I степени был > 2 единиц, что выше нормативных значений.
Проводя более детальный анализ липидного спектра крови мужчин, страдающих АГ II степени, нами было выявлено достоверное (Р<0,001) повышение содержания в сыворотке их крови общего холестерина, по сравнению с аналогичным показателем у здоровых мужчин и больными АГ I степени. Кроме того, было зарегистрировано достоверное (Р<0,001) повышение концентрации триглицеридов у пациентов с АГ II степени, по сравнению со здоровыми мужчинами и больными АГ I степени. А так же было отмечено достоверное (Р<0,05) снижение уровня ЛПВП в сыворотке крови у пациентов с АГ II степени по сравнению с этим же показателем у здоровых лиц и достоверное (Р<0,05) повышение этого параметра по сравнению с пациентами, имеющими АГ I степени. Дальнейшие исследования показали, что у всех мужчин с АГ II степени содержание ЛПНП и ЛПОНП в сыворотке крови, а также коэффициент атерогенности были достоверно (Р<0,01; Р<0,001) выше, чем у практически здоровых лиц и больных АГ I степени. Коэффициент атерогенности у всех пациентов с АГ II степени был > 2 единиц. Данный факт может свидетельствовать о степени риска развития атеросклероза и ИБС у этих больных.
При сопутствующей патологии и развивающемся атеросклерозе, нарушаются процессы эстерификации холестерина в ЛПВП и его транспорт. Снижается уровень холестерина в составе ЛПВП. В результате молекула ЛПВП приобретает новые свойства. Она теряет способность выводить холестерин с поверхности эндотелиальных клеток. Дефицит холестерина в молекуле ЛПВП – фактор риска ишемической болезни миокарда [40].
Интактная сосудистая стенка практически не проницаема для липопротеинов и холестерина. Однако при гиперхолестеринемии, повышенной секреции адреналина, ангиотензина, брадикинина, серотонина, явлениях кислородной недостаточности и других экстремальных состояниях увеличивается поступление липопротеинов в сосудистую мембрану. При этом происходит сокращение эндотелиальных клеток и увеличение эндотелиальных щелей от 75 до 200 нм.
В щели эндотелиального слоя сосудистой мембраны поступают атерогенные липопротеины – ЛПОНП и ЛПНП. Прохождение липопротеинов через эндотелиальные щели осуществляется путем специфического и неспецифического эндоцитоза. В здоровом молодом организме липопротеины поступают в ткани с помощью специфического эндоцитоза: специфические белковые рецепторы на клеточной мембране связывают ЛПНП и втягивают их внутрь клетки [6, 22, 30].
Таким образом, гиперлипидемия, бесконтрольное поступление липопротеинов в стенку сосудов, освобождение холестерина из молекулы ЛПНП и нарушение выделения его из клетки сосудистой мембраны, задержка утилизации холестерина в печени ведут к возникновению атеросклероза и ишемической болезни миокарда [32].
При анализе лабораторных показателей липидного спектра сыворотки крови у мужчин, страдающих ИБС (табл. 4), были выявлены отклонения от нормативных параметров: повышенное содержание общего холестерина, триглицеридов, ЛПОНП, ЛПНП, а также увеличение коэффициента атерогенности и снижение концентрации ЛПВП.
При более детальном анализе параметров липидного спектра сыворотки крови у мужчин, страдающих ИБС, нами были получены следующие результаты: отмечено достоверное (Р<0,001) повышение содержания общего холестерина в сыворотке крови у мужчин с ИБС (умеренная гиперхолестеринемия), по сравнению с данным параметром мужчин из группы контроля. Содержание же триглицеридов в сыворотке крови у пациентов имеющих ИБС было достоверно (Р<0,001) выше, чем у здоровых мужчин. У мужчин, больных ИБС, содержание ЛПВП в сыворотке крови было достоверно (Р<0,001) снижено, по сравнению с этим же показателем у практически здоровых мужчин. Как видно из таблицы 4, концентрация ЛПОНП, концентрация ЛПНП и коэффициент атерогенности у больных, страдающих ИБС, были достоверно (Р<0,001) выше, чем у здоровых лиц.
Сравнивая показатели липидного спектра сыворотки крови больных ИБС с аналогичными показателями у пациентов с АГ I степени, нами было зарегистрировано достоверное (Р<0,001) повышение уровня холестерина у мужчин больных ИБС, по сравнению с пациентами, страдающими АГ I степени. Кроме того, у больных ИБС было достоверно (Р<0,001) повышено содержание триглицеридов в сыворотке крови, по сравнению с больными АГ I степени. У лиц, страдающих ИБС, также было зарегистрировано достоверное (Р<0,001) снижение концентрации ЛПВП и достоверное (Р<0,01; Р<0,001) повышение концентрации ЛПОНП и ЛПНП, а также увеличение индекса атерогенности, по сравнению с больными АГ I степени. Таким образом, коэффициент атерогенности у больных ИБС был выше 4 единиц, а это означает высокую степень риска развития атеросклеротических изменений кровеносных сосудов.
Наше исследование показало, что изменение липидного спектра крови у наших больных имеет место быть, эти изменения статистически значимы и зависят от типа патологии.
Согласно определению ВОЗ, атеросклероз – это вариабельная комбинация изменений в интиме артерий (в отличие от артериол), состоящая из очагового накопления липидов, сложных углеводов, фиброзной ткани и кальциевых отложений и связанная с изменениями в медии сосудов [54, 56].
Таким образом, подводя итог вышесказанному, у больных с ИБС, существует высокая вероятность развития атеросклероза, так как коэффициент атерогенности у них > 4 единиц; у больных АГ I, II степени - малая вероятность - коэффициент атерогенности < 3 единиц; умеренная вероятность коэффициент атерогенности - от 3 до 4 единиц. Нарушения липидного обмена при развитии атеросклероза характеризуются также качественными изменениями. Так, часть холестеринэстеров, увеличивающихся в сосудистой стенке, присоединив насыщенные жирные кислоты, становится метаболически малоактивной. Липопротеины также претерпевают качественные изменения в виде гиперлипопротеинемии определенного типа в результате увеличения содержания холестерина, фосфолипидов и белков. Изменяется содержание и состав фосфолипидов, их соотношение с холестерином, от которого зависит его коллоидная устойчивость в крови. При атеросклерозе развивается гиперлипидемия за счет гипертриглицеридемии, которая делает липопротеины грубодисперсными и малорастворимыми. Изменение агрегатного состояния липидов при небольших изменениях холестеринемии в сторону их укрупнения способствует увеличению сосудистой проницаемости и липоидозу [53].
Отмеченные у наших больных изменения липидного обмена могут рассматриваться как неблагоприятные, особенно если они протекают на фоне снижения адаптивных возможностей организма. Выявленные «возмущения» могут способствовать атерогенным изменениям в организме. Нарушению регуляции липидного обмена могло способствовать изменение нейроэндокринных факторов. Механизм регуляции липидного гомеостаза может быть нарушен в результате выраженного длительного нервно-мышечного напряжения на фоне подавления функции щитовидной железы. Резкие колебания могут быть истолкованы как показатель недостаточной адаптации к длительному напряжению ЦНС. Ведущая роль в нормализации сдвигов липидного обмена принадлежит щитовидной железе и коре надпочечников, это необходимо учитывать при оценке адаптивных возможностей организма [52].
Гиперлипидемия может быть связана с низкой лизосомальной активностью печени и торможением катаболизма липидов [36].
Гиперлипидемия и гиперхолестеринемия развиваются при недостаточно выраженной активности липопротеинлипазы сыворотки крови. В результате в крови увеличивается содержание ЛПНП и ЛПОНП. В нашем исследовании тоже наблюдалась такая закономерность. Обращает на себя внимание снижение ЛПВП у больных мужчин, функция которого заключается в удалении холестерина с наружной поверхности клетки. Потеря захваченного с поверхности мембраны холестерина сразу же восполняется поступлением его внутрь клетки. Этот процесс идет непрерывно. При увеличении в крови ЛПНП и ЛПОНП происходит задержка катаболизма этих атерогенных липопротеинов, тормозится образование ЛПВП, которые обычно задерживают проникновение холестерина в клетки сосудистой стенки в составе атерогенных ЛПНП, ЛПОНП за счет конкуренции с их рецепторами. Захваченный с поверхности мембраны холестерин в составе ЛПВП в плазме крови подвергается эстерификации при действии лецитинхолестеринацетилтрансферазы, и затем холестерин транспортируется в составе ЛПВП в печень, где частично выделяется с желчью, преобразуясь в желчные кислоты [30, 35].
Если содержание общего холестерина увеличивается на 6-28%, по сравнению с нормой, то при гистологическом исследовании сосудов сердца обнаруживаются изменения в артериях миокарда среднего и мелкого калибра в виде накопления кислых гликозаминогликанов в утолщениях интимы, а также сегментарной или циркулярной жировой инфильтрации внутренней и средней оболочек сосудов.
При более значительном увеличении содержания общего холестерина в сыворотке крови по сравнению с нормативным показателем - на 34-66%, в сосудах миокарда, наряду с липоидозом их стенок, обнаруживаются сформированные атеросклеротические бляшки, которые имеют хорошо выраженный соединительнотканный каркас и преобладание в основном веществе нейтральных гликозаминогликанов. Такие бляшки почти полностью облитерируют просвет сосудов. Так же имеет место распространенный липоидоз мелких фолликулярных и трабекулярных артерий селезенки, жировая инфильтрация наблюдается во всех слоях сосудистой стенки. Независимо от степени повышения конечного содержания общего холестерина в крови имеют место дистрофические изменения в тканях различных органов. Например, в корковом слое почек просветы многих канальцев расширены, эпителий с выраженными признаками дистрофического ожирения. В отдельных случаях капли жира обнаруживаются в эндотелии капилляров клубочка.
В клетках печени ожирение носит вариабельный характер. Гепатоциты с пылевидными каплями жира располагаются по периферии, в то время, как гепатоциты с крупными каплями жира, целиком заполняют цитоплазму печеночных клеток и располагаются диффузно по всей паренхиме печени. Имеется ожирение эпителия желчных протоков.
Сосуды внутренних органов при ожирении расширены и содержат липемическую плазму [17, 30, 53].
Установлено, что пациенты с низкой концентрацией ХС ЛПВП характеризуются повышенным риском развития ИБС даже при низких значениях содержания общего холестерина в сыворотке крови, поэтому определение концентрации ХС ЛПВП является обязательным для оценки липопротеинового спектра крови.
Уровень ХС ЛПВП снижается у курильщиков, но возрастает у лиц, регулярно подвергающихся интенсивным физическим нагрузкам [40].
Для понимания взаимосвязи между молекулярными процессами и физиологическими функциями клеток и организма необходимо использование в диагностике патологического процесса данных биохимического анализа сыворотки крови.
В области сердечно-сосудистой патологии биохимические исследования наибольших успехов достигли в диагностике ИБС и инфаркта миокарда. Данные методы позволяют диагностировать инфаркт миокарда в первые часы его возникновения, выявить тяжесть течения ИБС, гибель миоцитов и оценить эффективность тромболитической терапии. Практически значимыми маркерами гибели миоцитов являются активности энзимов - АСТ, КФК, ЛДГ.
Таблица 4
Некоторые показатели липидного спектра сыворотки крови мужчин г. Катайска, больных артериальной гипертонией I, II степени и ишемической болезнью сердца, M±m
| Показатели Группы | Общий холестерин, N – 5,2-6,5 ммоль/л | Триглицериды, N – 0,51-1,86 ммоль/л | ЛПВП, N – 0,9-1,8 ммоль/л | ЛПНП, N – 2,37-4,36 ммоль/л | ЛПОНП, N – 0,47-0,65 ммоль/л | Индекс атерогенности, N – не > 2 у.е. |
| Условно здоровые (n=20) | 4,68±0,08 | 0,86±0,04 | 1,73±0,03 | 2,48±0,06 | 0,41±0,02 | 1,71±0,05 |
| АГ I степени (n=20) | 4,78±0,11 | 1,49±0,03 *** | 1,51±0,04 *** | 3,46±0,08 *** | 0,68±0,02 *** | 2,20±0,07 *** |
| АГ II степени (n=28) | 5,92±0,21 ***; ΔΔΔ | 1,65±0,02 ***; ΔΔΔ | 1,65±0,04 *; Δ | 3,86±0,06 ***; ΔΔΔ | 0,76±0,01 ***; ΔΔΔ | 2,55±0,10 ***; ΔΔ |
| ИБС (n=20) | 5,53±0,04 ***; ΔΔΔ | 1,65±0,01 ***; ΔΔΔ | 1,04±0,01 ***; ΔΔΔ | 3,77±0,01 ***; ΔΔΔ | 0,75±0,01 ***; ΔΔ | 4,33±0,06 ***; ΔΔΔ |
Примечание: n - количество человек в выборке; N – норма [53]; ЛПВП – липопротеиды высокой плотности; ЛПНП - липопротеиды низкой плотности; ЛПОНП – липопротеиды очень низкой плотности; АГ – артериальная гипертония; ИБС – ишемическая болезнь сердца; достоверность различий по сравнению с условно здоровыми людьми - * - Р<0,05; *** - Р<0,001; достоверность различий по сравнению с больными артериальной гипертонией I степени – Δ - Р<0,05; ΔΔ - Р<0,01; ΔΔΔ - Р<0,001.
Медикаментозное лечение пациентов с сердечно-сосудистыми потологиями может оказать влияние на функциональное состояние гепатоцитов. Поэтому в своих исследованиях мы сочли необходимым провести оценку таких значимых биохимических параметров, как уровень билирубина и активность АЛТ в сыворотке крови пациентов, имеющих АГ I, II степени и ИБС.
Анализ результатов таблицы 5 выявил, что уровень общего билирубина в сыворотке крови у всех обследованных мужчин был в пределах физиологической нормы. Также нами было зарегистрировано достоверное (Р<0,05; Р<0,001) повышение концентрации общего билирубина в сыворотке крови у пациентов с АГ II степени и ИБС, по сравнению со здоровыми мужчинами и больными АГ I степени.
Возрастание концентрации билирубина в сыворотке крови называют гипербилирубинемия. Это состояние может быть следствием образования билирубина в количествах, превышающих способности нормальной печени его экскретировать; повреждений печени, нарушающих экскрецию билирубина в нормальных количествах, а также вследствие закупорки желчевыводящих протоков, что препятствует выведению билирубина [53].
При участии аминотрансфераз в организме человека осуществляются процессы межмолекулярного переноса аминогрупп с донорской гаммааминокислоты на акцептор альфакетокислоту без промежуточного образования аммония, т.е. трансаминирование. Наиболее часто их активность исследуют с целью дифференцировки диагностики патологии печени и миокарда. Следует учитывать и то, что изменение активности АСТ и АЛТ может быть вызвано употреблением лекарственных препаратов [53].
При исследовании активности аминотрансфераз, как видно из таблицы 5, у мужчин, больных АГ I степени, активности АЛТ и АСТ были достоверно (Р<0,05) ниже по сравнению со здоровыми мужчинами. Кроме того, было зарегистрировано достоверное (Р<0,05; Р<0,01) повышение активности АЛТ и АСТ у пациентов с АГ II степени, по сравнению со здоровыми мужчинами; также было выявлено достоверное (Р<0,001) повышение активности АЛТ и АСТ у пациентов с ИБС, по сравнению со здоровыми мужчинами.
У больных, страдающих АГ II степени, отмечалось достоверное (Р<0,01; Р<0,001) повышение активности в сыворотке крови АЛТ и АСТ по сравнению с аналогичными показателями у больных с АГ I степени; также было зарегистрировано достоверное (Р<0,001) повышение активности АЛТ и АСТ у мужчин с ИБС, по сравнению с больными АГ I степени.
Анализируя данные по активности аминотрансфераз нами было отмечено, что у мужчин, больных АГ I, II степени и ИБС, активность аминотрансфераз постепенно повышалась по мере тяжести течения заболевания, но находилась в пределах границ физиологической нормы.
Это вероятно связано с тем, что при стенокардии уровень активности аминотрансфераз в крови не повышается или повышается незначительно. При небольшом инфаркте миокарда в крови наблюдается рост активности АЛТ (застойные явления в печени, обусловленные правосторонней сердечной недостаточностью) и абсолютное большинство случаев инфарктов миокарда сопровождается ростом содержания в крови сердечного маркера АСТ. К тому же повышение АЛТ обнаруживается при заболеваниях сердца, сопровождающихся вторичным поражением печени. Как упоминалось выше, изменение (повышение) активности аминотрансфераз может быть вызвано употреблением лекарственных препаратов [53, 57].
При исследовании активности кардиоспецифических ферментов (КФК и ЛДГ) нами было отмечено, что у мужчин с АГ I степени их активность достоверно (Р<0,001) увеличивалась по сравнению с контрольными цифрами. Кроме того, было зарегистрировано достоверное (Р<0,001) повышение активности КФК и ЛДГ у пациентов с АГ II степени и ИБС, по сравнению со здоровыми мужчинами.
У больных, страдающих АГ II степени и ИБС, нами было выявлено достоверное (Р<0,05; Р<0,001) повышение активности в сыворотке крови КФК и ЛДГ по сравнению с аналогичными показателями пациентов, имеющих АГ I степени.
В заключении необходимо отметить, что при исследовании активности кардиоспецифических ферментов у мужчин с АГ I, II степени и ИБС активности креатинфосфокиназы и лактатдегидрогеназы умеренно повышались по мере тяжести течения заболевания и при ИБС достигали верхних значений физиологической нормы.
Повышение активности креатинфосфокиназы и лактатдегидрогеназы в крови обычно свидетельствует о поражении миокарда, при этом по степени изменения активности можно судить о размере зоны некроза. Характерно, что общая активность сывороточной ЛДГ сохраняется повышенной вдвое дольше, чем активность других ферментов.
Увеличение КФК наблюдается уже через 4-8 ч после острого приступа, максимум достигается через 12-24 ч, на третьи сутки активность изофермента возвращается к нормальным значениям.
Определение общей активности креатинфосфокиназы получило широкое применение для диагностики инфаркта миокарда. Поскольку у больных с острой коронарной недостаточностью скелетная мускулатура и ЦНС, как правило, не вовлекаются в патологический процесс, повышение активности КФК в этих случаях обычно свидетельствует о поражении миокарда. При мелкоочаговом инфаркте миокарда чувствительность теста составляет 92%, при крупноочаговом - 98%. Фермент лактатдегидрогеназа широко распространен в различных органах и тканях, но наибольшая активность ЛДГ определяется в почках, миокарде, печени и скелетной мускулатуре. Ценность определения активности ЛДГ особенно велика в неясных случаях заболевания, при нетипичной клинической и электрокардиографической картине инфаркта миокарда. Установлена достоверная прямая корреляционная связь между размером очага омертвения в миокарде и общей активностью ЛДГ [58].
Таблица 5
Некоторые биохимические параметры сыворотки крови мужчин г. Катайска, больных артериальной гипертонией I, II степени и ишемической болезнью сердца, M±m
| Показатели Группы | Общий билирубин, ммоль/л N – 8,5-20,5 | АЛТ, мкмоль/мл*ч N - 0,1-0,68 | АСТ, мкмоль/мл*ч N - 0,1-0,45 | КФК, U/ L N – 24-195 | ЛДГ, U/ L N – 225-450 |
| Условно здоровые (n=20) | 9,30±0,41 | 0,340±0,020 | 0,210±0,010 | 40,05±3,47 | 76,30±6,74 |
| АГ I степени (n=20) | 9,15±0,45 | 0,290±0,010 * | 0,180±0,010 * | 80,80±9,64 *** | 180,70±22,42 *** |
| АГ II степени (n=28) | 10,68±0,52 *; Δ | 0,420±0,020 **; ΔΔΔ | 0,320±0,040 *; ΔΔ | 152,29±20,12 ***; ΔΔΔ | 255,68±18,90 ***; Δ |
| ИБС (n= 20) | 11,70±0,25 ***; ΔΔΔ | 0,500±0,010 ***; ΔΔΔ | 0,300±0,005 ***; ΔΔΔ | 184,90±3,43 ***; ΔΔΔ | 413,90±8,97 ***; ΔΔΔ |
Примечание: n - количество человек в выборке; N – норма [53]; АЛТ - аланинаминотрансфераза; АСТ - аспартатаминотрансфераза; КФК - креатинфосфокиназа; ЛДГ - лактатдегидрогеназа; АГ - артериальная гипертония; ИБС - ишемическая болезнь сердца; достоверность различий по сравнению с условно здоровыми людьми - * - Р<0,05; ** - Р<0,01; *** - Р<0,001; достоверность различий по сравнению с больными артериальной гипертонией I степени - Δ - Р<0,05; ΔΔ - Р<0,01; ΔΔΔ - Р<0,001.
ВЫВОДЫ
1. Среди мужчин, страдающих артериальной гипертонией I, II степени и ишемической болезнью сердца, выявлен больший процент лиц, имеющих избыточную массу тела и ожирение 1 степени. Это свидетельствует о том, что лишний вес является фактором риска развития артериальной гипертонии и ишемической болезни сердца.
2. У мужчин, страдающих сердечно-сосудистой патологией, талиево-бедренный коэффициент увеличивается по мере тяжести течения болезни; при этом пациенты с артериальной гипертонией I, II степени имели периферический (гиноидный) тип ожирения, а пациенты с ишемической болезнью сердца - туловищный (андроидный) тип ожирения.
3. У мужчин, страдающих артериальной гипертонией I, II степени и ишемической болезнью сердца, частота сердечных сокращений, систолическое артериальное давление, диастолическое артериальное давление и пульсовое давление были выше контрольных и должных величин.
4. У всех пациентов выявлен дисбаланс липопротеинового спектра сыворотки крови (повышение уровня липопротеинов низкой плотности, липопротеинов очень низкой плотности, триглицеридов, снижение содержания липопротеинов высокой плотности и повышение коэффициента атерогенности).
Выявлено увеличение активности аланинаминотрансферазы, аспартатаминотрансферазы, креатинфосфокиназы и лактатдегидрогиназы у всех пациентов относительно аналогичных параметров, зарегистрированных у условно здоровых лиц. Активность креатинфосфокиназы и лактатдегидрогиназы значимо повышалась по мере тяжести течения заболевания.
СПИСОК ЛИТЕРАТУРЫ
1. Гафаров, В.В. Популяционное исследование социально–психологических факторов риска ишемической болезни сердца в мужской популяции Новосибирска /В.В. Гафаров, И.А. Гагулин //Терапевтический архив. – 2000. – Т. 72, № 4. – С. 40–43.
2. Мартынов, А.И. Систолическое артериальное давление и изолированная систолическая артериальная гипертензия /А.И. Мартынов //Кардиология. – 2002. – № 2. – С. 3–5.
3. Суслина, З.А. Артериальная гипертония и инсульт: связь и перспективы профилактики /З.А. Суслина, Л.А. Гераскина, А.В. Фонякин //Кардиология. – 2002. – № 2. – С. 13–15.
4. Рашмер, Р. Динамика сердечно-сосудистой системы /Р. Рашмер. – М.: Медицина, 1981. – 600 с.
5. Начала физиологии: учебное пособие /под ред. А.Н. Ноздрачева. – С-Пб.: Лань, 2001. – 1088 с.
6. Адо, А.Д. Патологическая физиология: учебное пособие /А.Д. Адо, В.В. Новицкий. – Томск.: Издательство Томского университета, 1994. – 466 с.
7. Маколкин, В.И. Внутренние болезни /В.И. Маколкин, С.И. Овчаренко. – М.: Медицина, 1994. – 464 с.
8. Матусова, А.П. Практическая кардиология /А.П. Матусова, Н.Н. Боровков. – Ростов-на-Дону.: Феникс, 1999. – 174 с.
9. Гогин, Е.Е. Гипертоническая болезнь: новое в диагностике и лечении: клиническая оценка причин и механизмов развития /Е.Е. Гогин. – М.: Медицина, 1997. – 399 с.
10. Оганов, Р.Г. Проблема артериальной гипертонии среди населения /Р.Г. Оганов //Кардиология. – 1994. – № 3. – С. 80–83.
11. Постнов, Ю.В. Молекулярная биология ренина: возможности супрессии ренин-ангиотензиновой системы /Ю.В. Постнов //Кардиология. – 1995. – Т. 35, № 10. – С. 46–50.
12. Погосова, Г.В. Депрессия – новый фактор риска ИБС и предиктор коронарной смерти /Г.В. Погосова //Кардиология. – 2002. – Т. 42, № 4. – С. 86–90.
13. Пауков, В.С. Элементы теории патологии сердца /В.С. Пауков, В.А. Фролов. – М.: Медицина, 1982. – 272 с.
14. Руда, М.Я. Инфаркт миокарда /М.Я. Руда, А.П. Зыско. – М.: Медицина, 1981. – 285 с.
15. Васильева, Г.С. Реактивные изменения сердечно-сосудистой системы /Г.С. Васильева, Д.Д. Савинов, В.П. Алексеев //Медицинская помощь. – 2001. – № 3. – С. 3–5.
16. Сердечно–сосудистые заболевания у пожилых /под ред. Т. Страссера. – Женева., 1988. – 218 с.
17. Гистология /под ред. Ю.И. Афанасьева, Н.А. Юриной. – М.: Медицина, 2001. – 744 с.
18. Гордон, Р. Болезни коронарных артерий /Р. Гордон. – М.: Медицина, 1980. – 336 с.
19. Чазова, И.Е. Метаболический синдром, сахарный диабет 2 типа и артериальная гипертензия /И.Е. Чазова, В.Б. Мычка //Сердце: журнал для практикующих врачей. – 2003. – Т. 2, № 3. – С. 102–144.
20. Шевченко, О.П. Метаболический синдром: монография /О.П. Шевченко, Е.А. Праскурничий, А.О. Шевченко. – М.: Медицина, 2004. – 141 с.
21. Алишева, Е.К. Методы диагностики инсулинорезистентности /Е.К. Алишева, Е.И. Красильникова, Е.В. Шляхто //Артериальная гипертензия. – 2002. – Т. 8, № 1. – С. 29–34.
22. Климов, А.Н. Липопротеиды, дислипопротеидемии и атеросклероз /А.Н. Климов, Н.Г. Никульчева. – Л.: Медицина, 1984. – 164 с.
23. Сидлина, И. Уровень липидов и поражение экстракраниальных артерий атеросклерозом у мужчин моложе 50 лет /И. Сидлина, И. Фомина, В. Швейкина //Врач. – 2003. – № 9. – С. 27–30.
24. Бритов, А.Н. Артериальная гипертония у больных с ожирением: роль лептина /А.Н. Бритов, О.В. Молчанова, М.М. Быстрова //Кардиология. – 2002. – Т. 42, № 9. – С. 69–71.
25. Шилов, А.М. Артериальная гипертензия и метаболический синдром /А.М. Шилов, М.В. Чубаров, М.В. Мельник //Русский медицинский журнал. – 2003. – Т. 11, № 21. – С. 1145–1149.
26. Гулевская, Т.С. Артериальная гипертония и патология белого вещества головного мозга /Т.С. Гулевская, И.Г. Людковская //Архив патологии. – 1992. – № 2. – С. 53–59.
27. Балкаров, И. Ожирение и артериальная гипертензия /И. Балкаров //Врач. – 2003. – № 9. – С. 22–26.
28. Моисеев, В.С. Метаболические нарушения при артериальной гипертонии /В.С. Моисеев, Ж.Д. Кобалава, Ю. Котовская //Врач. – 2001. – № 7. – С. 15–19.
29. Медицинские лабораторные технологии: справочник /под ред. А.И. Карпищенко. – С-Пб.: Интермедика, 1999. – Т. 2, 655 с.
30. Зайчик, А.Ш. Основы патохимии: учебное пособие /А.Ш. Зайчик, Л.П. Чурилов. – С-Пб.: ЭЛБИ-С-Пб, 2001. – 687 с.
31. Климов, А.Н. К спорам о холестерине /А.Н. Климов //Кардиология. – 1992. – № 4. – С. 5–8.
32. Титов, В.Н. Липопротеиды как специфическая транспортная система кровотока /В.Н. Титов //Вестник Российской академии медицинских наук. – 1998. – № 4. – С. 3–7.
33. Финагин, Л.К. Обмен холестерина и его регуляция /Л.К. Финагин. – Киев.: Вища школа, 1980. – 168 с.
34. Вихерт, А.М. Атеросклероз: руководство по кардиологии /А.М. Вихерт, Е.И. Чазов. – М.: Медицина, 1982. – Т. 1, С. 417–443.
35. Гаврилова, Р.Д. Содержание липидов крови при различных формах ишемической болезни сердца /Р.Д. Гаврилова, С.Б. Ханина, В.В. Симонов //Кардиология. – 1987. –№ 10. – С. 51–53.
36. Клебанов, Г.И. Гиперхолестериненмия в патогенезе атеросклероза /Г.И. Клебанов, М.П. Шерстнев //Кардиология. – 1983. – № 7. – С. 14–17.
37. Лопухин, Ю.М. Холестериноз: монография /Ю.М. Лопухин. – М.: Медицина, 1983. – 352 с.
38. Мясников, А.Л. Гипертоническая болезнь /А.Л. Мясников. – М.: Медгиз, 1954. – 391 с.
39. Перова, Н.В. Суммарный риск ишемической болезни сердца и показания к лечению гиперхолестеринемии /Н.В. Перова //Кардиология. – 1996. – Т. 3, № 2. – С. 47–53.
40. Герасимова, Е.Н. Гормоны и холестерин липопротеидов высокой плотности /Е.Н. Герасимова //В кн.: Биохимия липидов и их роль в обмене веществ. – М., 1981. – С. 28–42.
41. Конопля, Е.Ф. Ишемическая болезнь сердца и биологический возраст у мужчин старше 40 лет /Е.Ф. Конопля, В.А. Левданская, Э.И. Зборовский //Кардиология. – 1987. – № 9. – С. 22–24.
42. Практикум по нормальной физиологии /под ред. В.И. Торшина. – М.: Издательство Российского университета дружбы народов, 2004. – 609 с.
43. Благосклонная, Я.В. Проблемы лишнего веса /Я.В. Благосклонная, Е.И. Красильникова, А.Ю. Бабенко. – С-Пб.: ИК «Невский проспект», 2002. – 128 с.
44. Шейх-Заде, Ю.Р. Определение должных величин сердца у людей /Ю.Р. Шейх-Заде, Ю.А. Зудик, К.Ю. Шейх-Заде //Физиология человека. – 2001. – Т. 27, № 6. – С. 748-750.
45. Орлов, В.Н. Артериальное давление: норма и патология /В.Н. Орлов, В.А. Ольхин. – М.: Знание, 1981. – 64 с.
46. Биохимический автоматический анализатор /руководство для оператора. – М.: Диакит, 1999. – 27 с.
47. Лакин, Г.Ф. Биометрия: учебное пособие /Г.Ф. Лакин. – М.: Высшая школа, 1990. – 293 с.
48. Шляхто, Е.В. Патогенез гипертонической болезни /Е.В. Шляхто //Сердечная недостаточность. – 2002. – Т. 3, № 1. – С. 12–13.
49. Профилактика, диагностика и лечение артериальной гипертонии в Российской Федерации /Первый доклад экспертов Научного общества кардиологов и межведомственного совета по сердечно-сосудистым заболеваниям (ДАГ–1) //Кардиология. – 2000. – Т. 4, № 11. – С. 65-96.
50. Мак–Нили, У. Роль препарата меридиа (сибутрамин) в лечении ожирения /У. Мак–Нили, К. Гоа //Международный медицинский журнал. – 2000. – № 6. – С. 537–540.
51. Аронов, Д.М. Лечение и профилактика атеросклероза /Д.М. Аронов. – М.: Триада–Х, 2000. – 411 с.
52. Зезеров, Е.Г. Биохимические аспекты атеросклероза: этиология, патогенез, диагностика, лечение /Е.Г. Зезеров //Вопросы биологической, медицинской и фармацевтической химии. – 1999. – № 1. – С. 49–55.
53. Комаров, Ф.И. Биохимические исследования в клинике /Ф.И. Комаров, Б.Ф. Коровкин, В.В. Меньшиков. – Л.: Медицина, 1981. – 487с.
54. Фокин, А.С. Нейрогенная гиперхолестеринемия и атеросклероз /А.С. Фокин. – С-Пб.: ЭЛБИ, 2001. – 191 с.
55. Камышников, В.С. Справочник по клинико–биохимической лабораторной диагностике /В.С. Камышников. – Минск.: Беларусь, 2002. Т. 2, – 463с.
56. Чазов, Е.И. История изучения атеросклероза: истины, гипотезы, спекуляции /Е.И. Чазов //Терапевтический архив. – 1998. – № 9. – С. 9–16.
57. Бышевский, А.Ш. Биохимические сдвиги и их оценка в диагностике патологических состояний /А.Ш. Бышевский, С.Л. Галян, О.А. Терсенов. – М.: Издательский Центр «Академия», 2002. – 318 с.
58. Окороков, А.Н. Диагностика болезней внутренних органов /А.Н. Окороков. – М.: Медицинская литература, 2003. – Т. 6, 455 с.
Похожие работы
... клинического психолога. Проблемы с кожей делают людей злопамятными, а с печенью – обидчивыми. Страдающие хроническими кожными болезнями типа псориаза или дерматитов в период обострения нередко впадают в депрессии с оттенком стеснительности. Болезненно воспринимают внимание к своей внешности. Становятся очень подозрительны к людям и не выносят критики в свой адрес. При язве желудка или других ...
... агент в месте его внедрении. На МАС, как правило, накладывается ГАС, образованный развивающимися общими явлениями. Наоборот, ГАС вторично влияет на МАС с помощью нейрогуморальных механизмов (например, антивоспалительных гормонов). Шок (англ. shock – удар) – патологический процесс, возникающий при действии на организм сверхсильных патогенных раздражителей и характеризующийся фазным нарушением ...
... сахарным диабетом является профилактикой развития и прогрессирования у них диабетической микроангиопатии, атеросклероза и других осложнений данной патологии. 2. Особенности питания при сахарном диабете в пожилом и старческом возрасте В России, как и во всем мире, число людей старше 60 лет в обществе растет, самые высокие темпы роста численности отмечены для населения в возрасте 80 лет и ...
0 комментариев