Навигация
1.1.7 Питательные среды
Другим аспектом физиологии, животных клеток, которому уделяют все большее внимание, являются питательные среды. Исследования компонентов питательных сред, выполненные в различных лабораториях, явились основой; для создания ныне хорошо известных сред, а также понимания механизма гормонального регулирования.
Бессывороточные среды. В настоящее время наблюдается тенденция к производству моноклональных антител в средах с низким содержанием сыворотки или в бессывороточных средах, хотя публикаций о применении таких сред в промышленном масштабе очень немного. Преимущества таких сред по сравнению с обычными, содержащими 10 и более процентов сыворотки, заключаются в упрощении процесса и удешевлении продукции. В случае бессывороточных сред, кроме того, достигается более высокая воспроизводимость процесса, поскольку каждый компонент среды хорошо известен и может быть получен в очень чистом состоянии. Наконец, бессывороточные синтетические среды полезны и в научно-исследовательских работах, поскольку в них можно селективно варьировать концентрацию любого компонента. По сути дела, для проведения корректных научных исследований по росту гибридомных и других клеточных линий в первую очередь необходимо иметь хорошо охарактеризованную бессывороточную среду.
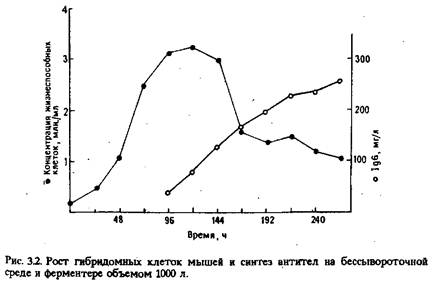
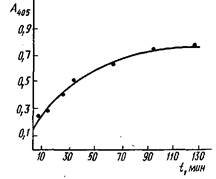
Кинетика роста. До появления бессывороточных сред закономерности роста животных клеток изучали на средах, содержащих различные сыворотки. Позднее оказалось, что кинетика роста и биосинтез антител гибридомными клетками на бессывороточных средах и в средах, содержащих сыворотку, очень близки. На рис. 2 представлены характеристики роста гибридомных клеток грызунов и образования IgG на бессывороточной среде в эрлифтом ферментере объемом 1000 л. Клетки росли с временем удвоения 18 ч, максимальная плотность популяции была равна 3,2 млн. жизнеспособных клеток в 1 мл. После 260 ч ферментации выход антител составил 26 г. В других случаях время ферментации зависит от конкретной линии клеток и изменяется от 140 до 400 ч. Время удвоения клеток при этом составляет 11–36 ч, а максимальная плотность популяции – 1,0–4,6 млн. клеток в 1 мл.
2.1.5. Биосинтез антител. Концентрация моноклональных антител, получаемых в эрлифтных ферментерах Celltech, в среднем составляет 109 мг/л и изменяется в диапазоне 40 – 500 мг/л. Эти изменения отражают характерные особенности каждой линии клеток. Отметим, что выход антител при культивировании в колбах или во вращающихся сосудах значительно ниже, чем в ферментерах. Более высокие выходы антител в ферментерах являются результатом оптимизации процесса, особенно в отношении состава культуральной среды.
1.2 Эффект фазы роста культуры
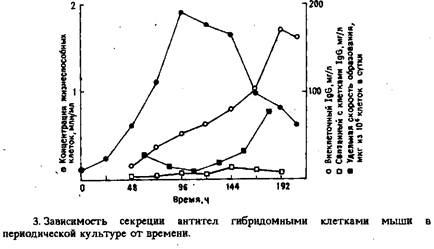
Как видно из приведенных на рис. 2 данных, образование антител продолжается даже после того, как клетки перестали пролиферировать. Было высказано обоснованное предположение, что синтезированные антитела не сразу секретируются клетками в культуральную среду. Позднее, в фазе отмирания, клетки лизируют и высвобождают находящиеся в них антитела. Полученные результаты побудили провести специальные эксперименты по определению содержания антител в клетках в фазах роста и отмирания. Оказалось, что количество антител, которые удается выделить из гибридомных клеток после их разрушения с помощью замораживания – размораживания, в течение всех фаз роста практически постоянно и слишком мало, чтобы можно было объяснить наблюдаемую кинетику синтеза антител.
Полученный осветленный раствор содержит моноклональные антитела в низкой концентрации, поэтому обычно для облегчения последующих операций его концентрируют с помощью ультрафильтрации в тангенциальном потоке. При этом удаляются вода и низкомолекулярные примеси. После этой стадии объем раствора уменьшается примерно в десять раз, а концентрация антител достигает 1–5 т/л.
2. Очистка антител
В зависимости от области применения антител и от их свойств можно использовать самые различные способы очистки. Для диагностических целей часто достаточно иметь препараты антител 70–95%-ной степени чистоты. С другой стороны, при применении антител in vivo их чистота должна быть намного выше. В сывороточных средах содержание антител не превышает 10% от общего количества белка. Хотя проведение процесса на бессывороточных средах и облегчает очистку, на практике относительно легко достичь 90%-й и даже более высокой степени чистоты независимо от содержания сывороточных белков. При очистке антител для их использования in vivo на последних стадиях очистки приходится решать одни и те же проблемы независимо от природы питательной среды. Высокоэффективные методы очистки необходимы для удаления следовых количеств не только примесных белков, но и пиротенов и ДНК. Ранее для очистки антител широко применяли фракционирование сульфатом аммония с последующей ионообменной хроматографией. Применение этих методов осложняется тем, что различные моноклональные антитела имеют разные изоэлектрические точки. Кроме того, после ионообменной хроматографии чистота антител не превышает 90%, поэтому для дальнейшей очистки необходимы другие методы, например гель-фильтрация. Однако в тех случаях, когда моноклональные антитела используют для диагностики или иммуноаффинной очистки, ионообменная хроматография или ее сочетание с предварительным осаждением позволяют получить препараты достаточного качества.
2.1 Очистка с помощью иммобилизованного белка А
Известен метод получения препаратов различных антител с чистотой более 95%, основанный на применении иммобилизованного белка А. Этот аффинный лиганд не нашел широкого применения для очистки моноклональных антител из-за его плохого связывания с иммуноглобулинами типа IgGi, к которому относится около 90% моноклональных антител. Можно, однако, подобрать условия, при которых связывающая способность иммобилизованного белка А по отношению к IgGi возрастает в пять раз. Тогда после одной стадии аффинной очистки можно получить высокочистые антитела с выходом более 90%. На рис. 3.6 представлены электрофореграммы, полученные в полиакриламидном геле в присутствии додецилсульфата натрия, после концентрирования и моноклональных антител после очистки на иммуносорбенте с белком А. Образцы были подготовлены так, чтобы в каждом из них содержались одинаковые количества моноклональных антител; таким образом можно наглядно сравнить общее количество белка в каждом образце после выдерживания с красителем кумасси голубым. Во многих случаях дальнейшая очистка антител уже не нужна. Кроме того, быстрая одностадийная очистка позволяет получить более активные антитела, чем медленные многостадийные методы. Колонку с иммобилизованным белком А часто можно использовать более тридцати раз, хотя ее аффинные свойства сильно зависят от способа регенерации. Таким образом, высокая цена белка А компенсируется длительным временем функционирования колонки и высокими качеством и выходом получаемых антител.
Использование микрокомпьютерной системы управления позволяет совершенствовать метод аффинной хроматографии. Свойства аффинных колонок после каждого цикла меняются, как бы точно ни выполнялись условия очистки. Поэтому система управления, основанная на регистрации времени или объема, не может реагировать на такие изменения. Высокая стоимость аффинных колонок, особенно белка А, а также ценность получаемых моноклональных антител требуют включения в систему управления приборов, реагирующих на любые отклонения и неполадки. Например, применение датчиков на воздух позволяет предотвратить высушивание колонки при прекращении подачи раствора, а использование клапанов давления перед входными фильтрами предотвращает разрушение системы, если колонка забьется.
2.2 Характеристика очищенных антител
При использовании in vivo к качеству моноклональных антител предъявляются очень высокие требования. Поэтому характеристике получаемых для этих целей в производственном масштабе антител следует уделять самое тщательное внимание. Необходимо, например, разработать методы определения пикограммовых количеств возможных примесей. Если же моноклональные антитела предполагается использовать для диагностических целей, важнее удостовериться в их функциональной пригодности. Как правило, для того чтобы показать, что препарат антител удовлетворяет принятым стандартам, его характеризуют двумя методами – изоэлектрическим фокусированием и электрофорезом в полиакри-ламидном геле в присутствии додецилсульфата натрия.
3. Дальнейшие перспективы
Для дальнейшего совершенствования процессов получения и очистки моноклональных антител необходимо провести исследования в нескольких направлениях. Используемые в настоящее время процессы ферментации очень эффективны. Однако более глубокое понимание физиологии гибридом и линий клеток человека должно позволить увеличить выход продукта. Например, очень перспективным представляется улучшение линий клеток путем повторного слияния гибридом с родительскими миеломами, имеющими особенно благоприятные характеристики. Кроме того, большое поле деятельности открывается в области инженерии моноклональных антител. Эта технология позволит создавать новые типы моноклональных антител с заранее заданными свойствами и получать их в больших количествах. Необходимо также развивать методы скрининга для поиска клонов, секретирующих антитела при культивировании на бессывороточных средах.
В заключение отметим, что получение и очистка моноклональных антител требуют новых как научных, так и инженерных разработок, чтобы можно было проектировать процессы, обеспечивающие как быстрый рост продуцирующих клеток, так и высокое качество конечного продукта. Создание таких процессов позволит получать большие количества моноклональных антител с очень высокой степенью чистоты. Ясно, что такие процессы являются идеальными для получения новых моноклональных антител, которые могут быть применены в иммуноанализе.
Похожие работы
... только гибридные клетки, унаследовавшие от родительских клеток способность размножаться и синтезировать специфические иммуноглобулины. Подготовительные этапы перед проведением слияния Полностью процедура получения моноклональных антител включает в себя следующие этапы: ﭼ иммунизация животных; ﭼ подготовка клеток к слиянию; ﭼ слияние; ﭼ отбор ...
... мкг инсулина в 0,7 мл физиологического раствора. Отбор крови проводят через 7-9 дней из сердца. Второй цикл иммунизации осуществляется после месячного отдыха животных по схемам 45, 46 и 47 дней. Для получения антисывороток с титром, удовлетворительным для проведения ИФА, часто требуется 4-5-кратное повторение циклов иммунизации. Отбор крови каждый раз проводится на 7 - 9-й день после последней ...
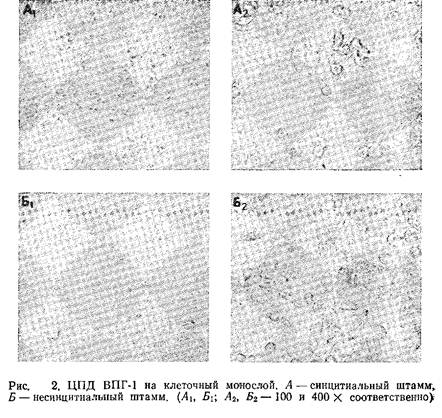
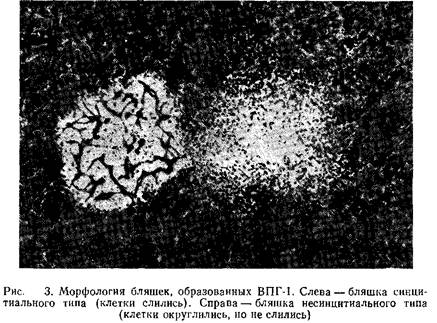
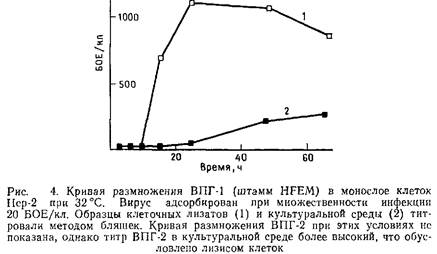
... круг хозяев и лучше всего размножается в клетках американского сомика-кошки. Методы культивирования и очистки этого вируса такие же, как и для ВПГ-1, за исключением того, что ВВ-клетки и вирус культивируют при 28°С. 2. Цитомегаловирус человека Р-субгруппа герпесвирусов включает в себя цитомегаловирусы различных животных. Цитомегаловирусы человека вызывают различные заболевания, особенно у ...
... процесс разделения нестабильных веществ можно проводить в холодильной камере. Выделенное соединение подвергают структурному химическому исследованию, а затем изучают его фармакологическое действие. Получение лекарственных веществ методом культуры тканей высших растений В нашей стране заготавливаются десятки тысяч тонн ЛРС. Однако потребность в БАВ, содержащихся в растениях, с каждым годом ...

0 комментариев