Навигация
Докажите на опытах, что нитроаммофоска содержит ионы;
1. Докажите на опытах, что нитроаммофоска содержит ионы;
![]()
2. Докажите, что в составе жидкого комплексного удобрения (ЖКУ)5 содержатся аммонийные группы.
Практическая работа, по распознаванию удобрений требует большой предварительной экспериментальной подготовки учащихся. При выполнении лабораторных опытов они знакомятся с азотными и фосфорными удобрениями (их внешним видом) растворимостью в воде), с качественными реакциями на соли аммония и нитраты. Сюда же необходимо включить краткое изучение карбамида (мочевины), который нашел широкое применение в сельском хозяйстве не только как ценное азотное удобрение, но и как добавка в корма животных. Учитель отмечает, что карбамид — органическое соединение, атомы в нем связаны ковалентной связью. Карбамид представляет собой белое кристаллическое вещество, хорошо растворимое в воде. При нагревании карбамид легко разлагается с выделением аммиака. Это свойство и можно использовать для распознавания данного удобрения.
В пробирку помещают 1—2 гранулы или немного порошка карбамида (покрывают им только дно) и слегка нагревают. К ее отверстию подносят влажную фенолфталеиновую бумажку. Предлагать учащимся полное уравнение реакции с образованием биурета не следует:
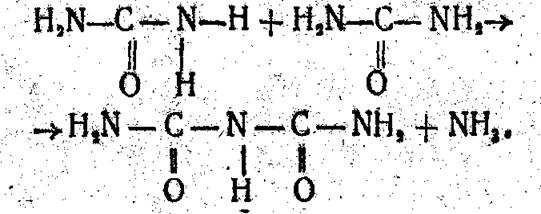
Кроме лабораторных опытов, предваряющих практическую работу, учащиеся, готовясь к занятию, должны повторить тему «Азот и фосфор», калийные» фосфорные и азотные удобрения. Желательно, чтобы они предварительно ознакомились с предлагаемой нами таблицей 1 «Распознавание удобрений», но не переносили ее в тетрадь. Главное, чтобы учащиеся поняли, что таблица позволяет распознавать минеральные удобрения, устанавливать ионы:
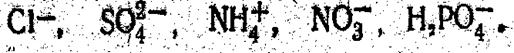
Рекомендуемая таблица определения удобрений отличается от той, которая помещена в стабильном учебнике для IX класса, не только отбором удобрений, но и методикой их установления, а также заменой дефицитных реактивов более доступными. Так, мы не используем нитрат серебра, который необходим для распознавания хлоридов и фосфатов. Это объясняется не только тем, что данная соль дефицитна и часто отсутствует в школе, но и тем, что суперфосфат может не давать желтый осадок, так как удобрение содержит различные примеси (в зависимости от сырья).
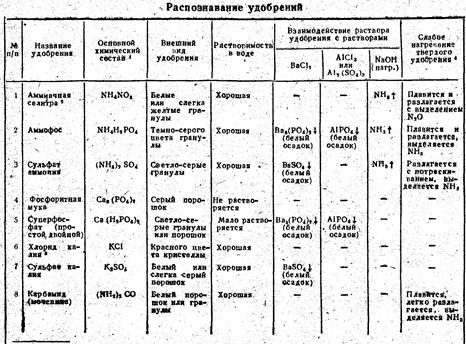
Для обнаружения фосфорных удобрений, можно использовать растворимую соль алюминия, которая приводит, к образованию нерастворимого фосфата алюминия AIPO4 белого цвета. Другие растворимые удобрения с солью алюминия осадков не дают.
Исключение нитрата серебра приводит к тому, что хлорид калия остается нераспознанным. Чтобы доказать, что данная соль является хлоридом, можно использовать ацетат свинца, который при взаимодействии с хлоридом дает белый осадок РЬСЬ. Однако при сравнительном анализе удобрений можно практически не прибегать к этой соли. Хлорид калия определяют методом исключения.
В таблицу не включена реакция удобрения с серной кислотой и медью по следующим соображениям:
а) для распознавания иона NCV представлено в таблице только одно нитратное соединение— нитрат аммония;
б) реакция небезвредна для учащихся, если не придерживаться определенных рекомендаций. Практика показывает: если в таблице указана реакция, учащиеся, как правило, проводят ее со всеми удобрениями. В связи с этим к указанной реакции следует прибегать только в необходимых случаях. Аммиачную селитру легко отличить от прочих удобрений, содержащих аммонийную группу, с помощью других реакций.
В таблицу введена новая графа: «Слабое нагревание твердого удобрения». Она дана последней не случайно. К нагреванию удобрений учащиеся прибегают в последнюю очередь, когда требуется распознать аммиачную селитру или карбамид. Другие, соли аммония должны быть уже определены с помощью химических реакций.
Карбамид и аммиачная селитра при нагревании ведут себя вначале аналогично: они плавятся. Но при дальнейшем нагревании карбамид разлагается с выделением аммиака, а нитрат аммония —с выделением оксида азота (I) NaO газа без запаха и цвета.
Известно, что большие трудности возникают при распознавании удобрений, содержащих ионы калия, по окраске пламени. Дело в том, что удобрения обычно содержат примеси. Например, в хлориде калия молено обнаружить хлорид натрия. Примеси скрадывают фиолетовую окраску пламени калия. Поэтому в таблице для распознавания удобрений этот показатель не указан.
Изучая таблицу для распознавания минеральных удобрений, учащееся могут заметить, что не растворяется в воде фосфоритная мука, мало растворяется суперфосфат, все остальные удобрения хорошо растворяются. К растворению удобрений прибегают тогда, когда речь идет об определения ионов С1~,
SO-, NH, НРО. Для этого 1—2 гранулы или немного порошка удобрения (покрыть им только дно пробирки) растворяют в 1 мл воды.
Распознавание удобрений учащиеся проводят только с малыми количествами.
Практическая работа может быть проведена по двум вариантам. Первый вариант: учащимся предлагаются два удобрения в пакетах (под номерами), и нужно определить их содержимое. Ученик начинает выполнять задание с процесса растворения удобрений. Это позволит установить фосфоритную, муку и суперфосфат (для распознавания удобрений по первому варианту нежелательно предлагать фосфоритную муку). Допустим, что в двух пакетах растворимые удобрения. Далее исследуется содержимое пакета № 1. Ученик переливает к нескольким каплям раствора удобрения 2— 3 капли раствора хлорида бария—выпадает белый осадок, Анион установлен. Согласно таблице, это удобрение может быть сульфатом аммония, аммофосом или сульфатом калия (суперфосфат устанавливается по растворимости). Проводя реакцию с раствором щелочи, учащийся обнаруживает аммиак. Отсюда он делает вывод: сульфат калия исключается, остается предположить, что в пакете находится сульфат аммония или аммофос. Чтобы установить удобрение, действуем раствором хлорида алюминия: исследуемое удобрение не дает реакции. Следовательно, это сульфат аммония.
Теперь исследуется, пакет № 2: раствор удобрения не дает осадков с хлоридом бария, хлоридом алюминия, не реагирует со щелочью (при нагревании) и не разлагается при слабом нагревании. Следовательно, исследуемое удобрение — хлорид калия.
Свои результаты опытов ученик может отразить в табл. 2 (отсутствие записи или прочерка показывает, что проводить соответствующий опыт нецелесообразно, так как удобрение уже определено).

Рассмотрим еще один пример, Удобрение из пакета № 1 не дает реакции с хлоридами бария и алюминия, при нагревании с раствором щелочи выделяется аммиак (обнаруживается фенолфталеиновой бумажкой), но аммиак не обнаруживается при нагревании твердого удобрения. Это нитрат аммония. Удобрение же из пакета № 2 не дает ни одной »из указанных реакций, но оно легко разлагается при нагревании с выделением аммиака. Это карбамид. Следует иметь в виду, что ряд аммонийных солей, также термически разлагается е выделением аммиака (дигидрофосфат аммония, сульфат аммония в др.), но, в отличие от карбамида, они дают реакции на соответствующие анноны.
С удобрением по первому варианту приходится иногда проводить до четырех реакций, поэтому в пакетах должно быть не менее 4-5 гранул удобрения. Если для распознавания требуется проводить меньше реакций, то соответственно уменьшается и число гранул удобрения.
По второму варианту каждому ученику предлагаются две экспериментальные задачи, в каждой из которых 3 известных удобрения. Приведем несколько примеров задач.
В трех пакетах под номерами даны следующие удобрения:
а) аммофос, аммиачная селитра, хлорид калия;
б) сульфат аммония, суперфосфат, сульфат калия;
в) карбамид, хлорид калия, фосфоритная мука.
Определите, какое удобрение находится в пакете с соответствующим номером».
Прежде чем приступить к решению задачи, ученик должен составить план ее решения. Например, для задачи «а» (см. табл. 3):
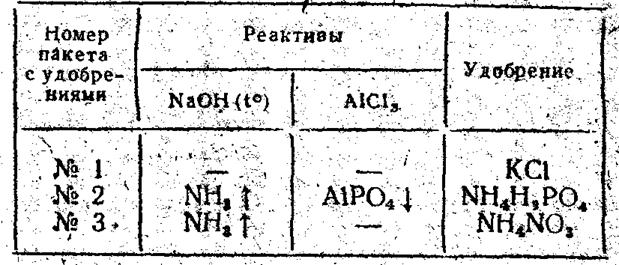
Необходимо обратить особое внимание учащихся на рациональное решение задач, исключающее проведение лишних реакций. При выставлении оценки следует это учитывать.
Проведением практической работы не завершается вопрос распознавания удобрений. На последующих уроках и практических занятиях необходимо продолжить закрепление знаний учащихся об удобрениях.
Глава 3. Методические разработки по теме: «Минеральные удобрения»Цели:
· усвоение учащимися состава азотных, фосфорных, калийных удобрений и их биологической роли,
· развитие умений применять имеющиеся знания в новых ситуациях,
· закрепление знаний о единстве живого и неживого,
· развитие интереса к истории и новым фактам науки.
Оборудование и реактивы: набор удобрений, вода, растворы нитрата серебра и ацетата натрия, два образца в пробирках, держалка, стенгазета «Роль ученых в развитии агрохимии», задания к уроку.
ХОД УРОКА
I. Актуализация знаний
Учитель:
Орешек знаний тверд,
Но все же мы не привыкли отступать.
Нам расколоть его поможет
Желание «хочу больше знать!»
– С таким желанием начнем урок.
В наши дни потребительские отношение к природе, расходование ее ресурсов без осуществления мер по их восстановлению уходит в прошлое. Не каждый регион, не каждый район может гордиться плодородием своей почвы, но любое наземное природное сообщество, тем более человек, своим существованием обязаны почве. Почему?
Ответ учащихся: Почва является средой обитания единственных на Земле автотрофных организмов – растений. Только растения из неорганических веществ синтезируют органические вещества. Все остальные животные, люди – потребители органических веществ. Вот почему мы обязаны почве.
Учитель: Поэтому мы должны знать, как поддерживать и приумножить плодородие почвы.
Изучение вопросов питания растений и повышения их урожайности путем применения минеральных удобрений является предметом агрохимии. Тема нашего урока «Минеральные удобрения».
II. Домашнее задание: §23, вопросы 7-10, задание 3,4 (по стр.70 уч. химии), §47 (по биологии)
Чтобы успешно выполнить домашнее задание, на уроке мы должны знать классификацию удобрений, их состав и влияние удобрений на развитие растений.
Для решения этих задач, мы будем опираться на знания, полученные на предыдущих уроках химии и биологии.
III. Изучение новой темы
Учитель: Основоположниками агрохимии являются немецкий ученый Либих. Юстус, в России Д.И.Менделеев, позже идеи Менделеева развивал Д.Н.Прянишников. Называя фамилию Д.И.Менделеева, я не ошиблась. Да, это тот ученый, который 140 лет тому назад открыл периодический закон химических элементов.
Как же были решены вопросы повышения плодородия почвы Д.И. Менделеевым?
Сообщение учащегося: Будучи великим естествоиспытателем, Д.И. Менделеев придавал большое значение экспериментальным исследованиям. Чтобы знать, как реагируют растения на те или иные питательные вещества при корневом питании, какую дозу и как вносить минеральные удобрения, он впервые в России поставил полевые опыты на полях своего имения в подмосковном селе Боблово. Ученый сам составил программу опытов, осуществил их закладку, проводил наблюдения, делал выводы, впоследствии привлек к этой работе студентов сельхозакадемии, в числе которых был и будущий ученый К.А Тимирязев.
За 5-6 лет запущенное и отсталое имение превратилось в образцовое, его урожай в 3 раза превышали урожаи соседних мужиков. В результате Менделеев заложил основы научного земледелия.
Учитель: Менделеев разработал оптимальные соотношения употребления минеральных удобрений с содержанием каких питательных элементов?
Ответ учащихся: Азота, фосфора, калия.
Учитель:Какое влияние оказывает азот на растения?
Сообщение учащегося: При недостатке азота задерживается образование зеленой части растений – листьев, стеблей. Растения плохо растут, листья становятся бледно – зелеными и даже желтеют. Азот – обязательная часть белков и нуклеиновых кислот. При среднем урожае пшеницы за один сезон выносится до 75 кг азота с каждого гектара земли.
Учитель: Какие же азотные удобрения производят в Менделеевском заводе? У вас на столе находятся образцы удобрений. Используя таблицу 19 на стр. 67, напишите формулы данных азотных удобрений, дайте им названия (работа в группах). Азотные удобрения характеризуются содержанием азота.
Выполнение задачи №1 (см. задания к уроку; 1, 2 группы решают 1а; 3, 4 группы – 1б; 5, 6 группы – 1в. В каждой группе ответственные проверяют выполнение заданий и оценивают их).
Во время встречи главный агроном района М.Х. Авзалов сообщил, что самым лучшим азотным удобрением для почвы нашего региона является нитрат аммония. Решив задачу, мы в этом убедились.
Выполнение задачи №2
Огромное значение для человека играет фосфор. Суточная потребность организма человека в фосфоре составляет до 1,5 г, он входит в состав нуклеиновых кислот, АТФ, ферментов, костной, нервной ткани. Недостаток фосфора вызывает нарушение обмена веществ в организме, поэтому академик А. Е. Ферсман фосфор назвал «элементом жизни и мысли». Поставщиком фосфора в организм человека и животных являются растения. Как же влияет фосфор на рост и развитие растений?
Сообщение учащегося: Энергия солнечного света в процессе фотосинтеза накапливается в растениях в виде АТФ только при достаточном количестве фосфорных соединений в клетке. Усиленное снабжение растения фосфором позволяет получать более ранний урожай и высокого качества. При недостатке фосфора плодоношение уменьшается и созревание плодов сильно замедляется.
Учитель: Наличие природных соединений – фосфоритов дает возможность производить фосфорные удобрения в соседней Кировской области. В состав фосфорита входит нерастворимый в воде фосфат кальция. Чтобы привести его в усвояемое растениями состояние в производстве используются два метода:
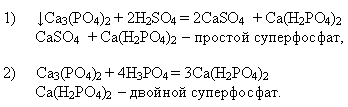
Питательную ценность фосфорных удобрений условно выражают через массовую долю оксида фосфора (V). Например, содержание оксида фосфора (V) вычисляется в двойном суперфосфате соотношением относительной молекулярной массы оксида фосфора (V) на относительную молекулярную массу двойного суперфосфата:
![]()
Выполнение лабораторной работы (см. задание к уроку №3) и обсуждение результатов исследования.
В корневом питании растений важное значение имеют калийные удобрения.
Сообщение учащегося: Калий ускоряет процесс фотосинтеза и содействует накоплению углеводов: сахара в сахарной свекле, крахмала в картофеле, а у злаковых – пшеницы, ржи, риса – он способствует укреплению стебля и устраняет их полегание. Калий откладывается в стебле. Поэтому современная зерноуборочная техника и измельчает солому, и разбрасывает ее по всей площади поля, так и частично пополняет убыль калия.
Недостаток калия вызывает куполообразное закручивание листьев, на них появляются ржавые крапинки.
Выполнение задачи №4 (в каждой группе ответственные проверяют выполнение заданий и оценивают их.)
Учитель:Как получают калийные удобрения?
Сообщение учащегося: Источником получения калийных удобрений служат естественные отложения калийных солей в районе Соликамска, на большой площади между верховьями р. Кама и предгорьями Урала, на территории Пермского края. Это минералы карналлит, содержащий хлориды калия и магния (КCl * MgCl2 * 6Н2O) и сильвинит, содержащий хлориды калия и натрия (КCl * NaCl).
Учитель: Калийные удобрения условно оцениваются содержанием оксида калия К2О:
![]()
Получаемая при сжигании растительных материалов зола является качественным, в то же время дешевым и приемлемым калийным удобрением. В ее состав входит карбонат калия. Вычислите питательную ценность этого удобрения.
IV. Заключение
Учитель: Почва тем замечательна, что может восстанавливаться. Главное, ценить ее и рационально ею пользоваться. Только тогда у каждого на столе будут вкусный пышный каравай и другие продукты питания, а полноценное питание – залог здоровья.
Учитель оценивает работу учащихся.
Задания к уроку по теме «Минеральные удобрения», 9 класс
1. Сопоставьте массовые доли азота в следующих удобрениях:
а) нитрат калия,
б) нитрат натрия,
в) нитрат аммония.
2. Вычислите массу нитрата аммония, который вносят на поля совхоза им. Токарликова площадью 100 га, если масса внесенного азота на 1 га составляет 60 кг.
3. Лабораторная работа. В двух пробирках даны образцы разных удобрений. Определите, в какой пробирке содержится фосфорное удобрение. Как вы думаете, когда: осенью или весной вносить это фосфорное удобрение в почву? Почему?
4. Какую массу 4%-го раствора можно приготовить из 120 кг хлорида калия для подкормки капусты на полях ООО «Агросоюз»?
Литература
1. В.Кармазин «Наш хлеб», М., Из-во «Правда», 1986 г.
2. Н.Л.Глинка «Общая химия», М., «Интеграл – Пресс», 2005 г.
3. И.Г.Хомченко Сборник задач и упражнений по химии для средней школы, М., «Новая волна», 2002 г.
4. Г.Е.Рудзитис, Ф.Г.Фельдман «Химия 9», М., «Просвещение», 2008 г.
5. С.Г.Мамонтов, В.Б.Захаров, Н.И.Сонин «Биология 9», М., «Дрофа», 2000 г.
6. Орлова А. Агрохимическая лаборатория. (Б-ка пионера «Знай и умей»), М.: Дет. литература, 1973, с. 83—84.
7. Федоров П. А. Агрохимические опыты по химии. Пособие для учителей. Мл Просвещение, 1965, с. 30.
8. Шибанов А. А., Щербаков М. И., Устаменко Г. В. Основы агротехники полевых культур. Учеб. пособие для учащихся 9— 10 классов сельской школы, 2-е изд. M.: Просвещение, 1976, с. 45.
Похожие работы
... учебного процесса; 4) Абсолютно неудовлетворительная объективность оценки знаний обучающихся, невозможность сопоставления оценок, полученных или разных обучающих или, тем более, в разных учебных заведениях [10]. 1.8 Тестовый контроль знаний на уроках химии В последние годы в связи с проведением в стране эксперимента по внедрению единого государственного экзамена (ЕГЭ) тестовые задания все ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... условиями и факторами при выборе конкретного эксперимента определялись его доступность, наглядность и простота исполнения, а также связь со школьным материалом и практикой. В любом случае предполагается возможность вариативного разноуровневого проведения курса на основе педагогики сотрудничества учителя и ученика с применением оптимального сочетания различных методов обучения. Повысить ...
... период многие страны приняли решение о полном или постепенном отказе от развития атомной энергетики. 1.3 Особенности альтернативной водородной энергетики Водородная энергетика включает следующие основные направления: Разработка эффективных методов и процессов крупномасштабного получения дешевого водорода из метана и сероводородсодержащего природного газа, а также на базе разложения воды; ...




0 комментариев