Навигация
Задачи с правильным ответом
3.2.2 Задачи с правильным ответом
Задача 1. В стратосфере на высоте 20-30 км находится слой озона O3, защищающий Землю от мощного ультрафиолетового излучения Солнца. Если бы не "озоновый экран" атмосферы, то фотоны большой энергии достигли бы поверхности Земли и уничтожили на ней все живое. Подсчитано, что в среднем на каждого жителя Белгорода в воздушном пространстве над городом приходится по 150 моль озона. Сколько молекул озона и какая его масса приходится в среднем на одного белгородца? (Ответ: 9,03*1025; 7,2 кг)
Задача 2. Одинаковое ли (и какое именно) число молекул содержится в 1г воды и в 1г кислорода? Какова роль этих веществ в биосфере Земли? (Ответ: 0,33*1023; 0,37*1027)
Задача 3. Чтобы приготовить бордосскую смесь (препарат против фитофторы – грибкового заболевания огородных растений), используют медный купорос CuSO4?5H2O. Рассчитайте число атомов кислорода и водорода, которые содержатся в 350 г этого вещества. (Ответ: 75,8*1023; 84,2*1023)
Задача 4. В сутки человек вдыхает приблизительно 25 кг воздуха. На каждые 100 км пути автомобиль расходует 1825 кг кислорода. Сколько суток сможет дышать человек воздухом, если одна из машин проедет на 100 км меньше? Используя приведенные факты и результаты ваших расчетов, подготовьте:
а) рекламный проспект автомобилей;
б) текст обращения к президенту России о защите природы.
(Ответ: 347 суток 14 часов 52 минуты)
Задача 5. Основной компонент природного газа – метан. Некоторые крупные месторождения природного газа, например Астраханское, Оренбургское, помимо углеводородных газов содержат значительное количество сероводорода. Эта примесь, с одной стороны опасна, так как вызывает сильную коррозию трубопроводов и перекачивающей аппаратуры. Кроме того, при сгорании такого газа получается оксид серы (IV), что вызывает загрязнение атмосферы. С другой стороны сероводород является ценным химическим сырьем, из которого можно получить, например, серную кислоту. Предложите рациональные, по вашему мнению, способы очистки природного газа от сероводорода.
Задача 6. Белгородский мел содержит карбонат кальция и карбонат магния в пересчете на CaO и MgO соответственно 54 и 0,5 %.
Сколько примеси содержит белгородский мел?
Какой объем CO2 выделится в атмосферу при обжиге образца такого мела массой 1 кг? (Ответ: 2,5%)
Задача 7. В природе постоянно происходит круговорот биогенных элементов: углерода, водорода, кислорода, фосфора, азота и др. Человек в процессе своей деятельности вмешивается в круговорот веществ, использую минеральное сырье для своих нужд. Какая масса углерода должна превратиться в CO2, чтобы получить 1 л минеральной газированной воды с концентрацией углекислоты 2%, ρ=1г/см3. (Ответ: 3,84 г.)
Задача 8. Азот – незаменимый биогенный элемент, поскольку входит в состав белков и нуклеиновых кислот. Атмосфера – неисчерпаемый резервуар азота, однако основная часть живых организмов не может непосредственно использовать этот азот: он должен быть предварительно связан в виде химических соединений. Существуют азотфиксирующие бактерии, способные фиксировать азот воздуха и превращать его в доступную для растений форму. С помощью таких бактерий при хорошем урожае клевер может накапливать за сезон 150-160 кг/га азота. Какой объем воздуха в м3 содержит такую массу азота? Какую массу 10 % раствора аммиачной воды (используемой в качестве удобрений) может заменить 1 га клевера, накопивший за сезон 100 кг/га азота? (Ответ: 120 м3, 2100 кг)
Задача 9. Растения поглощают минеральные вещества и углекислый газ и под действием ультрафиолета синтезируют глюкозу, выделяя кислород.
Какой объем CO2 усвоили зеленые листья сахарной свеклы для получения 100 г сахарозы, из которой можно изготовить 10 конфет (одна конфета содержит примерно 10 г сахара)? (Ответ: 26 л СО2).
Задача 10. Листья растения махорки содержат лимонную кислоту, примерно 3%. Какая масса зеленых листьев этого растения потребуется для получения 1 кг лимонной кислоты, если потери при производстве составляют 15 %? (Ответ: 39,1 кг). [21, 26-27].
3.2.3 Задачи для самостоятельного решения
1. Большой ущерб водным организмам наносят соединения мышьяка. Особенно ядовиты соединения мышьяка (III) Предложите способ очистки сточных вод от арсенатов и арсенитов, принимая во внимание, что мышьяк является аналогом фосфора.
2. Накопление углекислого газа в атмосфере становится опасным загрязнением – приводит к парниковому эффекту. Какой объем CO2 попадает в атмосферу при сжигании 100 г полиэтилена (100 шт. использованных пакетов)?
3. Поскольку нефтепродукты горючи, очистку от них водной поверхности можно было бы проводить путем сжигания нефтяной пленки. Такой способ, конечно, не экономичен, он связан с потерей топлива, но охрана природы, сохранение морской и прибрежной фауны и флоры важнее, чем экономия нефти. Трудность сжигания нефтяной пленки заключается в том, что поджечь можно только относительно толстый слой плавающей на поверхности воды нефти. Если же пленка тонкая (так бывает в большинстве случаев), поджечь ее не удается. Предложите способ сжигания тонких пленок нефтепродуктов на поверхности воды.
4. Большие неприятности доставляет наличие в сточных водах карбоновых кислот и их солей. Предложите физико-химический способ очистки воды от этих загрязнений.
5. При нейтрализации промышленных стоков белгородского завода "Ритм" было получено 300 кг осадка Cr(OH)3. Какую массу металлического хрома можно получить из осадка, если производственные потери составляют 10 %
6. Маршрутный автобус расходует за день 60 кг бензина. Сколько кубометров газа выделяет он в городе, загрязняя среду? Плотность этого газа при температуре 0°С равна 0,002 кг/м3. Какие способы защиты атмосферного воздуха от загрязнения выбросами автотранспорта вы можете назвать?
7. Для обогрева почвы в парниках применяется нагревательный элемент, изготовленный из стальной проволоки длиной 693 м и сечением 7 мм2. Определите количество теплоты, выделяемой ежесекундно нагревательным элементом, если по нему проходит ток силой 22,7 А. В чем сущность «парникового эффекта», играющего важную роль в тепловом балансе нашей планеты?
8. Во время пахоты на влажной почве колесный трактор забуксовал. Выполняется ли в этом случае трактором работа? Какая экологически нежелательная проблема возникает при этом?
9. Рыжие лесные муравьи обладают феромоном тревоги - кислотой, которая одновременно служит оружием. Установите его структурную формулу, если вещество разлагается при нагревании, дает реакцию серебряного зеркала.
10. Рассчитайте объем СО2, возвращенного в круговорот углерода в результате деятельности метанокисляющих бактерий, если ими было утилизировано из воздуха 4,8 т СН4. Процесс биологического окисления метана при этом идет ступенчато.
11. ПДК фенола у мест водопользования составляет 0,001 мг/л. Рассчитайте, во сколько раз концентрация фенола будет превышать ПДК, если в водоем вместимостью 104 м3 со сточными водами коксохимического предприятия было сброшено 47 кг фенола.
12. В лабораторных спиртовках этиловый спирт сгорает с выделением СО2 и Н2О. Вычислите объем СО2, который накопился в химическом кабинете объемом 288 м3, если на каждом из 18 столов за время работы учеников сгорает 2,3 г спирта.
Рассчитайте объемную долю СО2 и поясните, окажет ли он влияние на самочувствие учащихся, работающих в кабинете, если учесть, что объемная доля СО2 в атмосферном воздухе составляет 0,03%. Если же его содержание превышает 4%, то происходит раздражение дыхательных путей, возникают шум в ушах и головная боль.
13. В питьевой воде были обнаружены следы вещества, обладающего общетоксическим и наркотическим действием. На основе качественного и количественного анализов этого вещества было установлено, что это производное фенола и массовые доли элементов в нем равны: 55% С, 4,0% Н, 14,0% О, 27% Cl.
Установите молекулярную формулу вещества. Составьте уравнения реакции его получения, укажите возможные причины попадания этого вещества в среду.
14. Один из способов очистки коксового газа от оксидов азота(II) – использование метана:
![]()
Какой объем СН4 расходуется в час на взаимодействие с NO на установке по очистке коксового газа производительностью 130 тыс. м3/ч, если в 1 м3 коксового газа содержится 6 см3 NO?
15. В промышленности винилхлорид получают пиролизом дихлорэтана (1-я стадия):
![]()
В настоящее время осуществлен сбалансированный (безотходный) синтез винилхлорида. Для этого выделяющийся при пиролизе HCl смешивают с этиленом и кислородом, а затем эту смесь подвергают окислительному хлорированию в присутствии катализатора хлорида меди(II) CuCl2 на носителе (2-я стадия):
![]()
16. Рассчитайте объем НСl (н. у.), выделившегося при пиролизе 19,8 кг дихлорэтана, и массу винилхлорида, полученного при сбалансированном синтезе. Какой объем займет этилен (н. у.), необходимый для второй стадии процесса? Оцените новую технологию получения винилхлорида с позиции защиты окружающей среды от загрязнения [20, 25-28].
3.3 Тестовые задания и индивидуализация обученияОптимальным можно считать только такое обучение, которое способствует овладению приемам самостоятельного приобретения знаний и их применения.
Чаще всего используют тесты со свободно конструируемыми ответами и тесты с выборочными ответами. Последние дают возможности учащимся лучше понимать общие и отличительные качества изучаемых объектов, легче классифицировать различные явления.
Применение данного метода позволяет учителю получить сведения об усвоении того или иного материала, не затрагивая время на беседу с учащимися.
1. Впервые термин «экология» в науку ввел:
а) К. Мебиус;
б) В.Н. Сукачев;
в) Э. Геккель;
г) В.И. Вернадский.
2. Термин «экосистема» впервые предложил ученый:
а) Мебиус;
б) Фобс;
в) Тенсли;
г) Сукачев.
3. Способность экосистемы к поддержанию динамического равновесия называется:
а) выживаемостью;
б) гомеостазом;
в) плотностью;
г) дигрессией.
4. Минимальный уровень энергии в экосистеме будет у:
а) продуцентов;
б) консументов первого порядка;
в) редуцентов;
г) Консументов.
5. Закончите определение. Биосфера – это:
а) оболочка Земли, в которой существуют и взаимодействуют с окружающей средой (или когда-либо существовали и взаимодействовали) живые существа;
б) оболочка Земли, включающая часть литосферы, атмосферы и гидросферы;
в) Оболочка Земли, в которой существует человечество.
6. Вещество, сформировавшееся без участия живых организмов, В.И. Вернадский назвал
а) Живым веществом;
б) Биокосным веществом;
в) Биогенным веществом;
г) Косным веществом;
7. Круговорот углерода отличается от круговоротов воды, фосфора и азота тем, что
а) запасы углерода в горных породах недоступны;
б) не весь углерод усваивается растениями вновь;
в) углерод концентрируется в горных породах;
г) углерод вымывается в океан безвозвратно.
8. Процесс разрушения соединений азота до молекулярного состояния
а) аммонификация;
б) редукция;
в) денитрификация;
г) деструкция.
9. Определите, к каким факторам среды –– можно отнести следующие факторы: а)хищничество, б)вырубка лесов, в)влажность воздуха, г)температура воздуха, д) паразитизм, е)свет, ж)строительство зданий, з)давление воздуха, и)конкуренция, к)выброс углекислого газа заводами, л)соленость воды.
1. абиотическим – в, г, е, з, л.
2. биотическим – а, д, и.
3. антропогенным - ж, к
10. В каждом из предложенных примеров выберите тот фактор, который можно считать лимитирующим:
а) Для растений на глубине 6000 м:
Вода, температура, углекислый газ, свет
б) Для растений в пустыне летом:
Температура, свет, вода.
в) Для скворца зимой в подмосковном лесу:
Температура, пища, кислород, влажность воздуха, свет.
г) Для речной обыкновенной щуки в Черном море:
Температура, свет, пища, соленость воды, кислород.
д) Для кабана зимой в северной тайге:
Температура, свет, кислород, влажность воздуха, высота снежного покрова.
11. Расположите перечисленные источники энергии в порядке убывания их экологической опасности:
а) ГЭС;
б) ТЭЦ на природном газе;
в) солнечные электростанции;
г) АЭС;
д) ТЭЦ на угле;
е) приливно-отливные электростанции.
Правильный ответы-е, в, б, а, д, г
12. В крупных городах более половины выбросов в атмосферу производят:
а) Промышленные предприятия;
б) Энергетика;
в) Химическая и угольная отрасли промышленности вместе;
г) Транспорт.
13. Сохранение природной среды и решение экологических проблем бассейна р. Баксан относится к проблемам:
а) Локального характера;
б) Регионального характера;
в) Глобального характера;
г) Районного масштаба.
14. Проблема разрушения озонового слоя относится к проблемам:
a) Локального характера;
б) Глобального характера;
д) Районного масштаба;
с) Регионального характера;
15. Способность ядовитых веществ оказывать вредное действие на живые организмы называется
а) токсичность;
б) техногенез;
в) автогенез;
г) куммулятивность.
16. Тератогенное действие на живые организмы – это действие:
а) на поджелудочную железу;
б) на почки;
в) на плод в утробе матери;
г) на рядом находящиеся живые организмы;
17. Развитие злокачественных опухолей под воздействием вредных факторов, называется:
а) Онтогенез;
б) Канцерогенез;
в) Филогенез;
г) Биогенез;
18. Одними из самых сильных канцерогенов признаны:
а) Хлорорганические соединения;
б) Галогены;
в) Тяжелые металлы;
г) Фосфорорганические соединения;
19. Использованные люминесцентные лампы являются источником одного из наиболее опасных ядов – ионов:
а) Pb – свинца;
б) Cd – кадмия;
в) Hg – ртути;
г) Ni – никеля;
20. Свинец (Pb), негативное биологическое воздействие которого связано с замещением ионов кальция (Ca) в костях, используется в производстве:
а) Красок и автомобильного топлива;
б) Ламп и батарей;
в) Калийных и фосфорных удобрений;
г) Пестицидов;
21. Болезнь Минамата, приводящая к глухоте, параличу и смерти людей, вызывается:
а) Повышеным содержанием в пище кобальта (Co);
б) Повышеным содержанием в пище ртути (Hg);
в) Нехваткой микроэлементов;
г) Обезвоживанием организма;
22. Основным компонентом атмосферы является:
а) Кислород;
б) Водяные пары;
в) Аргон;
г) Азот;
23. Наиболее значимым для живых организмов из основных компонентов атмосферы является:
а) Кислород;
б) Водяные пары;
в) Аргон;
г) Азот;
24. Атмосфера защищает живые организмы, населяющие поверхность планеты, от воздействия:
а) Вулканических выбросов;
б) Жесткого ультрафиолетового излучения;
в) Хозяйственной деятельности человека;
г) Парникового эффекта;
25. Постепенное потепление климата на планете называют:
а) Озоновым экраном;
б) Парниковым эффектом;
в) Фотохимическим смогом;
г) Локальным загрязнением атмосферы;
26. Основной причиной глобального потепления климата является:
а) Изменение естественного радиоактивного фона;
б) Увеличение в атмосфере концентрации диоксида углерода (СО2);
в) Истончение озонового слоя;
г) Увеличение в атмосфере концентрации диоксида серы (SO2);
27. Озоновый слой атмосферы разрушается под действием:
а) Жесткой солнечной радиации;
б) Углекислого газа;
в) Хлорфторуглеводородов;
г) Изменения геомагнитных свойств атмосферы;
28. Основной причиной выпадения кислотных дождей считают воздействие на атмосферу:
а) Электромагнитных излучений;
б) Выбросов сернистого газа;
в) Высокотоксичных соединений;
г) Мелких частиц сажи.
29. Ядовитый туман, образующийся при воздействии солнечного света на смесь выбросов промышленных предприятий и транспорта, называют:
а) Фотохимическим смогом;
б) Задымлением атмосферы;
в) Лондонским смогом;
г) Парниковым эффектом.
30. Какие из нижеперечисленных органов и тканей человека наиболее чувствительны к радиационному излучению?
а) Кости;
б) Жировая ткань;
в) Костный мозг;
г) Мышечная ткань.
31. Воды Мирового Океана относятся к:
а) Неисчерпаемым природным ресурсам;
б) Возобновляемым (исчерпаемым) природным ресурсам;
в) Невозобновляемым (исчерпаемым) природным ресурсам;
г) Вечным природным ресурсам.
32 Запасы пресной питьевой воды сосредоточены в основном в:
а) Озерах и прудах;
б) Ледниках;
в) Реках;
г) Почве.
33. Возросший дефицит пресной воды вызван в основном:
а) Ухудшением климата;
б) Резким уменьшением объема грунтовых вод;
в) Загрязнением водоемов;
г) Глобальным засолением почв;
34. Приоритетным загрязнителем Мирового Океана является:
а) Бытовой мусор;
б) Нефть и нефтепродукты;
в) Биологические отходы;
г) Твердые промышленные отходы;
35. Незамерзание водоемов в холодное время года – один из признаков:
а) Естественной эвтрофикации водоема;
б) Теплового загрязнения водоема;
в) Здорового состояния водоема;
г) Засорение поверхностного водоема;
36. Эвтрофикацией водоемов называют:
а) Быстрое накопление органических веществ, ускоренное развитие микрофлоры и микрофауны
б) Быстрое бытовое загрязнение водоемов синтетическими моющими средствами;
в) Активное загрязнение водоемов продуктами нефтепереработки;
г) Активное поступление в водоемы солей тяжелых металлов;
37. Эвтрофикации водоемов в наибольшей степени способствует:
а) Энергетика;
б) Транспорт;
в) Металлургия;
г) Земледелие;
38. Наиболее чувствительными к загрязнителям воздуха (в первую очередь – к SO2) являются:
а) Газонные травы;
б) Широколиственные породы;
в) Многолетние травы;
г) Хвойные породы;
41.Сила наркотического действия и токсичность веществ возрастает:
а) с увеличением числа атомов углерода в молекуле;
б) с уменьшением числа атомов углерода в молекуле;
в) с увеличением содержания атомов кислорода в молекуле;
г) с увеличением содержания атомов азота в молекуле;
42.Наркотическое и токсическое действие веществ ослабляется:
а) при разветвлении углеродных цепей;
б) при замыкании углеродных цепей;
в) при увеличении длины углеродных цепей;
43. С увеличением кратности химической связи:
а) увеличивается токсическое действие;
б) уменьшается токсическое действие;
в) токсикологические свойства соединения не меняются;
44.Избыточное образование свободных радикалов в организме может привести:
а) К раковым заболеваниям;
б) К повышению иммунитета;
в) К простудным заболеваниям;
г) Не повлияет на работу организма;
45. Бром концентрируют в себе:
а) Боровики;
б) Опята;
в) Лисички;
г) Шампиньоны;
46. С живыми тканями организма совместим:
а) Тантал;
б) Ванадий;
в) Висмут;
г) Вольфрам.
47. Химический элемент селен извлекает из почвы и концентрирует цветок:
а) Астра;
б) Пион;
в) Роза;
г) Тюльпан;
48.В качестве консервирующего средства при сушении слив и абрикосов применяют
а) оксид серы;
б) оксид азота;
в) оксид фосфора;
г) оксид магния;
49. Фенол используется в качестве:
а) дезинфицирующего средства;
б) катализатора;
в) ингибитора;
г) инициатора;
50. Тривиальное название фенола:
а) муравьиная кислота;
б) царская водка;
в) уксусная кислота;
г) карболовая кислота.
51. Формальдегид применяют для изготовления:
а) игрушек;
б) пластмасс;
в) кирпича;
г) взрывчатых веществ;
52. Фенолформальдегидные смолы получают в результате реакции:
а) поликонденсации;
б) полимеризации;
в) присоединения;
г) замещения;
53. При производстве фенолформальдегидных смол в окружающую среду выделяется:
а) фенол;
б) аммиак;
в) формальдегид;
г) углекислый газ.
54. Одно из наиболее опасных соединений, которое выделяется при горении ДСП:
а) циановодород;
б) серная кислота;
в) азотная кислота;
г) бензапирен;
55. Формальдегид вызывает:
а) отеки;
б) бронхиальную астму;
в) экзему;
г) ринит;
56. Основной поставщик фенола и формальдегида в атмосферу:
а) медицина;
б) деревообрабатывающая промышленность;
в) химическая промышленность;
г) пищевая промышленность;
57. ПДК фенола в воздухе:
а) 1 мг/м3
б) 20 мг/м3
в) 17 мг/м3
г) 5 мг/м3
58. ПДК фенола в сточных водах:
а) 20 мг/м3
б) 1-2 мг/м3
в) 12 мг/м3
г) 4 мг/м3
59. ПДК формальдегида в воздухе:
а) 0,05 мг/м3
б) 0,007 мг/м3
в) 0,003 мг/м3
г) 2 мг/м3
60. Смертельная доза 35% водного раствора формальдегида равна:
а) 1 г;
б) 100 г;
в) 10-50г;
г) 200г;
61. Один из отходов при производстве фенолформальдегидных смол:
а) ацетон;
б) кумол;
в) фенольная смола;
г) метиловый спирт.
62. Норма образования фенольной смолы:
а) 200 кг/т;
б) 10 кг/т;
в) 130 кг/т;
г) 500 кг/т;
63. Одно из направлений использования фенольной смолы:
а) строительство;
б) добавка к топочному маслу;
в) медицина;
г) нигде не используется.
64. Метод утилизации фенольной смолы:
а) термическая деструкция;
б) конверсия;
в) закапывают в землю;
г) электрохимический метод;
65. При гидрировании фенольной смолы в качестве катализатора применяют:
а) никель, палладий, кадмий;
б) вольфрам, алюминий, никель;
в) алюминий, кобальт, молибден;
г) медь, платина, золото.
66. Отход при производстве фенолформальдегидной смолы:
а) фенольная вода;
б) метаналь;
в) уксусная кислота;
г) углекислый газ;
67. Норма образования фенольной воды составляет:
а) 100 кг/т;
б) 500кг/т;
в) 145кг/т;
г) 200-300кг/т
68. При получении фенола кумольным способом, кроме фенола образуется:
а) этиловый спирт;
б) ацетон;
в) уксусная кислота;
г) метан;
69. Один из методов получения формальдегида, который характеризуется очень малым количеством побочных продуктов:
а) окисление синтез-газа кислородом;
б) окисление метанола кислородом;
в) окисление метана кислородом;
г) окисление пропана кислородом;
70. Наименьшая опасность при получении фенола достигается при использовании в качестве катализатора:
а) перманганата калия;
б) диоксид марганца;
в) кислорода воздуха;
г) хромовой смеси;
71. Ионы водорода при диссоциации образуют
а) соли;
б) кислоты;
в) щелочи;
г) оксиды;
72. Гидроксид-ионы в результате диссоциации образуют
а) кислоты;
б) соли;
в) щелочи;
г) оксиды;
73. Кислотную реакцию раствора обуславливают илны
а) OH-;
б) Cl-;
в) H+;
г)SO42-.
74. Щелочную реакцию раствора обуславливают ионы
а) K+;
б) Na+;
в) OH-;
г) H+;
75. Белый осадок при введение ионов Ag+ образует раствор
а) NaCl;
б) NaNO3;
в) Ca(NO3)2;
г) KNO3.
76. По обильному выделению пузырьков газа при добавлении кислоты можно обнаружить ион
а) Cl;
б) SO24;
в) CO2-3;
г) H+.
77. В красный цвет лакмус окрашивается в растворе соли
а) Al(NO3)3;
б) K2CO3;
в) Na2CO3;
г) Ba(NO3)2;
78. В синий лакмус окрашивается в растворе соли
а) NaCl;
б) AlCl3;
в) KOH;
г) Ba(NO3)2;
79. Белый осадок при введении ионов SO2-4 образует раствор
а) Al(NO3)3;
б) FeCl3;
в) KOH;
г) Ba(NO3)2.
80. В трех пронумерованных пробирках находятся растворы хлорида бария, хлорида натрия, карбоната натрия. В каждую пробирку добавили раствор серной кислоты. В пробирке 1 выпал белый осадок, в пробирке 2 наблюдалось обильное выделение пузырьков газа, а в пробирке 3 видимых изменений не произошло. Растворы распределены по пробиркам следующим образом:
а) 1- BaCl2; 2 – NaCl; 3 – Na2CO3
б) 1- NaCl; 2 – Na2CO3; 3 – BaCL2
в) 1 – Na2CO3; 2 – BaCL2; 3 - NaCl
г) 1 - BaCl2; 2 – Na2CO3; 3 – NaCl
81. Во втором периоде, VI группе периодической системы химических элементов Д.И. Менделеева находятся элементы:
а) S;
б) Bа;
в) Br;
г) O.
82. Строение атома серы отображает электронная формула:
а) 1S22S22P3;
б) 1S22S22P63S23P4;
в) 1S22S22P4;
г) 1S22S22P5;
83. Формула серной кислоты:
а) H2SO4;
б) NaHCO3;
в) H2S;
г) H2SO3.
84. Формула гидросульфата натрия:
а) Na2SO3;
б) NaHCO3;
в) NaHSO4;
г) Na2CO3
85. Формула сернистой кислоты:
а) H2SO3;
б) H2S;
в) H2SO4;
г) HCL
86. Формула сульфата калия.
а) CaSO4;
б) KHSO4;
в) K2SO4;
г) K2SO3
87. Формула оксида серы (VI) (ангидрида серной кислоты)
а) SO4;
б) SeO3;
в) SO2;
г) SO3
88. Число электронов на внешнем энергетическом уровне атома теллура равно:
а) 7;
б) 6;
в) 5;
г) 4
89. Качественный реактив на серную кислоту и ее соли – это раствор.
а) AgNO3;
б) BaCl2;
в) лакмуса;
г) крахмала
90. В трех пронумерованных пробирках даны растворы серной и соляной кислот, сульфата калия. Лакмусовая бумага окрасилась в красный цвет в пробирках 2 и 3. Затем во все пробирки прилили раствор хлорида бария, отчего в пробирках 1 и 2 выпал белый осадок. Растворы распределены по пробиркам следующим образом:
а) 1 – H2SO4; 2 – K2SO4; 3 - HCl
б) 1 – K2SO4; 2 – HCl; 3 – H2SO4
в) 1 – HCl; 2 – H2S; 3 – K2SO4
г) 1 – K2SO4; 2 – H2SO4; 3 – HCl
91. Жесткость воды обусловлена содержанием в ней:
а) сульфатов и бикарбонатов кальция и магния;
б) сульфатов кальция и магния;
в) бикарбонатов кальция и магния;
г) сульфатов и бикарбонатов кальция;
92. Земная кора подразделяется на подслои: Это:
а) гранитный, базальтовый, метаморфический;
б) осадочный, гранитный, базальтовый;
в) осадочный, гранитный, метаморфический;
г) осадочный, базальтовый, метаморфический;
93. Естественные минеральные агрегаты, возникающие при
переотложении продуктов выветривания и разрушения горных пород. Это:
а) магматические горные породы;
б) осадочные горные породы;
в) метаморфические горные породы; г) вулканические горные породы;
94. Все элементы земной коры делятся на:
а) литофильные, халькофильные, биофильные;
б) литафильные, атмоильные, биофильные, сидерофильные;
в) литофильные, халькофильные, сидерофильные, атмофильные, биофильные;
г) литофильные, сидерофильные, атмофильные;
95. Растворимые элементы, жизненно необходимые организмам, называются:
а) макробиогенными; в) микробиогенными;
б) биогенными; г) биохимическими.
96. К невозобновимым энергетическим ресурсам относятся:
а) солнечная энергия, ядерное топливо, водородное топливо;
б) уголь, водородное топливо;
в) энергия фотосинтеза, ветровая энергия, гидроэнергия;
г) природный газ, геотермальная энергия, уголь, нефть;
97. К методам очистки сточных вод от примесей относятся:
а) экстракция, ректификация, адсорбция, флотация;
б) дистилляция, ионный обмен, обратный осмос;
в) электровоздействие, вымораживание;
г) отдувка, нагрев, реагентные воздействия;
98. Метаболические превращения включают процессы:
а) окисление, выделение, горение;
б) окисление, восстановление, выделение;
в) окисление, гидролиз, восстановление;
г) окисление, горение, восстановление;
99. Конъюгация - это:
а) взаимодействие с серной кислотой, аминокислотами;
б) взаимодействие с азотной кислотой;
в) взаимодействие с функциональными группами;
г) взаимодействие с ферментами;
100. В каких формах медь (Си) может содержаться в водной среде: а) взвешенной и растворенной;
б) коллоидной и растворенной;
в) взвешенной и коллоидной;
г) взвешенной, коллоидной и растворенной [23, 32, 37, 39-40].
Обсуждение результатов. Выводы
В эксперименте участвовали ученики 9 классов, общая выборка которых составляет 66 человек.
В этих классах проводились уроки традиционным методом, в 9 «А» классе, и по методикам, разработанным в данной работе, в 9 «Б» и в 9 «В» классах.
Для выявления результатов исследования проводилось анкетирование, самостоятельные и контрольные работы. Анкеты и тесты содержали вопросы как экологического характера, так и личностного.
Результаты проделанной работы показали, что у группы учеников, которые занимались по разработанной методике, заметно повышает мыслительная способность, создается благоприятная атмосфера для целостного восприятия окружающего мира, самостоятельность в преодолении негативных последствий.
Собранные анкетные данные, результаты контрольных и самостоятельных работ, наблюдения за учащимися дают возможность утверждать что, у 60 % учащихся повышается интерес к самостоятельному познанию предмета.
На диаграмме 1 показан уровень успеваемости и качество знаний учеников в контрольном и экспериментальном классе.
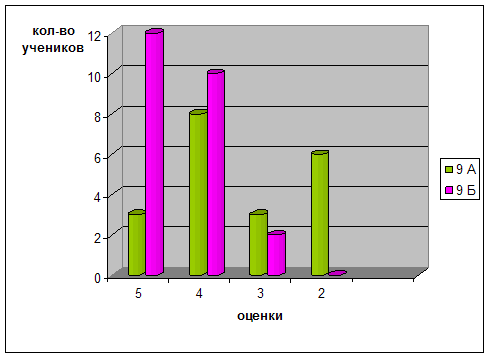
Диаграмма 1. Уровень успеваемости и качество знаний учеников в контрольном и экспериментальном классах
На диаграмме 2 показаны результаты контрольной работы по теме «Охрана атмосферы».
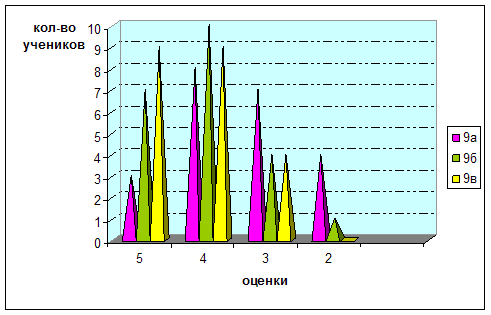
Диаграмма 2. Результаты контрольной работы по теме «Охрана атмосферы»
Таким образом, приведенные нами теоретические и экспериментальные исследования выявили потребность объемного использования самостоятельной работы в изучении экологических аспектов предмета.
Избранная тематика оказалась не только полезной в смысле интеграции и систематизации материала, умений, навыков из различных областей знания, но и способствовала повышению качества знаний, научного и экологического мировоззрения, а главное вызвала интерес учащихся к более глубокому изучению химии и экологии.
На основе проведенной работы можно сделать следующие выводы:
1. Показана возможность организации самостоятельных работ на разных этапах процесса обучения: при подготовке учащихся к восприятию нового материала, а также при совершенствовании знаний и повторений пройденного;
2. Проведена апробация разработанных занятий в МОУ СОШ.
3. Оценен уровень сформированности знаний при изучении тем по разработанным методическим подходам;
4. Доказано, что самостоятельные работы, содержащие конкретный материал, изучаемый школьниками и соответствующий целям и задачам урока, способствует развитию знаний и умений учащихся, постепенному и целенаправленному развитию познавательных потребностей, установки на самостоятельное пополнение знаний.
Литература
1. Программно-методические материалы. Химия 8-11 классы. – М.: Дрофа, 2001.
2. Боброва О.В. Организация самостоятельной работы учащихся при изучении нового материала // Химия в школе. – 1996. - №5. – С. 23.
3. Чернобельская Г. М. Методика обучения химии в средней школе: Учеб. для студ. высш. учеб. заведений. - М.: Владос, 2000. – С. 336.
4. Дьякович С.В. Методика факультативных занятий по химии. – М.: Просвещение, 1985. – С. 175.
5. Егорова Н.В. Вопросы экологического образования при изучении – химии // Химия в школе. - 2001. -№5. - С.46.
6. Ефимова Е.В., Чупанова Л.В. и др. Об экологической составляющей химического образования // Химия в школе. - 2003. - №9. - С.25-30.
7. Игнатьева С.Ю. Ролевая игра «Международный конгресс по охране атмосферы». // Химия в школе. – 2004. - №5. – С.22-25.
8. Иодко А.Г., Емельянова Е.О., Волков А.В. Система заданий для развития умения рассуждать // Химия в школе. - 2000. - №7. - С.11.
9. Монахов В.М. Некоторые вопросы построения системы факультативных курсов естественно-математического цикла // Педагогика. – 1977. - №5. – С.25.
10. Монахова В.М., Орлова В.А. Теория и практика проведения факультативных занятий. – М.: Просвещение, 1983. – С. 150.
11. Никитина М.А., Петровичев А.А. и др. интегрированный урок: пресс-конференция о воде и ее свойствах // Химия в школе. – 2005. - №6. – С.36-42.
12. Пидкасистый П.И. Самостоятельная деятельность учащихся. – М.: Педагогика, 1972. – С.200.
13. Скаткина М.Н. Дидактика средней школы. – М.: Просвещение, 1982. – С.180.
14. Соколова О.Е. Технология педагогических мастерских: развитие творческих способностей учащихся // Химия в школе. – 2001. - №7. – С.14-15.
15. Табуева Э.М. Экологическое образование как фактор формирования культурного потенциала личности // Химия в школе. – 2004. - №5. – С.18-19.
16. Шиленков Р.В., Чернобельская Г.М. Развитие самостоятельности учащихся в условиях индивидуализации обучения // Химия в школе. – 2004. - №5. – С.18-19.
17. Эпштейн Д.А. Факультативные занятия по химии. – М.: Просвещение, 1971. – С.175.
18. Т. Н. Кровельщикова, А. В. Коршунов. Из опыта реализации экологического подхода к обучению химии // Химия в школе.- 2002. - № 8. - С. 40-42.
19. H. В. Егорова. Вопросы Экологического образования при изучении химии //Химия в школе. – 2001. - № 5. - С. 46 – 49.
20. Зверев И. Охрана природы и экологическое воспитание школьников. //Воспит. школьников.- 1985.- N6.- С. 30-36.
21. Программы для средних общеобразовательных учебных заведений. Химия. // Под ред. В. И. Сивоглазова. - М.: «Просвещение», 1993.
22. Обучение химии в 11 классе. В 2 ч. Ч 1: Кн. Для учителя // Под ред. И. Н. Черткова. – М.: Просвещение, 1992. – С. 6 – 20.
23. Азотсодержащие органические соединения. // Химия в школе. – 1996. - № 6. - С. 18-22.
24. И. Г. Афонина. Тестовые задания в курсе химии. // Химия в школе. – 2002. - № 7. - С. 43 – 45.
25. Единый государственный экзамен 2002: Контрольные измерительные материалы: Химия // А. А. Каверина, Д. Ю. Добротин, М. Г. Снастина и др.; М-во образования РФ. – М.: Просвещение, 2002. – С. 20-35.
26. Безуевская В. А. Химические задачи с экологическим содержанием //Химия в школе. – 2000. - № 2. - С. 59 – 61.
27. A.B. Краснянский. Экологические проблемы расчетных задачах по химии // Химия в школе. – 1996. - № 6. - С. 22 – 27
28. А. В. Краснянский. Экологические проблемы в расчетных задачах по химии // Химия в школе. – 1996. - № 5. - С. 32 – 37.
29. H. В. Егорова. Наш подход к экологическому образованию учащихся // Химия в школе. – 2002. - № 5. - С. 40 – 43.
30. H. В.Егорова. Вопросы экологического образования при изучении химии // Химия в школе. – 2001. - № 5 - С. 46 – 49.
31. Ф. Г. Фельдман, Г. Е. Рудзитис. Химия, 8 кл. - М.: Просвещение, 1985.
32. Д. М. Кирюшкин, В. С. Полосин. Методика обучения химии. - М.: Просвещение, 1970. - C. 297 – 302.
33. Хомченко Г.П. Химия для поступающих в вузы. - М.: Высшая школа, 1993.
34. Малышкина В. Занимательная химия. – Санкт-Петербург.: “Тригон”, 2001;
35. Книга для чтения по неорганической химии. Сост. В.А. Крицман. - М.: Просвещение, 1984;
36. Степин Б.Д., Аликберова Л.Ю. Книга по химии для домашнего чтения. – М.: Химия, 1995.
37. Я иду на урок Химии. Книга для учителя. – М.: Первое сентября, 2000.
38. Кузьменко Н. Е., Еремин В. В. Химия. 2400 задач для школьников и поступающих в вузы.- М.: Дрофа, 1999;
39. И. Г. Афонина. Тестовые задания в курсе химии. // Химия в школе. -2002. - № 7. - С. 43 – 45.
40. Химия: Сборник тестовых заданий для подготовки к итоговой аттестации (варианты и ответы, решение расчетных задач). 9 класс (базовый уровень) / Н.В. Ширшина. – Волгоград.: Учитель, 2004. – С.81.
Похожие работы
... и воспитания младших школьников нашли отражение в работах Л.П. Салеевой, И.К. Блиновой, В.М. Минаевой, А.А. Плешакова, А.Е. Тихоновой, А.А. Вахрушева, О.В. Бурского. Реальные возможности для формирования основ мировоззрения у младших школьников содержат курс «Окружающий мир», Программа “Зеленый дом” А.А.Плешакова, факультативы “Экология для младших школьников” и “Планета загадок”, Программа “ ...
... ценностных приоритетов в определении целей и содержания, форм и методов построения учебной деятельности учащихся. Одно из направлений методического обновления уроков в начальных классах – конструирование интегрированных уроков и проведение их на основе интеграции учебного материала с нескольких предметов, объединённого вокруг одной темы. Это междисциплинарная форма учебного процесса, которая ...
... разработанной программы кружка «Юный эколог», способствует значительному повышению экологической культуры школьников. Подготовка дипломной работы убедила меня в большой важности разработки специальной программы, направленной на повышение экологической культуры учащихся начальных классов сельских школ.Литература. Артамонов В.И. Редкие и исчезающие растения. – М.: Агропромидат, 1989. – 383с. ...
... признаки слова, наблюдать, как видовое понятие соотносится с родовым. Все это дается в интересной форме (52,13). Так же нами проводились наблюдения исследовательской работы по использованию интегрированных уроков в процессе обучения младших школьников чтения. Приступая к работе по изучению и исследованию опытов интегрированных уроков мы исходили из гипотезы, что если учебный материал по курсу ...

0 комментариев