Навигация
Практическая работа на тему «Азотная кислота и ее соли»
4.1.3 Практическая работа на тему «Азотная кислота и ее соли»
Цель урока: Научиться применять полученные знания о свойствах азотной кислоты и ее солей на практике.
ХОД УРОКА
I. Организационный момент.
II. Фронтальный опрос:
- Какие реакции называют окислительно-восстановительными?
- Какие химические свойства HNO3 вы знаете?
- Дождевая вода после грозы содержит следы азотной кислоты. Чем это объясняется?
III. Индивидуальный опрос
1-й учащийся - задание №
2-й учащийся - задание №
IV. Самостоятельная работа
На оставшееся время учитель раздает всем карточки с тремя заданиями, два из которых уже разбирались на уроке, а третье задание - творческое, направлено на выявление дополнительных знаний по данной теме.
Например, такая карточка может выглядеть следующим образом:
Карточка № 1
1) Рассчитайте массовую долю азота в следующих веществах:
а) N2O; б) N2O4; в)Cu(NO3)2; г)NH4NO3; д)Fe(NO3)3.
2) Напишите уравнения реакций, с помощью которых можно осуществить цепь следующих превращений:
NO2 ® HNO3 ® Ba(NO3)2 ® KNO3
3) Почему молекула NO2 легко димеризуется, а для SO2 подобный процесс не характерен?
V. Домашнее задание:
Задача № 7; 2) Составить кроссворд на тему: «Азотная кислота и ее большое семейство». [3 (c. 55-60), 17-20]
ГЛАВА 5. ЗАДАЧИ И ТЕСТЫ
5.1 Задачи и тесты по теме «V-A группа ПС»
Задача 1. На гашеную известь, взятую в небольшом количестве подействовали 3,15 кг чистой азотной кислоты. Какую массу нитрата кальция Ca(NO3)2 получили, если практический выход составляет 98%?
Дано:
m(HNO3) = 3,15кг.
wвых (CaNO3) = 98%
m(CaNO3)-?
Решение:
Ca(OH)2 +2HNO3 ®Ca(NO3)2 + 2H2O
M (HNO3)=63 г/моль; m (HNO3)=2×63 =126 кг.; M (Ca(NO3)2)=164 г/моль; m (Ca(NO3)2)=164 кг.
Находим теоретический выход:
126:3,15=164×X1; m(Ca(NO3)2)теор =4,1кг.
Находим 98% - ный выход:
4,1 кг (Ca(NO3)2) соотв. 100% - ному выходу
X2 -//- 98% - ному выходу
![]() кг
кг
Ответ: m (Ca(NO3)2)практ. = 4,02 кг.
Задача 2. Химический завод выбрасывает в атмосферу 120 т. нитрата аммония. Какова ежесуточная потребность в аммиаке (в м3, при 0°С и 101,3 кПа)?
Дано:
m(NH4NO3)=120 т/сут.
M(NH4NO3) = 80г.
V(NH3)-?
Решение:
NH3 + HNO3 ®NH4NO3
M(NH4NO3) = 80г.
Составим пропорцию:
X литров NH3 соответствуют 120×106 граммам NH4NO3
22,4 литров NH3 соответствуют 80 граммам NH4NO3,
Тогда ![]()
![]()
Ответ: Ежесуточная потребность завода в аммиаке составляет 33600м3
Задача 3. Как известно, памятник Кузьме Минину выполнен из бронзы (75% Cu, 25% Sn), поэтому он постепенно разрушается под действием кислотных дождей. Написать реакцию коррозии памятника. Какой объем газа выделится при полном разрушении памятника? Какие меры принимаются для предотвращения коррозии? Масса памятника принимается равной 2750 кг.
Дано:
w(Сu) = 75%
m = 2750кг.
_____________
V(NO2) - ?
Решение:
4HNO3 + Cu = Cu(NO3)2 + 2NO2 + 2NO2
2750 кг.®100%
X1кг®75% Сu
![]() кг.
кг.
Составляем пропорцию:
2062,5 ×103г. Cu ® X2 л. NO2
64 л. Cu ® 44,8 л. NO2
![]() л.
л.
Ответ: 1) при полном разрушении памятника Кузьме Минину под действием кислотных осадков выделится 1443,75 м3 NO2; 2) для предотвращения коррозии памятник несколько раз в год протирают антикоррозионными органическими веществами.
Задача 4. Почва содержит 3,1 % органического вещества. Вычислить процентное содержание (W) углерода и азота в почве, если органическое вещество содержит 60% углерода и массовое отношение С:N=8:1.
Дано:
w(орг. в-ва) = 3,1%
w(C) = 60%
С:N=8:1.
_________________
Wс-? WN-?
Решение:
Допустим, что 100% - это 100 г, тогда m (орг. в-ва) = 3,1г.
m(С) = ![]() г.
г.
m(N) = ![]() г.
г.
Процентное содержание углерода и азота в 100 г почвы:
Wс=![]()
WN= (m(N) / m(почвы))× 100 %
WN = (0,23г./100г.) × 100 % = 0,23%
Ответ: Процентное содержание углерода и азота в 100 г = 1,86% и 0,23%.
Задача 5. Свекла, выращенная в г. Курске имеет содержание нитратов 3000 мг/кг(что в 2 раза больше предельно допустимой концентрации). Сколько килограммов этой свеклы надо счесть, чтобы смертельной дозы для человека (15гр.)?
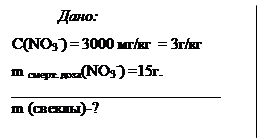 Решение:
Решение:
в 1кг. свеклы ® 3гр (NO3-)
d x кг. свеклы ® 15гр (NO3-)
Ответ: 5кг свеклы, выращенной в г. Курске, содержит смертельную дозу нитрат ионов [20, 26, 27].
Задача № 6. При нормальных условиях 12 л газовой смеси, состоящей из аммиака и углекислого газа, имеют массу 18 г. Сколько литров каждого из газов содержит смесь? Каковы объемные доли каждого компонента в смеси?
Решение
Обозначим V(NH3) = x л, V(CO2) = (12 - x) л.
Тогда n(NH3) = x/22,4 моль, n(СО2) = (12 – x)/22,4 моль,
![]() ,
, ![]() .
.
Составим уравнение:
![]() , х = 4,62 л NH3;
, х = 4,62 л NH3;
V(CO2) = 12 – 4,62 = 7,38 л.
Найдем объемные доли газов в смеси:
j (NH3) = 4,62/12 = 0,385 или 38,5%,
j (СО2) = 1 – 0,385 = 0,615 или 61,5%.
Задания для самоконтроля
1. Напишите уравнения практически осуществимых реакций:
| а) NH4Cl + AgNO3 ® …; в) AgCl + NH4NO3 ® …; д) HNO3 + SiO2 ® …; ж) Hg(NO3)2 и) Fe2O3 + HNO3 ® …; | б) (NH4)2SO4 + NaOH ® …; г) HNO3 (разб.) + Cu ® …; е) HNO3 + MgCO3 ® …; з) NH3 + O2 к) NH4Cl |
2. Напишите уравнения реакций следующих превращений:
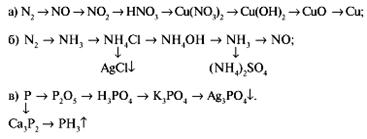
3. Составьте схемы электронного баланса, расставьте коэффициенты в уравнениях реакций:
а) HNO3 + С ![]() СО2 + NO + H2O;
СО2 + NO + H2O;
б) HNO3 + AsH3![]() H3AsO4 + NO2 + H2O;
H3AsO4 + NO2 + H2O;
в) HNO3 + P + H2O ![]() H3PO4 + NO;
H3PO4 + NO;
г) HNO3 + CuS ![]() Сu(NO3)2 + H2SO4 + NO + H2O;
Сu(NO3)2 + H2SO4 + NO + H2O;
д) MnO2 + K2CO3 + KNO3![]() K2MnO4 + KNO2 + CO2;
K2MnO4 + KNO2 + CO2;
е) K2CrO4 + (NH4)2S + H2O ![]() Сr(OH)3 + KOH + NH4OH + S.
Сr(OH)3 + KOH + NH4OH + S.
4. При взаимодействии 28 л (н. у.) аммиака с раствором азотной кислоты массой 400 г, в котором содержится 0,24 массовые доли HNO3, образуется нитрат аммония массой 90 г. Вычислите выход продукта реакции в процентах от теоретически возможного. Ответ. 90%.
5. При нагревании технического нитрата меди(II) массой 75,2 г выделяется кислород объемом 4 л (н. у.). Рассчитайте массовую долю примесей в образце нитрата. Ответ. 10,7%.
6. Имеется смесь хлорида, карбоната и нитрата натрия массой 50 г. Определите массовую долю каждого компонента смеси, если известно, что при действии на нее избытка соляной кислоты выделяется газ объемом 2,24 л (н. у.), а при прокаливании такой же массы смеси выделяется кислород объемом 2,24 л (н. у.). Ответ. w(NaCl) = 44,8%, w(Na2CO3) = 21,2%, w(NaNO3) = 34%.
7. При действии избытка разбавленной азотной кислоты на образец известняка массой 80 г, содержащий 20% примесей, выделяется оксид углерода(IV), который пропускают через раствор, содержащий 25,6 г гидроксида натрия. Определите, какая соль (кислая или средняя) образуется. Какова ее масса? Ответ. 53,76 г NaHCO3.
8. Определите, какая соль образовалась и какова ее масса, если раствор гидроксида кальция объемом 200 мл, концентрация которого 0,2 моль/л, прореагировал с 9,8%-м раствором ортофосфорной кислоты массой 200 г.
Ответ. 9,36 г Са(Н2РО4)2.
9. Оксид фосфора(V), полученный окислением 31 г фосфора, растворен в 495 г воды с образованием ортофосфорной кислоты. В этот раствор пропущено 44,8 л аммиака. Определите состав полученной соли и ее концентрацию в растворе (массовую долю в процентах). Ответ. 22% (NH4)2НРО4 [19-29].
.
5.2 Тесты
1. Определите содержание по следующей характеристике: применяется в домашних холодильниках в качестве охлаждающего средства, устойчив, сильно разрушает озоновый слой.
а) NH3
б) CF2Cl2 +
в) CFCl3
г) H2SO4
2. “Нашатырь” получают на производстве в результате взаимодействия аммиака с хлороводородом, реакция протекает ступенчато: NH3 + H2O = NH3×H2O, NH3×H2O + HCl = NH4Cl + H2O. Определите роль воды в суммарном процессе:
а) растворитель
б) промежуточный продукт
в) конечный продукт
г) катализатор +
3. Выберите вещество, которое при возгорании нельзя тушить водой:
а) метан
б) аммиак
в) калий +
г) фосфор
4. Выберите наиболее экологически чистое топливо из перечисленных ниже:
а) нефть
б) уголь
в) биомасса
в) природный газ
д) солнечная энергия +
5. В атмосфере какого газа производят сварку активных или средней активности металлов, хранят и перевозят произведения живописи:
а) неон
б) водород
в) азот +
г) аммиак
6. Как влияет уменьшение содержания связанного азота в почве на растения?
а) при недостатке азота задерживается рост и развитие растений, листья приобретают бледно-зеленую окраску, а затем желтеют; +
б) при недостатке азота задерживается рост и развитие растений и листья чернеют;
в) при недостатке азота растения начинают цвести и листья приобретают особый оттенок, так как азот является сдерживающим фактором.
7. В современных установках получения азотной кислоты нет постоянных источников сточных вод. Почему?
а) для получения азотной кислоты нет необходимости использовать воду;
б) эти установки потребляют большое количество оборотной охлаждающей воды, которую периодически сливают в приямок и нейтрализуют; +
в) системы, в которых используется для охлаждения вода, полностью заменены на системы с воздушным охлаждением.
8. Назовите важнейшие области применения аммиака в народном хозяйстве:
а) получение сложных и азотных минеральных удобрений;
б) производство синтетических красителей;
в) взрывчатые вещества, нитролаки;
г) пластические массы и лекарственные вещества;
д) все варианты. +
9. Что привело к существенному снижению количества сточных вод при производстве аммиака?
а) применение воздушного охлаждения; +
б) в результате замены поршневых компрессоров трубокомпрессорами; +
в) существенное снижение забора воды.
10. Какие выбросы в окружающую среду характеризуют крупнотоннажное производство NH3?
а) газовые, содержащие в своем составе NH3, оксиды азота и углерода и др. примеси;
б) сточные воды, состоящие из конденсата, продуктов промывки реакторов и систем охлаждения,
в) низкопотенциальную теплоту.
Ответ: все
11. Между атомами в молекуле азота существует:
а) двойная связь;
б) тройная связь; +
в) одинарная связь;
г) пять химических связей.
12. Азот достаточно инертен по отношению к металлам, но сравнительно легко протекает следующая реакция:
а) Cu + N2 = ... ;
б) Zn + N2 = ... ;
в) Al + N2 = ... ;
г) Li + N2 = ... . +
13. Летучее водородное соединение азота имеет формулу:
a) NH2;
б) N2H4;
в) NH3; +
г) NО2.
14. В какой реакции азот проявляет восстановительные свойства? (б)
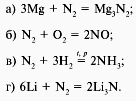
15. Вещество Mg3N2 называют:
а) нитрат магния;
б) нитрит магния;
в) сульфат магния;
г) нитрид магния. +
16. Сколько свободных электронных пар имеет азот в молекуле аммиака?
а) 2;
б) 4;
в) 1; +
г) 3.
17. Аммиак в лаборатории получают по реакции:
а) NH4Cl + Ca(OH)2 = ... ; +
б) N2 + 3H2 = ... ;
в) Са3(PO4)2 + (NH4)2SO4 = ... ;
г) (NH4)3РO4 + HCl = ... .
18. Выберите ряд веществ, соответствующий нарастанию молекулярных масс:
а) озон, аммиак, кислород;
б) аммиак, кислород, озон; +
в) кислород, аммиак, озон;
г) кислород, озон, аммиак.
19. Аммиак может реагировать с соляной кислотой по реакции NH3 + HCl = NH4Cl. Четвертый атом водорода присоединяется по донорно-акцепторному механизму, при этом донором является:
а) водород;
б) хлор;
в) азот; +
г) группа NH4+.
20. В аммиаке и катионе аммония степень окисления азота одинаковая: –3. Какие валентности у атомов азота в этих соединениях?
а) Обе – III;
б) обе – IV;
в) III и II;
г) III и IV. +
21. Нашатырный спирт – это:
а) NH3;
б) NH3•H2O; +
в) NH4Сl;
г) N2H4.
22. Для какой реакции повышение давления сместит равновесие вправо?
а) N2 (г.) + О2 (г.) = 2NO (г.);
б) Н2 (г.) + S (ж.) = Н2S (г.);
в) N2 (г.) + 3Н2 (г.) = 2NН3 (г.); +
г) Н2 + Сl2 = 2НCl.
23. В лаборатории азотную кислоту получают по реакции: (б)
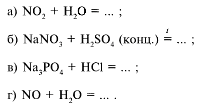
24. При взаимодействии концентрированной азотной кислоты с серебром помимо соли и воды выделяется газ:
а) NO2; +
б) NO;
в) N2;
г) N2О.
25. При термическом разложении нитрата калия выделяется газ:
а) N2;
б) NO2;
в) О2; +
г) N2О.
26. Формула аммиачной селитры:
а) КNO3;
б) (NH4)3PO4;
в) NH4NO3; +
г) (NH4)2SO4 [30-34].
ЛИТЕРАТУРА
1. Исидоров. Химия атмосферы. М.: Мир, 1991.
2. А.И. Бусев, И.П. Ефимов. Определения, понятия, термины в химии. М.: Просвещение, 1981, 192 с.
3. Рудзитис Г.Е. Химия: Неорган. химия. Орган. Химия: Учеб. для 9 кл. общеобразовательных учреждений. / Г. Е. Рудзитис., Ф. Г. Фельдман. – 10-е изд., испр. – М.: Просвещение, 2001, с. 133 – 139.
4. Экологическая химия азота / www.1september.ru
5. Ахметов Н.С. Учебник для 9 класса общеобразовательных учреждений. М.: Просвещение, 1998 г.
6. Программы для общеобразовательных учреждений: Химия. 8-11 кл. Сост. Н.И.Габрусева. — М.: Дрофа, 2000. — 192 с.
7. Примерная программа среднего (полного) общего образования по химии (профильный уровень). www.edu.ru
8. Асадник В.Н. Неорганическая химия. Блок-схемы, таблицы, формулы: Учеб. пособие. / В.Н. Асадник. – Мн.: Книжный Дом, 2004. – с. 28 – 41.
9. Реми. Неорганическая химия. Т. 1.
10. Олеин С.С., Фадеев Г.Н. Неорганическая химия. Учебник для с/х вузов. М., 1979.
11. Хомченко Г.П. Неорганическая химия. М., 1978.
12. М.Д. Гольдфейн, Н.В. Кожевников, А.В. Трубников, С.Я. Шулов. Проблемы жизни в окружающей среде. Учебное пособие. Химия. 1996г, №16.
13. Денисов В.В., Дрововозова Т.И. и др. // Химия. М.: Р- н/Д, Март, 2003
14. Алпатьев А.М. Развитие и преобразование окружающей среды. Л.: Наука, 1983
15. Богдановский Г.А. Химическая экология. М.: МГУ, 1994.
16. Тарасова Н.П., Кузнецов В.А. и др. Задачи и вопросы по химии окружающей среды. М.: Мир, 2002.
17. Химия в школе // Журнал. - М.: Просвещение, 2001, № 4, стр.16.
18. Кутепов А.М. и др. Общая химическая технология. Учеб. для техн. вузов. 2-е изд. М.: Высш. шк., 1990, стр.148-162.
19. Практикум по неорганической химии. Учеб. пособие для студ. хим.-биол. фак-в пединст-в. Изд. 2-е. М.: Просвещение, 1978. стр.180-183.
20. Бабич Л.И. Практикум по неорганической химии. Учеб.пособие.М.:Просвещение.1978,с. 312.
21. Система уроков по теме «Кислотные дожди» для 10–11 классов с углубленным изучением экологии http://www.1september.ru/ru/him/
22. Государственные доклады Госкомэкологии «О состоянии окружающей природной среды Российской Федерации». Российская экологическая газета «Зеленый мир», 1994–1998.
23. Миллер Т. Жизнь в окружающей среде. В 3 кн. М: Пангея, 1996, т. 3.
24. Фелленберг Г. Загрязнение природной среды. М.: Мир, 1997.
25. Небел Б. Наука об окружающей среде. В 2 т. М.: Мир, 1993.
26. Гольбрайх З.Е. Сборник задач и упражнений по химии. Учеб. пособие для хим.-техн. вузов. М.: Высш. шк., 1984, стр. 224.
27. Р.П. Суровцева, С.В. Сафронов. Задания для самостоятельной работы по химии. М.: Просвещение, 1993 г.
28. Сайт «Я иду на урок химии» www.1september.ru
29. Ахметов М.А. Система обучающих заданий: творческий уровень. / Химия в школе, 2004, № 1, с. 21 – 28.
30. Сорокин В.В., Злотников Э.Г. Проверь свои знания: Тесты по химии: Кн. для учащихся. – М.: Просвещение: Учеб. лит., 1997.
31. Н.Н. Черняев, М.А. Ахметов. Тестовые задания и индивидуализация обучения / Химия в школе, 2001, № 9.
32. Суровцева Р.П., Гузей Л.С., Останний Н.И., Татур А.О. Тесты по химии. 8-9 классы. Учебно-методическое пособие. М.: Дрофа, 1997.
33. Глориозов П.А., Рысс В.Л. Проверочные работы по химии. 7, 8, 9, 10 классы. М.: Просвещение, 1980, 1981, 1985.
34. Гаврусейко Н.П. Проверочные работы по неорганической химии. 8-9 классы. М.: Просвещение, 1990.
Похожие работы
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... виды связей, тогда как синхронные резко ограничены, а во внутрипредметных связях синхронный вид вообще отсутствует. 2. Планирование и осуществление межпредметных связей в процессе обучения. Разработка теоретических основ межпредметных связей в учебной теме сточки зрения раскрытия ее ведущих положений дает возможность применить механизм выявления и планирования межпредметных связей к ...
... и дидактические основы организации обучения позволяют более доступно объяснять изучаемый материал на уроках физики при изучении темы «Основы электродинамики». Анализ различных технологий позволил составить авторскую технологию развития у учащихся направленности на диалогическое общение при групповой форме обучения. От того, на сколько правильно будет построен процесс обучения при использовании ...
... с этим возникает необходимость рассмотрения вопроса взаимосвязи молекулярной физики и химии в курсе средней школы. При изучении молекулярной физики взаимосвязь ее с химией проявляется в двух главных направлениях. Первое из них заключаются в использовании знаний учащихся, полученных ими в процессе изучения химии в качестве материала для доказательства основных положений молекулярной физики. Второе ...
0 комментариев