Навигация
Выделение и фракционирование ДНК
4.1 Выделение и фракционирование ДНК
Основная проблема выделения нуклеиновых кислот заключается в получении клеток и отделении нуклеиновых кислот от связанных с ними белков и других клеточных компонентов. Помимо очистки нуклеиновых кислот от нежелательных компонентов, следует обратить внимание на то, что сами нуклеиновые кислоты требуют исключительно осторожного обращения, так как они чрезвычайно чувствительны к действию нуклеаз и гидродинамических сил. Клетки гомогенизируют различными методами, а из гомогената отделяют нуклеиновые кислоты. Из гомогената нуклеиновые кислоты можно выделить двумя методами, заключающиеся в "высаливании" ДНК различными смесями органических растворителей. Нуклеиновые кислоты остаются в водной фазе, в то время как другие денатурированные макромолекулы собираются на границе между фазами. Эти методы не позволяют выделить неповрежденными большие молекулы ДНК. Образовавшуюся гетерогенную смесь нуклеиновых кислот подвергают разделению на фракции методами ультрацентрифугирования, гель-фильтрации на сефадексах, хроматографированием. Полученные фракции ДНК подвергают секвенированию, для чего их подвергают действию эндонуклеаз рестрикции.
4.2 Расщепление ДНК рестрицирующими нуклеазами
Для защиты от молекул чужеродных ДНК, способных проникнуть в клетку и вызвать ее трансформацию, многие бактерии вырабатывают ферменты рестрицирующие нуклеазы, способные разрушить чужеродную ДНК. Каждый такой фермент опознает в ДНК специфическую последовательность из 4-6 нуклеотидов. Соответствующие последовательности в геноме самих бактерий замаскированы метилированием остатков А и Ц, но любая чужеродная молекула ДНК, попав в клетку, немедленно опознается нуклеазой, и обе цепи ее ДНК разрезаются. В настоящее время известно более 100 таких ферментов, большинство из которых опознает различные последовательности нуклеотидов.
Сравнение размеров фрагментов ДНК, полученных после обработки определенного участка генома набором рестрицирующих нуклеаз, позволяет построить рестрикционную карту, на которой указано положение каждого сайта рестрикции относительно других рестрикционных участков. Короткие фрагменты, разделенные электрофорезом или хроматографией, секвенируются, т.е. определяется последовательность нуклеотидов.
4.3 Секвенирование ДНК
Для определения нуклеотидной последовательности в ДНК были разработаны два метода:
1. Метод с использованием "минус- и плюс"-систем ("минус-плюс"-метод, метод Сенгера).
2. Метод с использованием диметилсульфата и гидразина (метод Максама-Гилберта).
Метод Сенгера заключается в получении коротких участков цепи ДНК на матрице родительской ДНК, при этом используются различные уникальные по свойствам ферменты. Сопоставление полученных фрагментов позволяет установить исходную последовательность.
Метод Максама-Гилберта построен на расщеплении фрагментов ДНК по определенным основаниям химическими агентами. Чередование этих расщеплений на однородном материале (сначала, допустим, по А, потом по Т, Г, С) позволяет получить наборы коротеньких фрагментов. Сопоставлением устанавливают общую последовательность.
Несмотря на коротенькое изложение сути методов, сами методы являются очень сложной технической процедурой. Но, все-таки, данные методы удалось автоматизировать, что позволяет довольно быстро устанавливать последовательности нуклеотидов в генах, а также привело к расшифровке генетических карт многих организмов, в том числе и человека.
4.4 Клонирование ДНК
Многие рестрицирующие нуклеазы вносят разрывы в две цепи ДНК со смещением на несколько нуклеотидов, так что на концах образуются короткие одноцепочечные участки. Эти одноцепочечные концевые участки обладают способностью образовывать комплементарные пары оснований с любым другим одноцепочечным участком, полученным с помощью того же фермента, и потому их называют липкими концами. Липкие концы, образованные рестрикционными ферментами, позволяют легко соединить два любых фрагмента ДНК воедино при условии, что эти фрагменты образовались после действия одной и той же рестрицирующей нуклеазы (рестриктазы). Таким образом, фрагмент ДНК любого происхождения можно встроить в очищенную ДНК автореплицирующегося генетического элемента, которым, как правило, является плазмида или бактериальный вирус. Исходный фрагмент может происходить прямо из геномной ДНК, или из кДНК (комплементарной ДНК), т.е. из ДНК, полученной копированием матричной РНК.
4.5 Гибридизация нуклеиновых кислот
Если водный раствор ДНК нагреть до 100 °С и сильно защелочить (рН 13), то комплементарные пары оснований, удерживающие две цепи двойной спирали вместе, разрушатся и ДНК быстро диссоциирует на две
цепи. Этот процесс, называемый денатурацией ДНК, ранее считался необратимым. Однако в 1961 году было обнаружено, что если комплементарные цепи ДНК выдержать при температуре 65 °С, они легко спариваются, восстанавливая структуру двойной спирали (процесс, получивший название ренатурации или гибридизации) Подобные процессы гибридизации могут происходить между двумя любыми одинарными цепями нуклеиновых кислот (ДНК—ДНК, РНК—РНК, ДНК—РНК) при условии, что они содержат комплементарные последовательности нуклеотидов.
Этот метод весьма эффективен для поиска неидентичных, но родственных генов; например, после клонирования интересующих исследователя генов мыши или курицы, их последовательности могут быть использованы для поиска соответствующих генов в геноме человека.
ДНК-зонды применяют и в реакциях гибридизации с РНК для выявления экспрессии данного гена в клетках. В этом случае ДНК-зонд, содержащий часть последовательности гена, пытаются гибридизовать с РНК, выделенной из анализируемой клетки. Если гибридизация происходит, проводят количественное определение экспрессии. Более усовершенствованные методики предполагают обработку ДНК-зонда специфическими нуклеазами для обнаружения участков, гибридизующихся с клеточной РНК. Таким образом можно определить начальные и концевые участки транскриптов РНК; этот же метод может быть полезен для выяснения точных границ участков, вырезаемых из транскриптов РНК в процессе сплайсинга РНК.
4.6 Методы рекомбинантных ДНК
Разработка методов рекомбинантных ДНК сделала доступными любые клеточные белки (включая минорные белки) в больших количествах. Для этого клонируют ген нужного белка и затем встраивают его в специальную плазмиду, именуемую клонирующим вектором. Этот вектор сконструирован таким образом, что будучи введенным в бактерии, дрожжи или клетки млекопитающих соответствующего типа, он обеспечивает крупномасштабный синтез этого белка. Таким образом, если раньше для детальных структурных или функциональных исследований были доступны лишь немногие белки, в настоящее время практически все белки клетки могут быть предметом подобных исследований.
Получить мутантов, у которых нарушена репликация ДНК или, например, развитие глаза, в принципе довольно просто. Однако, чтобы связать этот дефект с изменением конкретного белка, могут понадобиться годы. Технология рекомбинантных ДНК дала в руки исследователей совершенно иной подход: анализ начинается с белка и завершается созданием мутантной клетки или целого организма. Поскольку такой подход по сравнению с традиционным направлением генетического анализа от гена к белку представляется обратным, его обычно называют обратной генетикой.
Обратная генетика начинается с выделения из клетки нужного белка. Ген этого белка клонируют и определяют его нуклеотидную последовательность; затем эту последовательность меняют биохимическими методами, создавая мутантный ген, кодирующий измененную форму белка. Затем такой ген вводят в клетку, где он может встроиться в хромосому в процессе гомологической рекомбинации и превратиться таким образом в постоянный элемент генома. Если встроенный ген экспрессируется, то несущая его клетка и все ее потомки будут синтезировать измененный белок. В том случае, когда измененный in vitro ген вводят в оплодотворенную яйцеклетку, получается многоклеточный мутантный организм. Некоторые из таких трансгенных организмов передадут этот ген своим потомкам в качестве постоянного элемента клеток зародышевой линии. Такая генетическая трансформация в настоящее время становится обычной процедурой для плодовых мушек или млекопитающих. В принципе на сегодняшний день совершенно реальна и трансформация человека, но такие эксперименты не выполняют из страха перед возможными генетическими нарушениями, которые нельзя исключить у лиц, ставших объектом таких исследований.
Технология рекомбинантных ДНК оказала существенное воздействие на всю клеточную биологию, позволяя исследователям решать задачи, которые раньше казались неразрешимыми, например, определять функции многих вновь открытых белков и их индивидуальных доменов, расшифровывать сложные механизмы регуляции экспрессии генов у эукариот. С помощью методов генной инженерии удалось в большом количестве получить многие белки, участвующие в регуляции клеточной пролиферации и развитии.
Вывод
В ходе выполнения данной курсовой работы были рассмотрены разнообразные методы, которые используются для изучения клеток на современном этапе научного развития. Приведенные в формате данной работы методы можно систематизировать на основе их подхода к исследованию. Можно выделить методы статического исследования, такие как:
а) методы оптической микроскопии;
б) методы электронной микроскопии;
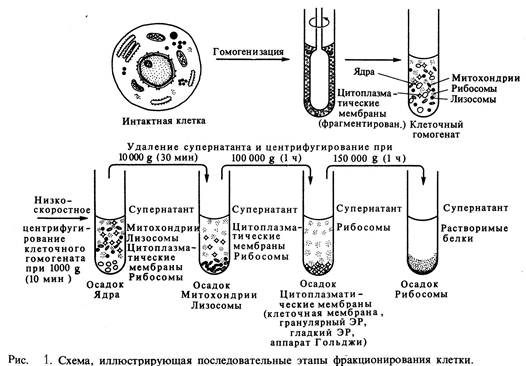
в) методы фракционирования клеточного содержимого;
г) рентгеноструктурный анализ и метод ЯМР.
Также выделим методы исследования функционирования клетки (т.е. непосредственно влияющие на ее функционирование):
а) методика меченых изотопов и антител;
б) методы внутриклеточных иньекций;
в) методы клеточных культур и тканей;
г) методы гибридизации и клонирования ДНК.
Набор функциональных методов очень богат и не полностью освещен в данной работе, поскольку не возможно описать все их разнооразие в таком формате, например, не учтено много разнообразных генетических методов, которые помогают установить функции многих молекул, а также механизмы наследования.
Из изложенного материала следует, что современная клеточная биология оперирует множеством методов, позволяющих исследовать клетку не только в ее статическом проявлении, но и разобраться в ее функционировании на молекулярном уровне. А некотором роде венцом современных достижений в клеточной биологии являются методы генной инженерии.
Список использованной литературы
1. Айала Ф. Кайгер Дж. Современная генетика. В 3-х т. Пер с англ.: - М.:Мир, 1987.
2. Албертс Б. и др. Молекулярная биология клетки. В 5-ти томах. М.: Мир, 1986 - 1987.
3. Зенгбуш П. Молекулярная и клеточная биология. В 3-х т. М.: Мир, 1982.
4. Ленинджер А. Основы биохимии. В 3-х т. М.: Мир, 1985.
5. Льюин Б. Гены. М.: Мир, 1987.
6. Страйер Л. Биохимия. В 3-х т. М.: Мир, 1985.
7. Третьяк А. П. Молекулярная биология. Чернигов. 1999.
Похожие работы
... новые возможности, которые возникали с появлением новых методов исследования, позволяли делать открытия, радикально менявшие взгляды на патологию, начинать качественно новые этапы её развития. Патологическая анатомия использует три основных метода исследования — вскрытие трупов людей, умерших от болезней (1); микроскопические методы изучения тканей (2); эксперимент, позволяющий моделировать на ...
... недоразумения, но затем он прочно закрепился за этими маленькими желеобразными тельцами. Современное представление о клетке тесно связано с техническими достижениями и усовершенствованиями методов исследования. Помимо обычной световой микроскопии, не утратившей своей роли, в последние несколько десятилетий большое значение приобрели поляризационная, ультрафиолетовая, флюоресцентная, ...
... физических и химических характеристик мочи: анализ содержащихся в моче твердых веществ, других растворенных веществ и микроскопическое исследование осадка мочи [4]. 2.1 Правила взятия мочи у животного исследование кровь моча животное Существует три обычных метода сбора мочи, а именно, прокол мочевого пузыря, катетеризация и сбор мочи, выделяющейся из организма естественным путем. Выбор ...
... заболевания. Определение маркеров опухолей хотя и дорогой, но очень важный метод исследования, без которого в ряде случаев обойтись просто невозможно. Большинство лабораторных методов исследования требуют специального оборудования. Так, для подготовки и сохранения проб при заданной температуре, а также проведения бактериологических и серологических исследований используют термостаты, а также ...
0 комментариев