Навигация
Креста, 1/4 — на один крест. Но эти оценки все же весьма условны
Формы ЦПД зависят от биологических свойств вируса, вида клеток, дозы заражения, условий культивирования и т. д. Одни вирусы проявляют ЦПД через 2—3 сут после заражения (энтеровирусы), другие — через 1—2 нед (аденовирусы).
Наиболее существенно различаются между собой три формы ЦПД: фрагментация клеток, округление клеток, симпластообразование (рис. 1,2)
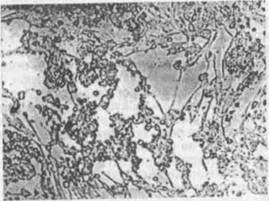
Фрагментация — разрушение клеток на отдельные фрагменты, которые отделяются от стекла и переходят в культуральную жидкость в виде клеточного детрита (вирус везикулярного стоматита).
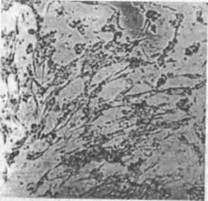
Округление — потеря клетками способности прикрепляться к стеклу, вследствие чего клетки, обычно распластанные по стеклу, принимают шаровидную форму, отделяются от стекла и свободно плавают в культуральной жидкости, где и погибают (энтеровирусы, аденовирусы и др.).
Симпластообразование — растворение клеточных оболочек, вследствие чего цитоплазмы соседних клеток сливаются, образуя одно целое, в котором располагаются (главным образом по периферии) ядра клеток. Такие образования из цитоплазматической массы с многими клеточными ядрами называются симпластами (гигантские многоядерные клетки). Их образование объясняют двояко: нарушением процесса деления клеток под влиянием вируса или тем, что некоторые вирусы содержат фермент (лецитиназу), который растворяет клеточные оболочки, в результате цитоплазмы расположенных рядом клеток сливаются. ЦПД в культуре клеток способно вызывать большинство вирусов, поэтому этот метод индикации вирусов в культуре клеток применяют очень широко. Однако есть вирусы, которые, размножаясь в культуре клеток, ЦПД не вызывают (вирусы бешенства, классической чумы свиней, некоторые штаммы вируса диареи крупного рогатого скота и др.). Клетки остаются жизнеспособными, но интенсивность клеточного деления понижается, со временем изменяется и их морфология.
При неопластической трансформации пораженных клеток в монослое образуются плотные фокусы трансформации различной величины и формы, белого цвета (вирус саркомы Рауса).
Отсутствие ЦПД в первом пассаже еще не говорит об отсутствии вируса, который не всегда размножается настолько быстро, чтобы вызвать ярко выраженное ЦПД. Поэтому и прибегают к "слепым" пассажам. Необходимо провести не менее трех "слепых" пассажей, прежде чем судить о наличии вируса в исследуемом материале.
РГАд. Гемадсорбция — соединение эритроцитов с поверхностью пораженных вирусом клеток — впервые была обнаружена Фогелем и Щелоковым (1957) на культуре ткани, инфицированной вирусом гриппа. В последующем выяснилось, что этой способностью обладает ряд других вирусов: парагриппозные, оспо-вакцины и оспы, ньюкаслской болезни, гриппа млекопитающих и птиц. Наиболее ценным оказалось применение этой реакции для выявления и идентификации парагриппозных вирусов животных (ПГ-3 крупного рогатого скота, парагриппа овец, вируса Сендай). В основе этого явления лежит родство рецепторов вируса, находящихся на поверхности пораженной клетки, с рецепторами эритроцита, что приводит к их взаимному сцеплению аналогично реакции гемагглютинации. Преимущество этой реакции состоит в том, что она становится положительной еще до появления отчетливых цитопатических изменений в инфицированных клетках. Для постановки реакции используют эритроциты морской свинки, обезьян, человека (группы О) и другие эритроциты, чувствительные к гемагглютинирующему действию изучаемого вируса.
Методика РГАд
Состоит в следующем. На 3—4-й день после инфицирования клеток берут две пробирки с одинаковой культурой клеток, из которых одна заражена вируссодержащим материалом, а вторая контрольная. Из обеих пробирок сливают культуральную жидкость и вносят в обе по 2—3 капли 0,5%-ной суспензии отмытых эритроцитов. Обе пробирки оставляют на 5—10 мин так, чтобы эритроциты были на поверхности клеток (кладут горизонтально на стол), а затем слегка споласкивают физраствором и исследуют под микроскопом (малое увеличение). В контрольной пробирке эритроциты полностью удаляются с физраствором, а некоторые из оставшихся плывут вместе с жидкостью. Если в зараженной пробирке эритроциты не удалились с физраствором и не плывут, а прикреплены к поверхности клеток, следует считать РГАд положительной
В зависимости от вируса и вида клеток расположение эритроцитов может быть трояким:
-эритроциты адсорбированы только по периферии клеточного пласта в виде "ожерелья" (вирус африканской чумы свиней);
![]() -эритроциты расположены на слое клеток очагами или скоплениями (вирус гриппа);
-эритроциты расположены на слое клеток очагами или скоплениями (вирус гриппа);
-эритроциты расположены на слое клеток диффузно (вирус парагриппа).
Каждый вирус способен адсорбировать эритроциты крови животных определенных видов. Если вирус на данной культуре клеток вызывает и ЦПД, и РГАд, то гемадсорбция проявляется раньше, чем ЦПД. Метод этот пригоден для индикации в культурах клеток только некоторых вирусов и поэтому применяется нечасто. Однако для индикации ряда вирусов (вирусы африканской чумы свиней, парагриппа-3 крупного рогатого скота и др.) он незаменим При отсутствии гемадсорбции на 3—4-й день после инфицирования через каждые 2—3 дня берут следующие пробирки с инфицированной культурой клеток и ставят РГАд по описанной выше методике. Пробирки с культурой клеток находятся под наблюдением в течение 14—20 дней. При отрицательной реакции гемадсорбции в первом пассаже проводят следующий пассаж и РГАд.
![]() РГАд используют для обнаружения вируса в культуре клеток, для титрования его и при постановке реакции нейтрализации с целью определения титра антител в сыворотках крови животных.
РГАд используют для обнаружения вируса в культуре клеток, для титрования его и при постановке реакции нейтрализации с целью определения титра антител в сыворотках крови животных.
Метод образования бляшек.
Этот метод обнаружения вирусов технически сложнее других и применяется главным образом для титрования вирусов.
Дальбекко и Фогт в 1954 г. впервые предложили методику получения бляшек под агаром в культуре куриных фибробластов с вирусом западного лошадиного энцефаломиелита. В последующие годы многие авторы с успехом применяли этот метод при изучении различных вирусов — ящура, везикулярного стоматита, ньюкаслской болезни, чумы птиц, полиомиелита, Коксаки и др. Метод бляшек стали широко применять в вирусологии для получения чистых популяций вируса, особенно при изучении их генетических свойств. Методику получения бляшек, предложенную Дальбекко и Фогтом, модифицировали, и в настоящее время есть целый ряд отличных друг от друга методов, связанных с изучением различных вирусов.
Метод бляшек основан на образовании вирусом в однослойных культурах, залитых агаровой средой, содержащей витальный краситель — нейтральрот, негативных колоний или бляшек. Бляшки представляют собой обесцвеченные участки культуры, состоящие из погибших под действием вируса клеток. Кроме агара в целях предотвращения переноса вируса на другие места можно использовать крахмал и метилцеллюлозу. Некоторые вирусы дают бляшки без покрытия слоем агара, например вирус чумы крупного рогатого скота, осповакцины, некоторые представители вирусов герпеса и др.
При постановке бляшек особое внимание должно быть обращено на качество культуры, она должна иметь сплошной рост клеток без признаков дегенерации. Лучше всего использовать культуры, выращенные во флаконах или матрасах различного типа. На клетки, промытые средой или раствором Хенкса, наносят вирус в определенных разведениях и обеспечивают контакт вируса с клетками при периодическом покачивании в точно установленный отрезок времени (1-2ч) при 37 -38 градусах Цельсия. Неадсорбировавшийся вирус удаляют путем промывания раствором Хэнкса или отсасывают пастеровской пипеткой, затем на слой клеток наносят специальное агаровое покрытие. Выбор среды покрытия определяется видом клеток и вируса.
Обычные компоненты агарового покрытия — агар, раствор Эрла, телячья сыворотка, нейтральный красный, раствор соды (NaHC03), среда, антибиотики.
После застывания (30—60 мин) с поверхности агара сливают конденсированную влагу, флаконы переносят в термостат и инкубируют клетками вверх. Время инкубации и температура должны быть оптимальными для бляшкообразования, вызываемого данным вирусом. Наблюдение за появлением бляшек проводят в течение нескольких дней. За это время вирусы, адсорбировавшиеся на клетках, проникают в последние, проходят цикл репродукции, выходят из клеток и поражают соседние клетки. В сплошном слое живых клеток возникают островки мертвых, погибших вследствие репродукции в них вируса клеток. Раствор красителя окрашивает только живые клетки. Поэтому в матрасе на ровном красновато-розовом фоне появляются бесцветные пятна, которые и называются негативными пятнами Дальбекко или бляшками. Каждая бляшка соответствует островку мертвых клеток. Бляшки в культуре клеток образуют многие вирусы. При большой плотности (соответствующей низким разведениям вируса) они часто сливаются друг с другом. Время появления и морфология бляшек зависят от вида и штамма вируса, типа клеток и условий культивирования.
В основу титрования вирусов положены наблюдения Дальбекко и Фогта, показавших линейную зависимость между дозой внесенного вируса и количеством образующихся бляшек. Они показали, что для образования одной бляшки достаточно одной инфекционной вирусной частицы. Однако это положение верно при определенных условиях, и, прежде всего, при внесении в культуру больших разведений вирусов, исключающих возможность множественного заражения клеток.
![]() Цветная проба.
Цветная проба.
Цветную пробу для лабораторных исследований впервые предложили Солк, Янгнер и Уорд в 1954 г. Предпосылкой для разработки данного метода явились наблюдения Эндерса, Уэллера и Роббинса, которые отметили, что в незаражен-ных тканевых культурах под влиянием продуктов метаболизма рН среды сдвигается вкислую сторону, что улавливается попожелтению фенолрота, добавленного в питательную среду. В то же время жидкость в тканевых культурах, зараженных вирусом, убивающим живые клетки, сохраняла свой красный цвет. Наиболее отчетливые результаты дают вирусы с высокой скоростью размножения при культивировании их на медленнорастущих клетках. Это способ не не отличается высокой достоверностью..
Обнаружение внутриклеточных включений.
При многих вирусных заболеваниях в клетках (в цитоплазме или ядре) различных органов и тканей появляются особые образования, называемые тельцами-включениями. Их классифицируют по локализации в клетке, составу нуклеиновой кислоты, тинкториальным свойствам и гомогенности.
Тельца-включения локализуются избирательно: при оспе, гриппе, бешенстве, парагриппе и других болезнях, как правило, развиваются цитоплазматические включения; при ринотрахеите крупного рогатого скота, ларинготрахеите птиц, аденовирусной инфекции и других — ядерные.
Для приготовления препаратов культур клеток с целью выявления телец-включений клетки выращивают на покровных стеклах в пробирках или пенициллиновых флаконах, заражают испытуемым материалом и через определенные сроки инкубации при 37 °С (что зависит от свойств инокулированного вируса) стекла вынимают, промывают в теплом растворе Хенкса или физиологическом растворе (рН 7,0—7,2), подсушивают фильтровальной бумагой и фиксируют в одной из фиксирующих смесей: растворе Буэна — 10—15 мин, фиксаторе Карнуа — 10, Ценкера—20—30, метиловом спирте —15 мин или в других фиксаторах. Затем препараты окрашивают.
![]() Вирусные тельца-включения хорошо обнаруживаются в препаратах, окрашенных гематоксилин-эозином. Для этого фиксированные на покровных стеклах клетки промывают в дистиллированной воде и погружают на 5—15 мин в раствор гематоксилина (гематоксилин Майера, Эрлиха, Карацци и др.). Время окрашивания подбирают эмпирически для каждой культуры клеток и краски. Затем препараты отмывают водой и помещают на 1—2 мин в аммиачную воду (на 200 мл дистиллированной воды добавляют 2—3 капли аммиака). В щелочной среде ядра клеток приобретают синий цвет. Далее препараты окрашивают 0,1%-ным водным раствором эозина 30—60 с, удаляют лишнюю влагу фильтровальной бумагой, проводят по спиртам возрастающей концентрации: 70, 80, 96 (первый раз), 96 (второй раз), 100° + ксилол (1 : 1), ксилол и заключают в бальзам. В каждом из спиртов и ксилоле препараты держат не более 1 мин. Перед перенесением препаратов в следующую бюксу обязательно снимают с него фильтровальной бумагой лишнюю влагу, иначе спирт будет обводняться. При окраске гематоксилин-эозином ядра клеток окрашиваются в синий цвет, цитоплазма — в розовый, а тельца-включения — в синий или розовый Для обнаружения телец-включений при гриппе довольно часто используют окраску культур клеток по методу Клисенко. Для этого стекла с зараженной культурой клеток споласкивают теплым (37 °С) физиологическим раствором и фиксируют в жидкости Дюбоска — Бразила—Буэна от 20 мин до нескольких недель. Тщательно отмытые (3—4 раза) в дистиллированной воде объекты окрашивают 10 мин 1%-ным раствором акридинового оранжевого, тщательно отмывают дистиллированной водой, затем снова окрашивают 1%-ным раствором эозина 30 мин, промывают дистиллированной водой и допропитывают раствором (1 : 1000) метиленового синего. Последний готовят перед употреблением из 1%-ного маточного раствора.
Вирусные тельца-включения хорошо обнаруживаются в препаратах, окрашенных гематоксилин-эозином. Для этого фиксированные на покровных стеклах клетки промывают в дистиллированной воде и погружают на 5—15 мин в раствор гематоксилина (гематоксилин Майера, Эрлиха, Карацци и др.). Время окрашивания подбирают эмпирически для каждой культуры клеток и краски. Затем препараты отмывают водой и помещают на 1—2 мин в аммиачную воду (на 200 мл дистиллированной воды добавляют 2—3 капли аммиака). В щелочной среде ядра клеток приобретают синий цвет. Далее препараты окрашивают 0,1%-ным водным раствором эозина 30—60 с, удаляют лишнюю влагу фильтровальной бумагой, проводят по спиртам возрастающей концентрации: 70, 80, 96 (первый раз), 96 (второй раз), 100° + ксилол (1 : 1), ксилол и заключают в бальзам. В каждом из спиртов и ксилоле препараты держат не более 1 мин. Перед перенесением препаратов в следующую бюксу обязательно снимают с него фильтровальной бумагой лишнюю влагу, иначе спирт будет обводняться. При окраске гематоксилин-эозином ядра клеток окрашиваются в синий цвет, цитоплазма — в розовый, а тельца-включения — в синий или розовый Для обнаружения телец-включений при гриппе довольно часто используют окраску культур клеток по методу Клисенко. Для этого стекла с зараженной культурой клеток споласкивают теплым (37 °С) физиологическим раствором и фиксируют в жидкости Дюбоска — Бразила—Буэна от 20 мин до нескольких недель. Тщательно отмытые (3—4 раза) в дистиллированной воде объекты окрашивают 10 мин 1%-ным раствором акридинового оранжевого, тщательно отмывают дистиллированной водой, затем снова окрашивают 1%-ным раствором эозина 30 мин, промывают дистиллированной водой и допропитывают раствором (1 : 1000) метиленового синего. Последний готовят перед употреблением из 1%-ного маточного раствора.
Окрашенные препараты промывают дистиллированной водой, дифференцируют в подкисленном (2—3 капли ледяной уксусной кислоты на 50 мл спирта) абсолютном спирте до появления розово-синего оттенка. Обезвоживают абсолютным спиртом и, проводя через ксилол, заключают в бальзам. Цитоплазма окрашивается в нежно-розовый цвет, ядро — в розово-сиреневый, ядрышки — в синий, вирусные включения — в ярко-красный .
Для окраски клеток крови, костного мозга или культур клеток из лимфоидных органов обычно применяют окраску по методу Романовского—Гимзы.
Обнаружение вирусов в реакции иммунофлуоресценции.
В том случае, если размножение вируса в культуре клеток не сопровождается цитопатическим эффектом, гемадсорбцией, его присутствие можно обнаружить с помощью флуоресцирующих антител. Этот метод широко используют при диагностике классической чумы свиней, парвовирусной инфекции свиней и других болезней.
Метод, основанный на интерференции вирусов.
Построен на том, что некоторые вирусы в культуре клеток снижают способность размножаться в ней других вирусов. Например, вирус чумы свиней снижает инфекционную активность вируса ящура, вирус ньюкаслской болезни — вируса везикулярного стоматита и т. д.
Получение первично-трипсинизированных культур клеток из кожномышечной ткани развивающихся куриных эмбрионов.
Куриные эмбрионы 9—11-дневной инкубации овоскопируют. Отбирают яйца с подвижными эмбрионами и хорошо выраженными сосудами. На скорлупе простым карандашом отмечают границы воздушной камеры и расположение зародыша.
Поверхность скорлупы протирают йодированным спиртом и обжигают. Стерильными ножницами срезают скорлупу на 2—3 мм выше границы воздушной камеры, разрывают подскорлупную и хорионаллантоисную оболочки и за шейку извлекают эмбрион в стерильную чашку Петри. У эмбриона удаляют голову, лапки, крылья и внутренние органы. Оставшийся кожномышечный мешок переносят в стерильную майонезную банку (250 мл) и измельчают ножницами на кусочки 3—4 мм.
Измельченную ткань 2—3 раза отмывают раствором Хенкса от слизи и кровяных элементов до получения прозрачных сливных вод и переносят в колбу для трипсинизации. В колбу наливают 0,15%-ный раствор трипсина, подогретого до 35—37 °С (соотношение ткани и трипсина 1 : 3), вносят стерильный магнитик и ставят на магнитную мешалку
Трипсинизацию проводят дробно, т. е. через каждые 3—5 мин отделившиеся клетки вместе с трипсином сливают в центрифужные флаконы и помещают на лед или в холодильник для прекращения действия трипсина на клетки. К оставшемуся в колбе содержимому добавляют новую порцию трипсина. Скорость вращения на магнитной мешалке регулируют так, чтобы не было пены. Процесс повторяют несколько раз (3—5) до полного истощения ткани.
После трипсинизации суспензию клеток в растворе трипсина центрифугируют при 1000 мин-1 10 мин, надосадочную жидкость сливают (выбрасывают), а осадок клеток ресуспендируют в теплой (37 °С) питательной среде (в заведомо известном объеме) и фильтруют через 3-слойный марлевый фильтр.
После тщательного перемешивания клеток берут 1 мл для подсчета клеток.
Успех культивирования клеток в значительной степени зависит от посевной дозы. При малом количестве клеток не наблюдается образование монослоя даже при длительном культивировании. При слишком большой дозе клеток происходит интенсивная их пролиферация, и образованный слой клеток значительно раньше подвергается старению и неспецифической дегенерации. Клетки подсчитывают в камере Горяева.
К 1 мл взвеси клеток добавляют равный объем 0,1%-ного раствора кристаллвиолета, приготовленного на 0,1 н. растворе лимонной кислоты. После перемешивания камеру заполняют взвесью клеток и подсчитывают все клетки, имеющие ядро и неповрежденную цитоплазму; группу клеток с явными контурами считают за одну клетку.
На основании подсчета клеток в двух камерах высчитывают среднее арифметическое в одной из них. Число клеток в 1 мл суспензии (X) определяют по формуле
Х**(А:2- 1000): 0,9,
где А — среднее число клеток в одной камере; 2 — коэффициент разведения суспензии краской; 1000 — число мм3 в 1 см3; 0,9 — объем камеры Горясва, мм3.
После подсчета суспензию клеток разводят питательной средой с таким расчетом, чтобы в 1 мл содержалось от 700 тыс. до 1 млн клеток (для куриных фибробластов).
Пример. В 1 мл полученной суспензии клеток (100 мл) содержится 4 млн клеток. Следовательно, всего в 100 мл суспензии 400 млн клеток. Посевная концентрация — 1 млн клеток в 1 мл. Исходную суспензию клеток (100 мл) доводят ростовой питательной средой до 400 мл.
Затем суспензию разливают в матрасы или пробирки. В пробирки заливают по 1 мл, в матрасы вместимостью 1000, 250 и 100 мл вносят соответственно 100, 40 и 15 мл взвеси клеток. Сосуды и пробирки плотно закрывают стерильными резиновыми пробками (для предупреждения защелачивания среды), делают надпись (вид культуры клеток и дату). На пробирках восковым карандашом проводят продольную черту, укладывают их чертой вверх в лотки с наклонным углом 5° и помещают в термостат при 37 °С.
Ежедневно культуры просматривают под малым увеличением микроскопа для определения характера роста. Если клетки не пролиферируют, выглядят округлыми, зернистыми, темными и отслаиваются от стекла, это свидетельствует о плохой обработке посуды или токсичности сыворотки, питательной среды. Пролиферирующие клетки светлые, связаны цитоплазматическими отростками, растут однослойным пластом. В процессе размножения клеток выделяются продукты обмена веществ, которые вызывают изменение рН питательной среды в кислую сторону (среда желтеет), что отрицательно влияет на клетки и может привести их к гибели. Такую среду заменяют свежей. Обычно сплошной монослой куриные фибробласты образуют через 36—48 ч.
От одного куриного эмбриона получают 70—120 млн клеток. Культуры клеток куриных фибробластов используют при работе с вирусом болезни Ауески, оспы птиц, ньюкаслской болезни, гриппа птиц, вируса саркомы Рауса и др.
Список литературы
1. Р.В. Белоусова, Э.А Преображенский, И.В. Третьякова "Ветеринарная вирусология" - М.: КолосС, 2007г.
2. В.Н.Сюрин, Р.В.Белоусова, И.В.Фомина "Ветеринарная вирусология" - М.: ВО " Агропромиздат", 1991г.
3. Р.В.Белоусова, Н.И.Троценко,Э.А.Преображенская "Практикум по ветеринарной вирусологии" - М.: КолосС, 2006г.
Похожие работы
... генетического аппарата клетки хозяина, что приводит к развитию онкологических заболеваний. 2. Вирусология в медицине Вирусология — наука о вирусах. Общая вирусология изучает природу вирусов, их строение, размножение, биохимию, генетику. Медицинская, ветеринарная и сельскохозяйственная вирусология исследует патогенные вирусы, их инфекционные свойства, разрабатывает меры предупреждения, ...
... скот) и дикими жвачными. Обязательным является профилактическое карантинирование с проведением при необходимости вирусологических и серологических исследований. В стационарно неблагополучной по инфекционной катаральной лихорадке овец местности необходимо вакцинировать восприимчивое поголовье не менее чем за месяц до наступления сезона болезни. При появлении болезни также следует проводить ...
... изменят одной из причин сравнительно высокой способности вирусов изменять свои свойства является то, что наследственное вещество этих микроорганизмов менее защищено от воздействия внешней среды. Мутация вирусов может возникать в результате химических изменений цистронов или нарушения последовательности их расположения в структуре молекулы вирусной нуклеиновой кислоты. В зависимости от условий ...
... сельского хозяйства как биосистемы (работа с живыми организмами), которая снижает привлекательность инвестиций в эту отрасль. Между ними и инновациями возникает противоречие. Так, извлечение сверхприбыли в короткий период от инновационных проектов в сельском хозяйстве невозможно, а оптимальным является вложение средств в долгосрочные проекты; получение прибыли в среднесрочных проектах рискованно, ...

0 комментариев