Навигация
2 Н2О + 2 А = 2АН2 + О2
Суть реакции в том, что к суспензии хлоропластов добавляют донор электронов (например краску - 2,6-дихлорфенолиндофенол) и по изменению окраски суспензии хлоропластов на свету судят об их фотохимической активности, характеризуя таким образом видовые и сортовые особенности растений.
Доказано, что количество АТФ, образовавшейся при фотофосфорилировании, соответствует количеству восстановленного окислителя в реакции Хилла. Этот процесс напрямую связан со свойствами пигментов.
Темновая фаза фотосинтеза или цикл Кальвина (С-3 путь фотосинтеза).
Запасенная в световой фазе фотосинтеза энергия тратится на процесс превращения неорганической формы углерода (углекислого газа или бикарбонат-иона) в органическую, то есть фактически тратится на создание простых сахаров, из которых затем формируются полисахариды. Практически у всех растений происходит процесс, называемый циклом Кальвина, в котором идет преобразование неорганического углерода в органический. Процесс разделяется на три этапа:
карбоксилирование, когда СО2 соединяется с рибулезо-1-5-дифосфатом, образует нестойкое шестиуглеродное соединение, которое распадается на две молекулы фосфоглицериновой кислоты - 3-углеродные молекулы,
фазу восстановления, когда образовавшаяся фосфоглицериновая кислота восстанавливается в фосфоглицериновый альдегид - это центральное звено цикла, так как ФГА по уровню восстановленности углерода соответствует углеводу с общей формулой (СН2О) 3,фазу регенерации, когда вновь образуется первичный акцептор СО2 - рибулезодифосфат - и, одновременно, происходит синтез конечных продуктов фотосинтеза - глюкозы и крахмала.
Поскольку в цикле Кальвина первичными продуктами включения неорганического углерода в органический являются трехуглеродные соединения, этот процесс носит название С-3 путь фотосинтеза.
Для синтеза одной молекулы глюкозы должно произойти шесть оборотов цикла Кальвина. В каждом обороте используются три молекулы АТФ (две для активирования двух молекул фосфоглицериновой кислоты и одна при регенерации рибулезодифосфата) и две молекулы НАДФ. Н2 для восстановления кислоты в альдегид. Таким образом для синтеза одной молекулы глюкозы необходимо потратить 12 молекул НАДФ. Н2 и 18 молекул АТФ.
Важно отметить, что физиологическое значение цикла Кальвина состоит не только в акцепции углекислого газа, но и в создании массы углеводных соединений, которые идут как на синтез запасных веществ, так и на создание компонентов хлоропласта и текущий метаболизм клетки. .
С-4 путь фотосинтеза.
Большинство растений усваивает неорганический углерод именно по пути цикла Кальвина. Однако довольно большая группа растений (около 500 видов) тропического происхождения выработала в процессе эволюции некоторую модификацию процесса, усваивая неорганический углерод путем образования в результате его акцепции четырехуглеродных соединений. Это растения, приспособившиеся к фотосинтезу в условиях повышенной температуры воздуха и избыточной освещенности, а также пониженной влажности почвы (засухи). Из культурных растений обладают таким метаболитическим процессом кукуруза, просо, сорго, сахарный тростник. У ряда сорных растений также наблюдается именно эта особенность метаболизма (свинорой, просо куриное, щирица) и т.д.
Особенностью анатомического строения таких растений является наличие фотосинтезирующих клеток двух типов, которые располагаются в виде концентрических кругов - радиально расположенные вокруг проводящих пучков клетки обкладочной паренхимы и мезофилла. Этот тип анатомического строения называется кранц-типом (от немецкого Кranz -венок).
Этот тип метаболизма был изучен в 60-е годы прошлого века, большую роль сыграли при этом исследования советских ученых Карпилова, Незговоровой, Тарчевского, а также австралийских ученых Хэтча и Слэка. Именно они предложили законченную схему цикла, поэтому принято этот процесс называть также циклом Хэтча-Слэка-Карпилова.
Процесс происходит в два этапа: поступающий в мезофилл СО2 вступает в соединение с трехуглеродным соединением (ФЕП) - фосфоенолпировиноградной кислотой - которая превращается в четырехуглеродное соединение. Это и есть ключевой момент процесса, из-за которого он и получил свое название, так как неорганический углерод, акцептируясь трехуглеродным соединением, превращается в четырехуглеродное соединение. В зависимости от того в какое именно четырехуглеродное соединение превращается неорганический углерод различают три группы растений:
НАДФ-МДГ образуют яблочную кислоту при участии фермента малатдегидрогеназы, а затем пировиноградной кислоты,
НАД-МДГ образуют аспарагиновую кислоту и аланин,
ФЕП-КК образуют аспарагиновую кислоту и фосфоенолпировиноградную кислоту.
Наиболее значимые для сельского хозяйства растения относятся к НАДФ-МДГ типу.
После образования четырехуглеродного соединения происходит его перемещение во внутренние клетки обкладочной паренхимы и расщепление или декарбоксилирование этой молекулы. Отделившаяся карбоксильная группа в виде CОО - входит в цикл Кальвина, а оставшаяся трехуглеродная молекула - ФЕП - возвращается опять в клетки мезофилла.
Такой путь фиксации углекислого газа позволяет растениям накапливать в виде органических кислот запас углерода, проводить процесс фотосинтеза в наиболее жаркое время дня при сокращении потерь воды на транспирацию за счет закрытия устьиц. Эффективность использования воды такими растениями в два раза больше, чем у растений, происходящих из умеренных широт.
Для С4-растений характерны отсутствие обратного потока углекислого газа при фотодыхании и повышенный уровень синтеза и накопления органических веществ.
САМ-фотосинтез.
У суккулентных растений семейства Crassulaceae - Толстянковые - процесс фотосинтеза также имеет свои особенности, связанные с особенностями климатической зоны происхождения этих растений. Поскольку эти растения, обитающие в условиях крайне засушливого климата, днем закрывают устьица, то есть дневная транспирация у них отсутствует, то поступление углекислого газа в листья возможно только ночью. При этом углекислый газ немедленно вступает в соединение с пируватом с образованием яблочной кислоты, то есть процесс совпадает с циклом Хэтча-Слэка. Однако, дальнейшее превращение яблочной кислоты в пировиноградную, отщепление карбоксильной группы и включение ее в цикл Кальвина происходит днем, при закрытых устьицах.
Основное отличие этого процесса от цикла Хэтча-Слэка состоит в том, что процессы акцептации углекислого газа и цикл Кальвина разделены во времени, акцептация происходит ночью, а цикл Кальвина - днем.
По английскому наименованию процесса - Crassulacean acid metabolism (САМ) - процесс называют - САМ-фотосинтез.
Фотодыхание.
Фотодыхание представляет собой процесс разложения рибулезодифосфата - ключевого вещества цикла Кальвина - на фосфоглицериновую кислоту и фосфогликолевую кислоту (С5 = С3 + С2). Этот процесс происходит в условиях наличия большого количества кислорода и осуществляется основным ферментом цикла Кальвина РДФ-карбоксилазой, которая в обычных условиях осуществляет собственно акцепцию углекислого газа и образование двух молекул фосфоглицериновой кислоты.
Анатомическая особенность состоит в том, что в процессе фотодыхания в отличие от обычного дыхания, происходящего в митохондриях, задействованы три типа органоидов - хлоропласты, пероксисомы и митохондрии.
Суть химизма процесса состоит в том, что образовавшаяся фосфоглицериновая кислота (С3) поступает в цикл Кальвина, а фосфогликолевая кислота (С2) подвергается дефосфорилированию с образованием гликолата.
Гликолат из хлоропласта поступает в пероксисому, где окисляется до глиоксилата, который затем превращается в аминокислоту глицин. Таким образом, фотодыхание позволяет связать в общем метаболизме синтез углеводов с метаболизмом аминокислот.
Глицин поступает затем в митохондрию, где превращается в серин, освобождая углекислый газ, а серин используется в циклах синтеза аминокислот.
На первый взгляд процесс фотодыхания ничего, кроме потерь не приносит. И, действительно, часть накопленных в процессе фотосинтеза углеводов теряется. Однако все попытки искусственно ингибировать фотодыхание приводили к общему снижению интенсивности фотосинтеза.
На современном этапе развития физиологии растений принято считать, что основное значение фотодыхания заключается в его защитной роли. Сбрасывая таким образом избыточную энергию, растение избегает разрушения фотосистем, обеспечивает сбалансированность световой и темновой фаз фотосинтеза.
Фотодыхание выполняет роль отводного канала в общем русле энергообеспечения растения.
Характеристика основных показателей фотосинтеза:
интенсивности и продуктивности.
Фотосинтез характеризуется следующими количественными показателями:
интенсивностью фотосинтеза,
продуктивностью фотосинтеза.
Интенсивность (скорость) фотосинтеза - это количество углекислого газа, которое усваивается единицей листовой поверхности за единицу времени. В зависимости от вида растения этот показатель колеблется от 5 до 25 мг СО2/дм2. ч.
Продуктивность фотосинтеза - это отношение суточного увеличения массы всего растения (в граммах) к площади листьев. В среднем эта величина составляет от 5 до 12 г сухого вещества на 1 м2 листовой поверхности в сутки.
Существует большое количество методов определения этих количественных показателей.
Интенсивность фотосинтеза можно определять:
газометрическими методами,
радиометрическими методами.
С помощью газометрических методов можно определить либо количество усвоенного углекислого газа, либо количество выделенного кислорода. При этом используют как весовые показатели поглощаемых или выделяемых газов, так и объемные показатели, показатели давления, показатели окраски, показатели теплопроводности определяемых газов.
С помощью радиометрических методов определяют интенсивность поглощения С14О2 растением по наличию в нем С14 или изменение радиоактивности газовой смеси.
Продуктивность фотосинтеза определяют по накоплению ассимилятов в растении. При этом используют такие методы, как:
изменение количества сухого вещества высечек из листа через определенный временной промежуток,
накопление углеводов в листе через определенный временной промежуток,
изменение теплоты сгорания сухого вещества листьев за период экспозиции их на свету.
В процессе вегетации интенсивность и продуктивность фотосинтеза возрастают постепенно от начала развития, достигают максимума в фазе цветения-плодообразования, а затем постепенно убывают.
Усвоение растением фотосинтетически активной радиации.
Фотосинтетически активная радиация (ФАР) - это та часть солнечного излучения, которая способна поглощаться хлорофиллами в процессе фотосинтеза. ФАР имеет спектр волн от 380 до 710 нм и состоит из прямыцх солнечных лучей и рассеянного света, интенсивность которого равна 1/3 прямой солнечной радиации. В рассеянном свете на долю ФАР приходится до 90%, то есть рассеянный свет в отличие от прямых солнечных лучей может быть поглощен растением почти полностью.
Интенсивность фотосинтеза максимальна в красной части спектра и минимальна в синей и зеленой частях.
ФАР по разному поглощается листьями разных растений. Этот процесс определяется количественным и качественным составом пигментов в листе. Утром и вечером фотосинтез у растений с достаточным запасом хлорофилла наиболее интенсивен.
О степени использования растением фотохимической активности хлорофилла судят по ассимиляционному числу - то есть по количеству углекислого газа, ассимилированного единицей хлорофилла в единицу времени.
У растений с темно-зелеными листьями ассимиляционное число невелико, это растения, обитающие в основном в тени, у растений со светло-зеленой окраской - этот показатель значительно выше, так как это светолюбивые растения.
Основное поглощение ФАР происходит в верхних ярусах посева, так же и содержится большее количество хлорофилла.
Поглощение лучистой энергии листом выражается формулой:
Q = R + T + A,
где Q - количество радиации, падающей на лист, R - отраженная радиация, в%, Т - пропущенная радиация, в%, А - поглощенная радиация, в%. Все три показателя зависят от содержания хлорофилла в листе.
Фотосинтез возможен при минимальной интенсивности света, при увеличении интенсивности света до 1/3 от полного солнечного освещения интенсивность фотосинтеза возрастает, при еще более высокой освещенности интенсивность фотосинтеза повышается незначительно, а при максимальном освещении наступает световое насыщение фотосинтеза и вступает в действие механизм фотодыхания.
Общее количество солнечной радиации, падающее на 1 га за период вегетации, составляет 21.109 кДж, из них ФАР - только 8.109 кДж, то есть всего около одной трети.
Количество ФАР, поглощенной посевом определяют по формуле:
П = Q - R - Тп + Rп
где П - поглощенная посевом радиация, Q - суммарная радиация, падающая на посев, R - радиация, отраженная от посева и вышедшая за пределы его верхней границы, Тп - радиация, проникшая к почве, Rп - радиация, отраженная от почвы под растительностью.
Коэффициент поглощения энергии ФАР (Qп) посевом определяют делением обеих частей формулы на Q:
Qп = П/Q = 1 - R/Q - Тп/Q + Rп/Q,
где R/Q - альбедо посева, показывающее, какая доля падающей радиации отражается посевом, Тп/Q - коэффициент пропускания, показывающий, какая доля падающей радиации (Q) достигает почвы под растительностью, Rп/Q - альбедо почвы под растительностью.
Эффективность фотосинтеза можно характеризовать коэффициентом полезного действия, который определяют по формуле:
Е% (КПД) = В.100/А,
где А - количество энергии, поступившей за период вегетации на 1 га посева, или энергии, которая была поглощена посевом, в кДж, В - количество энергии, накопившейся в органической массе урожая (биологического или хозяйственного), в кДж.
Доказано, что для образования продуктов фотосинтеза при всех благоприятных условиях (орошение, высокая концентрация СО2) солнечная энергия используется только на 2%. В среднем КПД фотосинтеза сельскохозяйственных растений в реальных условиях составляет около 0,5-1% (то есть около 16 кДж/м2 в час), теоретически же возможно повышение уровня этого показателя до 4-6%. Одной из самых насущных задач, стоящих перед практическим сельскохозяйственным производством, и является повышение эффективности фотосинтеза.
Условия, влияющие на интенсивность и продуктивность фотосинтеза.
На основные показатели фотосинтеза влияют как внутренние факторы, так и внешние абиотические факторы.
К внутренним факторам - то есть к эндогенным механизмам регуляции фотосинтеза у растений - относятся:
проводимость листа,
фотохимическое лимитирование фотосинтеза,
биохимическое лимитирование фотосинтеза,
гормональное воздействие,
донорно-акцепторные отношения,
накопление углеводов,
возраст листа или растения.
Проводимость листа бывает устьичная и остаточная. Она измеряется в сантиметрах в секунду и является величиной, обратной сопротивлению листа, колеблется от 1 см/с при открытых устьицах до 0,02 см/с при закрытых устьицах, показывает скорость прохождения углекислого газа по тканям листа.
Фотохимическое лимитирование фотосинтеза происходит при недостатке поступления энергии из световой фазы фотосинтеза, то есть при недостатке освещенности.
Биохимическое лимитирование фотосинтеза определяется недостаточным количеством необходимых для фотосинтеза ферментов, в частности рибулезодифосфаткарбоксилазы/оксигеназы, или недостатком собственно субстрата - рибулезодифосфата.
Гормональное воздействие проявляется в действии ингибиторов роста, например, АБК, повышение концентрации которой приводит к закрытию устьиц и к снижению интенсивности фотосинтеза.
Донорно-акцепторные отношения проявляются в том, что если у растения уменьшается число акцепторов продуктов фотосинтеза (число клубней, плодов), то интенсивность фотосинтеза снижается, если же уменьшается число доноров продуктов фотосинтеза (листьев) (например в результате повреждения вредителями, искусственная частичная дефолиация), то интенсивность фотосинтеза у оставшихся листьев увеличивается.
Накопление углеводов (крахмала) может вызвать снижение интенсивности фотосинтеза, хотя вопрос остается до конца не изученным.
Возраст листа (растения) определяет повышение интенсивности фотосинтеза у завершившего рост листа и постепенное снижение интенсивности фотосинтеза у стареющего листа за счет деградации хлоропластов.
На показатели фотосинтеза значительно влияют такие абиотические факторы, как:
освещенность,
температура,
водный режим,
минеральное питание,
содержание углекислого газа.
Освещенность растения влияет не только за счет количества ФАР, падающей на лист, но и за счет качества падающей световой энергии. Качество света влияет на превращение промежуточных продуктов фотосинтеза и на направленность дальнейшего процесса биосинтеза. Так коротковолновой свет способствует образованию аминокислот, белков, органических кислот, а длинноволновой - образованию углеводов. Интенсивность фотосинтеза максимальна в красной части спектра и минимальна в синей и зеленой его частях.
Интенсивность фотосинтеза незначительно меняется под воздействием количества падающей радиации, так как ее количество лист регулирует с помощью фототаксиса хлоропластов. При избытке света может наступать разрушение фотосинтетического аппарата.
Температура воздуха положительно влияет на интенсивность фотосинтеза, если повышается до 25-35оС, но при более высоких показателях может снижать интенсивность фотосинтеза за счет перегрева листа. Температура листьев зависит от угла падения на них солнечных лучей. При расположении листьев параллельно лини падения солнечных лучей, перегрева не наблюдается, таким образом растение может регулировать температуру с помощью движений листьев. Нижняя температурная граница, при которой может осуществляться фотосинтеза, составляет около -5оС (у хвойных пород зимой), оптимальна температура около 25оС.
Водный режим определяет степень обводненности тканей и, следовательно, поглощение энергии солнечной радиации, поступление и ассимиляцию углекислого газа, систему ферментативных реакций в фотосистеме П, интенсивность транспирации. При водном дефиците происходит деградация сформированных хлоропластов, изменяется структурная связь хлорофилла с белками, увеличивается количество прочносвязанной воды. Дефицит воды в листьях может быть общим показателем фотосинтеза, поскольку в нем отражается влияние влажности почвы и всех метеорологических факторов (температуры, влажности воздуха, радиационного режима).
Минеральное питание. Корневая система усваивает различные макро и микроэлементы, необходимые для процесса фотосинтеза, для формирования фотосинтетического аппарата: хлорофиллов, каротиноидов, ферредоксинов, других ферментов и коферментов. Необходимо поступление и микроэлементов (магния, марганца, серы, железа), и макроэлементов (азота, калия, фосфора), без которых невозможны ни процессы образования макроэргических молекул, ни биосинтез продуктов фотосинтеза. При недостатке азота и фосфора в почвенном растворе наблюдаются глубокие изменения ультраструктуры хлоропластов, нарушение синтеза пигментов. В свою очередь оптимальный световой режим в посевах способствует повышению эффективности действия минеральных удобрений.
Содержание углекислого газа. Обычное содержание в воздухе углекислого газа в объеме 0,03%, является минимальным, поэтому увеличение его концентрации в атмосфере всегда приводит к повышению энергии фотосинтеза и положительно влияет как на интенсивность, так и на продуктивность фотосинтеза. Так, при увеличении концентрации углекислого газа до 0,08% интенсивность фотосинтеза возрастает в 2-3 раза.
Пути повышения продуктивности фотосинтеза.
Основываясь на механизмах влияния внутренних и внешних факторов, действующих на показатели фотосинтетической активности растений, в практике сельского хозяйства используют ряд приемов, позволяющих увеличить интенсивность фотосинтеза и повысить урожайность сельскохозяйственных культур.
Прежде всего это точное соблюдение оптимальной технологии:
соблюдение режима орошения,
соблюдение режима минерального питания,
использование необходимых внекорневых подкормок микроэлементами,
повышение в защищенном грунте концентрации углекислого газа за счет применения органических удобрений (внесение навоза), использования сухого льда, поддымление парниковых рам. При этом у огурцов не только повышается интенсивность фотосинтеза, но и увеличивается количество женских цветков.
Соотношение между количеством усвоенного в процессе фотосинтеза углекислого газа и накопленного сухого органического вещества называется коэффициентом эффективности фотосинтеза.
Необходимо учитывать, что на итоговое накопление органического вещества влияют два процесса: фотосинтез и дыхание. Количество накапливаемых органических веществ зависит от интенсивности фотосинтеза и дыхания растений, то есть от положения компенсационной точки. Компенсационная точка характеризует такое состояние растения, когда в нем фотосинтез и дыхание полностью уравновешиваются, т.е. при таких условиях органическое вещество не накапливается.
Накопление органического вещества растением за определенный период или за всю его жизнь следует рассматривать как разницу между количеством созданного на свету органического вещества и израсходованного на дыхание.
Кроме того, в процессе преобразования веществ также может происходить уменьшение массы (например, масса клетчатки на 10% меньше массы глюкозы, из которой она образуется), на накопление органического вещества влияет также опадение или гибель частей растения (цветков, корневых волосков) в период вегетации.
При оптимальных условиях влажности и температурного режима важно также соблюдать оптимальное размещение растений. Для лучшего освещения растений рядки располагают с востока на запад или с северо-востока на юго-запад. Величина урожая в значительной мере зависит от оптимальной структуры посевов.
Структурой посевов называется создаваемая архитектоника сообщества растений, которое характеризуется определенными морфологическими признаками и физиологическими функциями, а оптимальная структура - это такой посев, который имеет высокий КПД фотосинтеза и обеспечивает максимальный урожай. Обычно потери энергии на дыхание составляют 15-25%, но при загущенном посеве нижние, а частью и средние листья становятся не столько синтезирующими, сколько потреблояющими.
Одной из важнейших задач селекции является создание сортов, способных развивать большую фотосинтезирующую поверхность, имеющих высокую продуктивность фотосинтеза и дающих большой биологических и хозяйственный урожай.
В сельском хозяйстве наибольший интерес представляет получение конечного продукта - полезной накопленной биомассы растений, то есть чистой продуктивности фотосинтеза.
Чистую продуктивность фотосинтеза определяют, пользуясь легко определяемыми величинами: площадью листовой поверхности и фактически накопленной биомассой:
В2-В1
Фч. пр. = - ---------------
(Л1+Л2).1/2п,
где В1 и В2 - масса сухого вещества пробы урожая в начале и конце учетного периода, т.е.
В2 - В1 - прирост сухой массы за учетный период (п дней), Л1 и Л2 - площадь листьев пробы в начале и конце периода, т.е. (Л1+Л2).1/2п - средняя площадь листьев за указанный отрезок времени, п - число дней в учетном периоде.
Кроме общей чистой продуктивности фотосинтеза определяют и интенсивность работы листьев, направленную на создание хозяйственной части урожая. В этом случае вместо В2 - В1 подставляют величины Х2 - Х1, то есть прирост сухой массы хозяйственной части урожая.
Фотосинтетический потенциал растений - это сумма ежедневных показателей площади листьев посева за весь вегетационный период (или за его часть), выраженная в
м2. дни/га.
Биологический урожай - это сумма суточных приростов за весь вегетационный период:
Убиол. = еС1,2... п,
где С - суточные приросты массы, в кг/га в сутки.
Ф. Кэф.
С= - ---------
Л
Х1000,где Ф - количество ассимилированного СО2, Кэф. - коэффициент фотосинтеза (суточный прирост урожая/ суточное усвоение углекислого газа), Л - листовая поверхность, 1000 - граммы (для пересчета в кг). В среднем при хорошей агротехнике сельскохозяйственные культуры накапливают 15-20 т/га сухой биомассы.
Хозяйственный урожай составляет ту долю биологического, которая используется человеком:
Ухоз. = Убиол. Кхоз.
Коэффициент хозяйственного использования у разных культур может сильно различаться (зерновые культуры и сахарная свекла).
Продуктивность фотосинтеза сельскохозяйственных культур целесообразно оценивать величиной выхода полезной энергии с гектара.
Демонстрация таблиц с данными по интенсивности фотосинтеза для разных культур.
Для определения площади листовой поверхности используют три основных метода:
фотопланиметрирование - когда с помощью специального прибора определяют уменьшение интенсивности светового потока, пропорциональное площади листа,
расчет по высечкам - когда, взвесив несколько высечек известной площади, делят общий вес листа на вес высечек и узнают общую площадь листа,
расчет по линейным размерам листа по формуле S=а. b. k, где а и b - ширина и длина листа, а k - коэффициент для данной сельскохозяйственной культуры. Для всех сельскохозяйственных культур он определен и приведен в справочниках: для кукурузы - 0,68; для ячменя - 0,65; для сахарной свеклы - 0,76; для яблони - 0,62-0,74.
Суточный ход фотосинтеза у светолюбивых и теневыносливых растений.
В связи с тем, что основой жизнедеятельности растений является фотосинтез, все растения любят свет. Однако, есть растения, выносливые к недостатку света, которые называют теневыносливыми. Светолюбивость или теневыносливость растений определяется сформировавшимися в процессе эволюции механизмами приспособления к окружающим факторам среды.
Светолюбивость проявляется в значительном уменьшении содержания зеленых пигментов и соответствующем повышении количества каротиноидов. У светолюбивых растений часто наблюдается усиленное развитие ассимилирующей ткани палисадной паренхимы, состоящей из нескольких слоев клеток меньшей величины, чем у теневыносливых; у них число устьиц больше и поэтому углекислый газ быстрее проникает внутрь листа. Внешне у светолюбивых растений листья всегда более мелкие и имеют более бледную зеленую окраску, чем теневыносливые.
Интенсивность фотосинтеза у светолюбивых растений повышается к полудню и уменьшается утром и вечером, у теневыносливых максимум фотосинтеза приходится на утро и вечер, и минимальна интенсивность фотосинтеза в полдень.
Роль зеленых растений в природе.
Зеленые растения, являясь основными автотрофами на нашей планете, определяют несколько существеннейших параметров жизни:
накопление кислорода в атмосфере,
накопление биомассы,
основное звено синтеза органики в пищевых цепях,
преобразование физической энергии Солнца в химическую энергию органических веществ.
В.И. Вернадский писал о значении растений так: "На нашей планете свободный кислород, находящийся на ней в виде газа или в форме раствора в природных водах, нацело создается жизнью. Мы не знаем пока ни одного случая, когда бы он выделялся в значительном количестве в результате какого бы то ни было химического процесса, независимо от жизни. Но нам известны тысячи земных химических процессов, в которых свободный кислород поглощается, переводится в новые соединения, исчезает как таковой. А между тем, количество его в биосфере не меняется, остается все тем же. Это достигается непрерывной работой зеленых растений, и это одно дает меру их значения на нашей планете, дает представление о размахе их геохимической энергии".
В ранние геологические периоды теплый и влажный климат и высокое содержание углекислого газа в атмосфере Земли содействовали пышному расцвету фотосинтезирующих растений. При этом все большее количество углерода переходило в состав органических веществ, которые затем превращались в залежи полезных ископаемых (уголь, нефть, торф) и гумус. Эти запасы ныне достигают 6.1015тонн.
Космическая роль зеленых растений выражается в их влиянии на изменение условий жизни на Земле и в обеспечении возникновения новых форм жизни.
Атмосфера обогащалась кислородом, уменьшалось количество углекислого газа. Имеющееся в современной атмосфере количество кислорода, равное 1,5.1015 тонн, близко к тому количеству, которое должно было выделиться при образовании органических запасов углерода на Земле (6.1015тонн).
По современным подсчетам годовая продуктивность всей растительности Земли оценивается в 100 миллиардов тонн сухой биомассы.
Преобладающую роль в продуктивности наземной растительности играют леса - 28,4 миллиарда тонн, затем идут пастбища (степи, луга) - 10,4 миллиарда тонн, затем сельскохозяйственные угодья, которые дают около 8,7 миллиардов тонн сухой биомассы.
Основное же количество сухой биомассы накапливает растительность океанов и других водоемов.
Ежегодно растения поглощают из окружающей среды 2.109 т азота, 6.109 фосфора, 158.109 т углекислого газа и 128.109 т воды, а выделяют 115.109 т кислорода.
В процессе дыхания растений окисляется 25.109 т органики, причем выделяется 34,5.109 т углекислого газа.
Весь животный мир разлагает 3,5.109 т органики с образованием 4,8.109 т углекислого газа.
За счет сжигания полезных ископаемых в промышленности и быту в атмосферу выделяется 15.109 т углекислого газа.
Тема: Дыхание растений.
Дополнительная литература по теме:
В.Л. Кретович "Основы биохимии растений". М, 1971,А. Ленинджер "Биохимия" М., 1974,Я. Мусил, О. Новакова, К. Кунц "Современная биохимия в схемах".М., 1981.
Перечень вопросов:
Общая характеристика дыхания.
Гликолиз.
Пентозофосфатный цикл.
Цикл Кребса.
Глиоксилатный цикл.
Цепь дыхательных ферментов.
Строение и функции митохондрии и дыхательных ферментов. Энергетика процесса дыхания.
Влияние условий окружающей среды на дыхание растений.
Регулирование дыхания сельскохозяйственных продуктов при хранении.
Общая характеристика дыхания.
Дыхание занимает исключительное положение среди других физиологических процессов. Окислительное дыхание свойственно всем многоклеточным живым организмам, как растительным, так и животным. Ряд видов прокариот также ведут этот процесс. Поэтому основные этапы дыхания являются одинаковыми для всех живых организмов, получающих энергию с помощью этого способа.
Дыхание является ключевым процессом метаболизма любого организма по двум причинам: при дыхании происходит освобождение химической энергии органических веществ, используемых в качестве дыхательного материала. Экзотермические реакции дыхательного процесса непосредственно связаны с эндотермическими процессами клеточного обмена и служат для них источником энергии. Таким образом, дыхание обеспечивает возможность течения эндотермических реакций обмена, процессов образования структур и осуществления движений, что требует затрат энергии, при дыхании протекают такие химические превращения, в результате которых образуются высокоактивные соединения, обладающие большой реактивной способностью и играющие исключительную роль в обмене веществ в организме.
Итоговое уравнение дыхания:
С6Н12О6 + 6 О2 = 6 СО2 +: 6Н2О + 686 ккал (2867 кДж)
Дыхание обеспечивает организм энергией, необходимой для поддержания процессов, протекающих с ее затратой и высокоактивными веществами, принимающими участие в клеточном обмене.
Подавляющее большинство живых организмов для поддержания своей жизни используют ту энергию, которая освобождается во время диссимиляции органических веществ, в первую очередь углеводов, образовавшихся в процессе фотосинтеза и являющихся по образному выражения К.А. Тимирязева, как бы "консервом" энергии солнечных лучей.
Остановка или значительное замедление дыхания вызывает остановку или глубокие изменения в ходе всех жизненных процессов организма.
В клетке непрерывно происходят различные процессы, направленные на биосинтез веществ, поддержание осмотического и электрического потенциалов, осуществление механических движений как клетки, так и ее отдельных органоидов. Все эти процессы идут с использованием свободной энергии, т.е. являются эндотермическими реакциями, а свободная энергия в клетке образуется только в результате преобразования высокомолекулярных соединений (например, АТФ) в более низкомолекулярные соединения (например, АДФ), и при этом выделяется определенная часть энергии. В процессе дыхания как раз и происходит на многих этапах осуществление процесса дефосфорилирования (АТФ = АДФ + Ф), что и определяет выделение энергии.
Дыхание состоит из трех основных этапов:
гликолиза (разложения субстрата (углеводов, жиров, аминокислот) до пировиноградной кислоты),
цикла Кребса (разложения пировиноградной кислоты до СО2 и Н+),
цепи дыхательных ферментов (по ним переносятся ионы Н+ на акцептор О2 и образуется Н2О).
При этом гликолиз и цикл Кребса являются стадиями анаэробными, а кислород включается в процесс уже на последнем этапе процесса. Гликолиз происходит в цитоплазме, а цикл Кребса и перенос по цепи дыхательных ферментов осуществляются в митохондрии.
Гликолиз.
Гликолиз является первым этапом разложения глюкозы, то есть сложного органического вещества (шестиуглеродного соединения) до пировиноградной кислоты, то есть более простого органического вещества (трехуглеродного соединения). Глюкоза, в свою очередь, образуется либо из поли - или олигосахаридов, либо из аминокислот, либо из жиров.
Гликолиз, в свою очередь, состоит из двух этапов:
фосфорилирование простых сахаров и их превращение в глицеральдегидфосфат, при этом происходит дефосфорилирование АТФ в АДФ, т.е. использование энергии АТФ,
превращение глицеральдегидфосфата в пировиноградную кислоту, при этом образуется АТФ, то есть происходит запасание энергии.
Второй этап гликолиза, в свою очередь, происходит в две стадии:
сначала глицеральдегидфосфат превращается в фосфоглицериновую кислоту,
затем фосфоглицериновая кислота через образование фосфоенолпировиноградной кислоты превращается в пировиноградную кислоту, при этом также происходит субстратное фосфорилирование АДФ, в результате чего образуется АТФ.
Гликолиз, происходящий таким традиционным путем, то есть дихотомическим деление глюкозы на две трехуглеродные молекулы, называют также путь Эмбдена-Мейергофа-Парнаса (ЭМП). У некоторых видов микроорганизмов этот этап дыхания может происходить с использованием другой схемы превращения веществ, например идти по пути Энтнера-Дудорова.
Физиологическое значение гликолиза состоит прежде всего в активировании гексоз, образовании ряда простых промежуточных соединений, а также в образовании молекул АТФ. При этом биохимическая составляющая функции гликолиза значительнее его энергетической составляющей.
Пентозофосфатный цикл.
Пентозофосфатный цикл является у растений дополнительным циклом к процессу гликолиза при преобразовании гексоз. Этот биохимический процесс характерен только для растений и чаще всего протекает у видов, склонных к накоплению крахмала в качестве основного запасного вещества. В отличие от гликолиза, происходящего, как правило, по пути дихотомического деления глюкозы, пентозофосфатный цикл является апотомическим путем деления глюкозы, при котором глюкоза сначала превращается в глюконовую кислоту, а затем подвергается реакции декарбоксилирования, в результате чего теряется карбоксильная группа в виде СО2 и происходит образование молекулы НАДФ. Н2, то есть идет процесс запасания энергии. При декарбоксилировании глюконовой кислоты образуется пентоза. В свою очередь, из двух молекул пентозы могут образовываться самые различные моносахара, что обеспечивает растению биохимическое разнообразие молекул.
Физиологический смысл пентозофосфатного цикла заключается в образовании большого разнообразия простых сахаров, образовании молекул НАДФ. Н2, как источника водорода, необходимого для восстановительного синтеза аминокислот и жирных кислот, а также дополнительном источнике энергии. Чистый выход энергии в результате пентозофосфатного цикла составляет в пересчете на 1 молекулу глюкозы 35 молекул АТФ.
Пентозофосфатный цикл может происходить как в цитоплазме, так и в пластидах.
Цикл Кребса.
Цикл Кребса, или цикл лимонной и изолимонной кислот, или цикл ди - и три-карбоновых кислот является основным этапом процесса дыхания. Этот процесс практически универсален, является главным путем окисления остатков уксусной кислоты у всех живых организмов.
Цикл Кребса состоит из двух стадий:
декарбоксилирование пировиноградной кислоты с образованием уксусной кислоты и СО2, в результате чего уксусная кислота соединяется с коферментом А и образует ацетилКоА, являющийся ключевым веществом, входящим в собственно цикл Кребса и образующийся также при прохождении ряда других биохимических реакций. АцетилКоА служит исходным продуктом для синтеза жирных кислот, для некоторых гормонов, терпенов, изопреноидов и стероидов.
включение ацетилКоА в цикл Кребса путем присоединения его к щавелевоуксусной кислоте (четырехуглеродному соединению, дикарбоновой кислоте), в результате чего образуется лимонная кислота (шестиуглеродное соединение, трикарбоновая кислота). После образования лимонной кислоты через ряд промежуточных соединений происходит образование щавелевоуксусной кислоты, при этом выделяется две молекулы СО2 и 8 Н+.
Физиологический смысл цикла Кребса состоит в том, что именно здесь происходит разложение органического вещества (уксусной кислоты) до неорганических веществ (углекислого газа и ионов водорода), при этом образуется большое количество энергии в виде молекул АТФ.
Цикл Кребса происходит в матриксе митохондрий.
Через образование пировиноградной кислоты и ряда других органических кислот в процесс дыхания поступают также продукты разложения белков - аминокислоты. При этом углеродные скелеты аминокислот подвергаются окислительному расщеплению на фрагменты. Аминогруппы большинства аминокислот переносятся в различных реакциях трансаминирования на пировиноградную, щавелевоуксусную или a-кетоглутаровую кислоты. В конечном счете a-кетоглутаровая кислота превращается при этом в глутаминовую кислоту. Такие аминокислоты как аланин, цистеин, глицин, серин и треонин образуют ацетил-Коа через пировиноградную кислоту, а лейцин, лизин, фенилаланин, тирозин и триптофан образуют ацетилКоА через ацетоацетилКоА. Пролин, гистидин, аргинин, глутамин и клутаминовая кислота включаются в цикл Кребса через a-кетоглутаровую кислоту, метионин, изолейцин и валин - через янтарную кислоту, фенилаланин и тирозин - через фумаровую кислоту, аспарагин и аспарагиновая кислота - через щавелевоуксусную кислоту.
Глиоксилатный цикл.
У многих растений, синтезирующих в качестве запасных веществ жиры, происходит дополнительный к циклу Кребса глиоксилатный цикл.
В этом процессе жирные кислоты сначала активируются в наружной митохондриальной мембране путем этерификации с образованием коферментА-эфиров. Эти эфиры превращаются затем в эфиры карнитина, которые могут проходить сквозь внутреннюю митохондриальную мембрану и попадать в матрикс, где снова превращаются в КоА-эфиры. Последовательное отщепление молекул ацетилКоА от КоА-эфиров жирных кислот называется b-окислением.
В глиоксилатном цикле ацетилКоА, также как и в цикле Кребса, вступает в реакцию с щавелевоуксусной кислотой, образуя лимонную кислоту, но в цепи дальнейших превращений разлагается на четырехуглеродное соединение (янтарную кислоту), которая уходит в цикл Кребса, и глиоксилевую кислоту, которая, соединяясь со второй молекулой ацетилКоА, образующегося при b-окислении жирной кислоты, превращается в щавелевоуксусную кислоту.
Физиологический смысл глиоксилатного цикла состоят в дополнительном пути разложения жиров и образовании ряда разнообразных промежуточных соединений, играющих важную роль в биохимических реакциях.
Цепь дыхательных ферментов.
Продукты разложения уксусной кислоты, образующиеся в матриксе митохондрий, в дальнейшем преобразуются различными путями. Углекислый газ перемещается в виде бикарбонат-иона в цитоплазму, где либо выделяется, либо вступает в другие биохимические процессы. Ионы водорода перемещаются в помощью дыхательных ферментов на кристы митохондрии, где постепенно переносятся на акцептор - молекулярный кислород.
Этот процесс переноса и является третьим этапом дыхания, осуществляется цепью специфических ферментов, в состав которых входят, в основном, гемсодержащие белки. Это цитохромы и флавинсодержащие ферменты, в состав которых входит железо, легко переходящее из окисленной формы (Fe3+) в закисную (Fe2+). Перенос электронов по цепи ферментов проходит по мере убывания окислительно-восстановительного потенциала, поэтому не происходит неэффективного выброса энергии, которая по мере перехода с одного фермента на другой запасается в виде АТФ (при фосфорилировании АДФ). Конечной стадией этого этапа является перенос ионов водорода на молекулярный кислород и образование второго конечного продукта дыхания - воды.
Физиологический смысл цепи дыхательных ферментов состоит в постепенном транспорте электронов, что позволяет клетке запасти максимально много молекул АТФ, то есть энергии.
Процессы, происходящие на третьем этапе дыхания, были теоретически обоснованы Митчеллом в 1961 году. Предлагаемая им хемиоосмотическая гипотеза основана на том, что энергия окисления субстрата (АН2) используется для образования электрохимического потенциала ионов водорода по обе стороны внутренней мембраны митохондрий и на векторном перемещении электронов через мембрану как движущей силе в реакции энергетического сопряжения.
Согласно гипотезе Митчелла дыхание и фосфорилирование связаны между собой через посредство электрохимического потенциала и ионов водорода на митохондриальной мембране. Функционирование дыхательной цепи, локализованной во внутренней митохондриальной мембране приводит к накоплению ионов водорода по одну сторону мембраны и образованию ионов гидроксила по другую. При этом снаружи остаются два иона водорода и окисленный субстрат, а на внутреннюю сторону передаются два электрона по дыхательной цепи, встроенной в толщу мембраны, соответствующему акцептору водорода, который затем присоединяет два иона водорода из водной фазы митохондриального матрикса. Ионы водорода сообщают внешней поверхности мембраны положительный заряд, а электроны, перенесенные на внутреннюю поверхность, заряжают ее отрицательно. В результате между двумя поверхностями мембраны возникает разность потенциалов. передвижение протонов водорода с наружной стороны мембраны к внутренней рассматривается как процесс, сопряженный с присоединением остатков фосфата к АДФ и образованием АТФ.
Кроме электрического поля мембрана имеет градиент концентрации ионов фодорода. Эти два градиента - электрический и концентрационный - и являются непосредственно источником энергии для синтеза АТФ: химическая энергия окисления энергия электрического поля и градиента концентрации энергия АТФ.
Хемиоосмотическая гипотеза объясняет необходимость мембран (крист митохондрий) и механизм действия веществ - разобщителей окисления и фосфорилирования.
Эти разобщители служат переносчиками протонов через мембрану. При этом перенос их осуществляется на той стороне мембраны, где дыхание создает избыток ионов водорода, затем происходит их диффузия через мембрану и освобождение
ионов водорода в противоположном отсеке, где ионы водорода в дефиците. Процесс осуществляется в виде двух реакций.
Реакция 1 - это окисление субстрата АН2 ферментом - акцептором электронов (на внешней поверхности мембраны), в результате чего электроны присоединяются к ферменту, а протоны перемещаются в воду. Затем электроны переносятся на внутреннюю сторону мембраны и там восстанавливают акцептор водорода В (чаще всего кислород). Этот акцептор связывает ионы водорода справа от мембраны, превращаясь в ВН2.
Реакция П - это отщепление двух ионов водорода и фосфата от АДФ с правой стороны мембраны, что компенсирует потерю двух ионов водорода при восстановлении акциптора В. Один из атомов кислорода фосфата переносится на внешнюю сторону мембраны и, соединяясь с двумя ионами водорода с этой стороны, образует воду (Н2О). Остаток фосфата, присоединяясь к АДФ, образует АТФ.
Строение и функции митохондрии и дыхательных ферментов. Энергетика процесса дыхания.
Митохондрия является одним из важнейших органоидов любой эукариотической клетки. Она, возможно, образовалась в результате деградирования прокариотной клетки при образовании либо симбиотических, либо паразитических отношений при формировании первых эукариотических форм. Митохондрия окружена двойной мембраной, внутри в матриксе имеются многочисленные выросты внутренней мембраны, которые называются кристами. В матриксе помимо белков, включающих многочисленные ферменты, катализирующие биохимические реакции цикла Кребса, глиоксилатного цикла, дыхательной цепи, имеются и молекулы РНК и фрагменты молекул ДНК, управляющие синтезом этих белков. Наружная мембрана метихондрий проницаема для малых молекул и ионов, что и позволяет легко проникать в митохондрию пировиноградной кислоте (основному продукту гликолиза) и столь же легко удаляться углекислому газу в ионной форме.
Расположенные на кристах ферменты относятся к оксидоредуктазам, так как обеспечивают окислительно-восстановительные реакции в процессе переноса электронов сквозь мембраны. Эти ферменты делятся на две большие группы:
дегидрогеназы,
оксидазы.
Дегидрогеназы по характеру действия также делятся на две группы:
аэробные,
анаэробные.
К аэробным дегидрогеназам относятся двухкомпонентные ферменты, содержащие кофермент (простетическую группу) рибофлавин (производное витамина В2). Именно ферменты этой группы переносят водород непосредственно на О2. Донорами электронов для аэробных дегидрогеназ служат анаэробные дегидрогеназы, а акцепторами - цитохромы и кислород.
К анаэробным дегидрогеназам относятся пиридиновые дегидрогеназы, способные к гидрированию и дегидрированию пиридиновых ядер. Коферментами пиридиновых дегидрогеназ являются НАД (никотинамидадениндинуклеотид) и НАДФ (никотинамидадениндинуклеотидфосфат). Анаэробные дегидрогеназы переносят водород на какой-либо акцептор водорода по схеме:
АН2 + дегидрогеназа + В (акцептор) = А + ВН2
При этом акцептором водорода может быть и другая дегидрогеназа.
Оксидазы активируют молекулярный кислород и придают ему способность восстанавливаться до перекиси водорода. Они действуют на конечном этапе дыхания, когда водород окисляемого вещества необходимо выделять из системы. Процесс был подробно изучен видным им биохимиком В.И. Палладиным в 40-ых годах 20 века. Реакция происходит следующим образом:
АН2+О2 = А + Н2О2
Н2О2 = Н2О + О
Группа оксидаз многочисленна, основная роль принадлежит оксидазам, содержащим медь (полифенолоксидазы, аскорбатоксидаза) и железо (цитохромы, каталаза, пероксидаза).
Полифенолоксидазы в присутствии молекулярного кислорода окисляют полифенолы в хиноны. Процесс идет только в неповрежденных клетках. Если же клетки повреждаются, то вместо восстановления хинонов образуются темноокрашенные пигменты, что в обиходе можно наблюдать при разрезании плодов (разрезанное яблоко или картофель быстро темнеют, что является следствием нарушения реакции восстановления хинонов).
Цитохромы делятся на четыре группы в зависимости от формы входящего в состав молекулы гемогруппы:
цитохромы а, содержащие железоформилпорфирин,
цитохромы b. содержащие железопротопорфирин,
цитохромы с, содержащие замещенный железомезопорфирин,
цитохромы d, содержащие железодигидропорфирин.
Каталитическая роль железа заключается в его способности к окислению и восстановлению путем отдачи и присоединения электрона. Железо в цитохроме легко переходит из двухвалентного в трехвалентное, что соответствует окислению, и, наоборот, что соответствует восстановлению. Обратимое окисление и восстановление цитохромов связано с изменением валентности железа в коферменте. Цитохромы являются переносчиками электронов, а цитохромоксидаза играет роль последнего звена, которое способствует их переносу на кислород воздуха.
Особенно важными компонентами ферментных систем являются ферменты каталаза и пероксидаза.
Каталаза - один из ферментов, простетическая группа которых представлена порфирином железа. Процесс разрушения перекиси водорода под действием каталазы описывается следующими уравнениями:
4{Fe+++каталаза} + 2 Н2О2 = 4{Fe++каталаза} + 4Н+ + 2 О2
4{Fe++каталаза} + 2 Н2О2 = 4{Fe+++каталаза } + 2 Н2О
Итог реакции: 2 Н2О2 = О2 + 2 Н2О
Пероксидаза с помощью перекиси водорода может окислять различные соединения, например полифенол в хинон.
В итоге процесса дыхания образуется при разложении одной молекулы глюкозы при условии прохождения трех основных этапов (гликолиза, цикла Кребса, цепи дыхательных ферментов) в стандартных условиях (температура 25 оС, давление 1 Па и концентрация реагирующих веществ 1 М) 38 молекул АТФ или 686 ккал или 2872 кДж. Энергетический выход в процессе дыхания по этапам составляет:
при гликолизе 2 молекулы АТФ,
в цикле Кребса - 12 молекул АТФ,
в цепи дыхательных ферментов - 24 молекулы АТФ.
Влияние условий окружающей среды на дыхание растений.
Основными количественными показателями процесса дыхания являются интенсивность дыхания и дыхательный коэффициент.
Интенсивность дыхания - это количество углекислого газа, выделяемое единицей площади листовой поверхности в единицу времени.
Дыхательным коэффициентом называется отношение количества выделившегося углекислого газа к количеству поглощенного кислорода. Дыхательный коэффициент обозначается буквами RQ и величина его колеблется в зависимости от природы субстрата, использующегося для дыхания, то есть от соотношения углекислого газа, выделяющего при окислении субстрата и кислорода, затрачиваемого на окисление субстрата.
Если субстратом служат сахара, то
RQ = 1 (6/6=1), (С6 Н12 О6 + 6О2 = 6 Н2О + 6СО2).
Если субстратом служат липиды, белки и другие соединения с высокой степенью восстановления, то
![]() RQ < 1 (18/26=0,7)
RQ < 1 (18/26=0,7)
(С18 Н36 О2 (стеариновая кислота) + 26О2 = 8 Н2О + 18СО2).
Если субстратом служат вещества с низкой степенью восстановления, например органические кислоты, то
RQ > 1 (4/2,5=1,6)
(С4 Н4О5 (щавелевоуксусная кислота) + 2,5О2 = 2 Н2О + 4СО2).
Методы определения дыхательного коэффициента основываются на количественном учете поглощенного кислорода и выделенного углекислого газа. Для измерения дыхательного коэффициента используют прибор респирометр Варбурга.
Наиболее интенсивно дышат молодые, быстрорастущие части растений с большим количеством эмбриональных тканей (верхушка стебля, кончики корешков, прорастающие семена).
При интенсивном дыхании и незначительном фотосинтезе у проростков в сутки теряется до 1% массы, у старых же растений, интенсивность дыхания которых невелика потеря массы составляет в 10-20 раз меньше. Интенсивность дыхания значительно варьирует в зависимости:
от вида растений (например, пшеница дышит в 3-5 раз интенсивнее бобовых культур, теневыносливые растения дышат менее активно, чем светолюбивые формы);
от органа растения (интенсивнее дышат периферические ткани, что связано с лучшим снабжением их кислородом; у древесных растений наиболее интенсивно дышит камбий, а минимальная интенсивность дыхания характерна для древесины. Высокая интенсивность дыхания клеток камбия связана с высоким содержанием в этой ткани белковых веществ);
от климатического пояса (северные формы дышат интенсивнее южных при пониженных температурах, а при высоких температурах - наоборот).
В процессе вегетации на интенсивность дыхания влияют температура, влажность, минеральное питание, свет, газовый состав среды, физиологически активные вещества и ингибиторы.
Температура.
Интенсивность дыхания увеличивается с повышением температуры (до жизненного предела). Минимум, оптимум и максимум интенсивности дыхания при различных температурах не остаются постоянными у растения и зависят прежде всего от фаз-0ы его развития, органа и физиологического состояния как органа, так и растения в целом.
Влажность.
Интенсивность дыхания определяется содержанием воды в тканях. С повышением содержания воды интенсивность дыхания возрастает. Это положение справедливо для семян и проростков. Напротив, у вегетирующих растений недостаточное водоснабжение стимулирует интенсивность дыхания, при этом растения переходят на анаэробное дыхание с интенсивным выделением углекислого газа, что свидетельствует о депрессии фотосинтеза и активации процесса дыхания. Недостаточное водоснабжение в течение длительного периода вызывает переход растений на обмен веществ с отрицательным дыхательно-ассимиляционным комплексом, что приводит к снижению урожайности.
Минеральное питание.
Разные элементы влияют на интенсивность дыхания неоднозначно. Например, недостаток калия приводит к повышению интенсивности дыхания (в результате сдвига в азотном обмене), избыток азота при нитратном питании снижает интенсивность дыхания, а при аммиачном питании - наоборот повышает его. Интенсивность дыхания обусловлена биосинтезом различных ферментов для формирования которых нужны как макро, так и микроэлементы, особенно такие, как медь, железо, марганец, молибден. Недостаточное минеральное питание может привести к нарушению структуры митохондрий и вызвать нарушение окислительного фосфорилирования и разобщение его с дыханием.
Свет.
В зависимости от вида растений дыхание может происходить и в темноте, и на свету. Например, пшеница поглощает углекислый газ и на свету, и в темноте, а горох - только на свету. Восстановительная активность тканей возрастает в течение дня и снижается ночью, а кислотность в листьях уменьшается днем и увеличивается ночью. У растений короткого дня поглощение углекислого газа постепенно возрастает в темноте и усиливается его выделение на свету. В условиях короткого дня происходит адаптированный синтез ферментных систем, которые катализируют реакции поглощения углекислого газа в темноте.
Темновое дыхание состоит из двух компонентов:
дыхания роста (Rq),
дыхания поддержания структур (Rm).
Затраты на дыхание поддержания структур составляют до 0,2 г углерода на 1 г углерода в растении. Расходы на этот тип дыхания пропорциональны фитомассе и резко возрастают к концу вегетации.
На дыхание роста расходуется до 17% усвоенного за день фотосинтеза углекислого газа.
Газовый состав среды.
При повышении концентрации кислорода в атмосфере интенсивность дыхания возрастает, а при повышении углекислого газа - уменьшается. При недостатке кислорода преобладают анаэробные процессы и гликолитический путь превращения глюкозы, в частности вмещение к процессу спиртового брожения, при избытке кислорода преобладает пентозофосфатный цикл превращения глюкозы.
Физиологически активные вещества и ингибиторы.
Различные стимуляторы роста: ауксины (ИУК, НУК) и гиббереллины - стимулируют общий уровень активности дыхания за счет усиления пентозофосфатного пути.
Ингибиторы (например, динитрофенол, гидразид малеиновой кислоты, фенилмеркурхлорид) значительно снижают интенсивность дыхания за счет изменения активности ферментных систем. Эта особенность используется при обработке посевов ингибиторами роста за 2-3 недели до уборки, для снижения потерь накопленных углеводов, ингибирования биохимических процессов.
Связь между дыханием растений и их урожайностью.
В конечном счете урожай растений определяет соотношение фотосинтеза и дыхания, при этом используется основная формула:
М+м= fРТ -аР1Т1,где М - сухая масса всего растения (без азота и золы) за весь период вегетации, м - масса опавших за время вегетации частей растения, f - интенсивность фотосинтеза, а - интенсивность дыхания, Р - фотосинтезирующая площадь, Р1 - масса растения, Т - длительность фотосинтетической деятельности растения, Т1 - время дыхания растения.
Оценка эффективность накопления растением биомассы определяется рядом показателей: суточным приростом биомассы растения, коэффициентом эффективности роста, соотношением фотосинтеза и дыхания.
Суточный прирост биомассы растения определяется по формуле:
∆ W = Pg - Rt,
где Pg - брутто-фотосинтез целого растения (количество поглощенного углекислого газа) и Rt - дыхание целого растения за сутки.
Если расход на дыхание относят к единице биомассы растения, то получают удельное дыхание (УД, г СН2О/г. сутки).
Коэффициент эффективности роста (КЭР) в результате дыхание варьирует в зависимости от вида растения от 0,3 до 0,8. Чем выше КЭР, тем ниже эффективность превращения субстрата в структурную биомассу. Чем выше содержание белка и липидов в биомассе и чем больше глюкозы используется для восстановления нитратов, тем ниже коэффициент эффективности роста.
Основной показатель накопления биомассы - это соотношение фотосинтеза и дыхания, которое высчитывается по формуле:
Rt / Pg
Это соотношение составляет 30-60%, что позволяет судить об эффективности продуцирования биомассы, и выявить, насколько сельскохозяйственные культуры и сорта экономно используют ассимиляты на дыхание. При этом в стрессовых ситуациях фотосинтез подавляется быстрее, чем дыхание.
Регулирование дыхания сельскохозяйственных продуктов при хранении.
В практике сельского хозяйства особенно важным является вопрос регуляции того или иного физиологического процесса. В открытом грунте регуляц3ия процесса дыхания практически невозможна. Однако в защищенном грунте и в условиях хранилищ, где происходит хранение разного рода сельскохозяйственных продуктов такая регуляция вполне возможна.
Наиболее широко распространенным и важным приемом регуляции дыхания является регуляция состава газовой среды. Так, увеличение концентрации углекислого газа в атмосфере ведет не только к увеличению интенсивности фотосинтеза, но и, автоматически, к уменьшению интенсивности процесса дыхания, что, безусловно, способствует повышению урожая культур в защищенном грунте.
Особенно важным процессом в практике сельского хозяйства является процесс сохранения семян, плодов, корнеплодов, клубней как семенного, так и продовольственного назначения. Сохранность указанной продукции обеспечивается соблюдением определенного режима влажности и температуры, а также газового состава среды и использованием ряда регуляторов роста. При этом все физиологические процессы внутри семян, корнеплодов, клубней, плодов снижаются до минимума, что и обеспечивает долгий период их сохранности. Очень важным моментом является закладка на хранение хорошо вызревших плодов, корнеплодов, клубней, семян. Недозрелые органы при дыхании переходят на систему анаэробного разложения органических веществ, накапливают этиловый спирт, ацетальдегид, поэтому их вкус значительно ухудшается и хранятся они хуже, быстрее заболевают, теряют нужные качества: всхожесть, способность к прорастанию.
Регуляция дыхания семян:
влажность 14-15% для семян злаковых и бобовых культур, 8-9% - для семян масличных культур,
температура - 10-20 оС.
Регуляция дыхания плодов:
влажность 80-95%,
температура - 0 - 7оС.
использование специальных газовых смесей в хранилищах с высоким содержанием углекислого газа,
использование ингибиторов роста (этилена и абсцизовой кислоты), как в составе газовой смеси, так и путем обработки хранящихся плодов.
Тема "Минеральное питание"
Дополнительная литература по теме:
Вопросы к теме:
Условия поглощения растениями минеральных элементов.
Системы классификаций элементов в растении.
Характеристика физиологической роли основных минеральных элементов.
Характеристика взаимоотношений элементов в растворах.
Особенности поглощения растениями элементов из почвенного раствора.
Корень как орган поглощения минеральных элементов.
Количественные показатели поглощения минеральных элементов.
Особенности поглощения отдельных элементов у различных сельскохозяйственных культур.
Роль растений в круговороте азота в природе.
Диагностика различных видов минерального голодания и меры борьбы с ними.
Влияние условий внешней среды на поглощение минеральных элементов.
Роль минерального питания в формировании урожая и регулировании роста и развития растений.
Условия поглощения растениями минеральных элементов.
Поглощение воды и минеральных веществ растением непосредственно не связано друг с другом. Поглощение воды протопластом основывается на гидрофильности биоколлоидов, а поглощение ионов - на образовании лабильных соединений с макромолекулами протоплазмы. Поэтому поглощение воды не может вызвать поглощения солей, а поглощение ионов может вызвать изменения в оводненности протоплазматических структур и повлечь за собой поглощение воды.
Определяющим условием поглощения растениями минеральных элементов является поглощающая способность почвы. Вопросы поглощения почвой различных ионов были изучены русским ученым Гедройцем. Согласно его теории катионы в коллоидах почвы способны обмениваться с катионами почвенного раствора. Эти катионы называются поглощенными или обменными, а общее их количество на 100 г почвы (в мг/экв) называется емкостью поглощения или емкостью обмена. Адсорбция и удерживание растворимых веществ - это свойство почвы, которое называется поглощающей способностью. Эта способность определяется коллоидной частью почвы, которая называется почвенным поглощающим комплексом. От состава обменных катионов зависят свойства почвы.
Различают пять видов поглощения веществ почвой:
механическая поглощающая способность (при этом почва выступает в качестве фильтра для грубых суспензий),
физическая поглощающая способность (при этом происходит либо положительная адсорбция катионов на поверхность твердых частиц, либо отрицательная фильтрация анионов,
физико-химическая поглощающая способность (при этом происходит адсорбция и обменные химические реакции между почвенным раствором и почвенными частицами, что играет существенную роль в создании плодородия почв),
химическая поглощающая способность (при этом происходит превращение веществ в трудно растворимые соединения, например, при внесении фосфорных удобрений в почву, богатую ионами кальция, образуется нерастворимый фосфат кальция,
биологическая поглощающая способность (при этом происходит иммобилизация минеральных веществ под влиянием деятельности микрофлоры почвы).
Благодаря поглощающей способности почвы минеральные элементы не вымываются из почвы, сохраняются в почвенном растворе и доступны растениям.
Минеральные вещества поглощаются из почвы одновременно с поглощением воды и транспортируются в восходящем направлении преимущественно по ксилеме. Минеральные вещества обычно накапливаются в тех клетках, где в них возникает необходимость.
Для удовлетворения потребности растений в соответствующем количестве минеральных веществ, необходимых для роста и развития, должно быть соблюдено несколько условий:
минералы должны содержаться в почве в форме, доступной для их поглощения клетками корня, т.е. они должны находиться в почвенном растворе,
почва должна хорошо аэрироваться, чтобы в клетках корня могло происходить окислительное фосфорилирование (дыхание), поскольку поглощение минеральных веществ требует непрерывного снабжения энергией за счет АТФ,
должна эффективно функционировать транспортная система по доставке минеральных веществ к потребляющим клеткам.
На разных этапах развития растительного организма питательные вещества потребляются ими с различной интенсивностью, неодинакова также скорость поступления различных соединений у разных видов растений.
Отрицательное действие высоких концентраций питательных солей в почве проявляется в основном на первых этапах жизни растения, особенно в момент прорастания семени, поэтому повышенное содержание минеральных элементов в почвенном растворе часто снижает всхожесть и энергию прорастания семян. В связи с этим важно обеспечить необходимый уровень влаги в почве и регулировать уровень минеральных удобрений непосредственно в послепосевной период.
Недопустимо однократное внесение всей рекомендованной дозы минеральных удобрений в период посева, поскольку это снижает эффективность усвоения азотных удобрений и вызывает превышение допустимых концентраций других элементов в почвенном растворе.
Системы классификаций элементов в растении.
Растение поглощает углекислый газ и кислород из атмосферы, а воду и другие минеральные элементы - из почвенного раствора. Все минеральные элементы за исключением азота происходят в конечном счете из материнской породы, из которой образуется почва и при сгорании остаются в золе, почему и называются зольными элементами. Азот же, находясь в атмосфере, переводится в форму, доступную для автотрофов при синтезе белка, азотфиксирующими микроорганизмами, находящимися в почве, и в результате их метаболизма поступает в виде аммиачных и нитратных ионов в почвенный раствор.
Минеральные вещества составляют всего от 1 до 15% живой материи. Количество золы в различных частях растения, а также в разных растениях неодинаково. Состав зольных элементов также весьма вариабелен в зависимости от органа растения. Например, калия в семенах зерновых культур почти в два раза больше, чем в листьях и стеблях. В стеблях и листьях пшеницы и кукурузы отмечено большое количество кремния.
Как правило, распределение зольных элементов в разных органах растения соответствует следующей таблице:
| Наименование органа растения | Содержание зольных элементов,% |
| древесина | 1 |
| семена | 3 |
| корни, стебли | 4-5 |
| листья | 10-15 |
Содержание зольных элементов в растительных тканях зависит от типа и влажности почвы и от фазы развития растений.
Принято делить минеральные элементы, входящие в состав растительных клеток, на группы, причем используются в основном две системы классификации элементов.
В основу первой системы классификации положен критерий количественного содержания элементов в растении:
макроэлементы (составляют от 10 до 0,01% в клетке) (органогены - О, Н, С, N, P и минералы - Si, K, Ca, S, Mg, Na, Al),
микроэлементы (составляют от 0,001 до 0,00001%) - Mn, B, St, Cu, Zn, Br, F, Sn, Ni, Ti, Rb, Fe, Ba, Mo, Co, Cl, I,
ультрамикроэлементы (составляют 10-6-10-12%) - As, Ge, Pb, Au, Ra, Hg, Ag, Li.
Вторая система классификации основывается на роли минеральных элементов в живой клетке:
основные компоненты органического вещества - C, H, O, N, P, S,
элементы, участвующие в осмотической регуляции, балансе электронов, и определяющие проницаемость мембран - K, Mg, Ca, Mn, Cl,
элементы, входящие в ферментные системы, - Cu, Zn, Mo, Fe. Эти элементы часто поглощаются в форме хелатов, находятся в протопласте и способны вытеснять друг друга при избытке какого-либо из них в следующем порядке Cu >Zn > Mo > Fe.
элементы, токсичные для высших растений - F, I, Ni, Cr, Pb, Cd.
Ряд элементов, весьма важных в малых концентрациях, при накоплении в избыточном количестве могут быть токсичными для растений, например Mn, Cu, Fe, B.
Для определения роли того или иного элемента в питании растений проводят специальные опыты с использованием водных или песчаных культур, других специализированных методик.
Характеристика физиологической роли основных минеральных элементов.
К основным минеральным элементам, входящим в любую живую клетку, в том числе и в растительную, и играющим существенную роль в метаболизме клетки, относятся N, P, S, K, Mg, Ca, Mn, Cl, Cu, Zn, Mo, Fe, В.
Каждый из этих элементов имеет свое назначение, входит в определенные группы органических соединений и влияет на прохождение определенных физиологических процессов и биохимических реакций.
Азот (N) является наряду с С, О, Н, основным органогеном, входит в состав аминокислот, азотистых оснований, пигментов, а значит и в состав белков, нуклеиновых кислот, липидов. Это элемент, который влияет на количество строительных компонентов клетки, мембран, пигментов. Его недостаток будет ограничивать количество синтезирующихся белков, нуклеотидов, транспортных, информационных РНК, хлорофиллов, каротиноидов. Этот элемент является определяющим в физиологических процессах биосинтеза белка, фотосинтеза, роста вегетативных органов.
Фосфор (Р) также является элементом, относящимся к основным органогенам клетки. Этот элемент входит в состав нуклеотидов, фосфолипидов, ауксинов, а значит в состав нуклеиновых кислот, макроэргических соединений, мембран, гормонов. Этот элемент является очень важным в обеспечении таких физиологических процессов, как дыхание, фотосинтез, развитие генеративных органов.
Сера (S) является компонентом серосодержащих аминокислот (цистеин, цистин, метионин), присутствует в глутатионе, который играет определенную роль в окислительно-восстановительных реакциях, благодаря своей способности к обратимому превращению из восстановленной (сульфгидрильной) формы (-SH-) в окисленную, или дисульфидную, форму (-S-S-), входит в кофермент А, в тиамин (витамин В1). Этот элемент также играет весьма важную роль в таких физиологических процессах, как биосинтез белка, дыхание.
Кальций (Са) включается в структуру срединной пластинки клеточной стенки, связывается с кислотными компонентами пектина и образует нерастворимую соль, что определяет плотность полужидкой структуры клеточной стенки. Кальций играет важную роль в регуляции избирательной проницаемости клеточных мембран, определяет механическую прочность клеточных стенок.
Магний (Mg) входит в молекулу хлорофилла, является кофактором ряда ферментов, обеспечивает стабильность нуклеиновых кислот. Магний участвует в процессе фотосинтеза, регуляции избирательной проницаемости клеточных мембран.
Калий (К) является осмотически активным элементом, находится чаще всего в виде неорганического катиона, входит в рад ферментов в качестве активатора. Калий участвует в регуляции тургора клетки, избирательной проницаемости клеточных мембран.
Хлор (Cl) в форме хлорид-аниона перемещается вместе с калием, обеспечивая электронейтральность клетки, входит в число активаторов ферментов, катализирующих фотосинтетическое фосфорилирование. Хлор участвует в регуляции тургора клетки, в процессе фотосинтеза.
Железо (Fe) входит в состав многих важных ферментов, таких как цитохромы, ферредоксины, пероксидаза, каталаза, нитратредуктаза. Железо играет значительную роль в осуществлении таких физиологических процессов, как фотосинтез, дыхание, восстановление нитратов.
Молибден (Мо) входит в состав ферментов, восстанавливающих азот как из нитратной формы, так и из молекулярной формы. Восстановление азота из молекулярной формы осуществляется ферментом нитрогеназой, синтезирующейся в организме симбионтов бобовых растений - бактерий рода Rizobium - обитающих на корнях бобовых растений. Восстановление азота из нитратной формы осуществляется ферментами из группы нитратредуктаз. Молибден играет существенную роль в процессе синтеза аминокислот, а, значит, и в процессе биосинтеза белка.
Медь (Сu) входит в состав оксидаз (тирозиназа, аскорбатоксидаза). Медь играет значительную роль в процессе дыхания.
Цинк (Zn) входит в состав карбоангидразы и участвует в качестве кофактора при синтезе индолилуксусной кислоты (гормона из группы ауксинов). Этот элемент играет существенную роль в процессе поддержания запасов углекислого газа в форме иона НСО3-, и в процессе формирования апексов побегов и корней.
Бор (В) входит в качестве кофактора в ряд ферментов. Этот элемент играет роль в таких физиологических процессах, как деление меристем, перемещение ассимилятов, прорастание пыльцы, фенольный обмен, образование клеточных стенок.
Характеристика взаимоотношений элементов в растворах.
Минеральные вещества, поглощаемые растением, находятся в природных условиях в растворенном состоянии в почвенном растворе. Они представлены, как правило, в ионной форме и вступают между собой во взаимоотношения, регулируемые рядом закономерностей. Так, компоненты смеси веществ в растворе могут взаимодействовать по одному из следующих механизмов;
аддитивное действие компонентов смеси (когда действие смеси равно сумме действия отдельных компонентов. Примером такого действия является осмотическое давление, которое у смеси солей равно сумме парциальных осмотических давлений солей, входящих в смесь),
синергическое действие компонентов смеси (когда смесь солей действует сильнее, чем каждая из солей в отдельности, то есть физиологический эффект солевой смеси превышает сумму эффектов компонентов смеси. Синергизм может быть как положительным (внесение смеси минеральных удобрений), так и отрицательным (смесь пестицидов может пагубно влиять на растения),
антагонистическое действие компонентов смеси (когда физиологическое воздействие смеси солей оказывается меньшим, чем действие каждой из солей в отдельности и чем сумма из действия. Типичным примером антагонизма является взаимодействие одновалентных и двухвалентных катионов в растворе, активное развитие жизни в морской воде.
Раствор смеси солей называется физиологически уравновешенным раствором, когда количество и соотношение ионов обеспечивают нормальный рост, развитие и высокую продуктивность растений. Особенно важным является составление физиологически уравновешенных растворов в практике сельского хозяйства при использовании гидропонных технологий выращивания растений. Определяющим моментом величины отношения концентраций катионов в уравновешенных растворах является их валентность. Чем выше валентность иона, тем ниже относительная концентрация данного катиона в уравновешенном растворе. Способность уравновешивать токсическое действие у ионов возрастает быстрее, чем валентность, поэтому для растений солевые растворы являются уравновешенными, если отношении концентрации одновалентных катионов к двухвалентным приблизительно равно 10:
Особенности поглощения растениями элементов из почвенного раствора.
Элементы, соединения которых подвижны, активно поглощаются на ранних этапах развития растений, они поступают со скоростью, превышающей накопление в растении сухих веществ. Элементы, дающие малоподвижные соединения, поглощаются пропорционально синтезу сухих веществ, а в ряде случаев часто отстают от скорости синтеза этих веществ.
Одним из факторов, определяющих ход поглощения веществ растением, является химическая природа соединений, в виде которых данный элемент находится в тканях растения. По этому признаку питательные вещества делят на две группы:
элементы, участвующие в построении мобильных соединений клетки. Эти элементы называют реутилизируемыми. К ним относятся азот, фосфор, калий и магний. При недостатке этих элементов в почве растение транспортирует их во вновь образуемые органы из нижних листьев, при этом нижние листья увядают и отмирают.
элементы, более прочно связанные с протоплазмой и менее подвижные, которые не используются вторично. Эти элементы называются нереутилизируемыми. К ним относятся бор, кальций, железо. При их недостатке в почве старые листья остаются долгое время жизнеспособными, но растение не образует новых органов, то есть не способно развиваться и расти.
Установлено, что концентрация реутилизируемых элементов в растении имеет акропетальный градиент содержания, а нереутилизируемых элементов - базипетальный градиент содержания.
В процессе поглощения минеральных элементов из почвы растение использует комплекс механизмов:
корневой перехват питательных веществ (поглощение питательных веществ из новых объемов почвенного раствора в процессе роста корней),
массовый поток ионов к поверхности корней с потоком воды при поглощении ее корнями растений,
диффузионный поток ионов по градиенту концентрации вещества от ризосферы к корню (ионофорные каналы).
Растения усваивают минеральные элементы через корневые волоски независимо от поглощения воды. Этот процесс обусловлен обменом ионов, выделяемых растениями при дыхании, на ионы почвенного раствора. При дыхании растений получается углекислота, которая в тканях образует катион Н+ и анион НСО3-. В процессе питания катион водорода обменивается на катионы почвенного раствора (калий, кальций, магний, ион аммония), а карбонатный анион - на анионы азотной, серной, фосфорной и других кислот. Поглощение ионов происходит из сильно разбавленных растворов, что определяет технологию внесения минеральных удобрений.
Растение всегда будет более активно поглощать ионы, содержащие азот, чем все другие ионы, поскольку азот относится к наиболее важным органогенным элементам и требуется в большем количестве, чем другие минеральные элементы. При таком избирательном поглощении растениями ионов будет происходить и изменение реакции почвенного раствора. В связи с этим все минеральные соли, используемые в качестве минеральных удобрений подразделяют на три группы:
физиологически кислые, которые в большей степени поглощаются растением в катионной части (например, (NH4) 2SO4),
физиологически щелочные, которые в большей степени поглощаются растением в анионной части (например, NaNO3),
физиологические нейтральные, которые поглощаются как в катионной, так и в анионной части с одинаковой скоростью (например, NH4NO3).
Поэтому при внесении удобрений в почву всегда необходимо учитывать характеристику свойств почвы на конкретном поле и подбирать соответствующие соли так, чтобы обеспечить растениям максимально благоприятные условия питания.
Корень как орган поглощения минеральных элементов.
Корень - один из основных вегетативных органов растения. К его функциям относятся:
прикрепление к субстрату,
поглощение воды,
поглощение минеральных веществ,
синтез органических веществ,
выделение продуктов обмена,
запасание питательных веществ.
Тонкая оболочка корневого волоска плотно склеивается с комочками почвы. Корневые волоски служат опорой для растущей верхушки корня, выполняют функцию поглощения воды и минеральных веществ из почвы. Длина корневого волоска - 0,6-10 мм, но общая длина волосков весьма значительна и может достигать в сумме 20 км. Волоски выделяют в почву различные вещества, растворяющие труднодоступные растению соединения в почве. Продолжительность жизни корневого волоска - 15-20 дней.
Функционально поглотительной тканью корня являются корневые волоски (у водных растений - ризодермис), а первичная ассимиляция ионов происходит в коре корня.
Корневая система поглощает из почвенного поглощающего комплекса через почвенный раствор все необходимые элементы, причем способна растворять и нерастворимые соединения за счет выделения органических кислот. Это явление подтверждается опытами с использованием мраморной пластинки в сосуде, на которой ясно образуется отпечаток корневой системы растения, растворяющей мрамор в местах соприкосновения с корневыми волосками. Лучшему усвоению минеральных веществ способствует внесение физиологически кислых солей (при этом происходит освобождение анионов из трудно растворимых соединений), например, внесение сульфата аммония в почвы высвобождает фосфорную кислоту из фосфоритов, а внесение натриевой селитры не производит такого действия.
Корневые выделения при бессменном возделывании одной культуры могут влиять на растения отрицательно, создавая неблагоприятную рН почвенного раствора. При этом происходит накопление вредной микрофлоры, возбудителей корневых гнилей, что приводит к увеличению степени поражаемости культуры болезнями.
Корневые выделения состоят из:
веществ, которые отчуждаются клетками в обмен на поглощаемые ионы питательных солей,
веществ, теряемых корнем вследствие выщелачивания наружным раствором и "вытягиваемых" их корня электростатическими силами,
веществ, которые освобождаются отмирающими клетками чехлика, эпидермиса и коры.
Корневая система растений - это и место синтеза многих важных органических соединений, таких как аминокислоты, алкалоиды, гормоны и ряд других веществ. О синтетической роли корневой системы свидетельствует факт прекращения жизнедеятельности срезанных растений, даже если их помещают в питательный раствор. Только если у срезанного побега образуются новые придаточные корни, рост растения возобновляется. В культуре in vitro рост корневой ткани неограничен, а культуру клеток из стебля получить не удается.
Количественные показатели поглощения минеральных элементов.
Между клетками корня могут существовать значительные электрические градиенты, которые возникают и исчезают, по-видимому, вследствие включения и выключения ионных насосов и изменения концентрационных градиентов в тканях корня.
Поглощенные ионы должны сначала пересечь плазмалемму, чтобы проникнуть в цитоплазму, а затем и в мембрану, окружающую вакуоль, или другую органеллу, чтобы попасть затем во внутренний компартмент цитоплазмы.
Ионы могут проникать через мембрану активно или пассивно, при этом они перемещаются благодаря своей кинетической энергии, не потребляя при этом энергию АТФ. Липидорастворимые молекулы проходят сквозь мембраны легко, многие неорганические ионы, не растворимые в липидах, проникают, по-видимому, через специальные водные белковые каналы в мембране, то есть используется механизм облегченной диффузии с участием пермеаз.
О скорости диффузии ионов сквозь мембрану судят по коэффициенту проницаемости Р.
Наибольшей скоростью диффузии обладает К+, поэтому значение Р для К+ принято за 1,0.
Существуют белки, способные образовывать каналы в мембранах для определенных ионов, их называют ионофорами. Ионофоры способны увеличивать скорость диффузии иона в миллион раз. Ряд специфических веществ, например, антибиотики (грамицидин), способны проникать именно через ионофоры, вызывая быструю гибель клетки.
Так как ионы заряжены, то скорость из диффузии определяется не только химическим потенциалом (концентрация ионов по обе стороны мембраны), но и электрическим потенциалом внешней и внутренней стороны мембраны. Обычно растительные клетки на внутренней стороне мембраны имеют отрицательный потенциал, поэтому катионы поглощаются в большей степени, чем анионы. Разность потенциалов внутри и снаружи клетки колеблется от 50 до 200 мВ. Эта разница в заряде сторон мембраны называется трансмембранным потенциалом.
Совокупность химического и электрического потенциала составляет электрохимический градиент, согласно которому и происходит диффузия ионов в клетку.
Когда транспорт осуществляется по электрохимическому градиенту ионы сначала присоединяются к особым участкам на мембране (пермеазам). Затем они проникают в клетку в соответствии с уравнением нернста, если общий эффект градиента их концентрации по обе стороны мембраны и электрический трансмембранный потенциал обеспечивают движущую силу, направленную внутрь.
Уравнение Нернста связывает электрический потенциал внутри клетки с распределением заряженных ионов:
Е = - 58/n. lgСi/Co,
где
Е - трансмембранный коэффициент, измеряемый в мВ, определяемый с использованием заземленного электрода вне клетки, n - валентность и заряд иона, Сi - концентрация (молярность) иона внутри клетки, Co - концентрация (молярность) иона вне клетки.
При перемещении ионов через ионофоры происходит транспорт ионов против электрохимического градиента благодаря использованию энергии АТФ. При этом происходит обмен одноименных ионов, например: в клетку перемещается поток К+, а из клетки - поток Н+, в клетку - поток NO3-, а из клетки - поток НСО3-.
Кроме того, существует еще диффузия нейтральных молекул, например, сахарозы, глюкозы, которые проникают обычно с ионами Н+. Этот процесс называется котранспортом и происходит при перемещении веществ в флоэму или из нее.
Трансмембранные потенциалы образуются двумя путями;
в результате диффузии анионов и катионов, движущихся сквозь мембрану с разными скоростями,
благодаря электрогенному транспорту с прямым использованием энергии для прокачивания протонов, анионов или катионов через0 мембрану против их электрохимических градиентов.
Оба этих процесса всегда действуют таким образом, что внутри клетки создается более отрицательный заряд по сравнению с зарядом вне ее.
Поглощенные корневыми волосками ионы и молекулы вследствие движения протоплазмы постепенно переносятся на внутреннюю сторону клетки и поступают в клетки коры корня, затем в паренхиму, затем в ксилему. передвижение ионов и молекул от клетки к клетке может происходить и без воды, но по неживым элементам ксилемы ионы переносятся с током поступающей воды. Во время передвижения от клетки к клетке многие вещества метаболизируются и в ксилемный сок (пасоку) поступают уже в виде нужных растению соединений.
Особенности поглощения отдельных элементов у различных сельскохозяйственных культур.
Для растений, образующих корнеплоды и клубни на первом году жизни характерно растянутое поступление фосфора и калия. Более сжаты сроки поступления азота и магния. В сахарную свеклу азот, фосфор и калий поступают за 150-170 дней. Поглощение магния заканчивается у свеклы за 30-40 дней до конца вегетации.
Из злаковых культур наиболее растянут период поглощения питательных веществ у озимых хлебов. У озимой пшеницы и ржи содержание азота и калия достигает максимума после окончания цветения - в начале созревания зерна, а поступление фосфорной кислоты продолжается вплоть до достижения семенами полной спелости. Таким образом у озимых хлебов период поглощения питательных веществ длится 7 месяцев. У яровых хлебов активное поглощение питательных веществ крайне сжато во времени, например, у овса оно продолжается всего 40-55 дней.
Соотношение между генеративными и вегетативными органами в урожае у злаковых культур, число зерен, абсолютный вес зерен определяются в первую очередь степенью обеспеченности растений фосфатами к началу дифференциации колосовых бугорков. При недостатке фосфора в этот период продуктивность растения снижается и уже никакое обильное снабжение злаков фосфором после выброса колоса не может исправить положение. Поэтому столь важно обеспечить растения нужным элементов в соответствующую фазу развития.
У бобовых культур период поглощения питательных веществ вдвое превышает таковой у яровых хлебов, особенно растянуто поступление фосфора, так как у этих культур период цветения и плодообразования сильно растянут по времени.
Роль растений в круговороте азота в природе.
Среди органогенов азот занимает одно из важнейших мест. Без азота не могут синтезироваться белки, нуклеиновые кислоты, а следовательно, и протопласт живой клетки. На азот приходится всего около 3% сухого вещества, но без достаточного его количества в почве жизнедеятельность растений невозможна. Низкая урожайность многих сельскохозяйственных культур чаще всего определяется недостатком именно азота. Для формирования урожая зерна в 20-30 ц/га нужно внести 150-200 кг азота в доступной растениям форме, т.е. от 50 до 150 ц/га в виде азотных удобрений. Молекулярный азот воздуха растениям, как известно из курса микробиологии, недоступен. В почве азот содержится в виде органических и минеральных соединений. Минеральные соединения представлены аммиачными (аммонийными) и нитратными солями.
Основная масса азота в почве - это органический азот. Он представлен продуктами разложения органики (компостов, навоза, естественных растительных остатков) мочевиной, аминокислотами, гуминовыми кислотами, витаминами, ауксинами. Наиболее легко усваиваются растениями мочевина и аспарагиновая кислота, другие аминокислоты более трудноусвояемы для растений, так же как и гуминовые кислоты, ауксины, витамины, однако они поглощаются растениями с помощью специфических механизмов поглощения, например ионофорных каналов.
Наиболее легко усваиваются растениями неорганические формы азота. При этом процесс взаимопревращения аммиачных соединений в нитратные определяется процессом нитрификации, а интенсивность процесса регулируется деятельностью соответствующей группы микрофлоры в почве. Интенсивность нитрификации свидетельствует о том, что почвы имеют хорошую комковатую структуру, обеспечены кислородом, что определяет процесс нитрификации (окисление аммиака). В плохо аэрируемых почвах накапливаются аммонийные соли.
Корневая система растений поглощает достаточно интенсивно и аммиачные катионы, и нитратные анионы. Определяющим фактором в этом процессе является рН среды. В слабокислой среде лучше усваиваются нитраты, а при рН=7 - аммиачные соли. Для использования аммиачных солей необходимо достаточное количество углеводов в растениях, иначе их превращение в амиды задерживается, накапливается аммиак, действующий на растения токсично. Преимущественное поглощение аммиачных солей свойственно растениям, склонным к усиленному образованию органических кислот.
У бобовых растений, образующих бактериоризу с родом бактерий Rhizobium имеется специфический механизм узнавания вида бактерии. Процесс определяется наличием на поверхности корневых волосков белка лектина, который обеспечивает "узнавание" соответствующего вида бактерий. После проникновения бактерий внутрь корневых тканей в коре корня синтезируется повышенное количество ауксина, что приводит к активному разрастанию тканей корня вокруг проникших и размножившихся бактерий и к образованию клубенька.
В круговороте азота в природе растения активно участвуют в качестве автотрофов на стадии превращения аммиака в органические соединения и на стадии ассимиляционной денитрификации.
При этом, поглощая аммиак, как правило в виде иона аммония, растения осуществляют реакции синтеза через соединение аммиачного катиона с a-кетоглутаровой кислотой в цикле Кребса, в результате чего образуется глутаминовая кислота, а затем глутамин. Другие аминокислоты синтезируются в ходе реакций переаминирования. Азот транспортируется по растению от клеток корня в основном в форме глутаминовой кислоты, глутамина, аспарагиновой кислоты и аспарагина.
В процессе ассимиляционной денитрификации поглощенные корнем растения нитраты восстанавливаются до аммиака с помощью фермента нитратредуктазы. При этом, если необходимых для синтеза аминокислот углеводов не хватает, нитраты могут накапливаться в клетках растений.
Диагностика различных видов минерального голодания и меры борьбы с ними.
Наиважнейшим условием для благополучного развития растений является наличие комплекса минеральных веществ в почве. Недостаток какого-либо элемента приводит к голоданию растений, при этом признаки голодания зависят от той физиологической роли, которую играет элемент в растительной клетке. Определение по внешним симптомам, проявляющимся у растения, типа минерального голодания называется диагностикой и применяется в практической деятельности при выращивании сельскохозяйственных культур. Для каждого типа голодания характерны свои симптомы, при этом некоторые симптомы могут совпадать при различных типах голодания, например, "желтый цвет листьев", и в этом случае необходимо оценивать всю совокупность признаков, чтобы правильно диагностировать тип голодания.
Азотное голодание.
Наблюдается сначала бледно-зеленая окраска листьев, которая при длительном голодании переходит в желтую, за счет недостатка хлорофилла, листья приобретают желтый, оранжевый или красный цвет, может наблюдаться высыхание и отмирание ткани. Образуются мелкие листья и плоды, задерживается рост растения, ослабляется образование боковых побегов, у злаков - кущение.
Азот является реутилизируемым элементом, поэтому симптомы пожелтения проявляются прежде всего на нижних листьях.
Азотное голодание приводит к ускорению фаз развития растений и вызывает более раннее созревание плодов и семян, но влияет на общую урожайность, резко снижая ее.
Особенно часто признаки азотного голодания отмечаются ранней весной, когда запасы нитратов в почве вымываются в глубокие слои, а микробиологические процессы еще идут слабо и азота в почве недостаточно.
Иногда у сортов с высокой урожайностью, активно выносящих азот, отмечаются признаки азотного голодания, что свидетельствует о необходимости подкормки их азотными удобрениями. Для таких сортов необходимо делать соответствующие поправки при использовании типовой технологии возделывания.
Меры борьбы с азотным голоданием: проводят подкормку аммиачной селитрой по 0,5-1,5 ц/га или навозной жижей по 5-10 т/га. Навозную жижу лучше вносить растениепитателем, тогда ее разбавлять не нужно, при поверхностном внесении ее нужно разбавлять водой в 2-3 раза.
Фосфорное голодание.
При фосфорном голодании содержание сахаров в листе повышается, так как меньше образуется фосфорорганических соединений. Накопление сахаров способствует накоплению антоциановых пигментов. Красная и лиловая окраска этих пигментов вместе с зеленой окраской хлорофилла придает листьям голубоватый оттенок, а при большом количестве антоцианов - лиловую окраску. Такой темный цвет листьев, часто зрительно воспринимаемый как темно-зеленый, производит обманчивое впечатление здоровых растений. Однако у них отмечается задержка фаз развития, особенно цветения, плодообразования, резко ослабляется скорость роста, задерживается образование новых побегов, ослабевает кущение, в итоге сильно снижается урожай. Связано это с недостатком нуклеиновых кислот и макроэргических соединений.
Причиной фосфорного голодания может быть антагонизм между фосфатами, нитратами и хлоридами, поскольку в сухой почве доступность фосфора для растений снижается, а хлор-ионы и нитрат-ионы поступают с прежней скоростью.
Меры борьбы с фосфорным голоданием: проводят подкормку суперфосфатом в дозе 1-2 ц/га во время междурядных обработок. При недостатке влаги иногда достаточно провести полив, чтобы восстановить доступность фосфатов для растений. Под культуры, требовательные к фосфору (сахарная свекла, кукуруза) необходимо под вспашку с осени вносить навоз или фосфорные удобрения. Кислые почвы следует известковать, так как это тоже повышает доступность фосфора для растений.
Калийное голодание.
Поскольку калий определяет проницаемость мембран клетки, то его недостаток сказывается прежде всего на транспорте веществ через мембраны. Поэтому первым признаком калийного голодания у большинства видов является изменение окраски листьев на темно-зеленую с голубоватым оттенком, так как в них происходит повышенное накопление азотных соединений и интенсивно синтезируется хлорофилл. Однако, у бобовых культур листья наоборот светлеют, то есть снижается эффективность метаболизма клубеньковых бактерий и поступление азота из клубеньков в листья замедляется. При значительном избытке азотных соединений в листе происходит повышение концентрации аммиачных форм азота, что ведет к отмиранию тканей прежде всего по краям листа, а затем между жилками. Признак "краевого ожога" или "запала" листьев является наиболее характерным симптомом калийного голодания. Характерны также нарушения тургора, наблюдается вялость и свисание листьев.
При сухой, жаркой погоде в связи с резким обезвоживанием тканей возможно отставание эпидермиса и появление на поверхности листьев серебристо-белых пятен и полос. Калийное голодание обуславлитвае6т недостаточное развитие поддерживающих тканей и элементов древесины, уменьшение толщины клеточных стенок.
Стебли становятся непрочными, с короткими междоузлиями, наблюдается полегание растений или поникание соцветий (колосьев, корзинок и головок). При калийном голодании листья по отношению к стеблю кажутся длинными и крупными. Неравномерный рост клеток вызывает морщинистость и закручивание краев листьев вниз. У растений с параллельным жилкованием (семейство злаковых) листья приобретают волнистый вид, скручиваются.
Калий является реутилизируемым элементом, поэтому в начале голодания, он передвигается из нижних листьев в верхние. При дальнейшем голодании его признаки распространяются снизу вверх. При сильном калийном голодании снижается устойчивость растений к болезням и вредителям, вероятно в связи с ослаблением механических такней и накоплением не используемых в биосинтезе углеводов.
Жаркая, сухая погода ускоряет и усиливает проявление недостатка калия у растений. Преобладание в почвенном растворе катионов кальция и магния ослабляет поглощение растениями калия. Известкование и гипсование почв усиливает потребность растений в калии.
Меры борьбы с калийным голоданием: проводят подкормку такими веществами, как хлоридом калия в дозе 0,5-1 ц/га или калимагнезией в дозе 2-3 ц/га, или золой в дозе 5-10 ц/га, или навозной жижей в дозе 5-10 т/га.
Магниевое голодание.
Поскольку магний входит в состав хлорофилла и является реутилизируемым элементом, то прежде всего признаки голодания в виде пожелтения или "межжилкового хлороза" появляются на нижних листьях. Отток магния идет по жилкам, поэтому сами жилки сохраняют зеленую окраску. Последующий признак - некроз тканей между жилками. Магний весьма важен и при формировании семян, поэтому его недостаток сильнее влияет на урожай зерна, чем на урожай соломы. Во время цветения и образования семян происходит усиленный отток магния из вегетативных органов, поэтому при его недостатке цветение и созревание затягиваются. Магний участвует в виде кофактора ряда ферментов в синтезе углеводов, поэтому при его недостатке снижается содержание крахмала в картофеле и сахара в сахарной свекле.
Антагонистами магния выступают калий и натрий. Имеет значение и форма вносимых азотных удобрений. Так при использовании аммиачных солей действие недостатка магния усиливается, а применение нитратных форм азота способствует ослаблению признаков магниевого голодания.
Меры борьбы с магниевым голоданием: при раннем проявлении голодания проводят подкормку такими веществами, как калимагнезией в дозе 1-2 ц/га, или золой в дозе 3-6 ц/га, или сульфатом магния в дозе 1-2 ц/га, или каинитом в дозе 2-4 ц/га. Если магниевое голодание проявилось в поздней фазе развития растений, то необходимо внести магниевые удобрения на данном массиве перед вспашкой почвы, а на кислых почвах этот процесс нужно совмещать с известкованием. Внесение доломита под вспашку в дозе 10-15 ц/га обеспечивает растения магнием на 5-8 лет.
Кальциевое голодание.
Кальций входит в состав клеточных стенок, поэтому при его недостатке протопектин образуется в недостаточном количестве и стенки клеток и межклеточное вещество ослизняются. При недостатке кальция происходит побеление верхушек и молодых листьев, вновь образующиеся листья мелкие, искривленные, с неправильной формой краев. На этих листьях появляются пятна из отмерших тканей. При остром недостатке верхушечная почка отмирает.
У зерновых культур молодые листья слегка перекручиваются и засыхают. Позднее наблюдается засыхание кончиков и старых листьев. У растений с плодами, богатыми оксалатамии пектинами, признаки кальциевого голодания проявляются в усугублении течения таких поражений, как вершинная гниль томата и горькая ямчатость яблок.
При вершинной гнили, обычно проявляющейся при колебаниях влажности, применение калийных и магниевых удобрений ослабляют поглощение кальция и усугубляют заболевание.
Горькая ямчатость яблок вызывается недостатком кальция, при этом в мякоти плодов развиваются коричневые пятна, затем пятна появляются на кожице, при этом ухудшается вкус яблок и понижается их товарная ценность.
Меры борьбы с кальциевым голоданием: на кислых почвах используется прием известкования, т.е. внесение карбоната кальция, на нейтральных почвах рекомендуется вносить кальциевую селитру, фосфогипс, на щелочных почвах используют прием гипсования, т.е. внесение сульфата кальция.
Рекомендуется также при необходимости опрыскивание растений 0,5-1% раствором кальциевой селитры или хлорида кальция, особенно в период роста плодов томата прием можно использовать 1-2 раза в неделю, в период вегетации яблонь прием используют 3-6 раз за 1-2 месяца до уборки яблок.
Проявление недостатка железа.
Поскольку железо, нереутилизируемый элемент, входит в ферментные системы, определяющие прохождение процесса фотосинтеза и дыхания, то типичными симптомами являются хлороз и отмирание верхушечных листьев и побегов, при длительном голодании на краях листа и между жилками пожелтевших листьев появляются коричневые пятна, отдельные побеги отмирают.
Меры борьбы с железным голоданием: поскольку недостаток железа наблюдается, как правило, у плодовых культур, способных истощать естественные запасы железа в почве, то часто используют внекорневые подкормки в виде опрыскивания 0,5% раствором железного купороса 2-3 раза за вегетационный сезон. Рекомендуется осенью, одновременно с внесением перегноя, вносить железный купорос из расчета на 40-60 кг перегноя 1-1,5 кг железного купороса, вся смесь разбавляется 5-10 литрами воды и выливается в кольцевую траншею вокруг дерева.
При сильном проявлении хлороза в период вегетации можно ввести железо в ствол или в корень путем вбивания ржавого гвоздя.
Диагностика нарушений в питании бором.
Бор относится к числу элементов, чей недостаток или избыток одинаково неблагоприятен для растения и вызывает соответствующие нарушения метаболизма. Бор входит в качестве кофактора в ферментные системы, определяющие процессы роста, поэтому
при недостатке бора проявляются:
у свеклы - гниль сердечка, отмирание молодых листьев и точки роста,
у яблони - в мякоти плодов образуются зеленоватые пятна диаметром до 1 см, которые затем буреют и плоды приобретают уродливую форму,
у томата - почернение точки роста стебля, черешки листьев становятся ломкими, плоды приобретают уродливую форму и покрываются бурыми пятнами.
При избытке бора:
у огурцов - листья среднего и нижнего ярусов желтеют, заворачиваются вниз, принимая куполообразный вид, позднее края листьев отмирают,
у картофеля - края долек листа заворачиваются вверх, затем буреют и отмирают.
Меры борьбы с нарушениями в питании бором:
При борном голодании нужно вносить до 6 - кг/га борнодатолитового удобрения или осажденного бората магния (обязательно соблюдать равномерность обработки), можно проводить внекорневую подкормку растений либо борнодатолитовым удобрением (в дозе 10-12 кг/га, растворив их в 500-600 л воды), либо 1,5 кг борной кислоты, растворив ее в 1000 литрах воды.
При избытке бора достаточно обильно полить растения, что вызывает вымывание бора в нижние слои почвы.
Марганцевое голодание.
Недостаток марганца вызывает хлороз между жилками листа, у листа окраска становится узорчато-пестрой, при длительном голодании хлорозные участки отмирают.
Меры борьбы с марганцевым голоданием: используют подкормки сернокислым марганцем в дозе 50-100 кг/га, можно использовать внекорневую подкормку, которую можно сочетать с обработкой бордосской жидкостью, часто используемой при борьбе с болезнями растений, при этом на 500 л бордосской жидкости добавляют 1 кг сернокислого марганца - этот объем рабочего раствора используют на 1 га.
Медное голодание.
Этот вид физиологического расстройства характерен для торфяных и кислых песчаных почв, может усиливаться при жаркой погоде. В южных регионах практически не встречается, так как в технологиях возделывания культур используются в достаточном объеме пестициды, имеющие в своем составе медь, и этого количества вполне достаточно для снабжения растений этим микроэлементом. Недостаток меди вызывает хлороз листьев, потерю тургора, увядание, задержку стеблевания, слабое образование семян.
Меры борьбы с медным голоданием: используют подкормки сернокислой медью в дозе 10-30 кг/га, добавляют медный купорос при обработке семян в дозе 50-100 г на 1 центнер семян, проводят опрыскивание растений 0,05% раствором медного купороса.
Цинковое голодание.
Поскольку цинк входит в состав ферментов, определяющих синтез гормонов роста, в частности, ауксинов, то его недостаток вызывает образование на молодых побегах розеток мелких узких листьев и укороченных междоузлий, у молодых листьев отмечается бледная окраска.
Меры борьбы с цинковым голоданием: используют подкормки сернокислым цинком в дозе 20-40 кг/га, проводят опрыскивание плодовых культур 0,05% раствором сернокислого цинка, при обработке семян добавляют до 100 г сернокислого цинка на 1 центнер семян.
Молибденовое голодание.
Поскольку молибден необходим для восстановления нитратов в аминную группу, то его недостаток вызывает образование симптомы нехватки азота, нарушается и азотфиксация у бобовых растений, имеющих развитые эффективные клубеньки, у листьев прежде всего отмечается бледная окраска.
Меры борьбы с молибденовым голоданием: проводят внекорневые подкормки 0,01 - 0,05% раствором молибденовокислого аммония, при обработке семян добавляют до 30 г молибденовокислого аммония (растворив его в 2 литрах воды) на 1 центнер семян.
Избыток хлора.
При избытке хлора, встречающемся иногда при внесении весной в больших дозах хлорсодержащих удобрений (сильвинит, хлористый калий, хлористый аммоний), могут наблюдаться такие симптомы, как свертывание лодочкой долек листа (у картофеля, малины), преждевременное усыхание листьев.
Меры борьбы с избытком хлора: необходимо провести подкормку аммиачной селитрой в дозе 1-2 ц/га с последующим поливом, при этом поступление нитратного азота усиливает рост растений и вызывает перераспределение хлора на большую массу растительной ткани, снимая таким образом его отрицательное влияние.
Влияние условий внешней среды на
поглощение минеральных элементов.
На поглощение растением минеральных элементов влияют многие абиотические факторы. Особенно важными являются такие факторы, как концентрация питательного раствора, температура воздуха и почвы, относительная влажность воздуха, интенсивность освещения, реакция почвенного раствора.
Концентрация питательного раствора.
Почвенный раствор должен содержать достаточное количество питательных элементов для создания концентрационного градиента, так чтобы элементы могли поступать в корневые волоски по механизму пассивной или облегченной диффузии. Однако, чрезмерно высокая концентрация почвенного раствора может вызвать физиологическую засуху у растений и вызвать их гибель. Оптимальная концентрация почвенного раствора варьирует не только в зависимости от вида растения, но и от фазы развития растения.
Поскольку передвижение растворимых удобрений в горизонтальной плоскости в почве практически отсутствует, то определенная мозаичность распределения удобрений наблюдается всегда, поэтому особенно важно тщательно соблюдать технологию внесения удобрений для достижения максимально возможной равномерности их заделки.
Благодаря наличию мозаичности почвенного раствора корневая система растений в очагах с повышенной концентрацией почвенного раствора поглощает минеральные элементы, а в очагах с пониженной концентрацией - поглощает воду.
Оптимальная концентрация почвенного раствора для каждой культуры определяется опытным путем и находит отражение в рекомендуемых для каждой зоны и фазы развития растений дозах удобрений.
Температура воздуха и почвы.
Оптимальные температуры изменяются в зависимости от фаз развития растений и они неодинаковы для надземных органов и корневой системы. Например:
| Культура | оптимальная температура, Со | |
| для надземных органов | для корневой системы | |
| пшеница яровая | 16-20 | 16 |
| табак | 29-31 | 23-25 |
| лук | 18-26 | 10-14 |
| картофель | 21 | 18 |
Интервал оптимальной температуры для корня и надземной части растения составляет 5-6 Со. При изменениях температуры немедленно изменяется и интенсивность поглощения растениями различных питательных элементов. Например, известно, что при низких температурах (10-12 Со) растения особенно трудно усваивают фосфор почвы. В этом случае неблагоприятное влияние пониженных температур можно преодолеть увеличением доз фосфорных удобрений.
Усвоение растениями питательных элементов в большей мере зависит от температуры корнеобитаемого пространства, чем от температуры воздуха. Кроме того, температура корнеобитаемого пространства сильнее влияет на передвижение питательных элементов, чем на их поглощение корневой системой.
Поглощение питательных элементов из почвенного раствора в значительной степени зависит от биологических особенностей вида, причем иногда теплолюбивые растения обладают лучшей способностью поглощать питательные элементы из растворов при низких температурах, чем холодовыносливые растения, но при этом передвижение элементов в надземную часть определяется именно температурой почвы. Например, огурец (теплолюбивая культура) поглощает 33% фосфора из почвенного раствора при температуре 0о, но почти весь фосфор при этом остается в корнях, тогда как лук (холодовыносливая культура), поглощая всего 2% фосфора при температуре 0о, переносит в листья более половины.
При крайних температурах, при которых жизнедеятельность изучаемого растения сильно подавлена, повышение концентрации питательных элементов в почве почти не улучшает его питания. Подкормка через листья может оказать положительное влияние на питание растений при низких температурах почвы в большей степени, чем подкормка, внесенная в почву.
Относительная влажность воздуха.
При высокой влажности воздуха надземная масса растения интенсивнее нарастает, чем при низкой, хотя масса корней может быть при этом меньше.
Влияние влажности воздуха, а, следовательно, и транспирации растений на поглощение питательных элементов растениями, в количественном выражении может сильно изменяться в зависимости от вида растений, интенсивности транспирации, концентрации питательного раствора.
Интенсивность освещения.
Снижение интенсивности освещения сильно уменьшает приросты массы как надземной части, так и корневой системы, причем у светолюбивых растений это угнетение проявляется значительнее, нежели у теневыносливых. При затенении хуже всего усваивается фосфор, затем азот, уменьшение освещенности меньше всего угнетает поступление калия.
Реакция почвенного раствора.
На почвах, обладающих большей емкостью поглощения и большей буферностью, растения легче переносят кислую реакцию (например, у чернозема лучшие буферные свойства, чем у подзолистых почв). Для развития растений решающее значение имеет РН в прикорневой зоне, этим в значительной мере обусловлено более резкое воздействие на растения кислой реакции на малобуферных почвах.
Еще Д.Н. Прянишниковым были получены данные о том, что при большом содержании кальция растения легче переносят кислую реакцию, и присутствие алюминия и железа усиливает вредное действие повышенной кислотности. При подщелачивании почвенного раствора наблюдается более интенсивное поступление катионов, тогда как при подкислении усиливается поглощение анионов.
Подщелачивание раствора снижает доступность микроэлементов, а значит затрудняется их поступление в растение. Изменение реакции почвы влияет и на почвенную микрофлору, что, в свою очередь, влияет на развитие растений. Например азотфиксация, осуществляемая свободноживущими бактериями, и нитрификация лучше всего проходят в почвенном растворе с рН, близкой к нейтральной.
В целом среди культурных растений можно выделить несколько групп:
1). Выносливые к кислой реакции почвы:
(выдерживают рН до 4,3, оптимальное значение рН - 6,3) - сельдерей и картофель,
(выдерживают рН до 4,8, оптимальное значение рН - 6,3) - брюква и кольраби,
2). Выносливые к щелочной реакции почвы (оптимальное значение рН - 7,2):
(выдерживают рН от 6,3 до 7,8 (лук, морковь),
(выдерживают рН от 6,3 до 8,0 (чеснок),
(выдерживают рН от 6,3 до 8,3 (томат).
Роль минерального питания в формировании урожая и регулировании роста и развития растений.
Минеральное питание является процессом, объединяющим совокупность ряда физиологических закономерностей в организме растения, обеспечивает прохождение других важнейших физиологических процессов, таких как водный обмен, фотосинтез, дыхание, накопление запасных питательных веществ.
Помимо участия таких минеральных элементов, как азот, фосфор, сера, в непосредственном синтезе органических соединений, все остальные минералы играют весьма важную роль в качестве кофакторов различных ферментов, регуляторов транспортных и обменных процессов, входят в состав гормонов, алкалоидов, сапонинов, фитоалексинов и других биологически активных веществ. В свою очередь, именно совокупность соответствующих ферментов и регуляторов позволяет растению осуществлять процессы роста, переходить в процессе онтогенеза от одной фазы к другой, накапливать необходимые вещества для формирования плодов и семян.
Осуществляя поглощение веществ, растение с помощью корневой системы обеспечивает и выделение ряда веществ, т.е. способствует процессу обмена с окружающей средой. Например корни люпина, гречихи, гороха выделяют органические кислоты, что позволяет им поглощать фосфаты из фосфорной муки, а выделение органических кислот корнями злаковых культур позволяет им поглощать калий из силикатов.
Для выделения веществ из корня служат те же механизмы, что и для поглощения веществ корневыми волосками. В связи с выделяющей функцией корней растения делят на две большие группы:
Не выделяющие в больших количествах фосфорную кислоту и другие минеральные вещества - это злаки, клубнеплоды, овощные культуры;
Выделяющие в больших количествах фосфорную кислоту и другие минеральные вещества - это бобовые и масличные культуры.
В первой группе растения характеризуются нейтральной реакцией клеточного сока и накоплением углеводов.
Во второй группе растения характеризуются кислой реакцией клеточного сока и накоплением белков и жиров.
Процесс выделения растениями фосфорной кислоты является ярким примером активного участия растений в круговороте веществ.
Например, люпин, горчица, рапс выделяют от 14 до 34% поглощенной фосфорной кислоты. Этот процесс определяется тем, что коллоидные структуры клеток этих растений, в частности белки, легко меняют свой заряд с положительного на отрицательный или нейтральный при поглощении фосфорной кислоты, а в силу высокой кислотности клеточного сока происходит их нейтрализация, фосфорная кислота легко отщепляется от белков и может выделяться с обратным током веществ в окружающую среду.
Напротив, у растений с нейтральной реакцией (у злаков) органические коллоиды в клетках находятся в изоэлектрическом состоянии, поэтому присоединившаяся к внутренним коллоидам в клетке фосфорная кислота, в силу высокой буферности содержимого цитоплазмы, уже не может легко высвобождаться, и, поэтому, не выделяется.
Помимо выделения корневой системой в почвенный раствор неорганических веществ в качестве обмена ионами, растения выделяют различные сахара, органические кислоты, аминокислоты, ферменты, витамины, сапонины и другие вещества. Все эти выделения обуславливают особое состояние почвы возле корневой системы и определяют наличие таких явлений, как:
аллелопатия, то есть взаимодействие ризосферных выделений растений друг на друга, что особенно актуально в подборе растений на небольших площадях, например в условиях огорода,
бактериориза, то есть развитие в ризосфере особого комплекса бактериальных организмов, участвующих в процессе азотфиксации,
микориза, то есть развитие в ризосфере особого комплекса грибных организмов, которые играют важную роль в процессе поглощения веществ растениями, особенно многолетними, участвуют в какой-то степени и в процессе азотфиксации, а также и в усвоении азота растениями, поскольку переводят неорганические формы азота в аминокислотную форму. Среди растений существуют даже облигатные микотрофы, то есть такие растения, которые в отсутствие особых видов грибов не развиваются (орхидея, вереск). Особенно важную роль играет микориза для лесных пород, тогда как среди плодовых деревьев такой тесной зависимости не отмечено.
Для эффективного применения удобрений необходимо знать:
качественные и количественные индексы потребности растения в элементах минерального питания в онтогенезе для создания запланированного урожая,
индексы степени плодородия почвы,
возможные коэффициенты использования питательных веществ, находящихся в почве и вносимых с удобрениями,
обеспеченность растений водой.
Растение в первую фазу развития питается в основном запасом питательных веществ в семени, в дальнейшем потребность в элементах питания возрастает и достигает максимума в период цветения и завязывания плодов. С прекращением накопления органического вещества в растении наблюдается резкое снижение потребности в минеральном питании и даже происходит обратный переход части веществ из растения в почву.
Важно вносить удобрения в умеренных дозах, так как в противном случае слишком высокая концентрация почвенного раствора может вызвать увядание растений, особенно молодых.
Сочетание основного предпосевного внесения удобрений с дополнительным в виде подкормок дает возможность наиболее полно обеспечить растений в соответствующие фазы развития элементами питания.
Наиболее эффективным способом внесения минеральных удобрений является локальный с заделкой в почву.
В ряде случаев применяют внекорневую подкормку растений, как способ дополнительного снабжения растений элементами минерального питания в период вегетации.
Кроме того, внекорневую подкормку можно эффективно использовать для воздействия на обмен веществ растения:
подкормка калийно-фосфорными удобрениями за две-три недели до уборки способствует переводу сахарозы в сахарной свекле из листьев в корни,
подкормка азотными удобрениями в период налива зерна у зерновых культур способствует большему накоплению клейковины,
подкормка калийно-фосфорными удобрениями в период поражения растений тлей снижает вредоносность этого вредителя, так как происходит уменьшение количества аминокислот, что вызывает у тли бесплодие,
применение ионофоров - мембраноактивных соединений для регуляции интенсивности ионных потоков в растениях [например, диметилсульфоксида (ДМСО) -
(СН3) 2SO] приводит к усиленному поглощению фосфора корнями и активизации транспорта фосфатных и нитратных потоков, а также вызывает отток ассимилятов из листьев в корнеплоды, что особенно благоприятствует увеличению урожайности и сахаристости у сахарной свеклы.
Весьма важной в сельском хозяйстве является нетрадиционная технология возделывания растений, то есть гидропоника или культивирование растений без почвы. Особенно массово эта технология внедрена в странах Северной Европы, в Шотландии, в Гренландии, где суровые условия открытого грунта не позволяют выращивать там в традиционной технологии овощные и ягодные культуры. Гидропоника подразделяется на три типа:
выращивание растений на инертных субстратах (песок, вермикулит, перлит),
выращивание растений в питательных растворах,
аэропоника.
Все эти разновидности требуют хороших знаний именно в области минерального питания растений и создания микроклимата в зависимости от особенностей как культуры, так и выращиваемого сорта, поскольку все необходимые вещества растение получает только извне с питательным раствором.
Каждая из этих разновидностей имеет свои положительные и отрицательные стороны, поэтому выбор используемой технологии зависит прежде всего от технических возможностей.
Более подробно об этом аспекте возделывания растений также можно прочитать в дополнительной литературе.
Подводя итог теме "Минеральное питание", необходимо отметить, что успешное выращивание растений, получение высоких урожаев достигаются непременно в совокупности обеспечения:
оптимального уровня снабжения растения всеми необходимыми элементами питания, как минерального характера, так и источником углерода,
оптимального соотношения элементов минерального питания в почве или в искусственном субстрате в течение вегетации в зависимости от фазы развития растения,
высокого уровня снабжения энергией с помощью регуляции светового режима,
сохранения относительного постоянства обводненности листьев за счет регуляции поливного режима.
Тема: Взаимопревращение органических веществ в растении.
Дополнительная литература:
В.Л. Кретович "Основы биохимии растений", М., 1971
Вопросы к теме:
Взаимопревращение в растении углеводов.
Синтез и распад белков в растении.
Синтез и распад жиров в растении.
Связи между тремя основными группами органических веществ.
Передвижение органических веществ в растении.
Метаболизм или обмен веществ - это совокупность всех химических реакций, направленных на самоорганизацию и самовоспроизведение, это важнейшее свойство жизни и непременный ее признак у всех клеточных организмов.
Поступившие в растение неорганические вещества превращаются в органические, последние входят в отрегулированную систему превращения веществ и энергии.
Метаболизм растения - это огромное количество физических и химических реакций, находящихся в состоянии непрерывного взаимодействия между собой, а также с окружающей средой.
Наряду с интенсивно превращающимися первичными органическими соединениями (углеводами, белками, липидами, нуклеиновыми кислотами, аминокислотами, органическими кислотами) в растительных организмах существуют медленно перемещаемые и локально синтезируемые вещества, называемые вторичными, так как они образуются в процессах вторичного обмена и не являются ни источниками энергии, ни запасными веществами (гликозиды, алкалоиды, сапонины).
Взаимопревращение в растении углеводов.
Биосинтез глюкозы и других углеводов из более простых предшественников является в количественном отношении наиболее важным биосинтетическим процессом в биосфере.
Растения образуют огромные количества гексоз из углекислого газа и воды, а гексозы, в свою очередь, превращаются в крахмал, целлюлозу и другие полисахариды.
Превращение глюкозы в пировиноградную кислоту, катализируемое ферментами гликолиза (первый этап дыхания), является центральным путем катаболизма углеводов.
Превращение пировиноградной кислотыв глюкозу является наиболее важным путем биосинтеза моно и полисахаридов в процессах обмена веществ в клетке.
В этот центральный биосинтетический путь вливаются два главных "питающих" пути начинающихся с двух различных наборов неуглеводных предшественников:
первый состоит из ряда реакций, посредством которых промежуточные продукты цикла Кребса превращаются в пировиноградную кислоту.
Этот процесс называют глюконеогенезом.
второй состоит из реакций, приводящих к восстановлению углекислого газа до глюкозы, т.е. реакции цикла Кальвина.
Образование глюкозо-6-фосфата в центральном пути биосинтеза приводит к последующему появлению:
свободной глюкозы,
запасных полимерных сахаридов (крахмала у растений, гликогена у грибов, гетеротрофных бактерий и животных организмов),
других моносахаридов и их производных,
дисахаридов и олигосахаридов,
компонентов клеточной стенки и клеточной оболочки (целлюлозы, ксиланов, муреина, мукополисахаридов).
Синтез полисахаридов происходит в процессе трансгликозидирования, т.е. реакций переноса гликозидных остатков с участием ферментов гликозилтрансфераз.
Например, в основе синтеза сахарозы лежат следующие реакции:
АТФ + УДФ (уридиндифосфат) Ы УТФ + АДФ
УТФ + глюкозо-1-фосфат Ы УДФГ (уридиндифосфатглюкоза) + Н4Р2О7, УДФГ + фруктоза Ы сахароза + УДФ.
Нуклеозиддифосфатсахара играют большую роль в биосинтезе крахмала. Основная реакция при синтезе крахмала выглядит следующим образом:
УДФГ + "затравка" (полисахарид из 3-4 остатков глюкозы) ® УДФ + крахмал
Основной фермент в этой повторяющейся много раз реакции при создании разветвленной многоцепочечной молекулы крахмала - крахмалглюкозилтрансфераза.
Часто более активным соединением при синтезе крахмала является не УДФГ, а АДФГ (адениндифосфатглюкоза).
Углеводы в растительном организме служат основным питательным и скелетным материалом клеток и тканей растения. В прорастающих тканях сложные запасные вещества распадаются на более простые. Процесс распада крахмала на олигосахариды и моносахариды, жиров на жирные кислоты и глицерин, белков на аминокислоты - относится к гидролитическому типу и проходит с присоединением воды.
Превращение крахмала по гидролитическому типу в простые сахара происходит под воздействием фермента амилазы. Количество амилазы в проростке гораздо выше, чем в покоящемся семени. Осахаривание крахмала в эндосперме идет до конце только в контакте с растущим побегом, использующим сахар, образующийся при гидролизе.
Второй путь расщепления крахмала по фосфоролитическому типу осуществляется под действием фермента фосфорилазы. При этом глюкоза переносится на неорганический фосфат, в результате чего образуется глюкозо-1-фосфат, включающийся затем в различные циклы синтеза углеводов.
Ключевыми звеньями в обмене углеводов являются пировиноградная кислота и глюкозо-1-фосфат или глюкозо-6-фосфат. Через пировиноградную кислоту осуществляется переход от метаболизма углеводов к метаболизму других органических веществ.
Синтез и распад белков в растении.
Характерной особенностью растений является способность к синтезу всех входящих в состав белков аминокислот непосредственно за счет неорганических азотистых соединений - аммиака и нитратов.
Свободный аммиак ядовит для растений, поэтому растения сразу используют его на синтез аминокислот. Нитраты же могут накапливаться в тканях растений и в довольно больших количествах. Нитраты, прежде, чем вступить во взаимодействие с углеводами, подвергаются восстановлению до нитритов, а затем до аммиака. Промежуточным продуктом при этом является гидроксиламин.
Схема восстановления нитратов до аммиака:
НNO3 ® НNO2 ® (НNO2) 2 ® NH2OH ® NH3
гипонитрит гидроксиламин
Этот процесс имеет универсальное значение.
Аммиак, либо образовавшийся из нитритов, либо поглощенный, немедленно вступает в реакцию с кетокислотами, образуя аминокислоты. Прямое аминирование кетокислотаммиаком - общий способ построения аминокислот. Это основной путь синтеза аминокислот. Протекание этих реакций - процесс обратимый, так как разложение амсинокислот (например при прорастании семян) или дезаминирование, протекающее по окислительному типу, заканчивается образованием кетокислоты и аммиака.
Процесс идет в две стадии:
Образование иминокислоты:
NH3 + CH3COCOOH Ы CH3C=NHCOOH + H2O
пировиноградная аланиндегидрогеназа иминокислота кислота
Образование аминокислоты:
CH3C=NHCOOH + 2Н+ Ы СН3СНNН2СООН
НАД. Н2 аланин
Образование аминокислот может также происходить в результате ферментативного превращения одной аминокислоты в другую, например:
орнитин Ы пролин Ы глютаминовая кислота
Биосинтез белка - один из сложнейших процессов в клетке. Он осуществляется в рибосомах, важным компонентом которых является магний, который составляет до 2,5% от сухого веса и поддерживает активную структуру рибосом. В биосинтезе белка задействована информационная система - ядерная ДНК ® информационная РНК® рибосомальная (матричная) РНК - и большое количество АТФ, так как это процесс эндэрготический, при котором потребляется большое количество энергии.
Аминокислоты, синтезирующиеся в клетке, активируются своими специфическими ферментами и с помощью транспортных РНК переносятся к рибосоме, где собственно и происходит процесс построения первичной цепочки любого пептида. Транспортная РНК имеет антикодон, который должен соответствовать кодону матричной РНК для того, чтобы аминокислота отсоединилась от т-РНК и встроилась в пептид.
Диссимиляция белка начинается с его гидролитического расщепления, происходящего под воздействием протеолитических ферментов и сопровождающегося образованием свободных аминокислот. Этот процесс активно происходит при прорастании семян, при этом образующиеся аминокислоты идут на построение тканей проростка. Важнейшим этапом диссимиляции аминокислот является их дезаминирование с образованием свободного аммиака.
Окислительное дезаминирование (с образованием кетокислоты и аммиака) является процессом, обратным синтезу аминокислот, и происходит через образование иминокислоты. Именно этот процесс происходит при брожении, в частности, при спиртовом брожении, когда используются натуральные продукты (зерно, сахарная свекла), имеющие в своем составе белки. При брожении из белков образуются в результате дезаминирования кетокислоты, которые и придают специфический неприятный запах и вкус бродильной жидкости и называются "сивушными маслами".
Разложение белков может также проходить по механизмам восстановительного дезаминирования и гидролитического дезаминирования.
Восстановительное дезаминирование является путем, соединяющим метаболизм белков и липидов:
RCHNH2COOH + 2H+ Ы RCH2COOH + NH3
Гидролитическое дезаминирование является путем, соединяющим метаболизм белков и углеводов:
СООНСН2СНNH2COOH + HOH (H2O) Ы COOHCOCH2COOH + NH3 + 2H+
аспарагиновая кислота щавелевоуксусная кислота
Водород, отнятый у аминокислоты дегидрогеназой, передается хинону, который превращается в полифенол, а затем опять окисляется до воды и хинона:
2Н+ + хинон Ы полифенол + О Ы Н2О + хинон
Дезаминирование аминокислот является основным способом превращения азотистых веществ в безазотистые соединения, которые могут быть затем использованы для дальнейшей переработки в углеводы и жиры.
Аммиак либо вступает в реакцию аминирования и образует с кетокислотами новые аминокислоты, либо связывается с органическими кислотами, образуя аммиачные соли (особенно у кислых растений - щавеля, ревеня). У большинства растений обезвреживание аммиака происходит путем образования амидов - аспарагина и глютамина (т. е. амидов аспарагиновой и глютаминовой аминокислот).
Физиологическая роль амидов заключается в:
обезвреживании (связывании) аммиака,
создании резерва диаминодикарбоновых аминокислот, необходимых для ферментативного переаминирования,
предохранении от окисления дикарбоновых аминокислот.
Синтез амидов проходит по схеме:
Синтез аспарагиновой или глютаминовой кислот,
Амидирование аспарагиновой или глютаминовой кислот в следующем порядке:
а). АТФ + глютаминсинтетаза ® глютаминсинтетазафосфат + АДФ,
б). глютаминсинтетазафосфат + НООС-СН2СН2СНNH2СООН Ы
РООС-СН2СН2СНNH2СООН + глютаминсинтетаза
в). РООС-СН2СН2СНNH2СООН + NH3 Ы NH2-CO-СН2СН2СНNH2СООН + Н3РО4
глютамин
Кроме дезаминирования при диссимиляции аминокислот важную роль играет и процесс декарбоксилирования, сопровождающийся образованием углекислого газа и аминов. Амины либо вступают в реакции синтеза новых аминокислот, либо появляются при гнилостных распадах белков и входят в круговорот веществ уже в качестве питания для других организмов. Ферменты, определяющие этот процесс, называются декарбоксилазами.
Особенно легко амины используются растением для синтеза алкалоидов. Алкалоиды образуются из аминов путем выделения аммиака и образования соответствующего азотистого гетероцикла. Кроме того, амины могут подвергаться дальнейшему окислению, образуя аммиак и альдегид. При этом альдегид снова вступает во взаимодействие другими аминами и карбонильными соединениями, образуя алкалоиды.
Кроме образования алкалоидов одним из путей дальнейшего превращения аминов является их метилирование, проходящее с помощью метилтрансфераз. С помощью этого процесса происходит, например, образование никотина в табаке, холина, который играет важную роль в метаболизме клетки, являясь частью фосфатидов, или встречается в свободном виде.
Метилированию могут подвергаться не только амины, но и аминокислоты, в результате образуются бетаины, которые затрудняют кристаллизацию сахара.
Белковый и аминокислотный обмен тесно связан с обменом витаминов, так как некоторые из них являются составной частью активных групп ферментов, катализирующих превращения аминокислот. Кроме того, некоторые витамины образуются из аминокислот, например, никотиновая кислота из триптофана. Из ряда аминокислот образуются также гормоны роста типа ауксина, b-индолилуксусной кислоты.
В растении метаболизм азота начинается процессом гидролитического и окислительного распада белков, образованием аминокислот и амидов, которые поступают из эндосперма или семядолей в росток и служат в нем исходным материалом для синтеза белков протоплазмы. Когда росток начинает ассимилировать углекислый газ, главными местами новообразования белков становятся лист и корень. По мере развития растения начинается перетекание аминокислот и белков из листьев к соцветиям и плодам, а, следовательно, к семенам.
Синтез и распад жиров в растении.
Главные этапы синтеза жира в растении представлены следующими процессами:
из сахаров образуются глицерин и жирные кислоты, как насыщенные, так и ненасыщенные,
из глицерина и жирных кислот образуются жиры при участии фермента липаза.
Все эти процессы обратимые и постоянно происходят в клетке.
Главным источником образования компонентов жира являются гексозы, хотя могут использоваться и другие простые сахара. Особенно легко используется для синтеза жира уксусная кислота.
Глицерин, из которого синтезируются жиры, образуется в процессе анаэробной диссимиляции углеводов путем восстановления глицеринового альдегида, получающегося из фруктозодифосфата под действием фермента альдолазы.
Включение сахарного остатка в галактолипиды происходит благодаря действию трансгликозилаз, причем часто источником остатков сахара является уридиндифосфатгалактоза.
Процессу синтеза жирных кислот из сахара предшествует распад сахара на уксусную кислоту, этиловый спирт и пировиноградную кислоту (процесс дыхания).
Например, масляная кислота образуется путем конденсации двух молекул уксусной кислоты в ацетоуксусную и последующим ее восстановлением до масляной:
Похожие работы
... , в которых выращивают растения и проводят опыты в условиях определенного состава воздуха, нужной температуры и освещения. Применяя эти методы, физиологи исследуют растения на молекулярном, субклеточном, клеточном и организменном (интактное растение) уровнях. Сейчас в биологических исследованиях широко применяют электронные микроскопы просвечивающего типа с разрешающей способностью 0,15—0,5 нм, в ...
... или транспирация представляют совокупность химических и физических процессов. Чтобы понять механизм физиологического процесса, необходимо выделить его физические и химические компоненты. В связи с этим физиология растений все более нуждается в усовершенствованных методах биохимии. Биохимический подход оказался очень плодотворным в исследованиях таких сложных процессов, как фотосинтез и дыхание. ...
... насекомое тем временем усердно собирает сладкий нектар, предложенный цветком в награду за труды. Цветки правильной формы, то есть имеющие насколько осей симметрии, называются актиноморфными. В классе двудольных растений наблюдается богатое разнообразие цветковых форм. 3. Описание некоторых семейств класса двудольных Семейство лютиковых объединяет около 1500 видов трав и кустарников, многие ...
... Областного Университета в период с июня по сентябрь 2003 года. Объектом изучения являлись растения кукурузы сорта Россо. Изучение влияния 6-БАП на рост и биометрические показатели растений кукурузы при разном уровне засоления проводилось в условиях вегетационного опыта (почвенные культуры). Семена кукурузы проращивались при температуре 20оС в термостате в течение 3 дней, а затем высаживались в ...
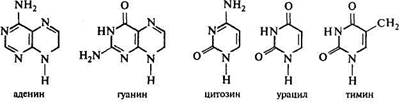
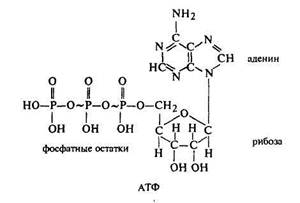
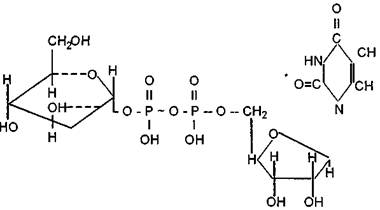

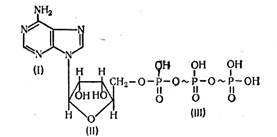
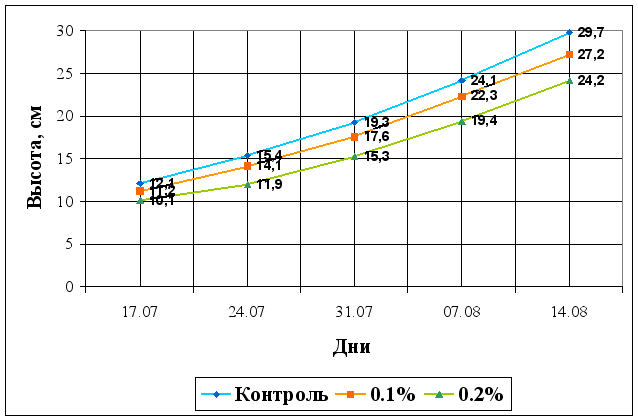
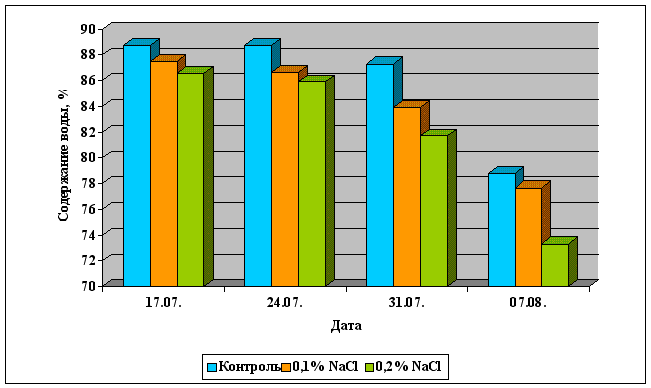
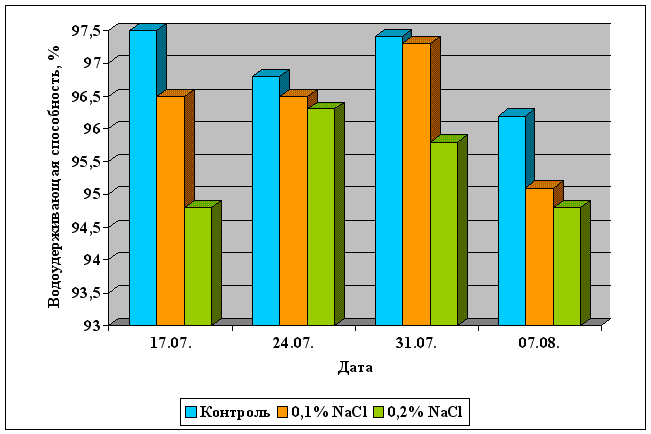
0 комментариев