Навигация
Содержание
Введение
1. Историческая справка
2. Свойства белка, выделение
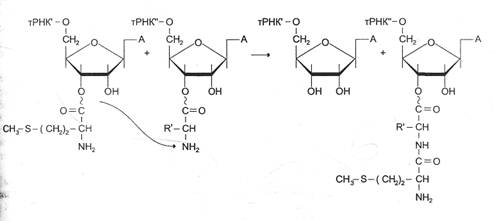
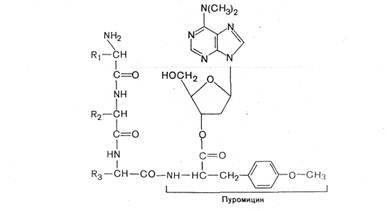
3. Синтез белка
4. Значение белков в питании
Заключение
Список использованной литературы
Введение
Белки – высокомолекулярные природные полимеры, построенные из остатков аминокислот, соединенных амидной (пептидной) связью – СО-NH-. Каждый белок характеризуется специфической аминокислотной последовательностью и индивидуальной пространственной структурой (конформацией). На долю белка приходится не менее 50% сухой массы органических соединений животной клетки. Функционирование белка лежит в основе важнейших процессов жизнедеятельности организма. Обмен веществ (пищеварение, дыхание и др.), мышечное сокращение, нервная проводимость и жизнь клетки в целом неразрывно связаны с активностью ферментов – высокоспецифических катализаторов биохимических реакций, являющихся белками. Основу костной и соединительной тканей, шерсти, роговых образований составляют структурные белки. Они же формируют остов клеточных органелл (митохондрий, мембран и др.). Расхождение хромосом при делении клетки, движение жгутиков, работа мышц животных и человека осуществляются по единому механизму при посредстве белков сократительной системы. Важную группу составляют регуляторные белки, контролирующие биосинтез белка, и нуклеиновых кислот. К регуляторным белкам относятся также пептидно-белковые гормоны, которые секретируются эндокринными железами. Информация о состоянии внешней среды, различные регуляторные сигналы (в т.ч. гормональные) воспринимаются клеткой с помощью специальных рецепторных белков, располагающихся на наружной поверхности плазматической мембраны. Эти белки играют важную роль в передаче нервного возбуждения и в ориентированном движении клетки (хемотаксисе). В активном транспорте ионов, липидов, сахаров и аминокислот через биологические мембраны участвуют транспортные белки, или белки-переносчики. К последним относятся также гемоглобин и миоглобин, осуществляющие перенос кислорода. Преобразование и утилизация энергии, поступающей в организм с питанием, а также энергии солнечного излучения происходят при участии белков биоэнергетической системы (например, родоксин, цитохромы). Большое значение имеют пищевые и запасные белки, играющие важную роль в развитии и функционировании организмов. Защитные системы высших организмов формируются защитными белками, к которым относятся иммуноглобулины (ответственны за иммунитет), белки комплемента (ответственны за лизис чужеродных клеток и активацию иммунологической функции), белки системы свертывания крови и противовирусный белок интерферон.
По составу белки делятся на простые, состоящие только из аминокислотных остатков, и сложные. Сложные могут включать ионы металла (металлопротеиды) или пигмент (хромопротеиды), образовывать прочные комплексы с липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеиды), а также ковалентно связывать остаток фосфорной кислоты (фосфопротеиды), углевода (гликопротеины) или нуклеиновой кислоты (геномы некоторых вирусов). В соответствии с формой молекул белки подразделяют на глобулярные и фибриллярные. Молекулы первых свернуты в компактные глобулы сферической или эллипсоидной формы, молекулы вторых образуют длинные волокна (фибриллы) и высокоасимметричны. Большинство глобулярных белков, в отличие от фибриллярных, растворимы в воде. Особую группу составляют мембранные (амфипатические) белки, характеризующиеся неравномерным распределением гидрофильных и гидрофобных (липофильных) участков в молекуле: погруженная в биологическую мембрану часть глобулы состоит преимущественно из липофильных аминокислотных остатков, а выступающая из мембраны – из гидрофильных.
1. Историческая справка
Первые работы по выделению и изучению белковых препаратов были выполнены еще в 18 в., однако в тот период исследования белков носили описательный характер. В начале 19 в. были сделаны первые анализы элементного состава белков (Ж.Л. Гей-Люссак, Л. Ж. Тенар, 1810) положившие начало систематическим аналитическим исследованиям, в результате которых было установлено, что все белковые вещества близки не только по внешним признакам и свойствам, но и по элементарному составу. Важное следствие этих работ – создание первой теории строения белковых веществ, согласно которой все белки содержат общий гипотетический радикал – «протеин», имеющий эмпирическую формулу C40H62N10O12 и связанный в различных пропорциях с атомами серы и фосфора. Получив сначала всеобщее признание, эта теория привлекла интерес к аналитическим исследованиям белков, совершенствованию препаративных методов белковой химии. В этот период были разработаны простейшие приемы выделения белков путем экстракции растворами нейтральных солей и осаждения, получены первые кристаллические белки (гемоглобин, некоторые растительные белки), для анализа белков стали использовать кислотный и щелочной гидролиз.
Создание теории протеина совпало по времени с формированием представлений о функции белков в организме. В 1835 г. И.Я. Берцелиус высказал идею о важнейшей функции белка – биокаталитической. Вскоре были открыты первые протеолитические ферменты – пепсин (Т. Шванн, 1836) и трипсин (Л. Корвизар, 1856). Открытие протеаз стимулировало интерес биохимиков к физиологии пищеварения, а следовательно, и к продуктам переваривания белков. К середине 19 в. было показано, что под действием протеолитических ферментов белки распадаются на близкие по свойствам фрагменты, получившие название пептоинов (К. Леман, 1850).
Важное событие в изучении белков – выделение из белкового гидролиза аминокислоты глицина (А. Браконно, 1820). К концу 19 в. было изучено большинство аминокислот, входящих в состав белка, синтезирован аланин (А. Штреккер, 1850). В 1894 г. А. Коссель высказал идею о том, что основными структурными элементами белков являются аминокислоты.
В начале 20 в. значительный вклад в изучение белка внес Э. Фишером, впервые применившим для этого методы органической химии. Путем встречного синтеза Э. Фишер доказал, что белки построены из остатков ![]() - аминокислот, связанных амидной (пептидной) связью. Он также выполнил первые аминокислотные анализы белка, дал правильное объяснение протеолизу.
- аминокислот, связанных амидной (пептидной) связью. Он также выполнил первые аминокислотные анализы белка, дал правильное объяснение протеолизу.
В 20-40-е гг. получили развитие физико-химические методы анализа белков. Седиментационными и диффузионными методами были определены молекулярные массы многих белков, получены данные о сферической форме молекул глобулярных белков, выполнены первые рентгеноструктурные анализы аминокислот и пептидов, разработаны хроматографические методы анализа. Существенно расширились представления о функциональной роли белка.
В начале 50-х гг. была выдвинута идея о трех уровнях организации белковых молекул (К.У. Линдерстрём-Ланг, 1952) – первичной, вторичной и третичной структурах. Определены первичные структуры инсулина (Ф. Сенгер, 1953) и рибонуклеазы (К. Анфинсен, С. Мур, К. Херс, У. Стайн, 1960). По данным рентгеноструктурного анализа были построены трехмерные модели миоглобина (Дж. Кендрю, 1958) и гемоглобина (М. Перуц, 1958) и, таким образом, доказано существование в белках сторичной и третичной структур, в т.ч. ![]() -спирали, предсказанной Л. Полингом и Р. Кори в 1949-51.
-спирали, предсказанной Л. Полингом и Р. Кори в 1949-51.
В 60-е гг. в химии белков развивалось синтетическое направление: были синтезированы инсулин и рибонуклеаза. Дальнейшее развитие получили аналитические методы: стал широко использоваться автоматический аминокислотный анализатор, созданный С. Муром и У. Стайном в 1958, существенно модифицированы хроматографические методы, до высокой степени совершенства доведен рентгеноструктурный анализ, сконструирован автоматический прибор для определения последовательности аминокислотных остатков в белке – секвенатор. Благодаря созданию прочной методологической базы стало возможным проводить широкие исследования аминокислотной последовательности белка. В эти годы была определена структура несколько сотен сравнительно небольших белков (до 300 аминокислотных остатков в одной цепи), полученных из самых различных источников как животного, так и растительного, бактериального, вирусного и другого происхождения. Среди них – протеолитические ферменты (трипсин, химотрипсин, субтилизин, карбоксипептидазы), миоглобины, геомоглобины, цитохромы, лизоцимы, иммуноглобулины, гистоны, нейротоксины, белкоавых оболочек вирусов, белково-пептидные гормоны и др. В результате были созданы предпосылки для решения актуальных проблем энзимологии, иммунологии, эндокринологии и др. областей физико-химической биологии.
В 70-80-е гг. наибольший прогресс был достигнут при изучении белков-регуляторов матричного синтеза биополимеров (в т.ч. белков рибосом), сократительных, транспортных и защитных белков, ряда мембранных белков (в т.ч. белков биоэнергетических систем), рецепторных белков. Большое внимание уделялось дальнейшему совершенствованию методов анализа белка. Значительно повышена чувствительность автоматического анализа аминокислотной последовательности б. Широкое применение нашли новые методы разделения белков и пептидов (жидкостная хроматография высокого давления, биоспецифическая хроматография). В связи с разработкой эффективных методов анализа нуклеотидной последовательности ДНК (А. Максам и У. Гилберт, Ф. Сингер) стало возможным использовать полученную при таком анализе информацию и при определении первичной структуры белков. В результате установлена структура ряда белков, доступных в ничтожно малых количествах (интерферон, ацетилхолиновый рецептор), а также белков, большой молекулярной массы. Успехи структурного анализа позволили вплотную приступить к определению пространственной организации и молекулярных механизмов функционирования надмолекулярных комплексов, в т.ч. рибосом, хроматина (нуклеосом), митохондрий, фагов и вирусов. Существенные результаты получены в эти годы советскими учеными: определена первичная структура аспартатаминотрансферазы (1972), бактериородопсина (1978), животного родопсина (1982), некоторых рибосомальных белков, фактора элонгации G (1982), важнейшего фермента – РНК-полимеразы (1976-82), нейротоксинов и др.
Похожие работы
... как в результате их жизнедеятельности азот, находящийся в виде соединений, недоступных для усвоения растениями, превращается в соли азотной кислоты, которые хорошо ими усваиваются. 2. Биосинтез белков Любая живая клетка способна синтезировать белки, и эта способность представляет одно из наиболее важных и характерных ее свойств. С особенной энергией идет биосинтез белков в период роста и ...
... приближается к 100%. Очень высока степень усвоения и других продуктов животного происхождения: молока (75—80%), мяса (70—75%), рыбы (70—80%) и т. д., Многие растительные продукты, особенно злаковые, содержат белки пониженной биологической ценности: в кукурузе, например, обнаружен значительный дефицит лизина и триптофана, в пшенице — лизина и треонина. В большинстве растительных материалов ...
енетическом и на физическом уровне и это относится к производству любых рекомбинантных белков. 1. Методы генной инженерии при получении рекомбинантных белков Генетическая инженерия - конструирование in vitro функционально активных генетических структур (рекомбинантных ДНК), или иначе - создание искусственных генетических программ (Баев А.А.). По Э.С. Пирузян генетическая инженерия - ...
... , вызывает уменьшение количества синтезируемых ферментов. Это последнее явление получило название репрессии синтеза ферментов. Оба явления — индукция и репрессия — взаимосвязаны. Согласно теории Жакоба и Моно в биосинтезе белка у бактерий участвуют по крайней мере три типа генов: структурные гены, ген-регулятор и ген-оператор. Структурные гены определяют первичную структуру синтезируемого белка. ...
0 комментариев