Навигация
Аудит качества на ООО «МКС ФАРМ»
2 Аудит качества на ООО «МКС ФАРМ»
ООО «МКС ФАРМ» – одно из крупных фармацевтических предприятий Калининградской области. Система управления качеством ООО «МКС ФАРМ» - это комплексный подход к организации производственного менеджмента, жёстко регламентирующий все аспекты жизнедеятельности предприятия от заключения контрактов на изготовление продукции до отгрузки её потребителю. Система управления качеством через свои процедуры обеспечивает правильное выполнение всех работ, необходимых и достаточных для достижения стабильно высокого уровня качества продукции.
Основа политики ООО «МКС ФАРМ» в области качества - это соблюдение установленных требований, предъявляемых к каждому виду деятельности.
Эта политика получает развитие за счёт эффективных механизмов управления материально-техническим снабжением, проектно-конструкторскими разработками, изготовлением, контролем и испытанием продукции, службами качества и техническими службами нашего предприятия. Управление качеством осуществляется в соответствии с планом качества и технической документацией.
Основными составляющими качества продукции являются применяемые современные, эффективные технологические процессы изготовления продукции, входной контроль всех применяемых исходных материалов, контроль и испытания продукции в процессе производства, полная прослеживаемость каждого изделия в долотном производстве.
В данный момент на предприятии происходит внедрение "Правил организации производства и контроля качества лекарственных средств (GMP)", что отразиться и на организации процесса аудита качества.
Для российских фармацевтических предприятий отраслевой версией стандарта в области управления качеством может быть признан ОСТ 42-510-98 "Правила организации производства и контроля качества лекарственных средств (GMP)", который разработан Минздравом России в 1998 году и рекомендован к внедрению на отечественных фармацевтических предприятиях.
Данный стандарт основан на международно признанных руководствах в данной области, главным образом, на документации GMP (Good Manufacturing Practic) Всемирной организации здравоохранения (ВОЗ). По определению ВОЗ, Правила GMP предназначены, в первую очередь, для снижения риска, присущего любой фармацевтической продукции. Это одна из немногих позиций глобального межгосударственного взаимодействия, где принята единая методология, основу которой составляет перенос акцента с контроля качества готовой продукции на обеспечение качества на всех этапах производства и реализации лекарственных средств.
Впервые требования GMP были сформулированы в 1963 г. в США. В последствии получили развитие в ряде других стран: в 1968 г. в Италии и Канаде, в 1969 г. - в Сингапуре и Швеции, в 1971 г. - в Австралии, Великобритании, Норвегии, Польше, в 1974 г. - на Филиппинах.
Следует отметить, что этому в значительной степени содействовала ВОЗ, которая уже в 1967 г. сформулировала, а в 1969 г. рекомендовала всем странам принять и применять международные правила организации производства и контроля качества ЛС1 . В дальнейшем эти правила были включены в дополнение ко II изданию Международной фармакопеи2 . Существенную поддержку развитию концепции GMP оказала также Международная федерация ассоциаций производителей лекарств (IFPMA), организовавшая в 1971 г. первый международный симпозиум по GMP . В настоящее время около 140 государств присоединились к Системе Всемирной организации здравоохранения (ВОЗ) удостоверения (сертификации) качества медикаментов в международной торговле, основанной на стандартах GMP.
В России с 1999 по 2004 г.г. Минздрав РФ выражал полное и непоколебимое желание полностью перейти на новые стандарты производства лекарств до начала 2005 г. Однако подобный переход не был подготовлен организационно и методически т.к. отсутствовал приемлемый вариант отечественного стандарта GMP, не была создана система инспектирования производств и др. Сейчас сроки внедрения стандарта GMP перенесены на 2009-2010 г.г.
Проведенный анализ стандартов GMP показывает, что в целом они базируются на необходимости устранения негативных моментов в производственном процессе, в результате учета тех факторов, которые могут нанести ущерб готовой продукции. Кроме того, в основе концепции GMP лежит понимание ограниченных возможностей контроля качества лекарственных средств путем лабораторных испытаний образцов готовой продукции. Подобные испытания рассматриваются лишь в качестве составной части общей системы гарантий качества лекарственных средств, обеспечиваемой в их производстве комплексом правил GMP. Правила GMP носят системный и предупреждающий характер. В сфере производства и общего управления фирмой требования GMP сводятся к положению, что производство лекарственных средств должно иметь все необходимые условия включая: квалифицированный персонал; достаточные и пригодные для работы помещения; соответствующее оборудование; надлежащие исходные материалы; утвержденные технологические регламенты и инструкции; подходящие условия складирования и транспорт; достаточные возможности и ресурсы для проведения контроля качества. При этом ключевые стадии производственных процессов четко определены, описаны и валидированы.
Система GMP требует четкого ведения документации. Так, например, все производственные операции протоколируются по мере их выполнения. Протоколы производственных операций и все данные по отгрузке сохраняются таким образом, чтобы можно было проследить движение каждой серии лекарственных средств. Предусматривается также необходимость анализа жалоб и рекламаций в отношении проданных лекарственных средств с целью принятия мер корректирующего характера.
Отечественный ОСТ 42-510-98 в целом базируется на основных положения GMP. Классификация помещений производства стерильных ЛС соответствует классификации GMP ЕС по количеству и наименованию классов чистоты, а также по допустимому содержанию в воздухе производственных участков механических частиц и микроорганизмов. Кроме того, документ содержит классификацию помещений производства нестерильных ЛС, что является весьма актуальным для отечественных фармацевтических предприятий, так как в настоящее время в стране организуется большое количество предприятий по производству таблеток, капсул, мазей и других нестерильных лекарственных форм.
Отечественный стандарт включает существенно переработанные и дополненный раздел "Процесс производства", в контексте подразделов "Документация", и "Валидация". При этом следует заметить, что впервые ссылка на правила GMP России содержится в руководстве ВОЗ5 именно в связи с разделом "Валидация".
Соответственно в ОСТ 42-510-98 введены ряд новых терминов и даны их международно признанные определения. В документе описаны понятия "Управление качеством" и "Система обеспечения качества".
Под управлением качеством (Quality Management) в фармацевтической промышленности понимается обеспечение надлежащего производства и контроля качества на всех этапах процесса производства лекарственных препаратов. Понятие управления качеством базируется на обеспечении качества, включающем аудит качества и правила правильного производства.  В соответствии с ОСТ 42-510-98 обеспечение качества представляет собой "широко распространенную концепцию, включающую мероприятия, которые оказывают влияние на качество готового продукта и гарантируют соответствие его требованиям нормативной документации". Система обеспечения качества включает в себя выполнение требований GMP, а также "Правила доклинической оценки безопасности фармакологических средств" ("Good Laboratory Practice" - GLP), "Правила клинических испытаний" ("Good Clinical Practice -GCP).
В соответствии с ОСТ 42-510-98 обеспечение качества представляет собой "широко распространенную концепцию, включающую мероприятия, которые оказывают влияние на качество готового продукта и гарантируют соответствие его требованиям нормативной документации". Система обеспечения качества включает в себя выполнение требований GMP, а также "Правила доклинической оценки безопасности фармакологических средств" ("Good Laboratory Practice" - GLP), "Правила клинических испытаний" ("Good Clinical Practice -GCP).
Система обеспечения качества предназначена того, чтобы фармацевтическое предприятие могло гарантировать, что:
- разработка, испытания и изготовление лекарственных препаратов приведены с учетом требований GMP, GLP,GCP;
- производство обеспечено утвержденными технологическими регламентами и методиками, инструкциями, учитывающими правила GMP;
- четко определена ответственность руководящего персонала за качество готового продукта, что должно быть установлено должностными инструкциями;
- контроль качества исходного сырья, вспомогательных, упаковочных и маркировочных материалов проведены на стадиях их изготовления и/или поставки и перед применением в производстве;
- проведена регистрация всех производимых контрольных испытаний сырья, вспомогательных упаковочных и маркировочных материалов, полуфабрикатов и готовых продуктов постадийного контроля процесса производства, калибровки приборов и валидация;
- готовый продукт произведен в соответствии с утвержденными технологическими регламентами;
- реализация готового продукта осуществлена только после получения соответствующего разрешения руководителя отдела контроля качества;
- имеется документация, позволяющая контролировать условия хранения продукта, сроки годности у производителя, а также при транспортировке и реализации.
Система аудита качества, включающая объекты контроля, контрольные операции и их последовательность, техническое оснащение, методы, средства механизации, автоматизации и компьютеризации контрольных операций, являются неотъемлемой частью производственного процесса.
Стандартом определено, что каждое фармацевтическое предприятие должно иметь отдел контроля качества (ОКК), который является самостоятельным и независимым структурным подразделением фармацевтического предприятия. Установлены основные требования, предъявляемые к ОКК, среди которых требования к персоналу, оборудованию, документации, видам и методам контроля.
Составной частью системы обеспечения качества на фармацевтическом предприятии являются "Правила правильного производства (GMP", которые гарантируют, что производство и контроль осуществляются на предприятии согласно требованиям соответствующей документации. "Правила..." позволяют минимизировать риск производственных ошибок, которые не могут быть устранены или предотвращены только посредством контроля качества продукта. При этом выделяют наиболее часто встречающиеся ошибки: перекрестная контаминация и смешивание и/или перепутывание готовых продуктов.
Соответственно "Правила..." предусматривают четкую регламентацию всех производственных процессов и контроля процесса для подтверждения его пригодности для выпуска готовых лекарственных средств требованиям качества; проведение валидации всех стадий производства, которые могут оказывать влияние на качество продуктов и всех существенных изменений в нем; соответствующее ресурсное обеспечение процесса производства (персонал, оборудование, помещение, сырье и т.д.); наличие документации, подтверждающей выполнение требований к качеству производственного процесса и готовых продуктов; хранение и реализацию готового продукта таким образом, чтобы свести к минимуму возможность риска снижения качества.
Кроме того, в "Правилах..." важное место отводится работе, связанной с анализом возможных отклонений, причин снижения качества. Так, определено, что на фармацевтическом предприятии необходимо проводить "регистрацию всех этапов производства, подтверждающую, что все требуемые операции были выполнены, а полученные продукты по количеству и качеству соответствуют установленным требованиям. Все отклонения должны быть тщательно зарегистрированы и изучены. При необходимости должен быть определен порядок возврата любой серии готового лекарственного средства , продажи или поставки с последующим анализом причин нарушения его качества с целью предупреждения повторения выявленных ошибок".
Таким образом, давая в целом положительную оценку вышеизложенным положениям отечественного стандарта, следует отметить, что, преследуя в целом аналогичные цели и задачи, отечественный отраслевой стандарт отклоняется от международных правил GMP по значительному числу требований. Это признается и в самом отраслевом стандарте, в котором отмечается, "что в полном объеме требования, предъявляемые к производству лекарственных средств, должны быть изложены в специальных нормативных документах". Наиболее существенное отставание касается отсутствия связи между правилами GMP, изложенными в ОСТ, регистрационной и лицензионной документацией; использованием концепции "Специалиста ответственного за качество" ("Authorized Person" по терминологии ВОЗ); отсутствием требования по информированию профильных национальных государственных органов о возникновении проблем с качеством, а также зарубежных стран, куда могла быть направлена отзываемая продукция. Следует заметить, что эти проблемы не находят достаточного развития и в последующих специальных нормативных документах, регламентирующих реализацию (ОСТ) 42-510-98. Например, Методические указания "Производство лекарственных средств. Система документации. Примерные формы и рекомендации по заполнению", введенные в действие приказом Министерства промышленности, науки и технологий Российской Федерации в 2002 году.
Многие из элементов GMP предприятия могут и должны внедрять при имеющейся материально-технической базе и ограниченных финансовых ресурсов. Следует отметить, что для успешного внедрения ОСТа 42-510-98 на отечественных фармацевтических предприятиях, в первую очередь, необходимо создать или пересмотреть существующие документы по строительному проектированию, по организации производства стерильных и нестерильных ЛС, по валидации, инспектированию и лицензированию фармацевтических производств, положение об Уполномоченном лице, а также организовать обучение сотрудников, как фармацевтических предприятий, так и инспектирующих организаций. При этом, очевидно, следует согласовать основные положения ОСТа с таковыми разрабатываемых документов и Федерального закона "О лекарственных средствах" с тем, чтобы содержащиеся в них терминология и используемая методология организации фармацевтического производства были едины. Для проведения указанной выше работы необходимо привлечь специалистов различных организаций и ведомств, занимающихся рассматриваемыми вопросами.
В целом же внедрение (ОСТ) 42-510-98 на российских фармацевтических предприятиях осуществляется крайне медленно, что объясняется рядом причин. Так, следует отметить весьма распространенную точку зрения руководителей фармацевтических предприятий о необходимости значительных средств для модернизации и реконструкции производств, которые потребуются в связи с введением GMP. Соответственно, высказываются опасения о росте себестоимости, а, следовательно, и цен на отечественные лекарственные средства и снижению их конкурентоспособности в соответствии с зарубежными аналогами. В определенной мере связанной с этой точкой зрения является и другая позиция отечественных производителей, которая представляет GMP как некое нововведение придуманное "акулами фармацевтического рынка", с целью устранения конкурентов в лице российских производителей и расширения границ собственного влияния.
Подобная ситуация требует изменения менталитета всех участников процесса производства лекарственных средств: от лиц принимающих решения до исполнителей любого уровня и, соответственно, осознания неизбежности перехода к работе в рамках Правил GMP в кратчайшие, реально возможные, сроки. Учитывая данную ситуацию, Минздрав РФ и Министерство экономического развития и торговли РФ разработали программу действий по внедрению GMP, предусматривающую запрещение выдачи лицензий на фармацевтическое производство с 1 июля 2000 года, для вновь открываемых предприятий, не готовых работать в рамках установленных требований.
Между тем ситуация с качеством лекарственных средств, находящихся в обращении на российском фармацевтическом рынке, остается неблагополучной. По данным Департамента государственного контроля качества, эффективности, безопасности лекарственных средств и медицинской техники Минздрава России в 2005 году контролирующими органами из обращения было изъято 1644 серии недоброкачественных препаратов, из них 65% производства России, за 1 полугодие 2006 года - 1064 серии, из них 61 % отечественного производства.
При анализе рекламаций на качество препаратов, предъявленных производителям в 2005 году, установлено, что наиболее часто инъекционные препараты не соответствуют установленным требованиям по показателю "Механические включения", "Описание", "Цветность"; твердые лекарственные формы - по показателям "Описание", "Маркировка", "Количественное содержание"; мягкие лекарственные формы - по показателям "Описание" и "Количественное содержание". 63,8 % всех рекламаций на качество отечественных лекарственных средств являются результатом производственных ошибок7 .
Анализ нарушений, выявляемых при инспектировании предприятий, показывает, что все проблемы, связанные с качеством вызваны:
- снижением производственной дисциплины;
- низким качеством производственной документации;
- плохой организацией производственного процесса;
- отсутствием у ОТК достаточных материально-технических средств, полномочий при выборе поставщика сырья и упаковочных материалов, по регулярной проверке технологической дисциплины на производстве и т.д.
Внедрение и последующая реализация правил GMP позволит в значительной мере ликвидировать эти проблемы, что, в свою очередь, будет способствовать улучшению качества лекарственных средств в Российской Федерации. Между тем каждое предприятие должно реально оценить свои возможности и составить собственную программу по введению в практику ОСТ 42-510-98 (GMP). Как показывает практика, это достаточно сложная задача для российских фармацевтических предприятий, большинство из которых не имеют достаточно квалифицированных кадров для проведения данной работы.
Введение и соблюдение на предприятиях фармацевтической промышленности интегрированной системы менеджмента качества, построенной на основе согласования требований международных правил GMP и NfC ИСО серии 9000:2000 позволит обеспечить экономически эффективное производство лекарственных средств на современном уровне и гарантировать их высокое качество.
Следует заметить, что Госстандартом России зарегистрирована и внесена в Государственный реестр Система добровольной сертификации систем менеджмента качества производителей лекарственных средств Минздрава России "ЛЕКСИСТЕМС" и знак соответствия системы (св етельство о государственной регистрации от 26.11.2002 года № РОСС RU.0014.03JIC00).В соответствии с приказом Министерства здравоохранения Российской Федерации от 25.11.2002 года № 354 "Об организации работы по проведению сертификации лекарственных средств в Системе сертификации ГОСТ Р" выполнение обязанностей Органа по сертификации Системы "ЛЕКСИСТЕМС" возложено на ФГУ "Центр сертификации Минздрава России".
В обязанности Органа по сертификации Системы "ЛЕКСИСТЕМС" входит проведение работы по сертификации систем менеджмента качества предприятий - производителей лекарственных средств на соответствие требованиям стандартов ГОСТ Р ИСО серии 9000, ОСТ 42-510-98 "Правила организации производства и контроля качества лекарственных средств", с учетом международных правил организации производства и контроля качества лекарственных средств. Данная деятельность осуществляется на добровольной основе по договору с каждым заявителем.
Сертификаты соответствия на системы менеджмента качества и производства, выданные в Системе "ЛЕКСИСТЕМ", признаются Госстандартом России и применяются без переоформления при выдаче сертификатов соответствия на лекарственные средства, прошедшие обязательную сертификацию в соответствии с "Правилами проведения сертификации в Системе сертификации лекарственных средств Системы сертификации ГОСТ Р" (утверждены Постановлением Госстандарта России от 24.05.2002 года № 36, зарегистрированы МшШсг ом России 9.07.2002 года, регистрационный № 3556) по схеме 5. Данное положение закреплено Соглашением о признании сертификатов со-ответствия на системы менеджмента качества между Госстандартом России и Минздравом России, подписанным 22.11.2002 года.
Таким образом, на данном этапе фармацевтические предприятия могут сертифицировать интегрированную систему управления качеством с выдачей двух сертификатов, на соответствие ГОСТ Р ИСО серии 9000 и ОСТ 42-510-98.
Однако, данный проект создания и сертификации системы управления качеством является достаточно дорогостоящим. В этой связи, такой сценарий является приемлемым для крупных фармацевтических предприятий, ориентированных на экспортную продукцию, работающих с крупными зарубежными заказчиками в России, принимающими участие в тендерах, конкурсах и прочих подобных мероприятиях. Кроме того, внедрение интегрированной системы управления качеством позволит создать дополнительные конкурентные преимущества для повышения своего имиджа на внутреннем рынке.
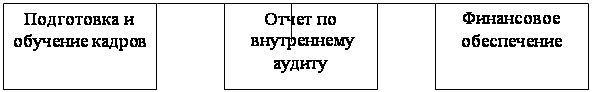
Для малый и средних предприятий, выпускающие лекарственные средства (фармацевтические субстанции), представляется целесообразным формирование системы управления качеством, основанной на ОСТ 42-510-98 (GMP). На рисунке представлен алгоритм реализации ОСТ 42-510-98 "правила организации производства и контроля качества лекарст-венных средств (GMP)".
 |  |
Рисунок - Алгоритм реализации ОСТ 42-510-98 "Правила организации производства и аудита качества лекарственных средств (GMP)" на фармпредприятии
 В соответствии с требованиями ОСТ 42-510-98 (GMP) необходимо разработать план внедрения, которому предшествует внутренний аудит, который проводится предприятием самостоятельно. При этом крайне важно получить реальную картину положения дел, что должно быть отражено в отчете по внутреннему аудиту.
В соответствии с требованиями ОСТ 42-510-98 (GMP) необходимо разработать план внедрения, которому предшествует внутренний аудит, который проводится предприятием самостоятельно. При этом крайне важно получить реальную картину положения дел, что должно быть отражено в отчете по внутреннему аудиту.
Основной целью внутреннего аудита является оценка соответствия производителя требованиям GMP по всем аспектам технологического процесса и контроля качества. Внутренний аудит позволяет руководству предприятия проанализировать процесс производства и выявить скрытые дефекты и явные проблемы.
Основными задачами внутреннего аудита на фармацевтическом предприятии являются:
1. Собственно контроль. Внутренний аудит, организованный надлежащим образом на постоянной основе, способствует выявлению недостатков и поддержанию должных условий производства и достижению заданного качества продукции фармацевтического производства.
Похожие работы
... -аудит баланса Согласно П(с)БУ 2 "Баланс" - это отчет о финансовом состоянии предприятий, который отражает его активы и пассивы. Экспресс-аудит баланса – оперативно полученная информация о финансовом состоянии предприятия и заключения в быстром подтверждении достоверности отражения в балансе данных о финансово-хозяйственных операциях. Источники проверки: Баланс (форма № 1), Главная книга, ...
... и законность списания доходов и расходов на счета, учитывающие финансовые результаты хозяйственной деятельности. Финансовый результат от прочей реализации включает результаты от реализации основных средств, товарно-материальных ценностей, нематериальные активы, ценные бумаги и др. Аудит финансовых результатов от прочей деятельности предполагает рассмотрение этих операций по существу, с точки ...
... организации («третьей стороны»). В силу этого заключения внешних специалистов, не подверженные воздействию местных факторов и обычаев, являются более объективными. Вместе с тем внешний аудит системы качества обладает по сравнению с внутренним не только достоинствами, но и недостатками, что видно из сопоставления его «плюсов» и «минусов». Внешний аудит в отличие от внутреннего проводится только ...
... и др. Для достижения поставленной цели аудиторы должны решить следующие задачи: установить соответствие организационной структуры бухгалтерии и формы бухгалтерского учета условиям функционирования организации и управления предприятием; охарактеризовать системы документации и документооборота; дать оценку учетной политики организации и проверить порядок ее соблюдения. Объем учетной работы ...
0 комментариев