Навигация
Процессы горения топлива
5.2 Процессы горения топлива
Горение топлива - химический процесс соединения горючих веществ топлива с кислородом воздуха, который сопровождается интенсивным выделением теплоты.
Процессы горения могут быть гомогенными и гетерогенными. Если топливо и окислитель (кислород) находятся в газообразном состоянии и образуют гомогенную смесь, то горение протекает в объеме и называется гомогенным. При гетерогенном горении топливо и окислитель находятся в различных агрегатных состояниях, реакции протекают на поверхности раздела фаз: твердой, жидкой и газообразной. Процесс горения топлива условно можно разделить на две стадии: воспламенение и последующее горение. При нагревании топлива происходит повышение температуры. При достижении определенной для каждого топлива температуры (температуры воспламенения) топливо воспламеняется, после чего начинается процесс устойчивого горения.
Расход воздуха. Теоретическое количество воздуха, необходимое для сгорания топлива, определяется по формулам горения составных элементов топлива. Так, для сгорания 1 кг углерода необходимо 32/12 = 8/3 = 2,67 кг кислорода, так как реакция горения углерода протекает следующим образом:
![]()
Для сгорания 1 кг водорода требуется 8 кг кислорода:
![]() ;
;
для сгорания 1 кг серы — 1 кг кислорода:
![]() .
.
Если учесть, что массовая доля содержания кислорода в воздухе равна 0,232, то теоретически необходимое количество воздуха для сгорания 1 кг твердого и жидкого топлива при нормальных условиях (в кг воздуха на кг топлива)
![]() .
.
Так как при нормальных условиях плотность воздуха ![]() , то объемный расход воздуха
, то объемный расход воздуха ![]() для сгорания 1 кг топлива
для сгорания 1 кг топлива
![]()
или
![]()
где ![]() — элементарный состав топлива на рабочую массу, %.
— элементарный состав топлива на рабочую массу, %.
В выражении ![]() коэффициенты m и n принимаются равными значениям индексов тех газов, перед которыми стоят эти коэффициенты.
коэффициенты m и n принимаются равными значениям индексов тех газов, перед которыми стоят эти коэффициенты.
Практически при горении часть кислорода воздуха не участвует в химических реакциях, поэтому для полного сгорания топлива подводят воздуха больше, чем необходимо теоретически. Отношение действительного количества воздуха (![]() ), подводимого в процессе горения, к теоретически необходимому (
), подводимого в процессе горения, к теоретически необходимому (![]() ), называется коэффициентом избытка воздуха
), называется коэффициентом избытка воздуха
![]()
Состав продуктов сгорания. Условно считают, что продукты сгорания топлива (в м3/кг)
![]()
где ![]() — сухие газы;
— сухие газы; ![]() — водяные пары.
— водяные пары.
Объем сухих газов
![]()
где ![]() .
.
При ![]() = 1 объем сухих газов минимальный, т.е.
= 1 объем сухих газов минимальный, т.е. ![]() . Если
. Если ![]() > 1, то
> 1, то
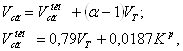
где 0,79![]() — объем азота в теоретически необходимом количестве воздуха; 0,0187
— объем азота в теоретически необходимом количестве воздуха; 0,0187 ![]() — объем трехатомных газов
— объем трехатомных газов
![]() .
.
Объем продуктов сгорания газообразного топлива определяется по той же формуле, что и для твердого или жидкого. При этом
![]() .
.
При ![]() = 1
= 1
![]()
где ![]() — влагосодержание газообразного топлива. При
— влагосодержание газообразного топлива. При ![]() > 1
> 1
![]()
Объем сухих газов при ![]() > 1
> 1
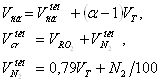 .
.
При атмосферном давлении с учетом температуры газов объем продуктов сгорания
![]() .
.
Состав продуктов сгорания определяется с помощью газоанализаторов.
Энтальпия продуктов сгорания. Энтальпия (теплосодержание) продуктов сгорания топлива определяется суммированием теплосодержаний отдельных составляющих дымовых газов и зависит от вида топлива (твердое, жидкое или газообразное). Энтальпия имеет размерность кДж/кг или кДж/м3 и равна
![]()
Энтальпия теоретического объема газов (![]() = 1) при температуре
= 1) при температуре ![]()
![]()
![]()
Энтальпия продуктов сгорания при ![]() > 1 больше чем
> 1 больше чем ![]() (т. е. при
(т. е. при ![]() = 1)
= 1)
![]()
![]()
Где ![]() — энтальпия теоретически необходимого воздуха
— энтальпия теоретически необходимого воздуха
![]() кДж/кг или кДж/м3;
кДж/кг или кДж/м3;![]() — энтальпия дополнительного объема водяных паров
— энтальпия дополнительного объема водяных паров
![]() кДж/кг или кДж/м3;
кДж/кг или кДж/м3;
![]() — энтальпия золы
— энтальпия золы
![]() кДж/кг,
кДж/кг,
где ![]() — доля золы топлива, уносимая газами из топки;
— доля золы топлива, уносимая газами из топки; ![]() — соответственно теплоемкости при постоянном давлении трехатомных газов, азота, водяных паров, воздуха и золы при температуре
— соответственно теплоемкости при постоянном давлении трехатомных газов, азота, водяных паров, воздуха и золы при температуре![]() .
.
Рабочий состав доменного газа, %:
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() .
.
Таблица 1. Состав рабочего доменного газа.
| Газ | СН4 | СО2 | H2 | CO | N2 | H2O | ∑ |
| Доменный | 0,285 | 12,039 | 1,337 | 25,596 | 55,553 | 5,19 | 100 |
Определение теплоты сгорания газов ![]() .
.
Природного газа:
![]() .
.
Доменного газа:
![]() .
.
Расчет состава смеси природного и доменного газов.
Принимаем долю доменного газа в природно-доменной смеси (ПДС) за x, тогда доля природного газа будет равна y = (1-x). Составляем уравнение:
![]() ,
,
где ![]() – исходная теплота сгорания смеси газов, МДж/м3.
– исходная теплота сгорания смеси газов, МДж/м3.
Находим, что
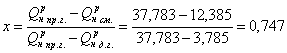 Мдж/м3.
Мдж/м3.
у = (1-х) = 1-0,747 = 0,253.
Состав смешанного газа, %.
![]() ;
;
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Похожие работы
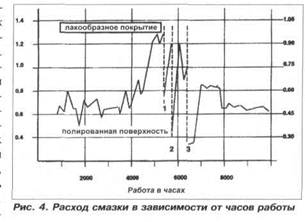
... тери эффективности смазки может производиться по величине толщины лакообразующих отложений в канавках втулки после 1000 час. работы двигателя и расходу смазки, который не должен превышать 0,2 ррт сгоревшего топлива. На рис. 4 показано влияние лакообразующего нагара на эффективность смазывания и расход смазки по результатам экспериментальных исследований на двигателе голланд ...
... направленного на сердцевину со стороны вентилятора. При То-1, кроме работ по ежедневному техническому обслуживанию, проверить и при необходимости подтянуть крепления всех деталей системы охлаждения двигателя (радиатора, жидкостного насоса, вентилятора, жидкостных патрубков и шлангов). Смазать трущиеся детали жидкостного насоса, вентилятора с помощью нагнетательного насоса через пресс-масленки ( ...
... его измеряют в кубических сантиметрах или метрах): где D - диаметр цилиндра. Отношение полного объема цилиндра Va к объему камеры сгорания Vc называется степенью сжатия: Степень сжатия является важным параметром двигателей внутреннего сгорания, т.к. сильно влияет на его экономичность и мощность. Все перечисленные характеристики двигателя прорционально зависят от размера и объема ...
... используется в паровых турбинах и т.д. Все это в свою очередь нашло широкое распространение в различных отраслях народного хозяйства. Например, двигатели внутреннего сгорания наиболее широко используются на транспортных установках и сельскохозяйственных машинах. В стационарной энергетике двигатели внутреннего сгорания широко используются на небольших электростанциях, энергопоездах ...

0 комментариев