Навигация
Общие вопросы радионуклидной диагностики
Днепропетровская государственная медицинская академия
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ № 8
"Общие вопросы радионуклидной диагностики "
Вступление
Первое применение радиоактивных индикаторов относят к 1911 году и связывают с именем Дьердя де Хевеши. Молодой ученый, живший в дешевом пансионе, начал подозревать, что остатки пищи, которые он не доел, подавали ему вновь на следующий день. Он добавил радиоизотопный индикатор к несъеденной порции и с помощью детектора излучения доказал своей хозяйке, что дело обстояло именно так. Хозяйка выгнала молодого ученого из пансиона. Он же продолжал начатую работу, результатом которой стала Нобелевская премия за использование радионуклидов в качестве индикаторов в биологии.
Радионуклидная (радиоизотопная) диагностика охватывает все виды применения открытых радиоактивных веществ в диагностических и лечебных целях.
В зависимости от конкретного вида исследования в настоящее время различают лабораторные и клинические радиологические методы, а также радиоизотопное сканирование.
В первом случае изучается скорость накопления или выведения вещества определенным органом, что отражает сохранность функционирования данного органа в целом.
Радиоизотопное сканирование позволяет отчетливо определить границы органа, размеры, форму, расположение, а также оценить распределение вещества в ткани органа, выявить гиперфункциональные «теплые» и «холодные» узлы, определить новообразования и др.
Методы диагностики, основанные на регистрации излучения радиоактивных изотопов и меченых соединений, введенных в организм больного принято называть – радионуклидная диагностика in vivo .
Суть его состоит в том, что после введения меченого вещества оно распределяется по телу человека в зависимости от функционирования его органов и систем. Регистрируя распределение, перемещение, превращение и выведение из организма радиактивных индикаторов, врач получает возможность судить об участии соответствующих элементов в биохимических и физиологических процессах. Современная аппаратура позволяет зарегистрировать ионизирующее излучение крайне малого количества радиоактивных соединений, которые практически безвредны для организма исследуемого.
Возможность получения искусственных радиоактивных изотопов позволила расширить сферу применения радиоактивных индикаторов в различных отраслях науки, в том числе и в медицине. Радионуклидная визуализация основана на регистрации излучения, испускаемого находящимся внутри пациента радиоактивным веществом. Таким образом, общее между рентген- и радионуклидной диагностикой – использование ионизирующего излучения. Радиоактивные вещества, называемые радиофармацевтическими препаратами (РФП), могут использоваться как в диагностических, так и в терапевтических целях. Все они имеют в своем составе радионуклиды – нестабильные атомы, спонтанно распадающиеся с выделением энергии. Идеальный радиофармпрепарат накапливается только в органах и структурах, предназначенных для визуализации. Накопление РФП может обусловливаться, например, метаболическими процессами (молекула-носитель может быть частью метаболической цепочки) либо локальной перфузией органа. Возможность изучения физиологических функций параллельно с определением топографо-анатомических параметров – главное преимущество радионуклидных методов диагностики. Для визуализации используют радионуклиды, испускающие гамма-кванты, так как альфа- и бета-частицы имеют низкую проникающую способность в тканях. В зависимости от степени накопления РФП различают «горячие» очаги (с повышенным накоплением) и «холодные» очаги (с пониженным накоплением или его отсутствием).
РАДИОНУКЛИДНАЯ ДИАГНОСТИКА (син. радиоизотопная диагностика) - распознавание патологических изменений органов и систем человека с помощью радиофармацевтических препаратов, в которые входят соединения, меченные радионуклидами (радиоизотопами).
Регистрация введенных в организм радиоактивных веществ осуществляется с помощью методов сцинтиграфии, сканирования, радиометрии, радиографии.
Сцинтиграфия является наиболее распространенным способом радионуклидной диагностики.
Сцинтиграфия позволяет получать изображение органа и по нему судить о его размерах и форме, выявлять очаг патологии в виде участка повышенного или пониженного накопления радионуклида, оценивать функциональное состояние органа по скорости накопления и выведения радиофармпрепарата.
Сцинтиграфия – самый распространенный метод радионуклидной визуализации. Исследование проводится с помощью гамма-камеры. Основным ее компонентом является дисковидный сцинтилляционный кристалл йодида натрия большого диаметра (около 60 см). Этот кристалл является детектором, улавливающим гамма-излучение, испускаемое РФП. Перед кристаллом со стороны пациента располагается специальное свинцовое защитное устройство – коллиматор, определяющий проекцию излучения на кристалл. Параллельно расположенные отверстия на коллиматоре способствуют проецированию на поверхность кристалла двухмерного отображения распределения РФП в масштабе 1:1. Гамма-фотоны при попадании на сцинтилляционный кристалл вызывают на нем вспышки света (сцинтилляции), которые передаются на фотоумножитель, генерирующий электрические сигналы. На основании регистрации этих сигналов реконструируется двухмерное проекционное изображение распределения РФП. Окончательное изображение может быть представлено в аналоговом формате на фотопленке. Однако большинство гамма-камер позволяет создавать и цифровые изображения. Большинство сцинтиграфических исследований выполняются после внутривенного введения РФП (исключение – вдыхание радиоактивного ксенона при ингаляционной сцинтиграфии легких). При перфузионной сцинтиграфии легких используются меченные 99mТс макроагрегаты альбумина или микросферы, которые задерживаются в мельчайших легочных артериолах. Получают изображения в прямых (передней и задней), боковых и косых проекциях. Сцинтиграфия скелета выполняется с помощью меченных Тс99m дифосфонатов, накапливающихся в метаболически активной костной ткани. Для исследования печени применяют гепатобилисцинтиграфию и гепатосцинтиграфию. Первый метод изучает жёлчеобразовательную.и желчевыделительную функцию печени и состояние желчевыводящих путей – их проходимость, накопительную и сократительную способность желчного пузыря, и представляет собой динамическое сцинтиграфическое исследование. В его основе лежит способность гепатоцитов поглощать из крови и транспортировать в составе желчи некоторые органические вещества. Гепатосцинтиграфия – статическая сцинтиграфия - позволяет оценить барьерную функцию печени и селезенки и основана на том, что звездчатые ретикулоциты печени и селезенки, очищая плазму, фагоцитируют частички коллоидного раствора РФП. С целью исследования почек используются статическая и динамическая нефросцинтиграфия. Суть метода заключается в получении изображения почек благодаря фиксации в них нефротропных РФП.
Метод позволяет выявлять нарушения функции почек в начальных стадиях заболевания. На сцинтиграммах и сканограммах патологический. процессы в паренхиме почек выглядят как участки пониженного накопления радионуклидов. Введение радиофармпрепаратов в кровеносное русло и наблюдение за продвижением их с помощью гамма-камеры дает возможность исследовать кровоток в различных отделах сердечно-сосудистой системы.
Основной визуализирующей аппаратурой современной радионуклидной диагностики являются гамма-камера и гамма-томограф для однофотонной эмиссионной компьютерной томографии (ОФЭКТ). Большие перспективы имеет развитие методов ПЭТ-диагностики.
Классификация видов томографии
Взаиморасположение источника зондирующего излучения, объекта и детектора
С точки зрения взаиморасположения источника зондирующего излучения, объекта и детектора томографические методы могут быть разделены на следующие группы:
трансмиссионные — регистрируется зондирующее внешнее излучение, прошедшее через пассивный (неизлучающий) объект, частично ослабляясь при этом;
эмиссионные — регистрируется излучение, выходящее из активного (излучающего) объекта с некоторым пространственным распределением источников излучения;
комбинированные трансмиссионно-эмиссионные (люминесцентные, акустооптические и оптоакустические и др.) — регистрируется вторичное излучение от источников, распределенных по объему объекта и возбужденных внешним излучением;
эхозондирование — регистрируется зондирующее внешнее излучение, отраженное от внутренних структур пассивного объекта.
Развитие методов радионуклидной диагностики представляет собой увлекательное сочетание развития радиофармацевтики и физических методов регистрации ионизирующих излучений. Искусственные радионуклиды появились лишь после изобретения в 1931 г. Лоуренсом циклотрона, а первым в 1938 г. на циклотроне в Беркли был синтезирован радионуклид 99Тсm. Но эра ядерной медицины наступила вслед за пуском первого ядерного реактора (1942 г.) с момента начала поставок радиоактивных изотопов потребителям в 1946 г.
Методы получения изображений с помощью радиофармпрепаратов начали развиваться (не считая более раннего периода развития детекторов и методов регистрации излучений) с 1948 г., когда Энселл и Ротблат осуществили поточечную регистрацию изображения щитовидной железы. Затем последовал период интенсивного развития этих методов, который можно условно разбить на следующие этапы: автоматическое сканирование, гамма-камера, однофотонная эмиссионная компьютерная томография (ОФЭКТ), позитронная эмиссионная томография (ПЭТ). Процесс развития шел непрерывно и не всегда возможно назвать одного изобретателя того или иного аппарата, но можно назвать тех, кто внес основной вклад.
Так, методы сканирования начались в 1950-1951 г.г. с работ Кассена и Мейниорда. Идея гамма-камеры (1949) принадлежит Коупленду и Бенжамину, а основной вклад в развитие этого метода и создание принципиально новых приборов начиная с 1952 г. внесли Энгер и Мэллард.
В последующие годы, используя гамма-камеру Anger как прототип, ведущие мировые производители медицинского оборудования предложили на рынок множество самых разнообразных моделей этого аппарата. Гамма-камера дает возможность для одномоментной регистрации излучения инкорпорированного РФП без перемещения детектора над пациентом. Этим гамма-камера выгодно отличается от изобректенных ранее сканеров, которые позволяют получить картины пространственного распределения РФП лишь за счет механического перемещения детектора с тяжелой защитой, что делает невозможной визуализацию быстропротекающих физиологических процессов. Современные гамма-камеры, оснащенные специализированным или универсальным компьютером, обеспечивают хорошее пространственное разрешение и высокую скорость регистрации излучения.
Развитие однофотонной эмиссионной компьютерной томографии (ОФЭКТ) на первом этапе связано с именами: Кул и Эдвардс (1963-1964 г.г.), Мюленер и Боули с соавторами (1971-1977 г.г.). Сегодня гамма-камеры и ОФЭКТ имеют очень большое распространение в мире (десятки тысяч) и широкие диагностические возможности.
Ядерная медицина – это область медицинской практики, в которой для диагностики используют открытые радиофармацевтические препараты. Основная часть такой диагностики включает два различных подхода:
Исследования «in vivo», при которых радиоактивные вещества вводят в организм пациента как для оценки функции органа, так и для получения его изображения;
Исследования «in vitro», которые проводятся с помощью радиоиммунологического анализа (или родственных способов) без введения радиоактивных веществ в организм пациента.
Смысл радионуклидных диагностических исследований заключается в изучении как статических, так и биокинетических процессов в организме. Последним они принципиально отличаются от рентгеновской диагностики и, благодаря именно этому качеству в медицине существует потребность в данном виде диагностики, несмотря на определенные лучевые нагрузки на персонал и пациентов при проведении радионуклидных исследований.
Общее между рентгенологическими исследованиями и радионуклидной диагностикой - использование ионизирующего излучения. Все рентгенологические исследования, включая КТ, базируются на фиксации прошедшего через тело пациента, т.е. пропущенного, излучения. В то же время радионуклидная визуализация основана на регистрации излучения, испускаемого находящимися внутри пациента радиоактивным веществом.
РФП могут использоваться как для диагностических, так и для терапевтических целей. Все они имеют в своем составе радионуклиды - нестабильные атомы, спонтанно распадающиеся с выделением энергии. При синтезе РФП радионуклид соединяется с молекулой-носителем, определяющей его распределение в организме. Идеальный РФП распространяется в организме только в пределах, предназначенных для визуализации определенных органов и структур. Запись характеристик радиоактивности может в дальнейшем предоставить важную функциональную информацию. Способность изучения физиологических функций главное преимущество радионуклидной визуализации по сравнению с альтернативными радиологическими методиками. Относительный недостаток - низкое пространственное разрешение.
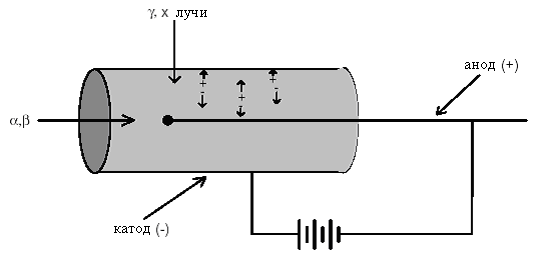
В идеальном случае период полураспада радионуклида должен быть примерно равен 1/3 продолжительности исследования, которая находится в диапазоне от десяти минут до нескольких часов. Это должно ограничить наличие существенной радиоактивности рамками обследования, без чрезмерного воздействия излучения на пациента после его завершения. Процесс радиоактивного распада может сопровождаться испусканием альфа-, бета-, или гамма-лучей. Для целей визуализации предпочтительнее использовать радионуклиды, испускающие гамма-кванты (высокоэнергетическое электромагнитное излучение). Альфа -частицы (ядра гелия) и бета-частицы (электроны) не используются для целей визуализации из-за плохого прохождения через ткани. Подобно рентгеновским лучам, проникающая способность гамма-излучения возрастает с увеличением энергии фотонов. С другой стороны, энергия не должна быть чрезмерно велика, чтобы фотоны не проходили через детектор без поглощения. Для радионуклидной визуализации предпочтительна энергия в диапазоне 50-300 кэВ, идеальная энергия 150 кэВ.
РНДИ основаны на использовании радиоизотопных индикаторов в медицинских целях, для чего применяются РФП – меченые радиоизотопом химические соединения. Они либо вводятся непосредственно в организм пациента (in vivo), либо смешиваются в пробирках с биологическими реагентами пациента (in vitro). В том и другом случае количество введенного препарата незначительно, но современная аппаратура (гамма-камера) позволяет измерять даже малые количества радиоактивности и с помощью компьютера расшифровывает полученное изображение, точно указывая местонахождение патологического очага. Это и разнообразные функциональные возможности позволяют РНДИ осуществлять своевременную диагностику на ранних стадиях развития болезней, оставаясь в ряде случаев единственным средством получения необходимой диагностической информации
В клинической практике все большее значение приобретают мало травматические средства определения состояния разных органов и систем организма, такие как иммуноферментный и радио иммунологический (РИА) анализы. Клиницистов привлекает безопасность и высокая информативность РИА. Этот очень точный и чувствительный метод (что обусловлено принципом иммунологических реакций), не связанный с лучевой погрузкой на пациента, который дает возможность проводить такие исследования в динамике всем категориям пациентов.
Среди радиофармацевтических препаратов, используемых в ядерной медицине, значительная часть приходится на генераторные, в частности, технеций-99м. Использование подобных короткоживущих радионуклидов обеспечивает заметное снижение дозы облучения пациентов, но при этом возрастают дозы на обслуживающий персонал. К МРП относятся радиоактивные фармацевтические препараты (РФП) (табл. 1), используемые при проведении радионуклидных диагностических исследований (РНДИ).
К МРИ относятся изделия, в конструкциях которых применяются радиоактивные источники ионизирующего излучения, используемые для проведения терапевтических процедур (табл. 2).
Группы РФП. Требования к РФП. Принципы использования в диагностике
Химические свойства разных изотопов одного элемента однотипны. Таким образом, как обычный химический элемент, так и его изотопы принимают одинаковое участие в биохимических реакциях организма.
Для медицинских целей используются не только "чистые" изотопы, но и их химические соединения с различными веществами. По этому правильно называть эти соединения радиофармацевтическими препаратами (РФП), в молекуле которых содержится радионуклид и химическое вещество которое разрешено для введения человеку с диагностическою или лечебною целью. Радионуклид должен излучать определенный спектр энергии, обусловливать минимальное облучение и отображать состояние исследуемого организма.
А) Методы синтеза РФП.
I. Первый метод - когда радионуклиды как химические элементы получают з продуктов распада урана в атомных реакторах.
Известно более 60 первичных продуктов распада 235U под влиянием нейтронов, большинство которых являются радиоактивными. Например:
235U (n, f)® 99Моb- ®99mТс.
а) путем облучения гамма-лучами, заряженными частицами (протонами) или нейтронами стабильных химических элементов, которые в результате облучения становятся радиоактивными;
б) облучения нейтронами (наиболее распространенный метод):
99Мо+ 1n = 99mMoβ-
Образованные в результате реакции нуклиды являются изотопами мишени:
15 31Р + o1n = 3215P + гамма-квант;
в) Образованные радионуклиды не являются изотопами мишени:
147N+o1n=148C+11p.
Для выделения и очистки радионуклидов используются физические или химические методы.
После облучения в реакторе изотопы получают в твердом состоянии, а в ускорителях - в газообразном или в жидком состоянии. Потом радионуклиды в состоянии простых соединений, например Na131I - йодида натрия или H332РO4 - фосфорнокислого натрия, вводятся путем химического, биохимического или биологического синтеза в большие молекулы в качестве радиоактивной метки (поэтому эти препараты еще называются мечеными). Пометить соединение можно также путем замещения стабильного элемента в молекуле на радиоактивный или путем биологического синтеза. Например, водород можно заместить без химической реакции если добавить к стабильному препарату радиоактивный тритий.
Получение трития:
63Li + о1n = 31Н + 24Не.
При биологическом синтезе к среде в которой культивируются микроорганизмы добавляют, например, радиоактивную серу. Микроорганизмы ее усваивают и вводят в процессе обмена веществ в состав метионина.
II. Второй метод получения радионуклидов - циклотронный.
а) реакция (d, п) - при облучении дейтронами из ядер мишени реализуются нейтроны и получаются гамма излучающие радионуклиды трех наиболее важных элементов углевода, азота, кислорода. Все они имеют малый период полураспада (от 2-х до 30-ти минут):
N14(d, n)® O15;
б) реакция (а, рп) - облучение α-частицами. При их взаимодействии образуются две частицы (нейтрон и протон):
О16(а, pn)®F18;
в) реакция (а, 2п) - облучения α -частицами. При их взаимодействии с ядрами мишени получаются два нейтрона:
Sb121(a, 2n) ®И123.
III. Третий метод - когда РФП получают в генераторных системах.
Основные требования к любой подобной системе состоят в том, что радионуклид, который нас интересует, должен иметь короткий период полураспада относительно материнского радионуклида (у которого большой период полураспада). Он может быть выделен из материнского физическим или химическим методом. Например, Тс-99м получают из Мо-99. Период полураспада молибдена - 67, а технеция - 6 часов. Молибден получают из продуктов распада урана в ядерном реакторе. Радионуклид технеция вымывают из генератора физиологическим раствором. Приготовление РФП простое и в большинстве случаев подразумевает добавление элюата во флакон с реагентом (фармпрепаратом) в асептических условиях.
б) Требования к РФП.
Все РФП проходят аттестацию, такую же, как другие лекарства и фармацевтические препараты. Они должны иметь соответствующую химическую, радиохимическую, радионуклидную чистоту, быть стерильными и апирогенными.
Химическая чистота РФП определяется наличием в нем других не радиоактивных веществ, особенно примесей тяжелых металлов.
Радиохимическая чистота РФП определяется частью радионуклида, которая находится в РФП в необходимой химической форме. Радиохимические примеси могут значительно влиять на достоверность получаемой информации. Радионуклидная чистота РФП состоит в отсутствии примесей радионуклидов которые могут создавать нежелательно высокие дозы облучения пациента, снижать точность и изменять результаты исследования. Этот вид чистоты контролируется радио- и спектрометрией.
Стерильность — достигается стерилизацией одним из 4-х способов:
паром, сухим теплом, фильтрацией, облучением (радиационная стерилизация).
Апирогенность - обеспечивается использованием апирогенных реагентов, растворов, посуды и соблюдения соответствующих требований в процессе производства и приготовления препаратов.
Наиболее важно, чтобы препарат дал полезную диагностическую информацию, был не дорогим и не вредным для пациентов.
в) Пути введения в организм РФП.
1. Энтеральный (per os). При таком пути введения РФП всасывается в кровь из желудочно-кишечного тракта и накапливается в исследуемом органе. (Всасывание радиоактивного йода при исследовании неорганического этапа обмена йода в организме).
2. Внутривенное введение РФП (используется для исследования функции и топографии печени, почек, сердечно-сосудистой системы, головного мозга и других органов).
3. Внутриартериальный.
4. Подкожный (для проведения непрямой лимфографии с целью оценки состояния лимфатических узлов при диагностике регионарных метастазов).
5. Внутрикожный (для оценки тканевой резорбции при заболеваниях сосудов).
6. Ингаляционный (для оценки вентиляционной способности легких и мозгового кровообращения).
7.В лимфатические сосуды (для проведения прямой лимфографии).
8. Непосредственно в ткани (для оценки мышечного кровообращения).
9. В спино-мозговой канал (для определения его проходимости).
г) Метаболизм РФП.
В состав радиофармпрепаратов могут входить химические элементы, являющиеся бета- или гамма-излучателями. Регистрируя излучение, определяют наличие, количество или метаболизм меченых препаратов. Выбирают такие препараты, метки которых имеют небольшой период полураспада (для уменьшения дозы облучения) и которые быстро выводятся. Если методика требует длительного времени для ее выполнения, то активность РФП должна быть достаточной для регистрации излучения к окончанию исследования.
РФП классифицируются:
1) по виду излучения:
- b-излучатели (32Р, тритий);
- γ-излучатели (99mТс, 123I, 113mIn);
- смешанные (131И, 198Аи).
2) по накоплению в органах и тканях:
- органотропные (198Аи-коллоид, 197Hg-промеран, 99mТс-пертехнетат);
- туморотропные (67Gа-цитрат);
- без селективного накопления в организме (тритиевая вода).
Органотропность может быть направленной, когда препарат выборочно концентрируется в органе и непрямой, когда РФП накапливается временно на пути его выведения из организма. Например, направленную органотропность к щитовидной железе имеет 131I, 125I; к печени - коллоидный раствор 198Аи; к поджелудочной железе – 75Se-метионин.
3) по периоду полураспада:
- ультракороткоживущие - период полураспада составляет минуты, часы;
- короткоживущие - период полураспада от нескольких часов до двух недель;
- долгоживущие - период полураспада более двух недель.
Радионуклидные методы исследования
Радионуклидная диагностика основана на возможности качественной и количественной регистрации излучений от радиофармацевтических препаратов (РФП), а также радиометрии биологических проб. Радионуклиды и их соединения подбираются таким образом, чтобы их поведение в организме человека не отличалось от поведения естественных веществ, а значит, отличие будет только в возможности давать излучение, т.е. «выдавать» свое местонахождение, количество и динамику содержания. Каждый РФП утверждается для использования Минздравом только после тщательных испытаний. Среди большого числа радионуклидов «зеленый свет» для диагностики получили лишь немногие: Tc-99m, In-113m, I-131, I-125, Se-75, In-111, Xe-133, Au-198, Hg-197. Из них наиболее часто используются лишь первые два: Технеций-99m и Индий-133m. Они – чистые гамма-излучатели (что и необходимо для эффективного исследования при минимальной дозе облучения) и их получают непосредственно перед исследованием в специальных генераторах. Лучевую безопасность при этом обеспечивает расчет оптимальной активности вводимого радионуклида. Активность подбирается таким образом, чтобы ее как раз хватило на проведение исследования. Дозы облучения пациента при этом четко регламентированы.
Возможность получения искусственных радиоактивных изотопов позволила расширить сферу применения радиоактивных индикаторов в различных отраслях науки, в том числе и в медицине. Радионуклидная визуализация основана на регистрации излучения, испускаемого находящимся внутри пациента радиоактивным веществом. Таким образом, общее между рентген- и радионуклидной диагностикой – использование ионизирующего излучения.
Радиоактивные вещества, называемые радиофармацевтическими препаратами (РФП), могут использоваться как в диагностических, так и в терапевтических целях. Все они имеют в своем составе радионуклиды – нестабильные атомы, спонтанно распадающиеся с выделением энергии. Идеальный радиофармпрепарат накапливается только в органах и структурах, предназначенных для визуализации. Накопление РФП может обусловливаться, например, метаболическими процессами (молекула-носитель может быть частью метаболической цепочки) либо локальной перфузией органа. Возможность изучения физиологических функций параллельно с определением топографо-анатомических параметров – главное преимущество радионуклидных методов диагностики.
Для визуализации используют радионуклиды, испускающие гамма-кванты, так как альфа- и бета-частицы имеют низкую проникающую способность в тканях.
В зависимости от степени накопления РФП различают «горячие» очаги (с повышенным накоплением) и «холодные» очаги (с пониженным накоплением или его отсутствием).
Существует несколько различных методов радионуклидного исследования.
Целью (общей) изучения данного раздела является умение интерпретировать принципы получения радионуклидного изображения и предназначение различных радионуклидных методов исследования.
Для этого необходимо уметь:
1) интерпретировать принципы получения изображения при сцинтиграфии, эмиссионной компьютерной томографии (однофотонной и позитронной);
2) интерпретировать принципы получения радиографических кривых;
3) трактовать предназначение сцинтиграфии, эмиссионной компьютерной томографии, радиографии.
Сцинтиграфия – самый распространенный метод радионуклидной визуализации.
Исследование проводится с помощью гамма-камеры. Основным ее компонентом является дисковидный сцинтилляционный кристалл йодида натрия большого диаметра (около 60 см). Этот кристалл является детектором, улавливающим гамма-излучение, испускаемое РФП. Перед кристаллом со стороны пациента располагается специальное свинцовое защитное устройство – коллиматор, определяющий проекцию излучения на кристалл. Параллельно расположенные отверстия на коллиматоре способствуют проецированию на поверхность кристалла двухмерного отображения распределения РФП в масштабе 1:1.
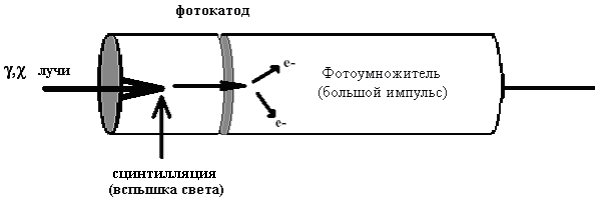
Гамма-фотоны при попадании на сцинтилляционный кристалл вызывают на нем вспышки света (сцинтилляции), которые передаются на фотоумножитель, генерирующий электрические сигналы. На основании регистрации этих сигналов реконструируется двухмерное проекционное изображение распределения РФП. Окончательное изображение может быть представлено в аналоговом формате на фотопленке. Однако большинство гамма-камер позволяет создавать и цифровые изображения.
Гамма-камеры – описание, конструкция, разновидности.
Уникальная архитектура SKYLight позволяет смонтировать гамма камеру по периметру комнаты, создавая таким образом “открытую” конструкцию без гентри. Избавившись от ограничений традиционных напольных систем, SKYLight может осуществлять визуализацию широкого круга пациентов на различных типах столов и в различных положениях. Воплощая следующее поколение платформ ядерной визуализации, SKYLight также позволяет медицинскому персоналу выполнять визуализацию двух пациентов одновременно (отделяемых друг от друга специальной ширмой, исключающей повышенную лучевую нагрузку больных друг на друга и на персонал радионуклидной лаборатории), обеспечивая для перегруженных отделений радионуклидной диагностики уникальную пропускную эффективность. Детекторы, перемещаемые свободными роботизированными потолочными подвесами, имеют возможность поворота вокруг собственной оси. Эта особенность конструкции, наряду с возможностью перемещать или полностью отсоединять стол пациента позволяет практически без ограничений проводить исследования пациентов на каталке, функциональной кровати и кресле-каталке, что особенно важно в онкологической практике.
Роботизированная система смены коллиматоров, осуществляемая за 3 минуты, и система выбора протокола сканирования гамма-камеры Philips SKYLight позволяет существенно повысить пропускную способность аппарата и существенно облегчает труд лаборанта радиоизотопной лаборатории.
В гамма-камере Philips SKYLight применяются специализированные длинноканальные коллиматоры высокого разрешения и программно-аппаратное обеспечение для автоматического позиционирования сердца в середину поля обзора детектора во время сбора данных. В совокупности с полностью автоматизированной цифровой системой коррекции энергии, линейности и однородности в режиме реального времени для коррекции артефактов движения, это позволяет получать высококачественные изображения без эффекта «мертвого пространства» при проведении SPECT сердца. При этом исследовании детекторы располагаются под углом 900, что является отраслевым стандартом. В гамма-камере Philips SKYLight работает система автоматического центрирования поля обзора при SPECT-исследованиях сердца.
Гамма-камера Philips SKYLight имеет систему автоматического управления позиционированием детекторов и сменой коллиматоров при выборе протоколов исследования. Применение цифровой коррекции энергии, линейности и однородности в масштабе реального времени в совокупности с высокой вычислительной мощностью дают возможность значительного улучшения качества изображения и повышения пропускной способости. Функция одновременной записи в различных энергетических окнах (до 16 окон по энергии), на разной матрице и т.д., позволяет записывать конкурентные изображения и открывает широкие перспективы при использовании системы для получения молекулярных изображений.
Внутреннее (собственное) разрешение детекторов гамма-камеры Philips SKYLight превосходит таковое у гамма-камеры e.cam на 0.4 мм (10%). Детекторы Philips SKYLight позволяют дифференцировать два излучающих объекта на таком расстоянии друг от друга, на котором другие гамма-камеры регистрируют их как один объект.
Камера Philips SKYLight позволяет, развернув оба детектора в одной плоскости и расположив их на одной оси, обследовать одновременно несколько областей тела, например, грудную клетку, брюшную полость и органы таза сразу (например, при поиске метастазов опухоли), что радикально сокращает время исследования, сокращая лучевую нагрузку и увеличивая пропускную способность отделения радионуклидной диагностики.
BrightView SPECT (ОФЭКТ)
Это не модифицированная гамма-камера, не просто более развитая модель с расширенной функциональностью. BrightView SPECT - это совершенно новый продукт, не менее революционный, чем камера SKYLight.
В силу того, что существует прямая зависимость между дистанцией "детектор-источник" и качеством изображения, BrightView располагает новой комплексной технологией CloseUp, ориентированной на сокращение такого растояния. Полностью автоматизированная, позволяющая детекторам комфортно и безопасно "парИть" над поверхностью исследуемой области, избегая соприкосновения с телом пациента, CloseUp предлагает клинике изумительное, ранее недостижимое для гамма-камер качество визуализации. Большую роль в получении таких изображений играют принципиально новые, более эффективные алгоритмы обсчета данных.
Кроме того, в камере BrightView используется новая, радиальная итерационная последовательность сбора информации. В то время как прочие разработчики придерживаются подхода, выработанного в 80-х годах прошлого столетия, т.е. фильтрованной обратной проекции. Прежняя технология позволяет ограничить большой поток данных, поступающих с детекторов, и была принята на вооружение в силу небольших вычислительных мощностей, которыми располагали производители в те времена. Новый принцип, реализованный в BrightView, резко увеличивает входящий поток информации, не подвергая её сомнительной коррекции и, таким образом, не искажая.
Обладая редкостно компактными размерами, BrightView может быть установлена в очень небольших помещениях.
Раскрываясь под теми углами, которые необходимы для обследования, в режиме MegaBody детекторы могут обследовать беспрецедентно большую площадь тела пациента.
Forte
Патентованная система прямого крепления детекторов к гентри с двумя независимыми кольцами обеспечивает высочайшую механическую стабильность и прецезионное позиционирование с выбором максимально возможного количества проекций сканирования.
Робот X-Act™ для автоматической установки гентри, детектора, коллиматоров и стола для укладки пациента, что позволяет достичь максимальной пропускной способности и эффективности использования системы.
Уникальный дизайн стола VersaTable™ пациента совмещает прочность и высокий комфорт для пациента. При этом стол может быть легко передвинут или отсоединен для обследования пациентов на каталке, кресле, функциональной кровати, в вертикальном положении и т.п.
Автоматическое устройство смены коллиматоров ColliMate™, рассчитанное на 4 пары коллиматоров (По специальному заказу - 2 дополнительные пары) позволяет заменить коллиматоры в течение 3-х минут, не подвергая их риску повреждения и не нагружая персонал.
Передовая технология цифровых детекторов с отдельным аналого-цифровым преобразователем для каждого фото-электронного умножителя обеспечивает получение выдающихся характеристик по пространственному и энергетическому разрешению, высокую скорость счета.
Автоматическое контурирование - максимальное приближение детекторов к телу пациента для получения изображений максимального качества.
Технология JetStream™ - автоматическое управление позиционированием детекторов и сменой коллиматоров при выборе протоколов исследования.
Цифровая коррекция энергии, линейности и однородности в масштабе реального времени.
Шестнадцать энергетических окон; каждое - с независимой матрицей, изменением масштаба изображения и остановки - получение конкурентных изображений - возможность получения молекулярных изображений.
Рабочая станция Pegasys™ Sunblade включает в себя более 250 пакетов самого современного клинического программного обеспечения.
Специализированные длинноканальные коллиматоры высокого разрешения для SPECT сердца Rembrandt™ позволяют получать высококачественные изображения без эффекта «мертвого пространства».
Полные пакеты специализированного программного обеспечения для исследований в кардиологии, созданные в кооперации с ведущими мировыми научными центрами: AutoQUANT™ Plus, CardiaQ™, Emory Tool Box™ и др., включающие реферативные базы для полуколичественного анализа и средства интерпретации и отображения данных исследований сердца в режимах SPECT и Gated SPECT. Оценка как перфузионных, так и функциональных данных. Используется в том числе алгоритм 3DMSPECT, разработанный в Медицинском Центре Университета Мичигана.
Уникальная функция Cardiotrac™ roving zoom автоматически позиционирует сердце в середину поля обзора детектора во время сбора данных, позволяя тем самым избежать эффекта усечения при кардиоисследованиях.
Полностью автоматизированная коррекция на движение InStill™ - для коррекции артефактов движения
Радиометрия предназначена для определения концентрации радиофармпрепарата в органах и тканях человека, что позволяет оценивать функциональное состояние изучаемого органа.
Различают
Лабораторную радиометрию (для регистрации активности различных биопроб и образцов)
Медицинскую радиометрию (для измерения активности от всего тела или отдельного органа)
Радиографию (для регистрации графиков изменений содержания РФП в органах и системах)
Сканирование (для регистрации накопления РФП в органах и тканях в виде изображения)
Профильное сканирование (для регистрации графиков накопления РФП в органах и тканях)
Сцинтиграфию (для регистрации динамики накопления и распределения РФП в органах и тканях)
Лабораторная радиометрия основана на измерении содержания того или иного меченного радионуклидом соединения в отдельных порциях крови, мочи, кала и других биологических средах.
Этим методом можно определять объем плазмы крови и массу эритроцитов, выделительную функцию почек, усвояемость жиров в кишечнике.
Сегодня одно из основных клинических применений лабораторной радиометрии – определение уровня гормонов и других биологически активных веществ и метаболитов в биологических средах.
Применяют разнообразные аппараты, принципы устройства и возможности у которых в общем мало отличаются.
Как пример приведем описание нескольких аппаратов для разных целей исследований.
Похожие работы
... и оснащением. Да и сами диагностические центры – это хоть и реальная, но все же перспектива, а не действительность. В наших условиях наиболее распространенными из перечисленных методов лучевой диагностики и лучевой терапии являются использование радиоактивных и рентгеновских излучений. В настоящем, осеннем семестре мы будем изучать возможности применения в медицине радиоактивных излучений. Что же ...
... для цитологического исследования, и косвенными, когда опухоли не видно, но определяются признаки, которые с той или иной степенью вероятности говорят о её наличии. В диагностике опухолей челюстно-лицевой области используются риноскопия. Передняя риноскопия. С помощью носового зеркала осматривают обе половины полости носа. При передней риноскопии можно: выявить изменения слизистой оболочки ...
... ). Из этих нуклидов только 271 нуклид стабилен, остальные радиоактивные. Около 300 из них находят или могут найти практическое применение в различных сферах человеческой деятельности. Основные источники производства радионуклидов для ядерной медицины следующие: ядерные реакторы, ускорители заряженных частиц, как правило, циклотроны и радионуклидные генераторы (как вторичный источник). В мировом ...
... . Измеряя выход химических реакций, т.е. количество вновь образованных конечных продуктов реакций, можно определить поглощенную энергию. На этом принципе основаны химические методы обнаружения и измерения радиоактивного излучения. Достоинство химических детекторов заключается в возможности выбора таких веществ, которые по воздействию на них ионизирующих излучений мало отличаются от тканей. ...


0 комментариев