Навигация
Фотодыхание, его значение. Сравнение фотодыхания у растений с различными типами метаболизма углерода
7 Фотодыхание, его значение. Сравнение фотодыхания у растений с различными типами метаболизма углерода
В растительных клетках, содержащих хлоропласты, помимо С3- и С4-путей фотосинтеза, осуществляется также фотодыхание, т. е. активируемый светом процесс высвобождения С02 и поглощения 02, который значительно, отличается от «темнового» дыхания митохондрий. Так как при этом первичным продуктом является гликолевая кислота, то этот путь получил название гликолатного. У некоторых С3-растений с малой эффективностью фотосинтеза интенсивность фотодыхания может достигать 50% от интенсивности фотосинтеза.
Фотодыхание у С3-растений обычно усиливается при низком содержании С02 и высоких концентрациях 02. В этих условиях РДФ-карбоксилаза в хлоропластах может функционировать как оксигеназа, катализируя окислительное расщепление рибулозо-1,5-дифосфата на 3-ФГК и 2-фосфогликолевую кислоту, которая затем дефосфорилируется в гликолевую кислоту (рис. 7.1). Молекулы С02 и 02 конкурируют между собой в каталитическом центре РДФ-карбоксилазы: при относительно высоких концентрациях С02 и низких 02 преобладает карбоксилирование, тогда как высокие концентрации 02 и низкое содержание С02 благоприятствуют окислению, а следовательно, и образованию фосфогликолевой кислоты. В том же направлении действует и повышение температуры.
Фотодыхание осуществляется в результате взаимодействия трех органелл — хлоропластов, пероксисом и митохондрий (рис. 7.1). Гликолат из хлоропласта поступает в пероксисому и там окисляется гликолатоксидазой до глиоксилата. Возникающая перекись водорода устраняется каталазой пероксисомы. Глиоксилат аминируется, превращаясь в глицин, причем в качестве донора аминогруппы функционирует глутамат.
Глицин транспортируется в митохондрию. Здесь из двух молекул глицина образуется серин и освобождается С02. Теперь цикл замыкается: серин может снова поступать в пероксисому и там передать свою аминогруппу на пируват. При этом из пирувата возникает аланин, из серина — гидроксипируват, который сразу после этого восстанавливается в глицерат. Затем глицерат может снова попасть в хлоропласты и благодаря фосфорилированию включиться в цикл Кальвина.
Последовательность реакций фотодыхания не обязательно образует цикл. Гликолатный путь С3-растений может завершиться в митохондриях. Конечными продуктами в этом случае является серин и С02. Освобождение С02 объясняет почему нетто-фотосинтез (чистая продуктивность) при интенсивном фотодыхании снижается (рис. 7.1).
У С4-растений С02, выделяющийся в результате фотодыхания, перехватывается в клетках мезофилла, где из ФЕП и С02 образуются оксалоацетат и малат. Затем малат «отдает» свой С02 хлоропластам обкладки, где функционирует цикл Кальвина. В связи с этим становится понятным высокий нетто-фотосинтез С4-растений.
Однако для чего же тогда нужно фотодыхание? Необходимо вспомнить, что гликолатный путь приводит к синтезу глицина и серина, в пероксисомах происходит восстановление NADP+; имеются косвенные данные о том, что в процессе образования серина может генерироваться и АТР. Показано, что С3-растения, помещенные в атмосферу с низким парциальным давлением 02 и высокой концентрацией С02, ведут себя подобно С4-растениям, т. е. имеют низкий уровень фотодыхания.
Из всего сказанного можно сделать вывод, что термин фотодыхание имеет лишь формальный смысл: 02 потребляется, С02 выделяется, однако в функциональном плане к дыханию этот процесс прямого отношения не имеет.
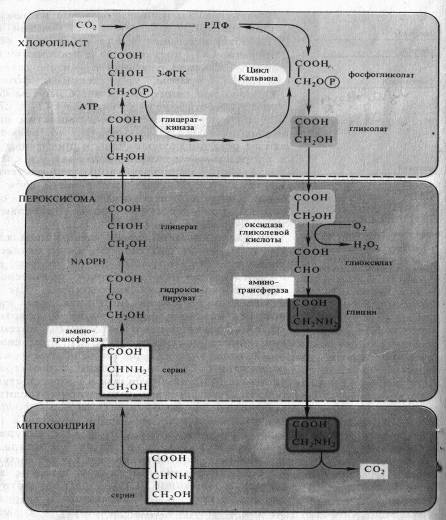
Рис. 7.1
8 Эндогенные механизмы регуляции процесса фотосинтеза
Регуляция фотосинтеза осуществляется на уровне фотохимически активных мембран, хлоропластов, клеток, тканей, органов и целого организма. Все системы регуляции принимают участие в этом процессе.
Процессы в хлоропластах при переходе к фотосинтезу. При освещении листьев хлоропласты уже через несколько минут начинают уменьшаться в объеме, становясь более плоскими (дисковидными). Тилакоиды и граны сдвигаются и уплотняются. Фотоиндуцируемое сокращение хлоропластов объясняется возникновением трансмембранных протонных градиентов и изменением электрического потенциала мембран хлоропластов. Определенная степень сжатия хлоропласта необходима для эффективной работы электронтранспортной цепи и для ее сопряжения с образованием АТР. Транспорт протонов внутрь тилакоидов приводит к подкислению их внутренней полости до рН 5,0—5,5 и одновременному подщелачиванию стромы хлоропласта от рН 7,0 в темноте и до рН 8,0 на свету. Вход ионов Н+ в тилакоиды сопровождается выходом из них в строму ионов Mg2 + .
Появление NADPH, ATP, 02, Mg2+ и изменение рН оказывают прямое и опосредованное влияние на реакции фотосинтетического усвоения С02 в строме. Экспериментально показано, что фиксация С02 изолированными хлоропластами практически не обнаруживается при рН ниже 7,2, но достигает максимальных значений при рН 8,0. Причина этого заключается в изменении активности ряда ферментов, имеющих оптимум рН в слабощелочной среде: рибулозофосфаткиназы (рН 7,9), дегидрогеназы фосфоглицеринового альдегида (рН 7,8), рибулозо-1,5-дифосфаткарбоксилазы (рН от 7,5 до 8,0), фруктозодифосфатазы (рН 7,5 — 8,5). Повышение рН стромы при освещении хлоропласта приводит к значительному связыванию С02 в виде Н2С03 и накоплению НСОз, из которого С02 освобождается с помощью карбоангидразы перед карбоксилированием рибулозо-1,5-дифосфата.
АТР участвует в фосфорилировании рибулозо-5-фосфата и ФГК, а также в реакциях, связанных с синтезом сахарозы и крахмала. NADPH необходим для восстановления ФГК до ФГА и для образования малата из щавелевоуксусной кислоты. Mg2+ нужен для функциональной активности РДФ-карбоксилазы, он также принимает участие в синтезе хлорофилла и белков.
Процесс фиксации С02 регулируется прежде всего светом.
Он активирует ряд ферментов цикла Кальвина: РДФ-карбоксилазу, дегидрогеназу 1,3-дифосфоглицериновой кислоты, фруктозо-1,6-дифосфатфосфатазу, седогептулозо-1,7-дифосфатфосфатазу и рибулозо-5-фосфаткиназу. Наиболее многообразна регуляция функционирования ключевого фермента цикла Кальвина — РДФ-карбоксилазы.
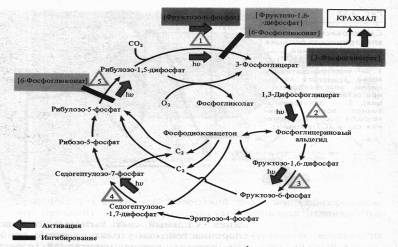
Помимо света, фермент активируется фруктозо-6-фосфатом, а ингибируется 6-фосфоглюконатом и фруктозо-1,6-дифосфатом. 6-Фосфоглюко-нат подавляет также активность завершающего цикл фермента — рибулозо-5-фосфаткиназы. Наконец, продукт цикла фиксации С02 — 3-фосфоглицериновая кислота положительно влияет на синтез крахмала. Повышение концентрации 02 в строме может привести к снижению интенсивности фиксации С02 за счет усиления фотодыхания.
Функциональные изменения в клетках мезофилла. Хлоропласты большинства растений способны перемещаться в клетке в зависимости от интенсивности и направления освещения. Сильный свет вызывает отрицательный фототаксис хлоропластов: они уходят от света, концентрируясь на боковых стенках клеток палисадной паренхимы; слабый свет вызывает положительный фототаксис. Предполагают, что освещенный хлоропласт меняет свое положение в клетке с помощью сократительных белков, связанных с оболочкой хлоропласта и взаимодействующих с сократительными белками цитоплазмы.
Мощное воздействие на клетку, определяющее ее метаболизм, оказывают образующиеся в хлоропластах ATP, NADPH и ассимиляты. При освещении отношение ATP/ADP в хлоропластах резко возрастает и вследствие быстрого обмена энергетическими эквивалентами почти тотчас же может воспроизводиться в цитоплазме, а через нее и в митохондриях. Так как оболочка хлоропласта лишь в слабой степени проницаема для АТР, перенос в цитоплазму высокоэнергетической фосфатной связи АТР осуществляется с помощью челночного механизма в результате реакции восстановления-окисления между ФГК и ФДА, так как скорость выхода триозофосфатов через мембраны оболочки хлоропласта приближается к скорости свободной диффузии. Одновременно это приводит к транспорту восстановительных эквивалентов (NADH).
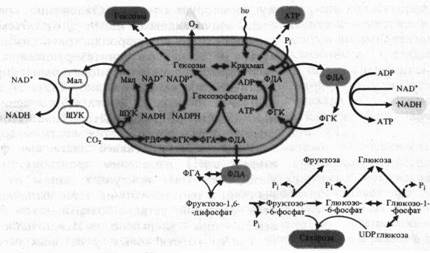
Переносчиком высокого восстановительного потенциала NADPH может служить система ЩУК-малат, каждый компонент которой легко проходит через мембраны, совершая циклические перемещения между хлоропластом и цитоплазмой. В пользу этой гипотезы говорит то, что в хлоропластах находятся NAD + - и NADP + -зависимые малатдегидрогеназы.
Появление АТР и восстановительных эквивалентов в цитоплазме приводит к активации на свету таких энергопотребляющих процессов, как синтез жирных кислот, восстановление нитратов и сульфатов. Общеклеточные нужды могут даже «отзывать» АТР с пути восстановления С02, конкурируя с реакциями цикла Кальвина.
Уже в первые секунды фотосинтеза происходит выход ассимилятов в цитоплазму. После кратковременного фотосинтеза с 14С02 в цитоплазме прежде всего появляются меченые фосфотриозы — ФГК и ФДА, а затем [14С] фруктозо-1,6-дифосфат. На изолированных хлоропластах показано, что оболочка хлоропласта практически непроницаема для сахарозы. По-видимому, основным местом синтеза сахарозы в клетке является не хлоропласт, а цитоплазма. На это указывает также присутствие основного сахарозосинтезирующего фермента сахарозофосфатсинтетазы и UDP-глюкозопирофосфорилазы преимущественно в цитоплазме.
Выход предшественников углеводов из хлоропластов в цитоплазму совершается в виде ФГК, ФГА и ФДА. Дальнейшие превращения, ведущие к синтезу гексозофосфатов и сахарозы, происходят уже в цитоплазме. Аналогичным превращениям могут подвергаться триозофосфаты и в хлоропластах, вследствие чего при достаточно интенсивном фотосинтезе в хлоропластах накапливается крахмал, служащий резервом углеводов, предназначенных для экспорта в цитоплазму во вторую очередь. Отложения крахмала часто бывают очень значительными (до 90% от объема хлоропласта).
Выходящие из хлоропластов ассимиляты могут использоваться в самой фотосинтезирующей клетке двумя путями: 1) в окислительно-восстановительных процессах, что обычно заканчивается освобождением С02, 2) для увеличения массы клетки в процессе ее роста и отложения запасных и вторичных веществ. Большая часть ассимилятов транспортируется из фотосинтезирующих клеток листа в другие органы и ткани.
Взаимодействие тканей листа при фотосинтезе. Под действием света изменения происходят не только в клетках мезофилла. Свет выступает одним из важнейших факторов регуляции работы устьиц. При включении света у большинства растений устьица открываются более широко, а при выключении — закрываются. Исключение из правила — растения семейства толстянковых, у которых ночью устьица открыты, а днем закрыты. На движения устьиц влияет и концентрация С02: ширина устьичных щелей увеличивается при снижении содержания С02 в межклетниках. Открывание устьиц под действием света связано с работой фотосинтетического аппарата в замыкающих клетках. У этиолированных растений свет не влияет на движения устьиц. В замыкающих клетках на свету включается механизм Н +-насоса в плазмалемме, усиливается поглощение К+ и синтез малата, в результате чего возрастает внутриклеточное осмотическое давление и устьица открываются.
Увеличение степени открывания устьиц приводит к усилению транспирации и, следовательно, к более интенсивному поступлению воды и веществ по ксилеме из корней в листья, что необходимо для нормальной функциональной активности клеток мезофилла.
Фотосинтетическая деятельность клеток мезофилла обогащает ткани листа сахарами и другими продуктами фотосинтеза. В результате возрастает функциональная активность проводящих пучков. Теоретически существуют два способа транспорта ассимилятов к проводящим пучкам: по симпласту (через плазмодесмы и цитоплазму последовательного ряда клеток) и по апопласту (по клеточным стенкам). Однако у многих видов растений между клетками мезофилла и флоэмы плазмодесмы развиты крайне слабо или совсем отсутствуют. В апопласте листовой пластинки может находиться около 1/5 сахаров, содержащихся в листе, и значительная доля свободных аминокислот. Клетки листовой паренхимы сравнительно легко выделяют ассимиляты в наружную среду и относительно слабо их поглощают. Клетки флоэмных окончаний, напротив, способны усиленно поглощать из внешних растворов сахара и аминокислоты против концентрационного градиента с помощью энергозависимых переносчиков. Есть основание считать, что, выходя из паренхимных клеток листа в клеточные стенки, сахароза расщепляется находящейся там инвертазой на гексозы (фруктозу и глюкозу), которые в проводящих пучках вновь образуют сахарозу.
Флоэмные окончания выполняют в листе роль коллекторов, аккумулирующих ассимиляты против градиента концентрации. Ведущая роль в загрузке проводящих элементов ассимилятами принадлежит сопровождающим и паренхимным клеткам флоэмы, а у некоторых видов растений и более специализированным передаточным клеткам. Есть данные о том, что клетки флоэмных окончаний поглощают сахара с участием ионов Н +, которые выкачиваются из клеток благодаря работе энергозависимого Н +-насоса.
При перегрузке тканей листа ассимилятами интенсивность фотосинтеза снижается. Переполнение крахмалом пластид вызывает обратимые, а позднее и необратимые изменения структуры хлоропластов, что значительно ослабляет фотосинтез. Отрицательное действие избытка крахмала на фотосинтез в пластидах может быть объяснено: 1) механическим воздействием на тилакоиды, 2) ухудшением светового режима в хлоропласте, 3) сорбцией ферментов на зернах крахмала, 4) сорбцией ионов, особенно Mg2 + , необходимых для поддержания высокой активности ферментов, 5) ухудшением диффузии С02.
Регуляция процессов фотосинтеза в целом растении.
Реализация фотосинтетической функции в целом растении, с одной стороны, определяется значительной генетической и биохимической автономностью структур низших порядков (хлоропласт, клетка), а с другой — сложной системой интеграции и кооперативных связей фотосинтеза со всеми функциями растительного организма. Процессы онтогенеза обеспечивают постоянное существование в растительном организме так называемых аттрагирующих (притягивающих питательные вещества) зон. В аттрагирующих центрах происходит либо новообразование и рост структур, либо интенсивный однонаправленный синтез запасных веществ (плоды, клубни, луковицы). В обоих случаях состояние аттрагирующих центров определяет величину «запроса» на фотосинтез. Донор ассимилятов (фотосинтез) и их акцептор (процессы роста и отложения веществ в запас) представляют собой взаимосвязанную систему. Если внешние условия не лимитируют фотосинтез, то ведущая роль в его детерминации принадлежит именно эпигенетическим процессам (появлению и развитию новых органов). Это положение может быть проиллюстрировано многочисленными фактами. Так, удаление молодых початков у кукурузы, плодов у томатов, баклажанов или яблони вызывает значительное и устойчивое снижение фотосинтетической активности листьев. Удаление части листьев растения при сохранении прежней активности аттрагирующих центров обычно сопровождается увеличением фотосинтетической активности оставшихся листьев.
Механизм этих взаимоотношений основан на явлении метаболической репрессии фотосинтеза. Чем мощнее центры, аттрагирующие ассимиляты, тем эффективнее фотосинтезирующий лист освобождается от ассимилятов, что служит необходимым условием интенсивного фотосинтеза.
Во всех этих процессах важнейшую роль играют фитогормоны и эндогенные ингибиторы роста и метаболизма (некоторые полифенолы). Участие фитогормонов в процессах фотосинтеза можно представить в виде следующей схемы, предложенной А. Т. Мокроносовым (1983):
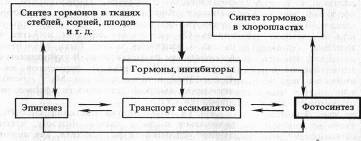
Согласно этой схеме, фитогормоны образуются в разных частях растений, в том числе в хлоропластах, и действуют на процессы фотосинтеза как дистанционно, так и непосредственно на уровне хлоропластов. Дистанционное действие осуществляется благодаря регулирующему влиянию фитогормонов на процессы роста и развития (эпигенез), на отложение веществ в запас, на транспорт ассимилятов, т. е. на формирование и активность аттрагирующих центров. С другой стороны фитогормоны оказывают прямое действие на функциональную активность хлоропластов через изменение состояния мембран, активность ферментов, генерацию трансмембранного потенциала. Доказана также роль фитогормонов, в частности цитокинина, в биогенезе хлоропластов, синтезе хлорофилла и ферментов цикла Кальвина.
Ряд фитогормонов (индолилуксусная кислота, гиббереллины, абсцизовая кислота), а также некоторые физиологически активные фенолы образуются в тканях листа. Цитокинин же, от которого во многом зависит формирование листа и его структур, поступает из других частей растения, прежде всего из корня. Такая система создает взаимозависимость всех органов, обеспечивая регуляцию функциональной активности в целом растении.
Похожие работы
... в трофических цепях. Именно в круговоротах биогенных химических элементов, по мнению В.И. Вернадского, заключается геологическая роль живого вещества планеты. Живые организмы формируют не только биологический, но и геологический лик планеты. Важной идеей В.И. Вернадского была мысль о космической роли живого вещества, которая заключается в аккумулировании солнечной энергии и преобразовании ее в ...
... период многие страны приняли решение о полном или постепенном отказе от развития атомной энергетики. 1.3 Особенности альтернативной водородной энергетики Водородная энергетика включает следующие основные направления: Разработка эффективных методов и процессов крупномасштабного получения дешевого водорода из метана и сероводородсодержащего природного газа, а также на базе разложения воды; ...
... взаимодействия – зависимость организма от среды – была полно раскрыта от Ламарка до Мичурина. Но обратное явление – отражение жизни на среде – почти не привлекало внимание до В.И.Вернадского. Указывая, что связь живого и неживого в биосфере является взаимной, ученый писал: «Организм имеет дело со средой, к которой он не только приспособлен, но которая приспособлена и к нему». Конечно, здесь ...
... голоса, слушают пение птиц, плеск волн и шум ветра, дышат свежим воздухом. Воспользоваться таким транспортом захочет каждый, кто любит совершать водные путешествия. 6. РОССИЯ, УКРАИНА И СОЛНЕЧНАЯ ЭНЕРГЕТИКА В России в настоящее время имеется восемь предприятий, имеющих технологии и производственные мощности для изготовления 2 МВт солнечных элементов и модулей в год. В 1992 году на ...
0 комментариев