Навигация
Электролиты и теория электролитической диссоциации
1.2 Электролиты и теория электролитической диссоциации
Электрический ток – это направленное движение заряженных частиц. В металлах такое направленное движение осуществляется за счет относительно свободных электронов. Говорят, что металлы обладают электронной проводимостью, их называют проводниками первого рода. Но, оказывается, проводить электрический ток могут не только металлы.
Вещества, растворы или расплавы которых проводят электрический ток, называются электролитами. Вещества, растворы или расплавы которых не проводят электрический ток, называются неэлектролитами.
Почему же электролиты проводят электрический ток?
В 1887 г. шведский ученый Сванте Аррениус сформулировал положения теории электролитической диссоциации. Основная идея этой теории заключается в том, что электролиты под действием растворителя самопроизвольно распадаются на ионы. Электропроводность электролитов обусловлена именно наличием в растворе свободных ионов, которые и являются носителями зарядов.
В дальнейшем теория электролитической диссоциации совершенствовалась. Современная теория водных растворов электролитов кроме теории С. Аррениуса включает в себя представления о гидратации ионов (И.А. Каблуков, В.А. Кистяковский), теорию сильных электролитов (П.Й. Дебай, Э.А. Хюккель, 1923 г.).
Основными положениями теории электролитической диссоциации являются следующие:
1. Электролиты в растворах под действием растворителя самопроизвольно распадаются на ионы. Такой процесс называется электролитической диссоциацией. Диссоциация также может происходить при плавлении твердых электролитов (термическая диссоциация электролитов).
2. Ионы отличаются от атомов составом и свойствами. В водных растворах ионы находятся в гидратированном состоянии. Свойства гидратированных ионов и ионов в газообразном состоянии вещества различны.
3. В растворах или расплавах электролитов ионы движутся хаотично. При пропускании через раствор или расплав электрического тока, ионы движутся направленно: катионы – к катоду, анионы – к аноду. Раствор или расплав электролита является проводником с ионной проводимостью – проводником II рода.
В свете теории электролитической диссоциации можно дать определения основаниям, кислотам и солям как электролитам.
Основания – это электролиты, в результате диссоциации которых в водных растворах образуется только один вид анионов – гидроксид-анионы ОНˉ.
КОН = К+ + ОНˉ Са(ОН)2 = Са2+ + 2ОНˉ.
Кислоты – это электролиты, в результате диссоциации которых в водных растворах образуется только один вид катионов – катионы водорода Н+ (точнее – катионы гидроксония Н3О+).
Катион гидроксония образуется при взаимодействии Н+ с молекулой Н2О. в результате образуется еще одна ковалентная связь кислорода с водородом по донорно-акцепторному механизму:
Н+ + Н2О = Н3О+
Примеры диссоциации кислот:
HCl = H+ + Clˉ или HCl + H2O = H3O+ + Clˉ.
Многоосновные кислоты диссоциируют многоступенчато:
H2SO4 + H2O = H3O+ + HSO4ˉ
HSO4ˉ + H2O ó H3O+ + SO42-
Соли – это электролиты, диссоциирующие в водном растворе на катионы металлов и анионы кислотного остатка.
Средние соли диссоциируют с образованием только катионов металла и анионов кислотного осадка, например:
Ba(NO3)2 = Ba2+ + 2NO3¯
Соли аммония вместо катиона металла содержат катион аммония.
Например:
NH4Cl = NH4 + Cl¯
Основные соли диссоциируют с образованием катионов металла, анионов OH¯ и анионов кислотного осадка.
Кислые соли диссоциируют с образованием катионов металла, катионов водорода (гидроксония) и анионов кислотного осадка, например:
Ca(HCO3)2 + 2H2O = Ca2+ + 3H3O+ + 2CO32-
Двойные соли – соли, в результате диссоциации которых образуются катионы нескольких металлов (или аммония какого-либо металла) и анионы одного кислотного остатка. Например, сульфат калия – хрома (хромокалиевые квасцы):
KCr(SO4)2 = K+ + Cr3+ + 2SO42-
Смешанные соли – соли, в результате диссоциации которых образуются катионы какого-либо металла и анионы нескольких кислотных остатков. Например, хлорид-гипохлорит кальция (хлорная известь):
CaClOCl = Ca2+ + Cl¯ + ClO¯
Электролитическая диссоциация – обратимый процесс. Обратный процесс – ассоциация ионов. При растворении одних электролитов равновесие диссоциации значительно смещено в сторону диссоциированных форм, в растворах таких электролитов диссоциация происходит почти полностью. Такие электролиты называют сильными. При растворении других электролитов диссоциация происходит в незначительной мере, такие электролиты называют слабыми электролитами.
Для количественной оценки силы электролита введено понятие степени электролитической диссоциации.
Степень электролитической диссоциации – отношение количества вещества электролита, распавшегося на ионы (νрасп) к количеству вещества электролита, поступившего в раствор (νобщ):
α = νрасп/νобщ, где α – степень ЭД, 0< α ≤ 1.
Степень электролитической диссоциации зависит от природы электролита, его концентрации в растворе и температуры. С разбавлением и с повышением температуры степень электролитической диссоциации возрастает.
Оценить силу различных электролитов можно, сравнивая степень их электролитической диссоциации при одинаковых условиях. Электролиты, степень диссоциации которых при 18 °С в растворах с концентрацией 0,1 моль/л электролита близка к 100% относят к сильным электролитам. Это щелочи, большинство солей, некоторые неорганические кислоты (HClO4, HI, HBr, HCl, HNO3, H2SO4). Электролиты, степень диссоциации которых при 18 °С в растворах с концентрацией 0,1 моль/л электролита значительно меньше 100% относят к слабым электролитам. Это многие неорганические кислоты: H2S, HCN, HClO, практически все органические кислоты (HCOOH, CH3COOH, CH3CH2COOH), водный раствор аммиака, вода.
Диссоциация слабых электролитов – обратимый процесс. Поэтому силу электролита также можно охарактеризовать с помощью константы химического равновесия процесса диссоциации электролита – константы диссоциации. Константа диссоциации зависит от температуры, но не зависит от концентрации электролита. В этом ее преимущество по сравнению со степенью электролитической диссоциации. Чем больше значение константы диссоциации, тем сильнее электролит.
Механизм электролитической диссоциации веществ
Рассмотрим механизм электролитической диссоциации на примере диссоциации хлорида натрия NaCl в водном растворе.
Молекулы воды полярны, они представляют собой диполи: на одном конце диполя δˉ (частичный отрицательный заряд), на другом – δ⁺ (частичный положительный заряд). При контакте кристалла NaCl с водным раствором, водородные связи между молекулами воды, находящимися вблизи кристалла, разрушаются. Диполи воды ориентируются своими полюсами относительно ионов на поверхности кристалла: отрицательным полюсом диполя – к катионам натрия, положительным полюсом диполя – к анионам хлора. Происходит процесс соединения ионов соли с молекулами воды – гидратация ионов. Молекулы воды, притягивающиеся к ионам растворяемой соли, во много раз ослабляют притяжение ионов друг к другу. Постепенно гидратированные ионы разъединяются (рис. 1).
Гидратированные ионы – это ионы, химически связанные с молекулами воды.
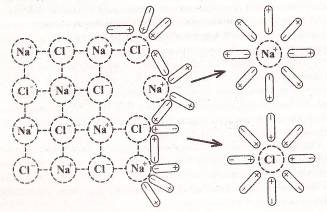 рис. 1.
рис. 1.
Одним из важных факторов. Обуславливающих возможность диссоциации электролитов в водных растворах, является высокая диэлектрическая проницаемость воды[3]. В ходе диссоциации ионных связей энергия затрачивается, а в ходе гидратации – выделяется. Если энергия гидратации с избытком компенсирует затраты энергии диссоциации ионных связей, то растворение таких электролитов – экзотермический процесс. Если энергия гидратации не полностью компенсирует затраты энергии диссоциации ионных связей, растворение таких электролитов будет эндотермическим процессом.
Электролитическая диссоциация электролитов с ковалентной полярной связью включает в себя еще и процесс поляризации полярной молекулы. Рассмотрим схему данного процесса на примере электролитической диссоциации молекул хлороводорода в воде (рис. 2.).
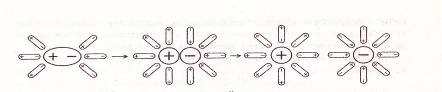 рис. 2.
рис. 2.
При растворении хлороводорода в воде диполи воды ориентируются относительно диполя НС1. Под действием диполей воды происходит поляризации связи Н-С1, в результате которой общая электронная пара полностью смещается к атомной частице хлора. Связь Н-С1 диссоциирует, и образуются гидратированные ионы. Ионы Н⁺ взаимодействуют с молекулами воды с образованием иона гидроксония Н3О⁺.
Похожие работы
... задач; построение квазисолитонных решений для реакций первого и второго порядков и изучение зависимостей плотности кислоты от пористости и времени, пористости от времени и коэффициента химической реакции; · применение метода асимптотического разложения к многослойным задачам о температурных полях, получение системы уравнений для коэффициентов разложения искомого решения в виде ряда по параметру ...
... воздействие. Принцип Ле Шателье – Брауна является одним из следствий второго начала термодинамики и применим к любым макроскопическим системам, находящимся в состоянии истинного равновесия. Типы химических связей На этой концептуальной основе была разработана стройная атомно-молекулярная теория того времени, которая впоследствии оказалась не в состоянии объяснить многие экспериментальные ...
... в уравнениях реакций и не забывать о том, что складываемые, вычитаемые или сокращаемые моли вещества должны находиться в одинаковом агрегатном состоянии. 2. Применение теплового эффекта на практике Тепловые эффекты химических реакций нужны для многих технических расчетов. Например, рассмотрим мощную российскую ракету "Энергия", способную выводить на орбиту космические корабли и другие полезные ...
... коэффициенты в уравнениях реакций и не забывать о том, что складываемые, вычитаемые или сокращаемые моли вещества должны находиться в одинаковом агрегатном состоянии. 2. Применение теплового эффекта на практике Тепловые эффекты химических реакций нужны для многих технических расчетов. Например, рассмотрим мощную российскую ракету "Энергия", способную выводить на орбиту космические корабли и ...


0 комментариев