Навигация
Міністерство освіти і науки України
Нікопольського Медичного Училища
Самостійна робота на тему:
"Колоїдні розчини"
Виготовили:
Рогоза Анастасія
Ласкіна Наталія
Олійник Світлана
Бутко Яна
Мадай Анастасія
Кисельова Вікторія
Зміст
1. Колоїди та колоїдні системи
2. Грунтові колоїдни та поглинальна здатність грунту
3. Способи одержання колоїдних розчинів
* Метод конденсації
* Медод гідролізу
* Метод заміни розчинника
* Електричник метод
* Метод очищення колоїдних розчинів
*Метод обмінного розкладу
4. Броунівський рух
5. Броунівський рух у математиці
6. Дифузія
7. Рівняння дифузії
8. Осмотичний тиск
1. Колоїни та колоїдні системи
Коло́їд,— речовина, що складається з дуже маленьких часток матерії (дисперсна фаза), які присутні в іншому матеріалі.
Розмір дисперсних часток (1-1000 нанометрів, 1 нм = 10-9м) менший, ніж часток суспензії, але більший за молекули в справжньому розчині.
До колоїдів відносять аерозолі (дисперсії рідини і твердої речовини в газі, наприклад дим або туман) і піни (дисперсія газу в рідині), емульсії (обидва компоненти — рідини) і золі (тверді речовини в рідині). Золі, у яких обидві фази через тривимірну мережу молекул мають желеподібну форму, називаються гелі, прикладом можуть бути водні розчини желатину та крохмалю, а також силікатний клей.
КОЛОЇДИ, КОЛОЇДНІ СИСТЕМИ– мікрогетерогенні дисперсні системи (проміжний стан між справжніми розчинами й грубо-дисперсними системами), що складаються з дуже подрібнених частинок (від 1 до 1000 нм), рівномірно розподілених (розосереджених) в однорідному середовищі або фізично однорідні системи, що містять макромолекули як один з компонентів (молекулярний колоїд). На відміну від частинок грубодисперсних систем (суспензій, емульсій, пін тощо), розмір частинок яких звичайно перевищує 10-4 см, колоїдні частинки беруть участь в інтенсивному броунівському рухові і не седиментують в полі сил земного тяжіння. К.с. з газовим дисперсійним середовищем - високодисперсні аерозолі (дими, тумани), з рідким - золі, латекси, міцелярні розчини, мікроемульсії, з твердого - системи типу рубінового скла. Колоїдні системи утворюються внаслідок конденсації (при виділенні колоїдно-дисперсної фази з перенасиченої пари, розчину або розплаву) або диспергування. Найпоширеніші в природі та техніці колоїдні системи з рідким дисперсійним середовищем.
2. Грунтові колоїдни та поглинальна здатність грунту
О.Н.Соколовський (на фото) – батько українського грунтознавства, засновник і перший директор Науково-дослідного інституту грунтознавства та агрохімії (тепер національний науковий центр "Інститут грунтознавства та агрохімії ім. О.Н.Соколовського"), автор першого підручника українською мовою "Курс сільськогосподарського грунтознавства" (1934) і "Сельскохозяйственное почвоведение" (1956).
Досліджуючи склад і властивості гумусу, він дійшов висновку: "яким би не був хімічний склад гумусу, головна його властивість – колоїдність". Тому його підручник починається розділом "Колоїди грунту, їх динаміка і зв'язані з ними явища". О.Н.Соколовський поділив гумус грунтів на дві групи: активний і пасивний. Зразок грунту оброблявся 0,1н розчином NaCl; гумус, який перейшов після обробки до розчину, він назвав активним – ця фракція гумусу може рухатися по профілю, покривати структурні відокремлення тоненькою плівкою тощо. Та частина гумусу, яка не переходить (не пептизується) до розчину навіть після дії натрію (розчину NaCl) на грунтовий зразок, називається пасивною. Останній вид гумусу має важливе значення для утворення агрономічно-цінної структури з розміром агрегатів від 0,25 мм до 7-10 мм. Особлива його здатність – забезпечення водостійкості структури, тобто здатності не руйнуватися під дією дощової води. Отже, О.Н.Соколовський обгрунтував роль і значення у грунтоутворюючих процесах активного і пасивного гумусу або активних і пасивних колоїдів у житті грунту.
3. Способи одержання колоїдних розчинів
колоїдний дифузія броунівський осмотичний тиск
Колоїдні часточки можуть мати різну внутрішню структуру, що істотно позначається на способах утворення колоїдних розчинів і на їхніх властивостях.
Існують такі три типи внутрішньої структури первинних часточок колоїдних розмірів. І тип — суспензоїди (або необоротні колоїди, ліофобні колоїди). Так називають колоїдні розчини металів, їхніх оксидів, гідроксидів, сульфідів та інших солей. Первинні часточки дисперсної фази колоїдних розчинів цих речовин за своєю внутрішньою структурою не відрізняються від структури відповідної компактної речовини і мають молекулярну або іонну кристалічну решітку. Суспензоїди — типові гетерогенні високодисперсні системи, властивості яких визначаються дуже сильно розвинутою міжфазовою поверхнею. Від суспензій вони відрізняються вищою дисперсністю. Суспензоїдами їх назвали тому, що, як і суспензії, вони не можуть тривалий час існувати, коли немає стабілізатора дисперсності. Необоротними їх називають тому, що осади, які лишаються при випаковуванні таких колоїдних розчинів, не утворюють знову золю в разі контакту з дисперсійним середовищем. Ліофобними (з грецького: "ліос" — рідина, "фобіо" — ненавиджу) їх назвали, гадаючи, що особливі властивості колоїдних розчинів цього типу зумовлені дуже слабкою взаємодією дисперсної фази і дисперсійного середовище. Концентрація ліофобних золів невелика, звичайно менша за 0,1%'. В'язкість таких золів мало відрізняється від в'язкості дисперсійногосередовища. Ліофобні золі, як взагалі дисперсні системи, відповідно до їх проміжних положень між молекулами і великими тілами, можна добути двома способами: диспергуванням, тобто подрібненням великих тіл, і конденсацією молекулярно- або іоннорозчинених речовин. Подрібнення за допомогою дроблення, молоття, розтирання дає порівняно крупнодисперсні порошки (> 60 мкм). Більш тонкого подрібнення досягають за допомогою спеціальних апаратів — колоїдних млинів, або застосовуючи ультразвук.
* Метод конденсації
Метод конденсації полягає в утворенні нерозчинних сполук за допомогою реакцій обміну, гідролізу, відновлення, окислення. Здійснюючи ці реакції в сильно розбавлених розчинах і з деяким надлишком одного з компонентів, дістають не осади, а колоїдні розчини. До конденсаційних методів належить також добування ліозолів за допомогою заміни розчинника. Наприклад, колоїдний розчин каніфолі можна добути, виливаючи її спиртовий розчин у воду, в якій каніфоль не розчиняється.
II тип — асоціативні, або міцелярні, колоїди. Їх називають також напівколоїдами. Колоїдно-дисперсні часточки цього типу виникають при достатній концентрації дифільних молекул низькомолекулярних речовин за допомогою асоціації їх в агрегати молекул — міцели — сферичної або пластинчастої форми.
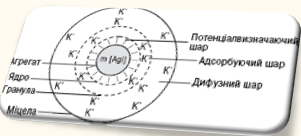
Схема будови міцели гідрозолю AgI
Міцели — це скупчення правильно розміщених молекул, що утримуються переважно дисперсійними силами. Утворення міцел є характерним для водних розчинів миючих речовин (наприклад, мил — лужних солей вищих жирних кислот) і деяких органічних барвників з великими молекулами; в інших середовищах, наприклад в етиловому спирті, ці речовини розчиняються з утворенням молекулярних розчинів.
Склад міцели виражають певною формулою. Напр. склад міцели гідрозолю йодиду срібла, утвореного при взаємодії нітрату срібла в розчині з надлишком йодиду калію, виражається формулою:
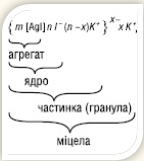
Дифільними називають молекули, які складаються з вуглеводневого радикалу, що має спорідненість до неполярних розчинників, і гідрофільної (полярної) групи, що має спорідненість до води. III тип — молекулярні коло їди. їх називають також оборотними, або ліофільними (від грецького "філіо" — люблю), колоїдами.
До них належать природні і синтетичні Високомолекулярні речовини з молекулярною масою від десяти тисяч до кількох мільйонів1. Молекули цих речовин мають розміри колоїдних часточок, тому такі молекули називають макромолекулами.
*Метод гідроліза
Гідролізом широко користуються при одержанні золей із солей, якщо в результаті реакції гідроліза утворюється погано розчинна речовина.
В якості приміру приведем утворення нерозчинного гідрату окисі заліза,яке одрежуємо при гідролізі хлорного заліза рівнянням:
FeCl3 + 3H2O = Fe(OH)3 + 3HCl,
Fe(OH)3 + HCl = FeCl + 2H2O ,
Частково утворююча в реакції хлор окис заліза дісоціїрує на іоні:
FeОCl = FeO + Cl,
Які забезпечують іоноген ний шар навкруги частин Fe(OH)3 і утримують їх в рівноваженому стані.
*Методи заміни розчинника
Метод заснований на виділення розчинної речовини із розчину в виді високодисперсної нерозчинної фази шляхом заміни розчинника. Молекули розчинної речі. Яка знаходиться в стані молекулярної дисперсності в одному розчиннику, попадаючи в умови поганої розчинності при заміні розчинника починає конденсуватися в більші частинки, досягаючи розмірів коллоїдних. Цим методом можна користуватись при приготовленні золя сірки, каніфолі, мастики, фосфору і др. при вливанні спиртових розчинів цих речовин в воду.
*Електричний метод
Метод одержання колоїдних розчинів з допомогою електрики, рекомендований Бредігом (1898 р.), можна використати головним чином для виготовлення гідрозолей благородних металів. Цей метод обґрунтований на одержанні електричної дуги між електродами створеними із диспергіруючого металу (срібла, золота та ін..) при пропусканні постійного струму. Під дією високої температури проходить випарування матеріалу електродів в дисперсійному водному середовищі. Після пари металу конденсуються в колоїдні частинки, утворюючи відповідну золу. Процес краще проводити при охолодженні.
*Методи очистки колоїдних розчинів
Для одержання колоїдних розчинів з найбільшою стійкістю і для вивчення їх якостей необхідно видалення із золи всяких домішок і в першу чергу остатків електролітів, які, як правило, утворюються при одержанні колоїдних розчинів.
*Метод обмінного розкладу
Цей метод заснований на взаємодії двох речовин, в результаті реакції обмінного розкладання утворюється нова трудно розчинна річ, здатна зберігатися високодисперсному стані при наявності ряду відповідних умов. Класичним приміром являється одержання зали зернистого миш’яку:
2Н2А5О3 + 3Н2S = А52S3 + 6H2O
або
BaCl2 + K2SO4 = BaSO4 + 2KCl
*Діаліз
Для очистки розчинів широко використовуються метод діаліза. Вилучення колоїдних розчинів від домішок, здатних проникати через рослинні і тваринні, штучні мембрани, називається діалізом, а прибори пристосовані для цього, одержали назву діалізаторів. Перші моделі діалізаторів представляли собою посудину, заповнену проточною водою, в якій поміщалась на глибину декількох сантиметрів внутрішня частина приладу, нагадуючи широкий зрізаний отвір, на більше вузьку частину якої натягаємо мембрану із пергаменту, коллоїда, целофану. У внутрішню частину наливається колоїдний розчин, який треба очистити. З допомогою діалізу поступово проходить видалення речовин,легко проходять черех мембрану, наприклад електролітів і других кристалоїдів. Очистка неколлоїдних розчинів таким способом протікає по мало, і тому для прискорення діаліза використовуємо електричний струм.
Похожие работы
... мірою перешкоджає її газо - і теплообміну, що при запальних процесах, безумовно, небажано. З цієї причини, а також через обмежену розчиняючу здатність, масло вазелінове в технології неводних розчинів застосовується рідше, ніж рослинні олії - головним чином у розтираннях і краплях для носа. Більш широко воно використовується при виготовленні мазей. Зберігати масло вазелінове слід у закритих є ...
... активність лікарських речовин, що зв'язано з їх глибоким проникненням і тривалим контактом із тканинами організму. Колаген – гарний носій очних лікарських форм (розчинів, плівок). Білки також відносяться до природних високомолекулярних сполук. В основі цих продуктів лежить поліпептидне угруповання, складні молекули якого побудовані з амінокислот. У залежності від форми молекул білки розділяють ...
... оболонками. При розведенні розчину вплив “іонної атмосфери” зменшується, а при безкінечному розведенні зникає, адже іони практично не взаємодіють між собою. Таким чином, можна вважати, що в усіх процесах у розчинах електролітів приймають участь лише “активні іони”, тобто іони, які не приймають участі в даний момент в між іонних взаємодіях. У зв’язку з цим для оцінки концентраційних ефектів у ...
... 4) 2I– + Pb2+ → PbI2 5) 2I– + 2NO2‾ + 4H+ → 2NO↑ + I2 + 2H2O 6) 10I– + 2MnO4‾ + 16H+ → 2Mn2+ + 5I2 + 8H2O № 96-97 Який аніон ІІІ-ї аналітичної групи можна відкрити за допомогою перманганату калію в кислому середовищі? Які ще реагенти застосовуються для його відкриття? Написати відповідні рівняння реакцій Це нітрит-іон: 5NO2‾ + 2MnO4&# ...

0 комментариев