Навигация
Лабораторный контроль эффективных доз АНД, внутри- и межлабораторный контроль качества анализов
4.6.2.3 Лабораторный контроль эффективных доз АНД, внутри- и межлабораторный контроль качества анализов
Лабораторный контроль
При приеме АНД более четырех дней, а особенно при продолжительном и интенсивном их применении, необходимы постоянное установление и оценка эффективности действия и коррекция терапевтической дозы лекарства. В настоящее время общепринятым в мире методом контроля АНД является ТВ или ПВ (одностадийное), выражаемое в секундах, в процентах или в единицах МНИ. В основе метода (более 60 лет назад предложенного А. Квиком и впоследствии многократно модифицированного) положено определение скорости образования сгустка фибрина в цитратной плазме крови больного при добавлении к ней смеси кальция и тромбопластина. Тромбопластин является фосфолипидно-белковым экстрактом из тканей животных и содержит тканевой фактор и фосфолипид, необходимые для активации фактора X фактором VII.
ПВ чувствительно к изменениям активности факторов II, VII, X, но плохо отражает изменения активности фактора IX. В первые дни от начала приема АНД ПВ отражает динамику изменений фактора VII, так как он первым подвергается влиянию АНД и только позже (обычно через 4-5 дней) начинают снижаться концентрации и других зависимых от витамина К факторов свертывания.
Проблема установления эффективной дозы АНД и ее поддержание на терапевтическом уровне согласно клинической ситуации осложняется тем, что разные лаборатории для определения ПВ используют различные методы, инструменты и аппаратуру, а главное – реагент тромбопластина разной активности и различного происхождения. Комплекс этих обстоятельств в значительной степени затрудняет получение сравнимых с другими лабораториями результатов, отвечающих современным требованиям контроля качества анализов и международным правилам по стандартизации этих анализов.
До сих пор значительно варьирует источник получения тромбопластина (мозг человека, мозг кролика, легкие, плацента человека, но чаще рекомбинантный продукт) и вид животных (кролик, крупный рогатый скот, обезьяны, человек). Различные тромбопластины неодинаково отражают вызванные АНД изменения протромбинового комплекса, что, в свою очередь, значительно снижает надежность подбора доз АНД и достижение оптимального терапевтического эффекта. Поэтому в конце 70-х годов Всемирная организация здравоохранения (ВОЗ) для стандартизации тромбопластиновых реагентов предложила использовать Международный референтный препарат тромбопластина и новую статистическую модель для калибрования тромбопластинов – международный индекс чувствительности (МИЧ), который на упаковке реагента обязан проставить изготовитель.
В зависимости от комплекса обстоятельств (доступность качественных сертифицированных реагентов, финансы, технологическое обеспечение лаборатории) возможны три уровня лабораторных анализов ПВ по возрастающей надежности результатов:
1. Определение ПВ ручным способом или полуавтоматическим анализатором с использованием любого тромбопластинового реагента. В таком случае для контроля качества анализов используется пул цитратных плазм от здоровых людей, не принимающих лекарств, влияющих на компоненты свертывания крови. Такой контрольный материал используется не больше недели и заменяется другим пулом путем “накладки” результатов определения ПВ обоих пулов в течение 1-2 дней. Результаты выражаются в секундах с обязательным указанием нормальных значений или как соотношение (индекс) ПВ больного к ПВ контрольной плазмы (пула). Надежность анализов наименьшая и зависит от тщательности приготовления пулов контрольных плазм и точности выполнения всех других технологических манипуляций. Каждая лаборатория вырабатывает свои нормальные и терапевтические значения, поэтому сравнение с другими лабораториями почти невозможно. Метод приемлем лишь в исключительных случаях и не может быть рекомендован для широкого применения (хотя раньше был единственным даже в больших лабораториях).
2. Определение ПВ ручным способом или полуавтоматическим анализатором с использованием коммерческого реагента тромбопластина с известной активностью и контрольных коммерческих плазм. Результаты выражаются как и в первом случае – в секундах, в процентах или по соотношению (индекс). Надежность анализов выше. Даже в этом случае каждая лаборатория самостоятельно устанавливает границы нормальных и терапевтических значений, зависящих от метода измерения, типа оборудования и реагентов. Метод может быть использован более широко, но не является абсолютно надежным и сравнимым.
3. Определение активности протромбинового комплекса полуавтоматическим или автоматическим анализатором с использованием коммерческого тромбопластина с обозначенным на каждой изготовленной партии (лот) реагента МИЧ и нормальных и патологических коммерческих контрольных плазм. Результаты анализов выражаются также в секундах или в процентах, но чаще всего, как это рекомендует международная стандартизация и ВОЗ, в единицах МНИ, который вручную или автоматически вычисляется по следующей формуле:
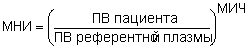
Международный комитет по изучению тромбозов и гемостаза и Международный комитет по стандартизации в гематологии с 1983 г. рекомендует выражать активность протромбинового комплекса больных в единицах МНИ, производителям реагентов обозначать МИЧ на упаковках препаратов, редакциям научных и профессиональных журналов, наряду с традиционным обозначением результатов, указывать и МНИ.
МИЧ коммерческих препаратов или препаратов тромбопластина собственного изготовления может быть установлен при сравнении их активности с принятым ВОЗ международным стандартным тромбопластином из человеческого мозга (тромбопластин сравнения Манчестера), имеющим МИЧ около 1,0.
Большинство коммерческих тромбопластинов непригодны для исследования ПВ при уровне гепарина выше 0,6 МЕ/мл стандартного гепарина или 0,6 анти-Xа МЕ/мл – низкомолекулярного, то есть при близких к терапевтическим концентрациям гепаринов в крови. Невозможность установления активности протромбинового комплекса в таких случаях не позволяет регулировать дозы АНД и контролировать безопасный переход от одного антикоагулянта к другому, особенно при развитии вызванной гепарином тромбоцитопении, или когда может развиться кратковременная гиперкоагуляция при ускоренной замене, недостаточной дозировке или преждевременной отмене АНД. Пренебрегая этим правилом, невозможно выполнить и следующее:
Доза АНД индивидуальна и предписывается только на основании данных стандартизированно установленного ПВ (ПИ) или МНИ, а поддерживающая доза АНД должна точно соответствовать клинической ситуации.
Краткая характеристика варфарина. В клинике применяется натриевая соль варфарина. Препарат представляет собой рацемическую смесь R и S оптически активных изомеров, которые в печени метаболизируются с различной скоростью. S-форма, как антагонист витамина К, примерно в 5 раз активнее. Такие же различия наблюдаются и при их элиминации. Варфарин быстро усваивается в пищеварительном тракте и соединяется с белками крови. Максимум концентрации наблюдается в крови через 90 мин, полупериод циркуляции – 36-42 ч. Снижают активность II, VII, IX, X факторов через их декарбоксилирование. Дозы препарата подбираются по результатам определения ПВ, ТВ или МНИ (терапевтическое окно 2-3 единицы МНИ). Врожденная толерантность требует приема доз, в 20 раз превышающих обычные. При приеме АНД во время беременности (разрешено с ограничениями только в первый и третий триместры) может влиять на метаболизм костей плода, но существенно не меняет его у детей и взрослых. Целый ряд лекарств изменяет метаболизм варфарина в печени, его усвоение и выделение. Действие зависит от диеты больного, количества и качества употребляемых овощей и содержания в них филлохинона. Период полураспада от 12 до 36 ч. Форма выпуска – таблетки по 1, 2, 3, 4, 5, 6, 10 мг, а также по 2,5 и 7,5 мг. Для парентерального (только внутривенно) введения выпускаются ампулы по 5 мг.
Период полураспада варфарина – 36-72 ч. Максимальная концентрация в крови достигается через 2-8 ч.
Краткая характеристика аценокумарола (синкумара). Элиминация из плазмы R-формы происходит в 11 раз быстрее, чем S-формы. Максимум концентрации в крови возникает через 24-48 ч. Период полураспада несколько короче, чем варфарина, – 8,7 ч. Дозировка описана в разделе 4.1. Форма выпуска – таблетки по 2 мг.
Краткая характеристика фенилина (фениндиона). Дозировка в первый день 120-180 мг, второй – 90-150 мг, последующие – 30-60 мг под контролем ПВ или МНИ. Высшая доза для взрослых – 30 мг, суточная – 200 мг. Форма выпуска – таблетки по 30 мг.
Похожие работы
... поверхностной вены всегда сопровождается выраженной воспалительной реакцией ее стенки. Ввиду этого часто используется термин «тромбофлебит поверхностных вен». Этиология и патогенез тромбофлебита поверхностных вен нижних конечностей мало отличаются от таковых при тромбозе глубоких вен. Самой распространенной причиной является ВРВ нижних конечностей, преимущественно, в системе большой подкожной ...
... пальпации по ходу магистральных вен на бедре и в паховой области, отрицательный симптом Гоманса. На наличие у данного больного облитерирующего атеросклероза сосудов нижних конечностей также указывают: возникновение заболевания на фоне гипертонической болезни; поражение преимущественно крупных сосудов нижних конечностей; атеросклеротическое поражение других сосудистых бассейнов (венечных артерий ...
... проверки гемостаза (отсутствия кровотечения ) накладываются кожные швы. В послеоперационном периоде обязательно необходимо применять эластическое бинтование оперированной конечности. В наши дни классическая операция при варикозном расширении вен, радикальная флебэктомия в различных модификациях, чаще по Троянову - Тренделенбургу, Бэбкокку, Нарату, претерпела значительные изменения. На первое ...
... время беременности не применяют из-за возможной гибели плода и пороков развития. У выживших больных с ТЭЛА впоследствии может развиться легочная гипертензия и легочное сердце. Профилактика послеоперационного венозного тромбоза Профилактика включает различные физические (механические) и фармакологические средства. Венозный застой как один из важнейших факторов возникновения тромбообразования ...
0 комментариев