Навигация
Белковая буферная система состоит из "белка-основания" и "белка-соли"
4. Белковая буферная система состоит из "белка-основания" и "белка-соли".
СОО- СОО-
R – СН + Н+ Û R – СН
NН2 N+Н3
белок-основание белок-соль
Соответствующее кислотно-основное равновесие в средах, близких к нейтральным, смещено влево и "белок-основание" преобладает.
Основную часть белков плазмы крови (»90%) составляют альбумины и глобулины. Изоэлектрические точки этих белков (число катионных и анионных групп одинаково, заряд молекулы белка равен нулю) лежат в слабокислой среде при рН 4,9 – 6,3, поэтому в физиологических условиях при рН 7,4 белки находятся преимущественно в формах "белок-основание" и "белок-соль".
Буферная емкость, определяемая белками плазмы, зависит от концентрации белков, их вторичной и третичной структуры и числа свободных протон-акцепторных групп. Эта система может нейтрализовать как кислые, так и основные продукты. Однако вследствие преобладания формы "белок-основание" ее буферная емкость значительно выше по кислоте и составляет для альбуминов Вк = 10 ммоль/л, а для глобулинов Вк = 3 ммоль/л.
Буферная емкость свободных аминокислот плазмы крови незначительна как по кислоте, так и по щелочи. Это связано с тем, что почти все аминокислоты имеют значения рКа, очень далекие от рКа = 7. Поэтому при физиологическом значении рН их мощность мала. Практически только одна аминокислота – гистидин (рКа = 6,0) обладает значительным буферным действием при значениях рН, близких к рН плазмы крови.
Таким образом, мощность буферных систем плазмы крови уменьшается в направлении
НСО3-/ Н2СО3 > белки > НРО42-/ Н2РО4- > аминокислоты
Эритроциты. Во внутренней среде эритроцитов в норме поддерживается постоянное рН, равное 7,25. Здесь также действуют водородкарбонатная и фосфатная буферные системы. Однако их мощность отличается от таковой в плазме крови. Кроме того, в эритроцитах белковая система гемоглобин-оксигемоглобин играет важную роль как в процессе дыхания (транспортная функция по переносу кислорода к тканям и органам и удалению из них метаболической СО2), так и в поддержании постоянства рН внутри эритроцитов, а в результате и в крови в целом. Необходимо отметит, что эта буферная система в эритроцитах тесно связана с водородкарбонатной системой. Т. к. рН внутри эритроцитов 7,25, то соотношение концентраций соли (НСО3-) и кислоты (Н2СО3) здесь несколько меньше, чем в плазме крови. И хотя буферная емкость этой системы по кислоте внутри эритроцитов несколько меньше, чем в плазме, она эффективно поддерживает постоянство рН.
Фосфатная буферная емкость играет в клетках крови гораздо более важную роль, чем в плазме крови. Прежде всего, это связано с большим содержанием в эритроцитах неорганических фосфатов. Кроме того, большое значение в поддерживании постоянства рН имеют эфиры фосфорных кислот, главным образом фосфолипиды, составляющие основу мембран эритроцитов.
Фосфолипиды являются относительно слабыми кислотами. Значения рКа диссоциации фосфатных групп находятся в пределах от 6,8 до 7,2. Поэтому при физиологическом рН 7,25 фосфолипиды мембран эритроцитов находятся как в виде неионизированных, так ионизированных форм. Иначе говоря, в виде слабой кислоты и ее соли. При этом соотношение концентраций соли и слабой кислоты составляет примерно (1,5 – 4) : 1. Следовательно, сама мембрана эритроцитов обладает буферным действием, поддерживая постоянство рН внутренней среды эритроцитов.
Таким образом, в поддержании постоянства кислотно-щелочного равновесия в крови участвует ряд буферных систем, обеспечивающих кислотно-основной гомеостаз в организме.
В современной клинической практике кислотно-щелочное равновесие (КЩР) организма обычно определяют путем исследования крови по микрометоду Аструпа и выражают в единицах ВЕ (от лат. "би-эксцесс" – избыток оснований). При нормальном кислотно-щелочном состоянии организма ВЕ = 0 (в аппарате Аструпа этому значению ВЕ отвечает рН 7,4).
При значениях ВЕ от 0 до ± 3 КЩС организма считается нормальным, при ВЕ = ± (6 – 9) – тревожным, при ВЕ = ± (10 – 14) – угрожающим, а при абсолютном значении ВЕ, превышающим 14, - критическим.
Для коррекции КЩР при ВЕ<0 (ацидоз) чаще используют 4%-ный раствор гидрокарбонаната натрия, который вводят внутривенно. Необходимый объем этого раствора в мл рассчитывают по эмпирической формуле v = 0,5mВЕ, где m – масса тела, кг.
Если состояние ацидоза возникло в результате кратковременной остановки сердца, то объем 4%-ного раствора NаНСО3 (v мл), необходимый для компенсации сдвига КЩР в кислую область, рассчитывают по формуле v = m z, где z – продолжительность остановки сердца, мин.
Коррекция КЩР при алкалозе более сложна и требует учета многих привходящих обстоятельств. В качестве одной из временных мер целесообразно введение от 5 до 15 мл 5%-го раствора аскорбиновой кислоты.
Метод кислотно-основного титрования в одном из своих вариантов (алкалиметрия) позволяет определять количества кислот и кислотообразующих веществ (солей, составленных из катиона слабого основания и аниона сильной кислоты и т. п.) с помощью растворов щелочной известной концентрации, называемых рабочими. В другом варианте (ацидиметрия) этот метод позволяет определять количества оснований и веществ основного характера (оксидов, гидридов и нитридов металлов, органических аминов, солей, составленных из катионов сильных оснований и анионов слабых кислот и т. п.) с помощью рабочих растворов кислот.
Метод кислотно-основного титрования используется в практике клинических, судебно-экспертных и санитарно-гигиенических исследований, а также при оценке качества лекарственных препаратов.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://www.monax.ru
1 Согласно протонной теории, кислотой называют всякое вещество, молекулярные частицы которого (в том числе и ионы) способны отдавать протон, т.е. быть донором протонов; основанием называют всякое вещество, молекулярные частицы которого (в том числе и ионы) способны присоединять протоны, т.е. быть акцептором протонов.
Похожие работы
... профессиональных заболеваний [27]. 5.1.1 Требование безопасности в агрохимической лаборатории Исследование почвенных образцов на кислотно-основное состояние осуществляется в агрохимической лаборатории. К работе в агрохимической лаборатории допускаются лица, не имеющие медицинских противопоказаний и прошедшие медицинский осмотр (при поступлении на работу и периодически в процессе работы). Не ...
... ионов) и сохранению масс (количество вещества в данном растворе остается постоянным, если оно не добавляется или производится, не удаляется или разрушается). В норме в плазме существует равновесие между катионами (Na+, K+, Ca++, Mg++) и анионами (Cl -, НСО3-, белки, остаточные анионы). Оно равно 153 ммоль/л и представлено в диаграмме Гэмбла. При истощении бикарбонатных буферных оснований их ...
... R – СН + Н2О N+Н3 NН2 кислота ВН+ сопряженное основание В (соль белка-основания) (белок-основание) 3.2.Определение pH стандартных буферных растворов Используемые в качестве эталонов для измерений растворы введены давно. Одним из первых таких стандартных растворов использовали «буфер» Вейбеля, представлявший собой раствор ...
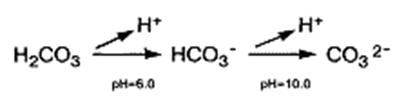
... система включает гемоглобин, различные белки и фосфаты. Она наиболее активно действует в крови и внутри клеток. Рис.1. Ион бикарбоната. Бикарбонат является ключевым компонентом главной буферной системы организма. Она состоит из двух кислотно-основных частей, находящихся в динамическом равновесии: угольная кислота / бикарбонатный ион и бикарбонатный ион / карбонатный ион. Кислоты, образующиеся в ...
0 комментариев