Навигация
Стандартизация измерения рН в неводных средах. Методы определения рН стандартных буферных растворов
МИНИСТЕРСТВО НАУКИ И ОБРАЗОВАНИЯ УКРАИНЫ
ХАРЬКОВСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
им. В.Н. Каразина
Кафедра физической химии
СТАНДАРТИЗАЦИЯ ИЗМЕРЕНИЯ рН В НЕВОДНЫХ СРЕДАХ. МЕТОДЫ ОПРЕДЕЛЕНИЯ рН СТАНДАРТНЫХ БУФЕРНЫХ РАСТВОРОВ
Курсовая работа
студентки III курса
химического факультета
****************
ХАРЬКОВ 2008
СОДЕРЖАНИЕ:
ВВЕДЕНИЕ
1.Понятие pH
2.Кислотность неводных растворов
2.1.Шкала рНр
2.2 Единая шкала кислотности
2.3 Метод Михаэлиса. Шкала рНHAc Конанта и Хелла
2.4 Определение кислотности методом Гамметта
2.5Метод нормального потенциала Плескова
2.6.Применение средних коэффициентов активности ![]() ионов для оценки единой шкалы кислотности
ионов для оценки единой шкалы кислотности
2.7 Нахождение единой кислотности рА с помощью ![]() протонов
протонов
3.Буферные растворы
3.1.Классификация кислотно-основных буферных систем
3.2.Определение pH стандартных буферных растворов
ВЫВОД
СПИСОК ЛИТЕРАТУРЫ
РЕФЕРАТ
Данная курсовая работа содержит 3 раздела, 35 страниц и 2 таблицы.
Целью работы является изучение кислотности неводных растворов, методы ее определения и стандартизация измерения, а также изучение методов определения pH стандартных буферных растворов.
В работе рассмотрено несколько методов определения кислотности неводных растворов, а также стандартных буферных растворов, проведено их сравнение в соответствии с допустимыми погрешностями измерения.
Ключевые слова: НЕВОДНЫЙ РАСТВОР, КИСЛОТНОСТЬ, КОЭФФИЦИЕНТ АКТИВНОСТИ, ПОТЕНЦИАЛ, БУФЕРНЫЙ РАСТВОР.
РЕФЕРАТ
Курсова робота містить 3 розділи, 35 сторінок та 2 малюнка.
Ціллю роботи є вивчення кислотності неводних розчинів, методи її визначення та стандартизація вимірювання, а також вивчення методів визначення рН стандартних буферних розчинів.
В роботі розглянуто кілька методів визначення кислотності неводних розчинів, а також стандартних буферних розчинів, проведено їх порівняння відповідно до припустимих похибок вимірювань.
Ключові слова: НЕВОДНИЙ РОЗЧИН ,КИСЛОТНІСТЬ, ПОТЕНЦІАЛ, КОЕФІЦІЄНТ АКТИВНОСТІ, БУФЕРНИЙ РОЗЧИН.
ABSTRACT
This term paper consists of 3 sections, 35 pages and 2 pictures.
The aim of the work is studying the acidity of nonaqueous solutions, methods of their determination, standartization of their measuring, and also studying the methods of measuring pH in standard buffer solutions.
In this work are considered several methods of acidity measuring. They were compared in accordance with acceptable errors.
Key words: ACIDITY, ACTIVITY COEFFICIENT, POTENTIAL, BUFFER SOLUTION.
ВВЕДЕНИЕ
Сложность явлений, происходящих в растворах, а также необходимость изучения растворов с широким диапазоном физических и химических свойств растворителя неизбежно привлекали внимание исследователей к неводным средам. Неводные растворители постепенно начали использовать не только для научных исследований, но и в практической деятельности. Они широко применяются в аналитической практике для улучшения условий титрования. Неводные растворители часто используются в химической, фармацевтической, нефтеперерабатывающей промышленности, в промышленности высокополимеров и в других отраслях народного хозяйства.
Быстрыми темпами осуществляется переход к проведению процессов органического синтеза в неводных средах. Замена воды органическими растворителями и переход на замкнутые системы производства позволяет, во-первых, резко интенсифицировать химические процессы, во-вторых, упрощает решение проблем, связанных с очисткой сточных вод и с нарастающей нехваткой пресной воды. Поэтому понятен интерес к методам оценки кислотности неводных растворов и растворов в смешанных растворителях.
Используемые в качестве эталонов для измерений буферные растворы введены давно. Стандартные буферные растворы используются для калибровки приборов, поэтому точность определения кислотности этих растворов должна быть высокой.
1.Понятие pH
Водородный показатель, pH — это мера активности(в случае разбавленных растворов совпадает с концентрацией) ионов водорода в растворе, количественно выражающая его кислотность, вычисляется как отрицательный десятичный логарифм концентрации водородных ионов, выраженной в молях на литр:
![]() (1)
(1)
Зависимость громадного количества химических, биохимических, природных, технологических и многих других процессов от величины рН стимулирует развитие теории и техники измерения этого показателя.
Трудно отыскать такую область науки, технологии и химии растворов, в которой не использовалась бы величина рН. Шкала рН была предложена датским химиком Зеренсеном. Изучая биохимические реакции, в частности гидролиз пепсина и усвоение протеинов в кислотно-солевых смесях, Зеренсен в 1909 году обнаружил их чрезвычайно сильную зависимость от изменения концентрации ионов водорода. Он нашел, что эффективная концентрация ионов водорода, непосредственно воздействующих на процесс, изменялась в широком диапазоне концентраций и часто оказывалась непривычно малой величиной. Для удобства Зеренсен предложил записывать ее в экспоненциальной форме сН + = 10-р = 1/10р. Позднее символ -р был заменен обозначением рН. На современном языке р понимают как оператор р = -lg, таким образом, pH = -lg[H+]. Именно так трактуется это обозначение в Номенклатурных правилах Международного союза по теоретической и прикладной химии (International Union for Pure and Applied Chemistry), ИЮПАК.
2.Кислотность неводных растворов.
2.1.Шкала рНр
Важным вопросом является определение рН в неводных и смешанных растворителях. Этот вопрос имеет практическое значение, так как в пищевой промышленности, промышленности пластмасс, фото- кино- промышленности и других отраслях промышленности широко используют измерения рН в неводных растворах.
При определении рН в неводных растворах делается еще большее количество ошибок, чем при определении рН в водных растворах.
При решении проблемы о кислотностях неводных растворов следует поставить два вопроса. Как поступать при сравнении кислотности двух растворов в одном и том же растворителе? Как поступать при сравнении кислотности растворов в двух разных растворителях? Эта задача отличается принципиально от задачи сравнения между собой кислотности в пределах одного растворителя.
Очень часто намерении pН в неводных растворах производят по отношению к водному каломельному электроду, потенциал которого определяется по водному стандарту. При этом фактически измерения сводят к измерению э.д.с цепи:
Pt(H2) | стандартный | исследуемый | Pt(H2) (2.1.1)
р-р в воде р-р в неводн р-ле
Таким образомзначения рН неводных растворов не могут быть получены путем непосредственного сопоставления потенциалов индикаторных электродов в водных и неводных растворах, а следовательно, и рН-метр, калиброванный по водным стандартам, не может дать правильных значений рН неводного раствора.
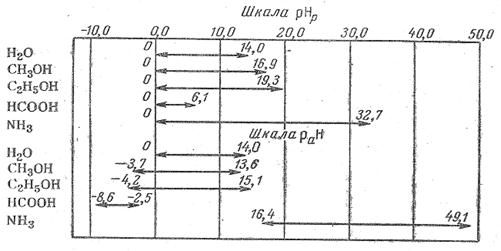
Рис. 1. Шкала рНр и шкала раН в различных растворителях.
По вопросу о стандартизации рН в неводных растворах нет единого мнения. Тем не менее расширение этого вопроса становится все более насущным в связи с широким распространением неводных растворителей, и особенно их смесей с водой, в промышленности и аналитической практике.
Задача сравнения кислотности в пределах одного неводного растворителя принципиально не отличается от задачи определения рН в водных растворах. Величина рН определяется отрицательным логарифмом активности ионов водорода в данном растворителе М:
pHp=-lga*=-lgc![]() *
*
т.е. отрицательным логарифмом произведения концентрации ионов лиония
на соответствующий концентрационный коэффициент активности. Коэффициент активности относится к бесконечно разбавленному раствору в данной среде как стандарту.
Переходя от воды в неводному растворителю, переходят от кислотности, выраженной в концентрациях или активностях одного иона - иона гидроксония, к кислотности, выраженном в концентрациях или активностях другого иона – лиония. Действительно, в воде носителем кислотных свойств является ион Н3О+. Когда по отношению к водному раствору мы говорим, что его рН = 5, это значит, что активность ионов Н3О+ равна 10-5. В спиртовом растворе носителем кислотных свойств являются ионы этоксония С2Н5ОН2+, в аммиаке носителем кислотных свойств — соответственно ионы аммония NH4+ и т. д.
При оценке рН растворов в пределах одного растворителя следует учитывать протяженность шкалы рН: в.воде вся шкала рН равна 14,0, но в этиловом спирте 19,3; в муравьиной кислоте. 6,1 и т. д. (рис. 1)
Стандартизация рН в неводных растворах может быть выполнена так же как и в водных растворах, т. е. путем изготовления стандартных растворов в том же растворителе, что и исследуемый раствор. Однако в этом случае возникает ряд затруднений. Например, коэффициенты активности сильных кислот значительно больше отличаются от единицы, чем в водных растворах; сильные в воде кислоты становятся в неводных растворах слабыми; хуже растворимы соли; значительно меньше имеется данных о коэффициентах активности.
В настоящее время единственным веществом, с помощью которого может быть произведена стандартизация рН в неводных растворах, является хлористый водород, так как для него имеются данные о коэффициентах активности в большинстве широко используемых растворителей и в их смесях с водой. В качестве электрода сравнения при измерениях в неводных растворах может быть использован хлорсеребрянный электрод в растворе НCl, который вполне пригоден для измерений в ряде чистых неводных растворителей и их смесях с водой.
Измеренная по отношению к стандарту в данном растворителю рН не является абсолютном мерой кислотности неводного раствора и может быть использована для характеристики кислотности только в пределах данного растворителя. Это следует из того, что начало шкалы кислотности раНр =0 не соответствует равенству абсолютных активностей ионов водорода во всех растворителях. Величины раН нейтральных растворов в разных растворителях не совпадают друг с другом, так как протяженность шкал, зависящая от ионного произведения растворителя, различна. В верхней части рис. 1 в качестве примера приведены шкалы рНр в воде и не которых неводных средах. В воде шкала рН изменяется от 0 до 14; нейтральным раствором называется раствор с рН = 7. Если раствор имеет рН=0, это раствор кислоты с активностью ионов Н+, равной единице; если раствор имеет рН = 14, это раствор щелочи с активностью ионов ОН--, равной единице, но это не значит, что не может быть растворов в воде с рН меньше нуля и больше 14.
Раствор, у которого рН =15, означает раствор щелочи с активностью, равной 10, растворы с рН=-1 являются растворами кислоты с активностью, равной 10.
В воде между одноактивным раствором кислоты и одноактивным раствором щелочей изменение рН равно 14, это является следствием того, что ионное произведение воды равно 10-14. В метиловом спирте ионное произведение равно 10-16,5. Это значит что между одноактивным раствором щелочи и одноактивным раствором кислоты изменение рН будет составлять 16,5 единицы. У нейтрального раствора рН будет не 7, как в воде, а 8,3. Этиловый спирт имеет шкалу протяженностью 19,3 единицы; следовательно, рН нейтрального раствора будет составлять 9,7. В аммиаке шкала имеет протяженность 32,7 единицы и нейтральный раствор в нем будет иметь рН = 16,3.
Таким образом, нужно иметь в виду, как относится величина рН данного раствора к рН нейтрального раствора.
Поэтому предложено отмечать показатель рН индексом, равным рН нейтральной точки. В воде рН-следует отмечать индексом 7 - рН7, в этиловом спирте индексом 9,7 — рН9,7 и т. д.
Мы уже говорили о невозможности определения рН в цепях, содержащих водный и неводный растворы. Измерение рН должно производиться в цепи, содержащей только один растворитель; стандартный и измеряемый растворы должны быть в одном и том же растворителе. При измерении рН в спирте стандартные растворы должны быть также спиртовыми.
Это положение не исключает практического применения водного стандарта. Можно пользоваться водным каломельным электродом и в этих случаях, но его потенциал следует измерять по отношению к неводному стандарту. В принципе стандартизация шкалы рНр всегда должна быть произведена по отношению к неводному раствору ионов водорода.
Похожие работы
... , основанной на поглощении атомами рентгеновского излучения. Ультрафиолетовая спектрофотометрия — наиболее простой и широко применяемый в фармации абсорбционный метод анализа. Его используют на всех этапах фармацевтического анализа лекарственных препаратов (испытания подлинности, чистоты, количественное определение). Разработано большое число способов качественного и количественного анализа ...
... , а затем строят калибровочный график, с помощью которого выполняют расчеты. Спектрофотометрия в УФ- и видимой областях — один из наиболее широко используемых физико-химических методов в фармацевтическом анализе. Анализируемые ЛВ должны иметь в структуре молекулы хромофорные группы (сопряженные связи, ароматическое ядро и др.), обусловливающие различные электронные переходы в молекулах и ...
... и, конечно же, за многими другими, которые будут получены, — будущее. В этом направлении и работают многие НИИ и исследователи. Аспекты поиска новых лекарств, изыскание новых лекарственных веществ состоит из трех основных этапов: химический синтез, установление фармакологической активности и безвредности (токсичности). Такая стратегия поиска с большой затратой времени, реактивов, животных, труда ...
... и природы вещества, участвующего в электрохимической реакции. Электрохимические параметры при этом служат аналитическими сигналами, при условии, что они измерены достаточно точно. Электрохимические методы анализа в практику химического анализа вошли сравнительно давно и занимают в ней важную роль. Впервые потенциометрическое титрование было проведено в 1893 г. в институте Оствальда в Лейпциге, а ...



0 комментариев