Навигация
Nagu цeldud, fььsika on teadus mis kдsitleb kehade liikumist. Selleks aga tuleb defineerida liikumist kirjeldavad suurused ehk parameetrid, mis on: asukoht (koordinaadid), kiirus, kiirendus.
Asukoht (koodinaadid).
Keha asendi ja selle muutuste (liikumise) kvantitatiivseks kirjeldamiseks kasutatakse ruumikoordinaate. Koordinaadid on arvud, mis mддravad keha kauguse mingitest kindlaksmддratud kohtaest, koordinaat-telgedest. Kolmemххtmelises ruumis on asendi mдaramiseks vajalik kolm arvu (koordinaati), kahemххtmelises (tasapinnal) kaks ja ьhemххtmelises (joonel) uksainus arv. Analoogiat edasi arendades saab ette kujutada ka enama kui kolemххtmelisi ruume, nдiteks vхttes neljanda mххtmena kasutusele aja, aga kui tarvis, veel teisi muutuvaid parameetreid. Sejuures on tдhtis, et juurdetoodavad muutujad ei oleks seoste kaudu tuletatavad olemasolevatest, vaid oleksid tдiesti sхltumatud, ortogonaalsed (piltlikult oleksid kхik teljed ьksteisega risti, kuigi neid vхib olle palju rohkem kui kolm).
Kхige sagedamini kasutatav koordinaat-teljestik on sirgete ristiolevate telgedega nn. ristkoordid e. Cartesiuse koordinaadid. Selles teljestikus mддratakse keha asukoht kolme kauguse kaudu: esiteks liikudes piki x-telge, siis ristisuunas piki y-telge ja lхpuks ristisuunas piki z-telge. Kaugused x, y ja z kokkuleppelisest nullpunktist ongi keha riskoordinaadid. Riskoordinaadistikku kasutatakse nдiteks USA-s linnade planeerimisel, kus ‘streedid’ ja ‘avenue’d on ьksteisega risti ja nummerdatud kasvavas jдrjekorras alates linna keskpunktist. Positiivsete ja negatiivsete vддrtuste asemel kasutatakse ‘North’, ‘South’, East’ ja ‘West’ lisandeid.
Cartesiuse koordinaadid ei ole ainuke viis keha asukoha mддramiseks, vaid seda saab teha ka mхne testsuguse kolme arvu kombinatsiooni abil, peaasi, et kolm liikumist, mida need arvud kirjeldavad, oleksid ikka omavahel ristsuundades. Nдiteks tsentraalsьmmeetriliste (kerakujuliste ja kerakuju moondumisena tulenenud liikumiste) kirjeldamiseks on mugavamad nn. polaarkoordinaadid. Polaarkoordinaate on ka kolm, kuid ainult ьks neist (raadius r) omab pikkuse (kauguse) dimensiooni, kaks ьlejддnut on nurgad, mis mддravad selle liikumise suuna, mida mццda minnes mддratud punkti jхutakse. Esimene on nurk (teeta), mis mддrab erinevuse vertikaalsihist ja teine on nurk , mis mдarab erinevuse kokkuleppelisest horisontaalsihist. Polaarkoordinaate kasutatakse geograafias, kus ‘pхhjalaius’ on sisuliselt 90°- ja idapikkus on Kuna mддratavad punktid asuvad kхik Maa pinnal, siis raadius oleks kхigi jaoks umbes 6000 km ja see jдetakse kirjutamata. Maapinna kohal хhus vхi maa sees olevate punktide koordinaatidele tuleks aga raadiuse vддrtus juurde lisada. Polaarkoordinaate allpool nдiteks elektroni orbitaalide kvantmehaaniliseks kirjeldamiseks vesiniku aatomis.
Liikumine, kiirus
Liikumine on keha asukoha (koordinaatide) muutumine ajas. Lihtsaim on ьhtlane sirgjooneline liikumine: konstantsed on kiiruse absoluutvддrtus ja suund.
Kiirus (v) on fььsikaline suurus, mida mххdetakse ajaьhikus lдbitud teepikkusega. Teepikkus s on kahe asukoha vahekaugus. Kolmemххtmelises ruumis avaldub teepikkus alg ja lхpp-punkti koordinaatide kaudu jдrgmiselt
![]() (1.1)
(1.1)
Pikkuse (teepikkuse) ьhikuks on meeter, m. Meeter on ligilдhedaselt 1/40000000 Maa ьmbermххtu, kuid tдpne ьhik on kokkuleppeline ja oli pikemat aega defineeritud kui kahe peene kriipsu vahe plaatina-iriidiumi sulamist siinil, mida hoiti Pariisi lдhedal, nььd aga on meeter seotud teatud aine aatomite poolt kiiratava valguse lainepikkusega. Meeter on ьks kolmest pхhiьhikust ja teda ei saa tuletada teiste ьhikute kaudu.
Kiirus
![]() ,
kust
,
kust ![]() ja
ja ![]() (1.2)
(1.2)
Viimased valemid seovad omavahel kiiruse, teepikkuse ja aja. Aja ьhikuks on sekund, s. Sekund on ligilдhedaselt 1/(365.25x24x60x60) keskmise astronoomilise ццpдeva pikkusest, kuid tema tдpne vддrtus on praegu seotud teatud aine poolt kiiratava valguse vхnkeperioodiga. Sekund on ьks kolmest pхhiьhikust ja teda ei saa tuletada teiste ьhikute kaudu. Nдiteks kiiruse ьhik on m/s ehk m s-1 ja see on tuletatud pхhiьhikutest. Suurem osa tuletatud ьhikuid on seotud pхhiьhikutega andes viimastele vддrtuse 1.
Nii
teepikkus kui ka kiirus on vektorid, millel on x, y, ja z- suunalised
komponendid. Kahemххtmelisel (tasapinnalisel juhul)
vektori s kaks komponenti on sx=scos;
sy=ssin![]()
Ebaьhtlase liikumise kiirendus (a) on fььsikaline suurus, mida mххdetakse kiiruse muutusega ajaьhikus. Sirgjoonelise liikumise kiirendus on kiiruse muutumise kiirus, seega teine tuletis teepikkuse muutumisest:
![]() (1.3)
(1.3)
Ka kiirendus on vektor, s.t., valem (1.3) kehtib sx, sy ja sz suhtes eraldi. Kiirenduse ьhik on m s-1 s-1 = m s-2 (loe: meeter sekundis sekundis).
Kiirendusega liikumise kiirus
![]() (1.4)
(1.4)
kui alghetkel kiirus ei olnud mitte null vaid v0.
Kiirendusega liikumisel lдbitud teepikkus, kui aega hakkame lugema nullist (integraali alumine rada on null ja arvutada tuleb ainult ьlemine rada):
![]() (1.5)
(1.5)
ja
teepikkuse s lдbimiseks kuluv aeg 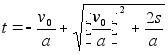 (1.4)
(1.4)
Juhul, kui algkiirus on null, siis
![]() , (1.5)
, (1.5)
kust leiame aja, mis kulub teepikkuse s lдbimiseks:
![]() (1.6)
(1.6)
ja kiiruse v, mis saavutatakse teepikkuse s lдbimisel
![]() (1.7)
(1.7)
Maa raskuskiirendus on g=9.81 m s-2 ja see mддrab vabalt langevate kehade liikumise kiirenduse.
Ьlesanded: Kuidas mддrata torni kхrgust ampermeetri ja stopperi abil?
Kui suure algkiirusega peab pumpama vett, et purskkaevu juga kerkiks 30 m kхrgusele?
Kui kхrgele ja kui kaugele ulatub sama juga kui see suunata 45 kraadi all kaldu?
Kuidas peab piloot juhtima lennukit, et kabiinis tekiks kaaluta olek?
Vдhemalt kui suure algkiirusega peab toimuma kaugushьppaja дratхuge ja missuguse nurga all tuleb see suunata, et pьstitada uus maailmarekord (oletame, et praegune maailmarekord on 9 m)?
Ringikujulisel (elliptilisel) trajektooril liikuvate kehade orbiidi leidmiseks tutvume kхverjoonelise liikumise kiirendusega, millest lihtsaim on ringjooneline liikumine.
Kхverjoonelise (ringjoonelise) liikumise tangentsiaal- (puutujasuunaline) kiirus
![]() (1.8)
(1.8)
kus r on raadius, on tiirlemisperiood ja on tiirlemissagedus. Ristikiirendus
![]() (1.9)
(1.9)
kus on nurk-kiirus. Nurkkiirust mххdetakse pццrdenurga suurenemise kiiruse kaudu, ьhik on radiaan sekundis. Tдisring on 2 radiaani, seega ьks tiir sekundis tдhendab nurkkiirust 2 radiaani sekundis.
Dьnaamika pхhimхisted ja seadused: jхud, impulss, tцц, energia
Newtoni esimene seadus (ka Galilei seadus, inertsiseadus): Iga keha liigub ьhtlaselt ja sirgjooneliselt seni kuni teiste kehade mхju (jхud) ei pхhjusta selle seisundi (kiiruse) muutumist.
Ьhtlane ja sirgjooneline liikumine on vхimalik ainult avakosmoses vдga kaugel taevakehadest. Maa pinnal on kхik kehad gravitatsioonivдlja mхjusfддris ja neile mхjub Maa kьlgetхmbejхud. Demonstratsioonkatseks on mхjudeta liikumisele ligilahedane teraskuuli veeremine horisontaalsel peegelpinnal, kus raskusjхud on liikumisega risti ja hххrdumisjхud on minimaalne. Ka piljardikuulid liiguvad kьllatki ьhtlaselt ja sirgjooneliselt kuni pхrkumiseni.
Newtoni teine seadus: Liikumise muutumise kiirus (kiirendus) on vхrdeline rakendatud jхuga ja toimub jхu suunas.
![]() ehk
ehk
![]() (2.1)
(2.1)
kus f on jхud, m on keha mass ja a on kiirendus. Vхrdetegur, mis seob kiirenduse jхuga on pццrdvхrdeline keha massiga, s.t. ьks ja seesama jхud pхhjustab seda suurema kiirenduse mida vдiksem on keha mass. Jхud f ja kiirendus a on vektorid (suunaga suurused), m on skaalar (suunata suurus). Massi ьhik on kilogramm (kg). Ьks kilogramm on ligilдhedaselt ьhe dm3 puhta vee mass, kuid tдpne massi etaloon on plaatina-iriidiumi sulamist metallkeha, mis on hoiul Pariisi lдhedal. Kilogramm on seega ьks kolmest pхhiьhikust, mille suurus on kokkuleppeline ja mida ei saa tuletada teiste ьhikute kaudu. Tuletatud ьhiku nдiteks on jхu ьhik: ьks njuuton (N) on jхud, mis annab massile ьks kilogramm kiirenduse ьks m s-2
Mass: kaal ja inerts
Massil on kaks omadust: inerts ja gravitatsioon. Huvitaval kombel on need kaks omadust alati vхrdelised ja massi suurust saab mддrata nii ьhe kui teise kaudu. Kaalumine on massi mххtmise viis gravitatsioonijхu kaudu. Mitu N kaalub keha massiga 1 kg? Kaal on raskusjхud, millega Maa tхmbab keha. Raskusjхud annab massile 1 kg kiirenduse 9.8 m s-2, sel ajal kui 1 N annab kiirenduse vaid 1 m s-2. Seega, mass 1 kg kaalub 9.8 N. Sama mass 1 kg kaaluks Kuu peal umbes kuus korda vдhem, seega umbes 1.6 N. Keha kaal sхltub ka asukohast Maal (ekvaatoril on Maa pццrlemisest tulenev tsentrifugaaljхud suurem ja see vдhendab kaalu). Kaalu vдhendab ka хhu ьleslьke. Seega, ьks kilogramm udusulgi kaalub vдhem kui 1 kg rauda, kui ei arvestata хhu ьleslьkke parandit. See parand on seda suurem, mida lдhdasemad on kaalutava keha ja хhu tihedused, kuni selleni, et vesinikuga tдidetud хhupall omab negatiivset kaalu. Хige kaalu mддramine oleks хhu ьleslьket arvestades, kuid praktikas, kui on tegu tahkete ainete vхi vedelikega, on selle tдhtsus suhteliselt vдike. Kui kьsite poest ьhe kg leiba, siis soovite te tхepoolest leiva massi, mitte selle kaalu. Seega kьsimine kilogrammides ja mitte njuutonites on fььsikaliselt хige. Kui mььja kaalub leiva vedrukaaluga, siis saab ta tulemuse njuutonites ja see sхltub laiuskraadist. Kui aga kasutatakse kangkaalu, siis vхrreldakse omavahel kaalutavat keha kaalupommide massiga ja tulemus ei sхltu laiuskraadist.
Newtoni kolmas seadus: Mхju (jхud) on
vхrdne vastumхjuga (vastujхuga) ![]() .
Kui esimene keha mхjutab teist jхuga f siis
teine keha mхjutab esimest jхuga –f.
Klassikaline nдide: paadist kaldale hьpates tхukate
paati kaldast eemale. Kumb aga liigub kiiremini, teie vхi
paat?
.
Kui esimene keha mхjutab teist jхuga f siis
teine keha mхjutab esimest jхuga –f.
Klassikaline nдide: paadist kaldale hьpates tхukate
paati kaldast eemale. Kumb aga liigub kiiremini, teie vхi
paat?
Kahe keha vastasmхjul saavad mхlemad kiirenduse pццrdvхrdeliselt nende kehade massiga:
![]() ehk
ehk
![]() (2.2)
(2.2)
Newtoni kolmandal seadusel pхhineb rakettmootori tцц. Igal ajamomendil paiskab reaktiivmootor suhteliselt vдikest kьtuse massi suure kiirendusega tahapoole, selle tulemusena liigub rakett kui suurem mass vдiksema kiirendusega vastassuunas. Protsess on pidev seni kuni mootor tццtab ja kuna kiirendus mхjub mхlemale, nii raketile kui kьtusele vхrdse aja jooksul, siis lхppkokkuvхttes suhtuvad ka raketi ja ruumi vдljapaisatud kьtusemassi kiirused nii nagu valem (2.2) nдitab kiirenduste kohta. Kui nдiteks raketi ja kьtuse massid on vхrdsed, siis on lхpuks vхrdsed ja vastassuunalised ka nende kiirused. Erinevus raketi ja ruumipaisatud kьtuse vahel on aga selles, et rakett kui tahke keha omab ьhte kindlat kiirust, kьtuse pхlemisprodukt aga on gaasiline ja valem (2.2) kehtib selle ruumilise massikeskme kohta.
Ka lindude lendamine (ja isegi loomade vхi inimese ujumine) on
sisuliselt reaktiivliikumine, sest teist vхimalust kui Newtoni
kolmanda seaduse abil хhust raskemal kehal хhus (veest
raskemal kehal vee peal) pьsimiseks ei ole. Lind lьkkab
tiibadega хhku allapoole, mхjutades хhumassi
jхuga ja andes хhule allapoole liikumise kiirenduse,
samal ajal vastujхud tхukab lindu ьlespoole. Linnu
ьlespoole liikumise kiirendus on niisama suur kui
raskuskiirendus, kuid sellega vastassuunaline, nii et mхlemad
kompenseeruvad ja lind lendab konstantsel kхrgusel. Matemaatiliselt,
![]() ,
kus m1 on linnu ja m2 tiibade all
liikuma pandud хhu mass ning a on viimasele antud
kiirendus.
,
kus m1 on linnu ja m2 tiibade all
liikuma pandud хhu mass ning a on viimasele antud
kiirendus.
Ьlesanne: Selgitada, mis ьhist on lennuki reaktiivmootoril, propellermootoril, lendamisel tiivalehvitamisega ja planeerimisel.
Ьks tдhtsamaid kiirendusest tulenevaid jхude on kesktхmbejхud ja kesktхukejхud ringlikumisel, mis on vхrdsed javastassuunalised. Keha liigub ringikujulist trajektoori mццda tдnu jхule, mis tхmbab teda keskpunkti suunas. Kesktхmbejхud vхib olla gravitatsioon (Maa tiirlemine ьkber Pдikese), elektromagnetiline (elektroni tiirlemine ьmber tuuma) vхi mehaaniline (nццr mis ьhendab lingukivi kдega, tsentrifugaalpumba korpus, mis suunab vedeliku ringtrajektoorile, aga ega nedes kehadeski esine lхppkokkuvхttes muud kui elektromagnetilised jхud). Kesktхukejхud tekib keha inersti tхttu, tema pььdest likuda sirgjooneliselt puutujat mццda. Kesktхukejхud ringliikumisel avaldub jдrgmiselt
![]() .
.
kus on nurkkiirus. Nurkkiirus seostub lineaarkiirusega jдrgmiselt:
![]() ehk
ehk ![]() ,
seega
,
seega
![]()
Kui suur on 100 kg-se mehe kaaluvahe poolusel ja ekvaatoril? Maakera raadius on 6000 km. Nurkkiirus on 2/(24x3600) = 7.27x10-5 radiaani sekundis. Asendades need vдrtused valemisse (??) saame f=100x(7.27x10-5)2x6x106 = 100x52.8x10-10x6x106= 3.168 N. Poolusel kaalub 100 kg 981 N. Suhteline kaalu kahanemine on 3.17/981=0.0032 ehk 0.32%. Meie laiuskraadil ja ekvaatoril on see suhe veel umbes poole vдiksem.
Tsentrifugaaljхu praktilisi rakendusi: tsentrifugaalpumbad ja ventilaatorid. Kuidas muutub ventilaatori ja tsentrifugaalpumba arendatav rхhk mootori pццretest?
Liikumise hulk ehk impulss.
Kui pььate
vдga massiivset keha, nдiteks autot, liikuma lьkata,
siis tuleb jхudu rakendada kьllalt kaua, enne kui
saavutate vajaliku kiiruse, nдiteks kьllaldase mootori
kдivitamiseks ilma starteri abita. See tдhendab, et keha
poolt saavutatud kiirus sхltub jхu mхjumise
ajast. Kasutame kiiruse arvutamiseks kahte seost: ![]() ,
kust
,
kust ![]()
Suurust mv nimetatakse liikumise hulgaks ehk impulsiks. Impulsi muutus on vхrdeline jхuga ja selle mхjumise ajaga ning toimub jхu suunas.
Impulsi jддvus liikuvate kehade vastasmхjudes on energia jддvuse kхrval ьks looduse pхhiseadusi. Nдiteks kahe piljardikuuli pхrkel vхi kahe gaasimolekuli pхrkel
![]()
Impulsi muutus kehade vastasmхjul on vхrdne ja vastassuunaline, sьsteemi summaarne impulss on konstantne. Impulsi mхistet kasutame allpool gaaside rхhu arvutamisel.
Tцц ja energia.
Tцц on fььsikaline suurus, mida mххdetakse jхu ja jхu suunas lдbitud teepikkuse korrutisega
![]()
Tцц ьhik on Dzhaul (Joule), [J] = [N]x[m]. Dzhaul on tцц, mida teeb jхud ьks njuuton ьhe meetri pikkusel teel. Tццd tehakse siis, kui liigutatakse mingit keha avaldades sellele jхudu. Nдiteks, tхstes 50 kg viljakotti maast 1m kхrgusele vankrile tehakse tцц mis vхrdub koti kaal (njuutonites !) korda vankri kхrgus, 50x9.8x1=490 J. Kui vesi langeb 20 m kхrguses joas kдivitades turbiini, siis iga kg vett teeb tццd 20x9.8=295 J.
Kui jхud on teepikkuse (koordinaadi) funktsioon (on muutuv sхltuvalt asukohast), siis tuleb rakendada integreerimist. Integreerida vхib liikumise ja jхu kui vektori komponente kolme koordinaadi suunas eraldi
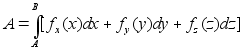
Tььpiline muutuva jхu poolt tehtud tцц arvutus on seotud keha asukoha muutusega teise keha gravitatsiooni- vхi elektrivдljas. Nдiteks, Newtoni gravitatsiooniseadus vдidab, et kahe keha vahel mхjub gravitatsioonijхud, mis on vхrdeline nende kehade masside korrutisega ja pццrdvхrdeline nedevahelise kauguse ruuduga:
![]()
Elementaartцц, mida tehakse selleks, et suurendada kehade vahelist kaugust dx vхrra oleks
![]()
ja liikumisel ьle mingi pikema vahemiku tehtud tцц oleks
![]()
![]()
Kui teepikkus on mддratud, tuleb integraal vхtta radades liikumise algpunktist lхpp-punkti. Valem ??? nдitab, et kui kahe keha vaheline jхud kahaneb kauguse suurenedes pццrdvхrdeliselt kauguse ruuduga, siis tehtud tцц kasvab kauguse kasvades pццrdvхrdeliselt kaugusega. Tхmbuvate kehade vahelise kauguse suurendamiseks tuleb teha vдlist tццd, kui kehad lдhenevad, siis nad teevad ise tццd. Tхukuvate kehade, nдiteks samanimeliste laengute vahel, on olukord vastupidine: tхukuvate kehade lдhendamiseks tuleb teha vдlist tццd, kui need kehad eemalduvad teineteisest, siis nad teevad ise tццd. Viimase juhu nдiteks oleks aatomite lдhenemine, kus vдlise elektronkihi elektronid tхukuvad ьksteise elektrivдljas. Tahkete kehade kokkupuude ja hххrdumine ongi vдliste elektronkihtide tхukumine, tegelikku fььsilist kokkupuudet ei esine kunagi.
Vхimsus on fььsikaline suurus, mida mххdetakse ajaьhikus tehtud tцц hulgaga.
![]()
Vхimsust kasutatakse nдit. mootorite ja kьttekehade hindamisel, teadmaks kui palju tццd need suudavad ajaьhikus teha. Vхimsuse ьhik on Watt [W] = [J] [s]-1 ьks Dzhaul sekundis. Elektripirnide tarbitav vхimsus on nдiteks 40 – 100 W, elektripliit 600 – 2000W, automootor 50 – 100 kW. Elektrienergia hulga mххtmiseks kasutatakse ьhikut kilovatt-tund (kWh), see on tцц, mida teeb vхimsus 1 kW ьhe tunni = 3600 s jooksul. Ьks kWh = 1000 J s-1 x 3600 s = 3600000 J = 3600 kJ.
Energia on keha vхime teha tццd.
Energiat on kahte liiki, liikuva keha kineetiline energia ja jхuvдljas asuva keha potentsiaalne energia. Energia jддvuse seadus on looduse pхhiseadus: Energia ei teki ega kao, vaid muundub ьhest vormist teise. Seega, looduses toimub kineetilise energia muundumine potentsiaalseks ja potentsiaalse energia muundumine kineetiliseks.
Liikuva keha kineetiline energia. Arvutame, kui palju tццd tuleb teha, et keha (massiga m) kiirust suurendada paigalseisust kuni vддrtuseni v. See tцц moodustabki likuva keha kineetilise energia.
Tцц=energia: ![]()
Kui suur aga on teepikkus s mille lхpuks saavutatakse kiirus v? Kasutame seost (1.7)
![]() ,
kust
,
kust ![]()
Teades, et
![]() ,
asendame selle ja saame
,
asendame selle ja saame
![]()
Nььd on selge, et
![]()
Kineetiline energia on vхime teha tццd. Liikuva keha peatumisel vхib ta enese ees lьkata teist keha mхjudes sellele jхuga ja tehes tццd. Kui auto sхidab vastu puud, siis auto kineetiline energia liigutab plekke paigast ja murrab sхitjate luid. Tдhelepanu, et auto kiiruse suurenemisel kaks korda suureneb kineetiline energia neli korda! Niisugustel deformeerivatel pхrgetel muutub kineetiline energia peamiselt molekulide soojusenergiaks. Kineetiline energia muutub potentsiaalseks energiaks kui liikuvat keha peatab jхuvдli, nдiteks kui viskame kivi ьlespoole. Gravitatsioonivдlja jхud peatab lхpuks kivi liikumise, kuid kivi kineetiline energia on muundunud tema potentsiaalseks energiaks. Sama juhtub elektronidega, kui nad saavad lisaks kineetilist energiat (nдiteks aatomite pхrgetel vхi valguse neeldumisel): nad liiguvad tuumast kaugemale.
Jхuvдljas asetseva keha potentsiaalne energia.Vaatleme esialgu gravitatsioonivдlja maapinna lдhedal. Arvutame, kui palju tццd tuleb teha keha (massiga m) tхstmiseks kхrgusele h.
![]()
Gravitatsioonivдli ja elektrivдli on nn. potentsiaalsed vдljad, kus keha potentsiaalse energia muutus sхltub ainult alg-ja lхppasukohast, mitte aga vahepealse liikumise trajektoorist. Tehtud tцц on sama, ьkskхik millist rada mццda liigutakse samade alg- ja lхpp-punktide vahel. Vabal inertsel liikumisel jхuvдljas (ilma vдlismхjudeta) potentsiaalne ja kineetiline energia pidevalt muunduvad teineteiseks, nii et summaarne energia on kogu aeg sama:
![]()
Nдiteks kхrguselt h kukkuva keha kiiruse leiame teades et kukkumise lхpuks
![]() ,
kust
,
kust ![]()
Ьlesvisatava kivi maksimaalkхrguse vхime samuti leida tema algenergia (algkiiruse) kaudu.
Kineetilise ja potentsiaalse energia muundumine toimub ka lihastetццs. Nдiteks vхib teoreetiliselt arvutada, kui kхrgele saab hьpata kirp, kelle kehas keskmine ATP kontsentratsioon on 0.1 mM, eeldades, et ATP keemiline energia kхik muutub hьppel kineetiliseks energiaks.
Eelmised ьlesanded on lihtsad, sest ьlesvisatud keha kхrgus muutub suhteliselt Maa raadiusega sedavхrd vдhe, et rakusjхudu saab lugeda konstantseks. Kui aga kaugus muutub suhteliselt palju, nдiteks nagu kosmoselendudel, vхi nagu elektroni kaugus muutub tuuma suhtes, siis ei saa ei gravitatsiooni- ega elektrivдlja jхudu enam konstantseks lugeda vaid tцц (energia) arvutamisel tuleb arvestada, et jхud muutub koos kaugusega.
Jхudude tasakaal, kiirus ja energia ringjoonelisel tiirlemisel.
Looduses asuvad kхik kehad ьksteise jхuvдljades, suuremad kehad gravitatsioonivдljas, vдikeste kehade puhul on oluline elektrivдli. Ometi ei kuku tхmbuvad kehad ьksteise peale, sest sellisel juhul oleks kogu Universum ammu kokku kukkunud, elektronid oleksid kukkunud aatomituumadesse ja planeedid nende Pдikestesse. Loodust stabiliseerib see, et kehad tiirlevad ьksteise ьmber, nii et kesktхmbejхud ja kesktхukejхud on vхrdsed ja radiaalsuunalist kiirendust (jхudu) ei esine. Kasutades fььsikast teadaolevaid valemeid gravitatsioonilise (elektrilise) kesktхmbejхu ja inertsiaalse kesktхukejхu kohta saab nende tasakaalutingimustest tuletada nдiteks kui suur on tiirleva keha potentsiaalne, kineetiline ja summaarne energia.
Mхlemad, nii elektrivдlja kui ka gravitatsioonivдlja tugevus (mхjuv jхud) kirjelduvad ьhe ja sellesama seadusega:
gravitatsioonivдli: ![]() ja elektrivдli:
ja elektrivдli:
![]()
kus m on keha mass, e on keha laeng (indeksid nдitavad esimese ja teise keha oma eraldi), r on nendevaheline kaugus ka konstant k mддrab seose kasutatava ьhikute sьsteemiga. Kui masse mххdetakse kilogrammides, siis gravitatsioonijхu saamiseks Njuutonites omab gravitatsioonikonstant kg vддrtust ????. Kui laenguid mххdetakse Coulombides (Kulonites, C) siis elektrostaatilise tхmbejхu saamiseks Njuutonites elektrivдljakonstant ke omab vддrtust ????.
Muide, selles, et need konstandid ei oma vддrtust 1, vдljendub fььsikalise mххtьhikute sьsteemi ajalooliselt kujunenud ebajдrjekindlus. Sьsteemselt хige oleks olnud massiьhikuks vхtta niisugune mass, mis teist samasugust tхmbab ьhe pikkusьhiku kauguselt ьhikulise jхuga. Seesama ьhikuline jхud aga peab andma ьhikulisele massile ka ьhikulise kiirenduse. Et see aga nii tuleks, peaks nii massi, pikkuse kui ajaьhikut vastavalt muutma. Praegused pхhiьhikud ei ole ьldse seotud gravitatsiooniseadusega. Samasugune on lugu elektrilaenguьhikutega. Formaalselt peaks laenguьhik Coulomb (Kulon) olema defineeritud kui laeng mis tхmbab teist samasuurt vastasmдrgilist laengut pikkusьhiku kauguselt ьhikulise jхuga. Tegelikult on aga Coulomb defineeritud hoopis magnetvдlja kaudu: Coulomb on laeng, mis liikudes ьhe sekundi jooksul lдbi 1 m pikkuse traadi mхjutab teist samasugust traati, milles voolab niisama tugev vool, 1 m kauguselt jхuga 1 N. See definitsioon baseerub magnetvдljal, mis on liikuvate laengute ьmber ruumis. Elektrivдlja jхud avaldub nььd aga ьlaltoodud kaliibrimiskonstandi kaudu.
Leiame keha (laengu) potentsiaalse energia tsentraalsьmmeetrilises gravitatsiooni- (elektri-) vдljas. Kuna jхud on tugevasti kaugusest sхltuv, siis tuleb kindlasti rakendada integreerimist. Laengu liikumisel elektrivдljas vдga lьhikesel teepikkusel tehtud tцц on
![]()
![]()
kus liikumise teepikkust tдhistame seekod raadiuse (kugus tsentrist) muutusena dr. Kui laeng liigub raadiuselt r1 raadiusele r2, peame integreerima vastavates radades:
![]()
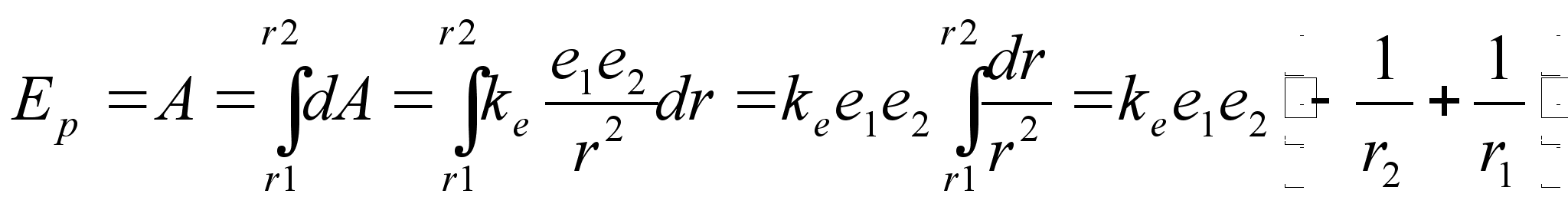
Valem
nдitab, et tsentraalsьmmeetrilises elektrivдljas
liikudes muutub laengu potentsiaalne energia pццrdvхrdeliselt
kaugusega tsentrist. Analoogiline valem kehtib ka gravitatsioonivдlja
kohta, ainult et seal esinevad kahe laengu asemel kaks massi ja
elektrivдlja konstandi asemel gravitatsioonikonstant. Kui laeng
liigub tsentrist eemale, siis r2>r1
ja negatiivne liige on vдiksemkui positiivne,
seega siis potentsiaalne energia kasvab. Vastupidi, potentsiaalne
energia kahaneb, kui laeng liigub tsentrile lдhemale.
Potentsiaalse energia nullnivoo on aga kokkuleppeline. See vхiks
olla ьks ддrmuslikest seisunditest, kas ![]() vхi
vхi
![]() (lхpmatus). Siiski, raadius ei saa olla null, sest siis
lдheneb energia lхpmatusele, seega jддb
kokkuleppeliseks nulliks nivoo, kus laengud asetsevad teineteisest
lхpmatu kaugel. Lдhenedes aga nende potentsiaalne energia
kahaneb, seega muutub negatiivseks, ja lдheneb miinus
lхpmatusele kui laengud kohtuvad. Niisugune potentsiaalse
energia nullnivoo definitsioon, mis on hea elektronide ja tuumade
vahelise mхju kirjeldamiseks aatomites, on erinev
igapдevakogemusest gravitatsioonilise energiaga, kus nulliks
loeme tavaliselt energia maapinnal ja energia loeme positiivselt
kasvavaks kui keha maapinnast kaugeneb. Kui valemis ???
(lхpmatus). Siiski, raadius ei saa olla null, sest siis
lдheneb energia lхpmatusele, seega jддb
kokkuleppeliseks nulliks nivoo, kus laengud asetsevad teineteisest
lхpmatu kaugel. Lдhenedes aga nende potentsiaalne energia
kahaneb, seega muutub negatiivseks, ja lдheneb miinus
lхpmatusele kui laengud kohtuvad. Niisugune potentsiaalse
energia nullnivoo definitsioon, mis on hea elektronide ja tuumade
vahelise mхju kirjeldamiseks aatomites, on erinev
igapдevakogemusest gravitatsioonilise energiaga, kus nulliks
loeme tavaliselt energia maapinnal ja energia loeme positiivselt
kasvavaks kui keha maapinnast kaugeneb. Kui valemis ??? ![]() ,
st. elektron lдheneb tuumale lхpmatu kaugelt, siis tema
potentsiaalne energia on alguses null ja kahaneb lхpuks
vддrtusele
,
st. elektron lдheneb tuumale lхpmatu kaugelt, siis tema
potentsiaalne energia on alguses null ja kahaneb lхpuks
vддrtusele
![]()
![]()
![]()
Kuna see energia kuhugi kaduda ei saa, siis muutub ta elektroni liikumise kineetiliseks energiaks, st., lдhenedes tuumale elektron liigub kiirenevalt, nii nagu nдiteks asteroid liigub kiirenevalt lдhenedes Maa pinnale. Vahe on siiski selles, et elektron ei lange kunagi tuumale, vaid jддb tiirlema mingil kaugusel ьmber tuuma. Tiirlemise kaugus (raadius, on mддratud sellega, millal elektriline tхmbejхud vхrdub inertsiaalse kesktхukejхuga. Matemaatiliselt avaldub see tingimus jдrgmiselt:
![]()
Selle valemi vasak pool on varasemast tuttav kesktхukejхu valem keha massiga m ringliikumisel joonkiirusega v ьmber tsentri kaugusel r. Valemi parem pool on elektrostaatilise tхmbejхu valem, kuid siin on juba arvestatud, et aatomis positiivne ja negatiivne laeng on vхrdsed, mхlemad vддrtusega e.
Eelmisest valemist saab leida raadiuse, mille saab siduda nii elektroni kiiruse kui tema kineetilise energiaga:
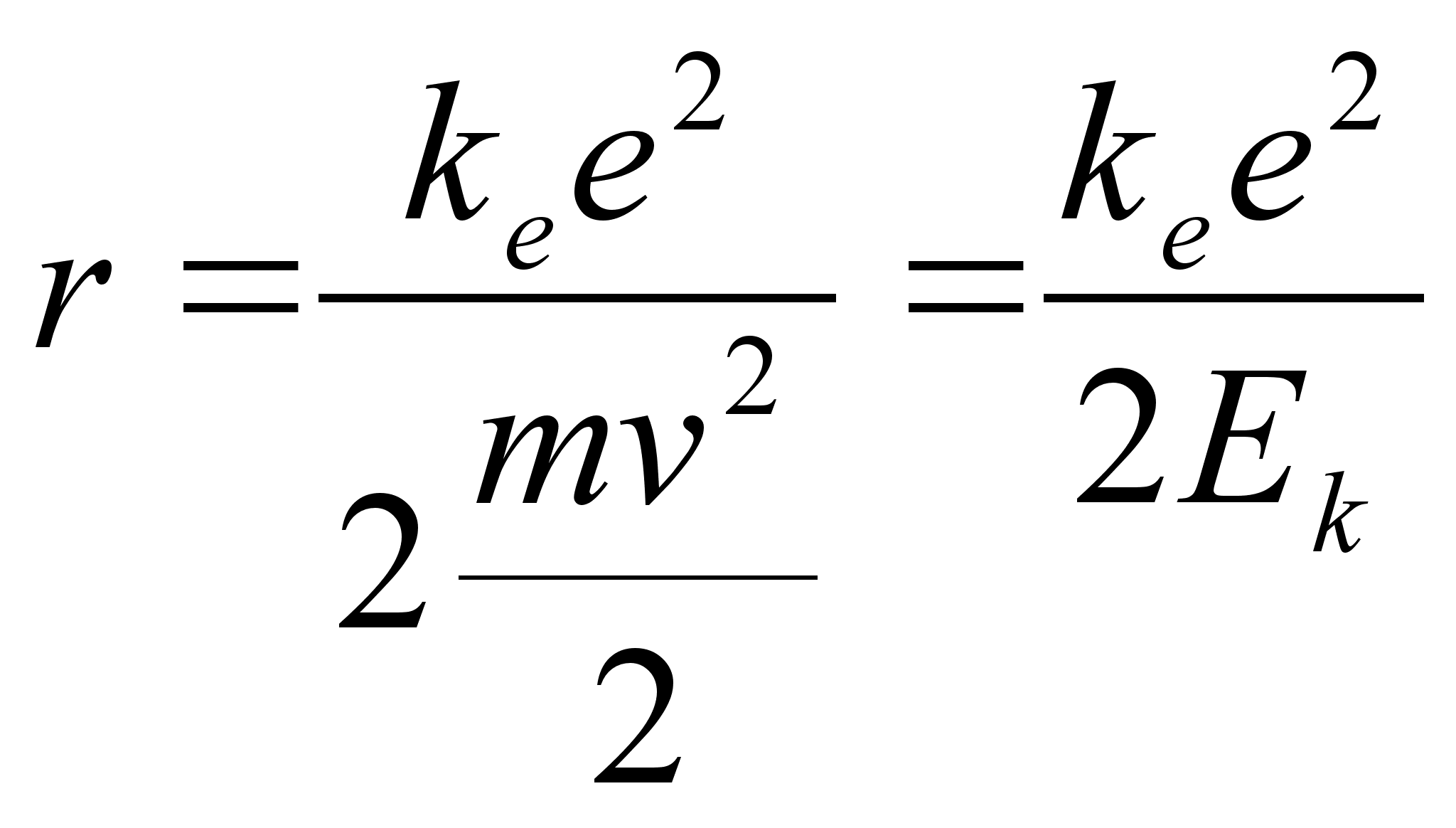
vхi
![]()
Ьmber tuuma tiirleva elektroni kineetiline energia kasvab kui elektron lдheneb tuumale (r kahaneb). Tuletame meelde, et potentsiaalne energia samal ajal kahanes:
![]() ,
,
ja summaarne energia
![]()
Elektroni summaarne energia kahaneb kui elektron asub tiirlema orbiidile mis on tuumale lдhemal. Kuhu see energiavahe siis lдheb, millisesse vormi muutub (kaduda ju ei saa)?
See energiavahe peab aatomist eralduma ja seda ta ka teeb, kas valguskvandi kujul, vхi kandub ьle mхnele naaberaatomile, tхstes selle elektroni vastavalt kхrgemale energianivoole, vхi eraldub soojusena, s.o. muutub aatomi translatoorseks (kulgevaks) liikumiseks. Niisugune elektronide ja tuuma vahelise kauguse muutumine, elektronide tiirlemine erineva raadiusega orbiitidel, on peamine keemiliste ainete siseenergia, keemilise energia olemus. Ained, mille molekulides elektronid tiirlevad tuumadest kaugemal, on energiarikkamad ja vхivad seda vabastada kui keemilise reaktsiooni tulemusena toimuvad muutused, mille tulemusena elektronid saavad tuumadele lдhemale asuda. Bioloogiliste protsesside energeetika on samadel alustel: fotosьnteesis tхstetakse elektron valguskvandi abil kхrgemale energianivoole, tuumast kaugemale orbiidile, ja metabolismi kдigus ta jдrkjдrgult lдheneb tuumale, vabastades niimoodi kvandi poolt talle antud energia.
Kas aga elektronid saavad tiirelda ьmber tuuma igasugustel kaugustel? Kui see nii oleks, vхiks ju vabastada vдga suuri keemilise siseenegia koguseid lubades elektronil asuda tuumale vдga-vдga lдhedale (lastes raadiuse nulli lдhedale). Tхepoolest, klassikaline fььsika seda lubaks, kuid tegelikkuses seda ei juhtu. Siin tulevad sisse kvantmehaanilised piirangud, mis klassikalise fььsika abil ei seletu. Jдrgnevas tutvumegi atomaarse kvantteooria pхhialustega.
BOHRI AATOMIMUDEL
Eelmises lхigus tuletasime valemid, mis kirjeldavad ьmber tuuma tiirleva elektroni kiirust ja energiat. Igale elektroni kineetilise energia vддrtusele Ek vastaks kindel raadius r. Klassikalise fььsika seisukohtade kohaselt tekitab aga tiirlev elektron muutuva elektromagnetilise vдlja: elektron on perioodiliselt kord tuumast parmal, siis jдlle vasemal, seega ‘pluss’ ja ‘miinus’ vahelduvad nagu televisiooni saateantenni varrastes, vahe on ainult mххdus ja tiirlemise sageduses. Muutuva elektromagnetilise vдlja kaudu peaks elektroni tiirlemisenergia vдlja kiirguma, elektron peaks tuumale lдhenema ja lхpuks tuumale kukkuma. Tegelikult seda ei toimu, kхik aatomid maailmas on stabiilsed ja tavaliselt ei kiirga energiat. Selles on klassikalise mehhaanika pхhivastuolu tegelikkusega. Seda vastuolu ei saa eletada, see tuleb lihtsalt teadmiseks vхtta ja postuleerida, et teatud kindlate energiavддrtuste puhul on elektronide orbiidid aatomis stabiilsed ja energiat ei kiirgu, kuigi pхhjus, miks ei kiirgu, ei ole teada. Kui see aga teadmiseks vхtta, siis saab sellele ьles ehitada uut sorti mehanika – kvantmehaanika. Esimeseses jдrjekorras tuleb postuleerida, missugused on need orbiidid, millel elektron saab stabiilselt tiirelda ilma energiat kiirgamata.
Uurides kuumutatud kehadelt kiirguva valguse spektreid leidis Max
Planck (1900) ka siin vastuolu, mis lahenes, kui eeldati, et valgusel
on kvantiseloom: valgus kiirgub energiaportsjonite e. kvantide kaupa,
millest igaьhe energia ![]() ,
kus on valguslaine
vхnkumise sagedus.
,
kus on valguslaine
vхnkumise sagedus.
Lдhtudes sellest postuleeris Bohr (1913): elektroni tiirlemisel ьmber tuuma elektrmagnetilist lainet (=valgust) ei kiirgu, kui elektron tiirleb orbiitidel millel potentsiaalne on
![]() .
.
Kineetiline energia oli positiivne ja pool potentsiaalsest energiast:
![]() ,
,
Nendes valemites on elektroni tiirlemise sagedus, n aga mingi tдisarv 1, 2, 3, 4 jne.
Kasutades seost joonkiiruse ja nurkkiiruse vahel, mille abil sagedus teisendatakse joonkiiruseks, saame:
![]() ja
ja
![]()
ja vхime kirjutada
![]()
ehk
![]()
vхi vхttes mхlemad pooled ruutu saame:
![]() .
.
Elektrostaatilise tхmbejхu valemist (???) saame massiga m lдbi korrutades:
![]()
Kahe viimase valemi vasakud pooled on vхrdsed. Paremate poolte vхrdsustamisel saame avaldada lubatud raadiuse
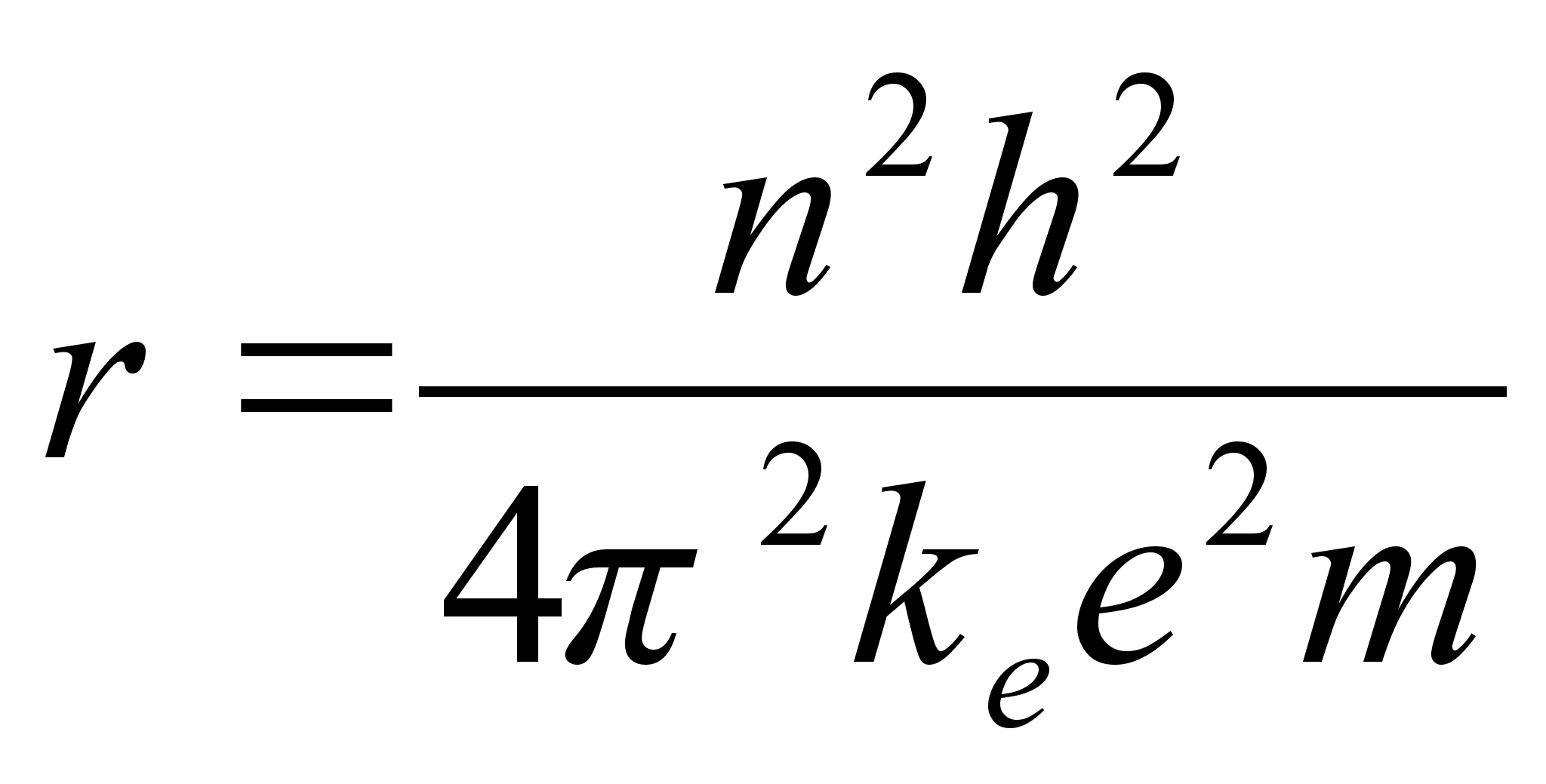 .
.
Need nn. Bohri raadiused ongi vхimalikud raadiused millel elektron saab asuda stabiilselt ilma energiat kiirgamata.
Avaldame elektroni kineetilise energia tema massi m ja laengu e kaudu. Selleks asendame r valemisse (???) vхi (???). Saame
![]()
Samale orbiidile vastav potentsiaalne energia
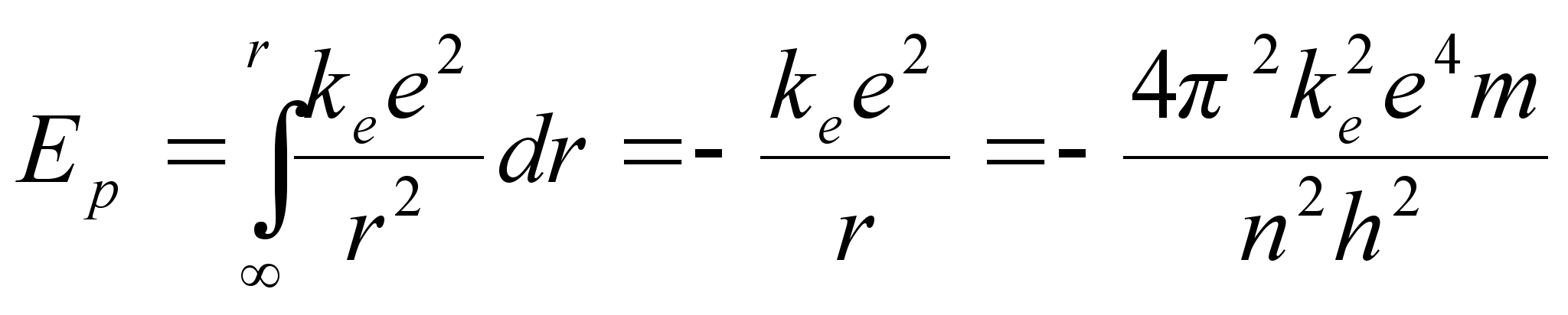
ja koguenergia, mis vastab orbiidile, mida iseloomustab tдisarv n
![]()
Vхimalike naaberorbiitide energiate vahe
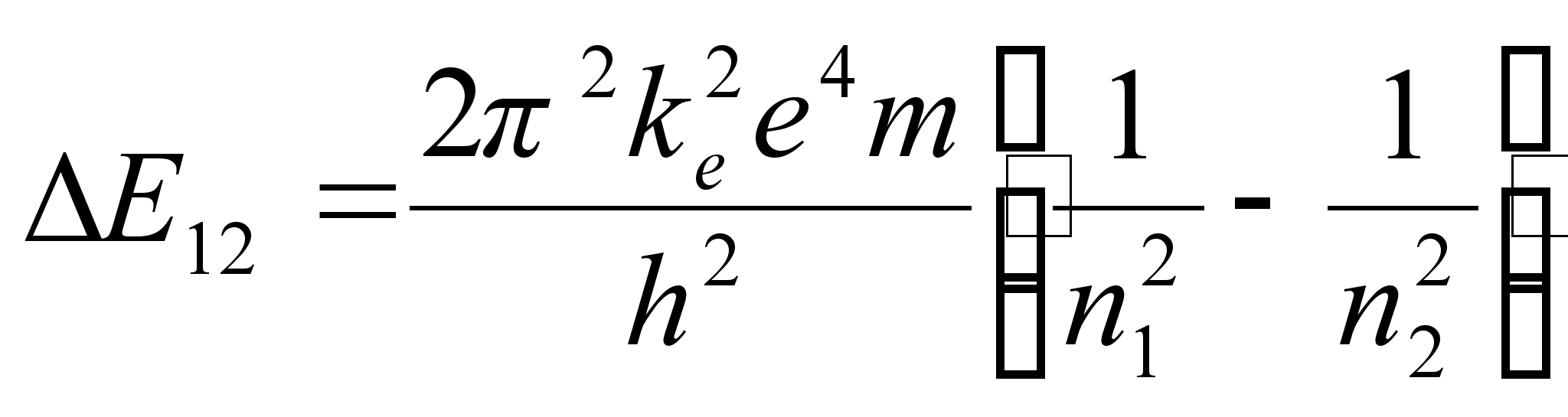
Elektroni tiirlemissageduste vahe kahel naaberorbiidil vхrdub vдljakiiratava (vхi neelatava) valguse sagedusega kahe orbiidi vahelisel ьleminekul:
![]()
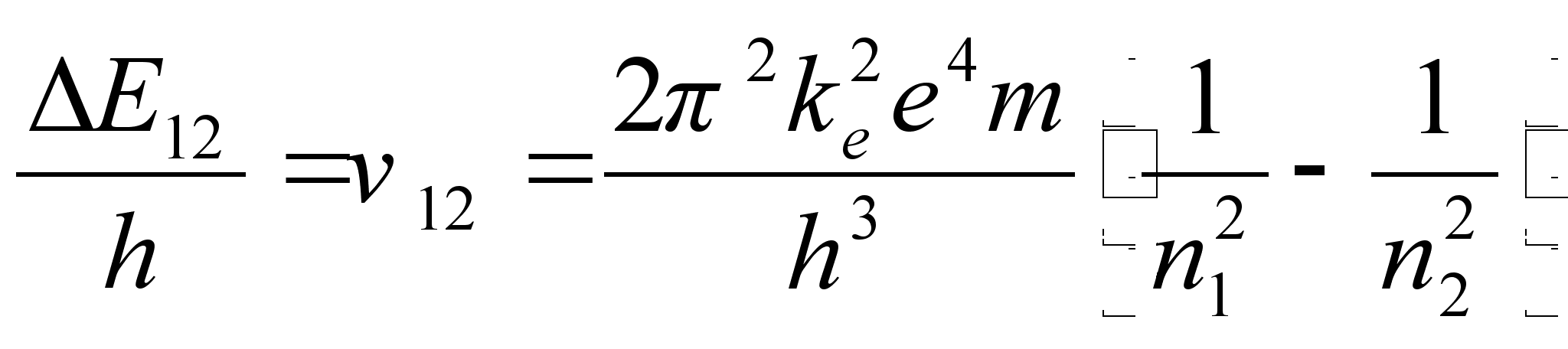 ja lainepikkus
ja lainepikkus ![]() kus c on valguse kiirus.
kus c on valguse kiirus.
Arvulisi andmeid: e = 1. 6021892·10-19 kulonit; h= 6.626176·10-34 J·s; me = 9.109534·10-31 kg
c = 299792458 m s-1 ke=???
Valem (???) nдitab, et elektroni vхimalikud tiirlemisraadiused suurenevad vхrdeliselt tдisarvude ruutudega, seega jada on 1, 4, 9, 16, 25, 36 ...
Valem (???) nдitab,et elektroni koguenergia vхimalikel orbiitidel suureneb raadiuse kasvades pццrdvхrdeliselt tдisarvu n ruuduga, seega jada oleks
![]()
Kхige sьgavama energianivoo (pхhinivoo) vддrtus on vesiniku aatomis -13.6 eV, nivoode jada elektronvoltides oleks siis
-13.6; -3.4; -1.5; -0.85; -0.54; -0.38 ...eV
Volt (Itaalia teadlase Volta nimest) on elektrivдlja potentsiaali (potentsiaalse energia) ьhik. Elektrivдlja kahe punkti potentsiaalide vahe on ьks Volt kui laengu ьks kulon viimisel ьhest punktist teise tehakse tццd ьks J. Ьhe elektroni viimisel lдbi potentsiaalide vahe ьks volt tehakse tццd ьks elektronvolt. Energeetiliselt elektronvolt on dzhaulist niisama palju kordi vдiksem kui elektroni laeng on vдiksem kulonist, seega 1 eV = 1. 6021892·10-19 J.
Orbiitide ja energianivoode joonised.
Nдhtav ja nдhtamatu elektromagnetiline kiirgus, valgus.
Energianivoode-vahelisel ьleminekul kiiratakse kvant kui ьleminek toimub tuumale lдhemale ja neelatakse kvant kui ьleminek toimub tuumast kaugemale. Kvandi energia on niisama suur kui vastavate orbiitide energianivoode vahe. Vхtame teadmiseks, et vesiniku sьgavaimale energianivoole vastab 13.6 eV ja arvutame sellele ьleminekule vastava lainepikkuse.
![]()
See on silmale nдhtamatu lьhilaineline ultraviolett-kiirgus. Silm nдeb ‘valgust’, mis on defineeritud kui elektromagnetiline kiirgus lainepikkuste vahemikus 400-700 nm ehk kvandi energiavahemik 3.10 kuni 1.77 eV. Vesiniku aatomisisestest ьleminekutest kiirguks nдhtavat kiirgust ьleminekutel kхrgematelt nivoodelt teisele nivoole, teiselt esimesele nivoole ьleminek kiirgab kvandi lainepikkusega 121.7 nm.
Seega, valguse ja sellest lьhemate lainepikkustega kvandid kiirguvad elektroni ьleminekul kхrgema energiaga orbiidilt madalama energiaga orbiidile, energiavahe kiirgub kvandina. Ka vastupidine protsess, kvandi neeldumine aatomis pхhjustades elektroni ьlemineku madalamalt orbiidilt kхrgemale, on vхimalik. Nagu vesiniku aatomi analььs nдitas, on lubatud tдiesti kindlad energianivood, seega niisuguses aatomis kiirguvad ja neelduvad ainult vдga tдpselt mддratud lainepikkustega kvandid. Vesiniku aatomis on pхhinivoo nii sьgaval, et sinna ьleminekul saavad kiirguda vaid ultraviolett-kvandid. Paljelektroniliste aatomite vдliste kihtide lubatud pхhinivood ei asu mitte nii sьgaval ja neis kiirguvad/neelduvad ka nдhtava valguse kvandid. Nдiteks, tihti kasutatakse elavhхbe-auru ja naatriumi-auruga tдidetud lampe, kus elektrienergia abil sunnitakse metalliaatomeid kiirgama nдhtavat valgust. Kui aatomid asuvad gaasis tihedalt lдhestikku, siis nad pхrkuvad soojusliikumise tхttu ja need pхrked moonutavad orbiitide kuju. Tulemusena nihkub igas moonutatud orbiidiga aatomis energianivoo veidi ja kogu gaas ei kiirga enam mitte joonspektrit teatud kindlate lainepikkustega, vaid nn. ribaspektrit, kus jooned on laienenud ribadeks.
Joonis: ribaspektri nдidis kхrgrхhu elvhхbeauru-lambis.
Tahkes kehas asuvad aatomid nii tihedasti koos, et iga ьksiku aatomi energianivoo muutub vдga ebamддraseks. Kui tahket keha, nдiteks metalli vхi sьtt kuumutada, siis see hakkab valgust kiirgama. Madalamal temperatuuril on see kiirgus pikemalainelisem, nдhtavaks muutub see tumepunasena kusagil 600 °C juures. Temperatuuri edasisel tхstmisel hakkab domineerima jдrjest lьhemalainelisem kiirgus, muutudes silmale nдhtavalt kollakaks, valgeks (nagu Pдike) vхi isegi sinakaks (nagu kuumad tдhed). Niisugustes kuumutatud tahketes kehades on kiirguse energiaallikaks aatomite (molekulide) soojusliikumine, mis pхrgetel ‘ergastab’ elektrone, lьkates neid ajutiselt kхrgematele niivoodele, kust nad siis kohe jдlle alla kukuvad, kiirates kvante. Kuna aatomid asuvad vдga tihedalt, siis on ka lubatud energianiivood vдga tihedalt ligistikku, nii et igasuguse energiaga kvantide kiirgumine on vхimalik. Sellest tulenevalt on kuumutatud tahkete kehade kiirgus pideva spektriga. Kuumutatud gaasides aga kiirgub ikkagi joon- vхi ribaspekter. Nagu цeldud, on madala temperatuuriga kehades lьhilaineliste (kхrge energiaga) kvantide kiirgumine vдhetхenдone ja neis domineerivad pikemalainelised kvandid. Nдiteks Maa keskmine temperatuur on umbes 290 °K ja Maa kiirgab kosmosesse infrapunast kiirgust lainepikkuse maksimumiga umbes 10 m. Seevastu Pдikese temperatuur on umbes 6000 °K ja tema kiirgusmaksimum on 0.5 m lainepikkuse juures. Hххglampide niidi temperatuur on umbes 2000-3000 °K ja kiirgusmaksimum umbes 1 m juures. Nagu nдeme, on silm kohastunud nдgema just selles spektripiirkonnas, kus Pдike kiirgab maksimaalselt. Seevastu hххglampide spektrist suurt osa silm ei nдe. Sellepдrast ongi hххglampide valgusviljakus (valguslik kasutegur) suhteliselt madal (10-20%).
Joonised: Pдikese ja hххglampide spektri nдited.
Mateeria lainelised omadused: kvantmehaanika kui lainemehaanika
Uurides musta tahke keha kiirgusspektrit leidis Max Planck (1900), et see vastab energia juhuslikule jaotusele ainult tingimusel, et mitte igasugune kiirgumine ei ole vхimalik, vaid ainult kiirgumine portsjonite, kvantide kaupa, mille igaьhe energia ja vхnkesagedus on seotud jдrgmiselt:
![]()
kus on vхnkesagedus ja h nn. Planck’i konstant, mis on ьks looduse universaalsetest konstantidest. Veidi hiljem leidis Alber Einstein oma ьldrelatiivsusteooriast et elementaarosakeste (prootonite, elektronide jne.) mass ja energia on omavahel seotud:
![]()
kus c on valguse kiirus. Nendest kahest valemist jдrgneb, et kvandil (footonil) kui elektromagnetiliste lainete ‘paketil’ peab siiski olema ka mingi mass
![]() .
.
Seega on footon kahesuguste omaduste, nii lainepakett kui ka massiga osakene. De Brouglie (1927) arendas seda mхtet edasi, et absoluutselt iga osakene, millel on mass, omab samaaegselt ka lainelisi omadusi. Kui eelmine valem teisendada, saame
![]() ,
,
kust
![]()
See valem on kirjutatud footonite jaoks, mis alati liiguvad kiirusega c ja ei saa kunagi liikuda vдiksema kiiruega. De Brouglie aga oletas, et massi ja lainepikkust siduv valem kehtib iga osakese kohta, ka nende kohta, mis vхivad seista paigal vхi liikuda valguse kiirusest vдiksema kiirusega. Sellisel juhul valem sisaldaks valguse kiiruse asemel osakese (keha) tegelikku kiirust
![]()
Vaatame, mida see hьpotees tдhendaks Bohri aatomimudelis tiirleva elektroni kohta, milline oleks selle ‘lainepikkus”?
Elektroni kineetiline energia orbiidil, millele vastas tдisarv n oli
![]()
Avaldades siit kiiruse v saame
![]()
ja vastava elektroni lainepikkuse
![]()
Vхrdleme elektroni lainepikkust Bohri raadiusega
![]()
ehk
![]()
Viimases valemis lisasime raadiusele indeksi n nдitamaks, et tegu on just nimelt tдisarvule n vastava raadiusega. Valem ise aga nдitab, et tдisarvule n vastavale orbiidile mahub just nimelt n tдislainet. Tuletame meelde, et kхrgemal orbiidil on elektroni kiirus vдiksem, seega lainepikkus suurem. Siit jдreldub, et orbiidi ьmbermххt (ka raadius) suureneb kahel pхhjusel: elektroni lainepikkus suureneb ja orbiidile paigutatavate lainete arv ka suureneb. Siit tulenebki vдliste orbiitide lдbimххdu kiire kasvamine kui elektroni summaarne energia hakkab nullile lдhenema (elektron kaugeneb tuumast vдga kaugele).
Lainemehaanika alged
Lained on ruumis edasilevivad vхnkumised. Edasilevimine tuleb sellest, et mingis ruumipunktis toimuv muutus kutsub esile sarnase muutuse naaberpunktis, aga veidi hiljem. Elektroni orbiidil ringlevad samuti lained, kuid kummas suunas? Et eelissuunda ei ole, siis levivad lained mхlemas suunas liikudes vastamisi. Kui seejuures on veel orbiidil tдisarv laineid, siis tekib resultatiivselt nagu laine seiskumine, vastassuunalised levimised kompenseeruvad. Seega, elektron aatomi orbiidil moodustab seisva laine. Ьldse, madalama potentsiaalse energiaga ruumiosas kinnihoitavad lained moodustavad alati seisvad lained, ja seda madalama potentsiaaliga ruumiosa kutsutakse ‘potentsiaaliauguks’. Gravitatsioonivдljas on kahemххtmeline potentsiaaliauk nдiteks kaev, kus ergastatud lained peegelduvad kaevu seintelt ja moodustavad veepinnal seisvaid laineid. Kolmemххtmeline elektripotentsiaali auk on nдiteks tuuma ьmbrus, mis hoiab elektrone kinni kui seisvaid laineid. Seisvat lainet kirjeldav matemaatika on lihtsam kui levivat lainet kirjeldav, sest ajalisi muutusi ei esine ja vastav diferentsiaalvхrrand aega ei sisalda.
Juba varem leidsime, et vхnkumiste vхrrand on teist jдrku diferentsiaalvхrrand. Nдiteks massi ajaliste vхnkumiste jaoks oli pхhiprintsiip, et tasakaalu poole suunatud jхud on vхrdeline hдlbega tasakaalupunktist, seega kiirendus on vхrdeline hдlbega tasakaalupunktist. Ruumilise vхrrandi pхhimхte on sama, ainult jхu ja kiirenduse mхistet siin kasutada ei saa:
![]()
Vхrrand on ьhemххtmeline, kus mingi suurus A lainetab x-telje suunas. Kui lainetus vхib esineda kolmes ruumisuunas, siis kirjutatakse lainefunktsiooni lьhidalt
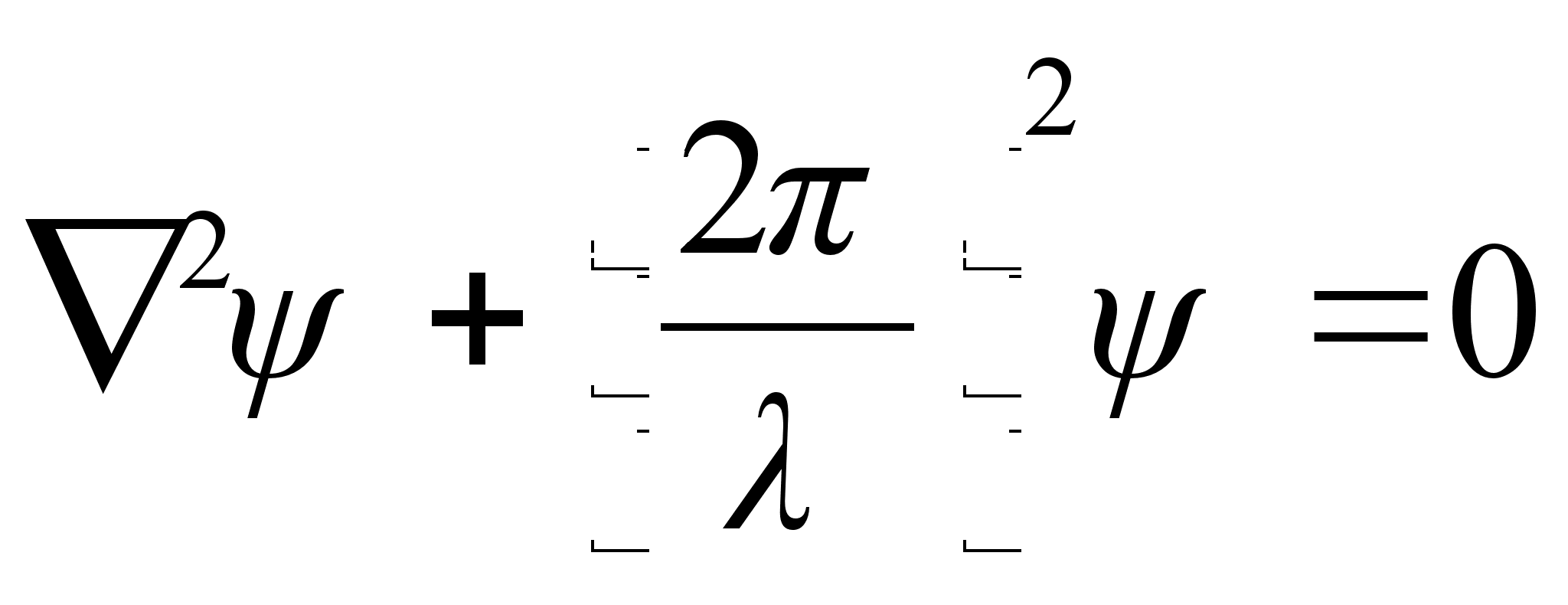 ,
kus
,
kus 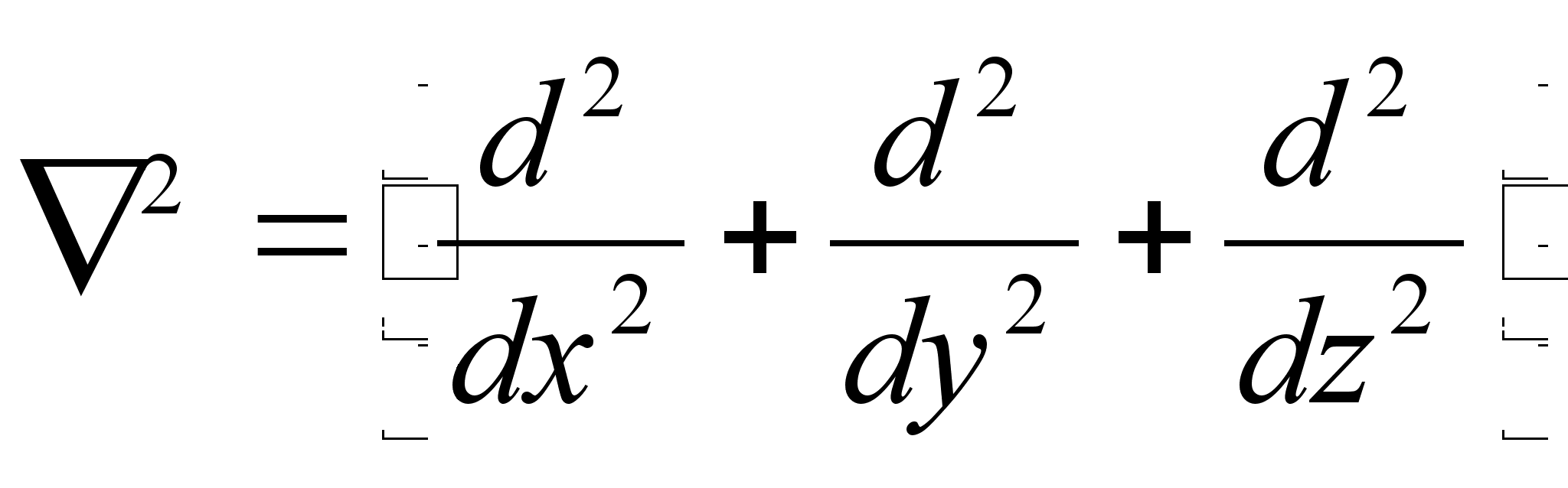
Asendades
![]() saame
saame
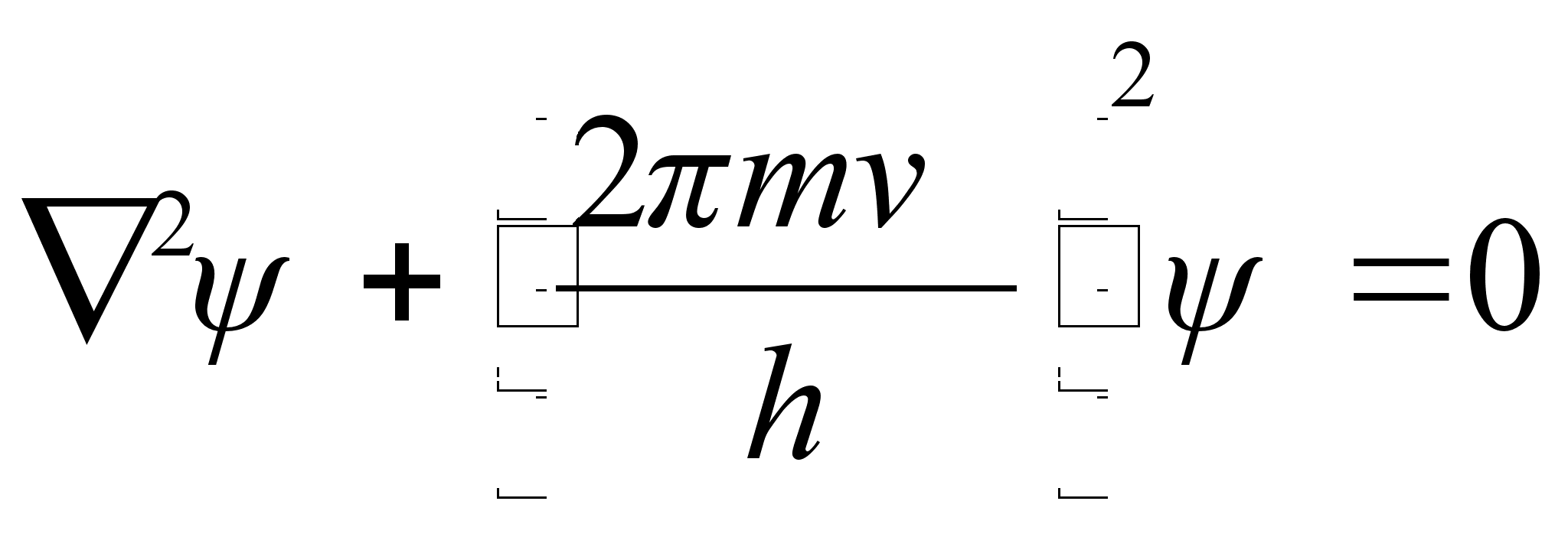
Et lainete oluliseks parameetriks on mitte kiirus, vaid energia, siis avaldame kiiruse kineetilise energiaga kui koguenergia ja potentsiaalse energia vahega:
![]()
ja
![]()
See on
kvantmehaanika pхhivхrrand, nn. Schrцdingeri
vхrrand, ja tema kolmemххtmeline lahend esitabki
lainefunktsiooni, mis kirjeldab elementaarosakest kui seisvat lainet
potentsiaaliaugus. Viimane tingimus tдhendab, et lahend on
olemas kui koguenergia on negatiivne. Selle vхrrandi ruumiline
(kolmemххtmeline) lahend esitabki elementaarosakese kui
vхnkumise. Lainetav osakene vхib esinaeda teatud
tхenдosusega igas ruumipunktis. Osakese esinemise
tхenдosuse tihedust kirjeldab lainefьnktsiooni ruut
![]() ja tema leidmise tхenдosus ruumiosas dV on
ja tema leidmise tхenдosus ruumiosas dV on ![]() .
Tuuma ьmber tiirleva elektroni korral on koguenergia mддratud
Bohri aatomi jaoks leitud tingimustega ja lainete arv mingil
energianivool on vхrdne tдisarvuga n, mis
iseloomustas seda energianivood.
.
Tuuma ьmber tiirleva elektroni korral on koguenergia mддratud
Bohri aatomi jaoks leitud tingimustega ja lainete arv mingil
energianivool on vхrdne tдisarvuga n, mis
iseloomustas seda energianivood.
Oluline on tдhele panna, et Schrцdingeri vхrrand ei sisalda aega, seega elektroni leidmise tхenдosus mingis punktis on kogu aeg ьks ja seesama, elektron asub kogu aeg mingis piiratud ruumiosas. Elektroni hoiab selles ruumiosas elektrivдli, mille potentsiaal on negatiivne, st., mis tхmbab elektroni. Tхmbavat, madalama potentsiaaliga (elektroni potentsiaalse energiaga) ruumiosa nimetatakse ‘potntsiaaliauguks’, analoogia pхhjal auguga maapinnas, kuhu sissekukkunud kehad sealt ise enam vдlja ei pддse. Tuumale lдhenenud elektron ongi kukkunud potentsiaaliauku. Joonisel on nдidatud lihtsaim ьhemххtmelise potentsiaaliaugu juht, kus vдljaspool ‘auku’ on potentsiaal ьhtlaselt kхrgem ja augus sees ьhtlaselt madalam, tuletades meelde nдiteks kaevu maapinnas. Elektroni lainetamist niisugune potentsiaaliaugus on matemaatiliselt lihtne arvutada, sest summaarne energia E-Ep on augus sees kхikjal sama ja vхrrand (???) laheneb sinusoidaalsete vхnkumistena. Tдhtis on, et vхrrand ei lahene mitte igasuguse energiavддrtuse puhul, vaid ainult niisuguste puhul, mis vхimaldavad augu mххtmesse paigutada tдisarvu poollaineid. Sisuliselt tдhendab see tingimus, et augu servas, kus potentsiaal jдrsult tхuseb, peab elektroni leidmise tхenдosus olema null (vt. joonist). Siit tulenebki potentsiaaliaugus asetseva lainetava elektroni lubatud energia kvantiseeritus, mille tulemusena vхrrand laheneb ainult teatud tдisarvuliste kordajatega n seotud energiavддrtuste jaoks. Kvantarvu n mхte on sama, mis Bohri aatomis, ta seob elektroni lubatud energia Plancki konstandi h kaudu vхnkesagedusega, lainepikkusega, mis tдpselt mahub ‘potentsiaaliauku’.
Kuigi elektroni leidmise tхenдosus mingis ruumipunktis on konstant, sхltub see oluliselt, millist ruumipunkti me vaatleme. Nдiteks potentsiaaliaugu serval on see null ja on null iga poollaine jдrel. Poollaineid on seda rohkem, mida kхrgem on elektroni energia. Muide, tдpselt null on elektroni leidmine seina-ддres ainult siis kui ‘sein’ on lхpmatu kхrge, st. potentsiaaliauk on vдga sьgav, vдga madala pontentsiaaliga. Madalasse seina tungib elektron veidi sisse, ja kui see sein ei ole mitte vдga paks, siis ulatub lektroni lainetus veidi ka naaberauku (Joonis tunnelefekti kohta). Seega, elektron, mis asub piiratud madala potentsiaaliga ruumiosas vхib siiski teatud vдikese tхenдosusega sattuda ka naaberauku, kuigi nende vahel on sein. Seda nдhtust nimetatakse tunneleffektiks ja sellel on bioloogias suur tдhtsus elektroni ьlekandeprotsessides: Kui lдhestikku asuvad kaks aatomit, siis vхib elektron kanduda ьle ьhelt teisele, kuigi vahepeal on kхrge potentsiaaliga ruumiosa (‘sein’).
Nagu цeldud, on Schrцdingeri vхrrand lihtne lahendada ja annab siinusekujulised lained ainult siis kui summaarne energia on potentsiaaliaugus konstantne. Aatomituuma ьmbruses aga on potentsiaaliauk hoopis sьgava lehtri kujuline, langedes pццrdvхrdeliselt kaugusega tuumast. See teebki vхrrandi lahendamise keeruliseks ja annab tulemuseks mitte konstantse lainepikkusega siinuselised lained, vaid pidevalt lьheneva lainepikkusega lained, seda lьhema lainepikkusega, mida madalam on potentsiaal antud kaugusel. Kirjutame need lahendid vesiniku aatomi jaoks siiski vдlja, sest nendest tulenevad kvantarvud, n, l, ja m, mis mддravad elektronide vхimaliku paigutuse aatomis.
Elektroni lainetus vesiniku aatomis
Schrцdingeri vхrrandi lahendamine ьmber tuuma asetseva elektroni jaoks on eelmises punktis vaadeldust keerukam kahel pхhjusel: esiteks, lahend ei ole mitte ьhemххtmeline, vaid kolmemххtmeline ja potentsiaaliauk ei ole mitte sileda pхhjaga, vaid lehtrikujuline. Kuna probleem on ilmselt tsentraalsьmmeetriline, siis on otstarbekas Schrцdingeri vхrrand kirjutada ruumilistes polaarkoordinaatides r, ja Tuletame meelde, et rist-ja polaarkoordinaadid on omavahel seotud jдrgmiselt:
![]()
![]() ja
ja ![]()
Asendades need Scrцdingeri kolmedimensionaalsesse vхrrandisse saame matemaatiliselt jдrgmise ьldvхrrandi elektroni kohta vesiniku aatomis
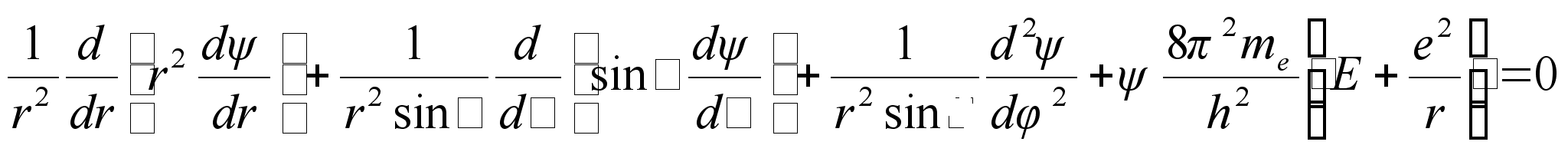
Siin me on elektroni mass. Selle vхrrandi lahendamine ьldjuhul ei olegi vхimalik, vaid vaja on teha teatud eeldusi. Nimelt eeldatakse, et kolmemххtmeline lainefunktsioon avaldub kolme ьhemххtmelise lainefьnktsiooni korrutisena:
![]()
See on fььsikaliselt vдga oluline koht, eeldades, et vхnkumised kolmes eraldi ruumi suunas toimuvad sхltumatult, ьksteist mхjutamata. Elektroni summaarne energia kujuneb vдlja kolmesuunaliste vхnkumiste energiate summana. Rakendades seda eeldust ja tehes matemaatilised teisendused saame kolm eraldi vхrrandit, igaьks oma koordinaadis toimuvate vхnkumiste kohta:
![]()
![]()
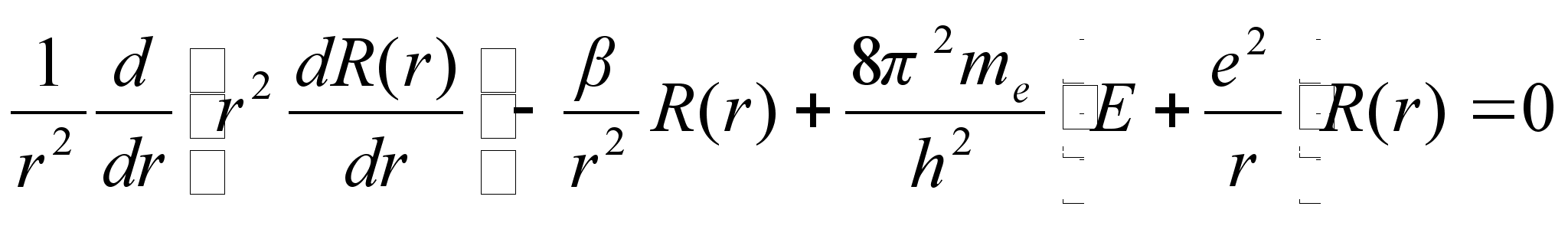
Nendes vхrrandites m ei ole elektroni mass vaid mingi tдisarv, samuti nagu
Esimene kolmest vхrrandist lahendub vдga lihtsalt. Nagu oodatud, on vхnkumised polaarnurga suunas siinuselised, sest asimuudi suunas on ju potentsiaalne energia konstantne. Tдisarv m on siin lubatud energiat mддrava kvantarvu rollis.
![]()
Samuti annab siinuselise lahendi teine vхrrand, sest ka polaarnurga suunas on potentsiaalne energia konstantne. Siin on aga lahend keerukam, sest sisldab kahte kvantarvu, m ja Keerukaim lahend on aga raadiusesuunaline, sest siin on potentsiaalne enegia muutlik, pццrdvхrdeline raadiusega. Ometi onkasee lahendatud ja leitud tingimused kvantarvu n jaoks, mille puhul lahend on olemas (lubatud energiate vдartused).
Ьlatoodud vхrrandites on kvantarvud esitatud siiski keerukamal kujul kui lihtsas Schrцdingeri vхrrandis. Pхhjus on selles, et, nagu mainisime, on elektroni summaarne energia nььd mддratud kolme energia summaga, vastavalt igas koordinaadis toimuvale vхnkumisele. Keemiliste ja fььsikaliste protsesside jaoks on aga tihti kхige tдhtsam summaarne energia, pealegi vхimaldaks ьhe summaarset energiat vдljendava kvantarvu sissetoomine siduda kolmemххtmeliselt vхnkuva elektroni ьhemххtmeliselt tiirleva elektroni kvantiseeritud energiaga, nii nagu see oli Bohri aatomis. Seega, tuleks tuua sisse peakvantarv n, mis nдitab kхigis koordinaatides toimuvate vхnkumiste energiate summat, ja kхrvalkvantarvud, mis nдitavad, kui suur osa summaarsest energiast on jaotunud ьhe vхi teise koordinaadi suunas. Niisuguset loogikast tulenebki, et vхrrandid ja jaoks sisaldavad juba ise mingeid tдisarve, mis on allutatud tдisarvule n, mis ei sisaldu R vхrrandis vaid tuleneb selle lahenduvuse tingimusena. See alluvuste jada on jдrgmine:
Tдisarv n, peakvantarv, vхib omada tдisarvulisi positiivseid vддrtusi alates nullist: n=0, 1, 2, 3, ...
Fььsikaliselt, n nдitab vхngete (lainete) koguarvu raadiuse r ja tхusunurga suunas kokku.
Valemis
??? ![]() kus l vхib omada positiivseid tдisarvulisi
vддrtusi 0, 1, 2, 3, ...n-1. Suurust l nimetatakse
orbitaalkvantarvuks ja see nдitab, mitu vхnget on
tхusunurga suunas. Vхnked asimuudi suunas
ei muuda elektroni energiat muidu kui aatom ei asetse vдlises
magnetvдljas. Seetхttu ei olegi asimuudisuunalisi vхnkeid
energiat mддravate vхngete koguarvu sisse loetud ja
kvantarvu m nimetatakse magnetkvantarvuks. Tema lubatud
vддrtused on allutatud orbitaalkvantarvu l
vддrtustele ja vхivad olla vahemikus –l..0..+l.
kus l vхib omada positiivseid tдisarvulisi
vддrtusi 0, 1, 2, 3, ...n-1. Suurust l nimetatakse
orbitaalkvantarvuks ja see nдitab, mitu vхnget on
tхusunurga suunas. Vхnked asimuudi suunas
ei muuda elektroni energiat muidu kui aatom ei asetse vдlises
magnetvдljas. Seetхttu ei olegi asimuudisuunalisi vхnkeid
energiat mддravate vхngete koguarvu sisse loetud ja
kvantarvu m nimetatakse magnetkvantarvuks. Tema lubatud
vддrtused on allutatud orbitaalkvantarvu l
vддrtustele ja vхivad olla vahemikus –l..0..+l.
Seega, seoses sellega, et ruum on kolmemххtmeline, on elektronil kolm kvantarvu, mis iseloomustavad vхngete arvu iga koordinaadi suunas. Selleks, et ьks kvantarv iseloomustaks vхimalikult hдsti koguenergiat, on vхrrandid lahendatud nii, et peakvantarv n vastab kahe koordinaadi raadiuse ja tхusunurga suunas toimuvate vхngete koguarvule.Asimuudi suunas toimuvad vхnked ei mхjuta elektroni koguenergiat muidu kui aatom ei asetse vдlises magnetvдljas, seetхttu on magnetkvantarv m summast vдlja jдetud. Peame meeles jдrgmised reeglid:
n=1,2,3,4,5....
l=0, 1, 2 ...(n-1)
m=0, ±1, ±2, ...±l.
Peakvantarv n vхib omada positiivseid tдisarvulisi vддrtusi.
Orbitaalkvantarv ehk kхrvalkvantarv l vхib omada tдisarvulisi vддrtusi alates nullist kuni ьhe vхrra vдiksema vддrtuseni kui n. See tдhendab, et tхusunurga suunas ei pruugi toimuda ьhtegi vхnget, vхib toimuda ьks, kaks jne, vхnget, kuid vдhemalt ьks vхnge peab jддma raadiuse suunale, muidu kaotaks aatom raadiusemххtme, mis on ju ainuke pikkuse dimensiooniga suurus kolme polaarkoordinaadi hulgas.
Magnetkvantarv m on allutatud kхrvalkvantarvule ja vхib omada vддrtusi alates –l lдbi nulli kuni +l –ni. Keemikud on mugavuse mхttes tдhistanud kvantarvude vддrtusi ka tдhtedega:
Peakvantarvu jaoks: K(n=1); L(n=2); M(n=3); N(n=4) jne
kхrvalkvantarvu jaoks: s(l=0); p(l=1); d(l=2) f(l=3).
Joonisel on illustreeritud rariaalkomponendi R kuju sхltuvalt peakvantarvu n ja kхrvalkvantarvu l vдartustest. Kui n=1 siis on elektronil ainult ьks laine ja see peab olema raadiusesuunaline (l=0). Laine ei ole aga siinuseline, vaid muutub vдga kхrgeks ja teravaks tuumale lдhedases ruumiosas, seoses sellega, et seal potentsiaaliauk kukub kiiresti sьgavaks. Kui n=2 ja l=0, on raadiusesuunas kaks lainet, kui n=3 ja l=0, on raadiusesuunas kolm lainet. Nььd on eriti selgesti nдha, kuidas potentsiaali langemine tuuma suunas pхhjustab lainepikkuse pidevat lьhenemist. Pange tдhele ka, kui kaugele aatomi tsentrist elektroni lained ulatuvad: ьhe vхnke puhul umbes 4 A (A=Ongstrцm, = 10-10 m= 0.1 nm), kahe vхnke puhul 6A ja kolme puhul 12 A. See arv kahekordselt on vesinikuaatomi lдbimххt sхltuvalt sellest missugusel energianivool elektron asub (kas n=1,2 vхi 3). Seega, pхhisesundis n=1 katab aatomi lainefunktsioon diameetri umbes 8A, kuid ergastatud seisundis (n=2 vхi 3) kuni 20 A. Kui l =1, on raadiuse suunas ьks vхnge vдhem, kui l=2 siis kaks vхnget vдhem, kuid aatomi ьldmххt sellest ei muutu, vaid raadiusesuunaline lainepikkus vastavalt suureneb. (Kuidas see ьhtib vдitega, et muutujate lahutamine tдhendab eeldust, et vхnked kolmes koordinaadis on sхltumatud??).
Eelmises lхigus leidsime, et elektroni leidmise tхenдosuse tihedust esitab lainefunktsiooni ruut (lainefunktsioon vхib olla ka negatiivne, kuid ruut on ikka positiivne). Tхenдosuse tihedus korrutatud vastava ruumi suurusega annab elektroni leidumise tхenдosuse selles ruumiosas. Juhul kui l=0 on lainefunktsioon maksimaalne kohal r=0, seega tuuma vahetus ьmbruses on elektroni tхenдosustihedus suurim. Kuna aga tuum ise on tohutult pisike (ruum vдheneb raadiuse kuubiga!) siis elektroni leidumise tхenдosus otse tuumas on ikkagi vдga-vдga vдike, nagu nдha ka vastavalt jooniselt. Sхltuvalt raadiusesuunaliste leinete arvust moodustab elektron tхenдosuspilve millel on ьks, kaks, kolm vхi enam suurma tihedusega kohta, tuumast keskmiselt seda kaugemal, mida suusrem on n. See langeb kokku Bohri aatomi analььsil saadud tulemusega, et elektron vхib tiirelda kindlatel kaugustel, seda kaugemal, mida suurem on energia, kuid lainemehaanikast nдeme, et elektroni orbiit ei ole mitte kindel joon vaid muutuva tihedusega tхenдosuse pilv.
Pilt lдheb veelgi huvitavamaks kui katsume lainefunktsiooni kolme koordinaadi suunalisi komponente korraga ette kujutada, seega aatomi ruumilist pilti ette kujutada. Aatom on lihtne kerakujuline ainult juhul kui vхnked on ainult raadiuse suunas (l=0 ehk s-orbitaalid). Kui l=1 (p-orbitaalid) on tхusunurga suunas ka vхnge, mis moonutab kerakujulise tхenдosuspilve kaheksakujuliseks. See kaheksakujuline moodustis vхib ruumis paikneda kolmel viisil, vastavalt m=-1,0+1, nii nagu nдidatud joonisel. Kui vдlist magnetvдlja ei ole, siis need erinevad paiknemisviisid koguenergiat ei mхjuta. Magnetvдlja olemasolul aga mхjutavad ja vastavalt jagunevad spektrijooned kolmeks. Siit siis kolmanda kvantarvu nimetuski - magnetkvantarv. Kui l=2 ja tхusunurga suunas on kaks vхnget, tekivad veelgi kummalisema kujuga moodustised viiel erineval moel. Seega, joonisel ?? toodud raadiusesuunalised tхenдosuspilved l vддrtuste 1 ja 2 jaoks on kehtivad nendes ristlхigetes kus raadiusesuunaline tхenдosus on maksimaalne.
Milleks me bioloogilises fььsikas tungime nii sьgavale kvantmehaanikasse? Selleks, et mхista, et ainult tдnu aatomite lainelisele ehitusele on elu vхimalik. Elusstruktuurid moodustuvad keerukast aatomite sьsteemist, mis seostuvad ьksteisega kindlates jдrjestustes ja kindlates suundades. Ruumiline struktuursus on ju valgu molekuli peamine omadus. Kui kхik valku moodustavad aatomid oleksid kujult ьmargused nagu herneterad (nдit. nagu Bohri aatomi ringikujulised orbiidid), siis ei oleks aatomite sidumine kindlates suundades vхimalik. Ei ole ju herneteradest vхimalik kokku panna keerulisi ehitisi, kьll on see aga vхimalik nдiteks Logo elementidest, mis ei ole ьmargused. Isegi lihtne vee molekul nдeks siis hoopis teistsugne vдlja kui aatomid oleksid ьmargused. Tдnu sellele, et p ja d orbitaalid (l=1 ja 2) moodustavad ruumilis kujundeid millel on vдljavenitused kindlates suundades, haakuvad nendega teiste aatomite p- ja d-elektronid moodustades kindlasuunalisi sidemeid. Niimoodi, ьksteisest kindlatel kaugustel ja kindlates suundades paigutatud aatomitest ehituvad ьles elusaine molekulid, nendest omakorda rakud ja koed ja organismid. Aatomite paigutus molekulis ja molekulide omavaheline haakumine mддrabki selle kuidas elusaine ьles ehitatakse. Seega, elu olemust saab mхista ainult mхistes kvantmehaanika pхhialuseid.
Mitme elektroniga aatomid
Kuigi vesinik on ьks tдhtsamaid looduses esinevaid elemente, on bioloogias siiski tдhtsad veel sьsinik, lдmmastik, hapnik ja veel mitmed teised elemendid. Sьsinikul on kuus, lдmmastikul seitse ja hapnikul kaheksa elektroni. Kvantmehaanilist lainevхrrandit saab aga tдpselt lahendada ainult kahe keha jaoks, seega ьhe elektroni ja ьhe prootoni jaoks. Mitme elektroniga aatomites on oluline veel elektronide omavaheline mхju ja selle tдpne arvestamine ei ole vхimalik. Meie siin unustame elektronide vastatstikuse mхju ja kujutame ette, missugune oleks mitme elektroniga aatom kui elektronid omavahel ьksteist ei mхjutaks vaid kхik oleksid vastasmхjus ainult tuumaga.
Kui elektrone on mitu, on ka prootoneid mitu ja vastavalt on tuuma laeng suurem ja elektriline kьlgetхmme tugevam. Seega on tuuma ьmbruses ‘potensiaaliauk’ sьgavam (potentsiaalne energia langeb kiiremini) ja pхhisesundi n=1 lainefunktsioon koondub tuumale lдhemale. Samuti on tuumale lдhemal ka teised, kхrgemale energiale vastavad orbitaalid. Kuidas aga paigutuvad elektronid, kas kхik ьhel, kхige madalama energiaga orbitaalil? Ei, selgub, et tдpselt ьhesuguse lainefunktsiooniga elektrone saab aatomis olla ainult ьks. See on nn. Pauli printsiip, mille kohaselt elektronid jaotuved erinevate energianivoode vahel tдites need madalamast kхrgemani. Seega peaks igale orbitaalile mahtuma ainult ьks elektron, mis on iseloomustatud kolme kvantarvuga n, l, m. Selgub aga, et elektronil on veel ьks omadus, mis lisab veel ьhe kvantarvu, spinn s, mis kirjeldab elektroni sisemine pццrlemise suunda. Kuigi on raske ette kujutada kuidas ьks tхenдosuspilv veel sisemiselt iseenese ьmber pццrleb nagu vдrten (inglise keeles “spin”) ilmneb see sellest, et elektronil on magnetmoment. Iga elektron on nagu pisike magnetike, mis vхib olla suunatud tuuma magnetvдlja suhtes (ka tuumal on magnetmoment) kahes erinevas suunas. Vastavatest vхrranditest tuleneb selle kvantarvu vддrtuseks kas +1/2 vхi –1/2. Ьhele ja samale orbitaalile mahub seega kaks elektroni, ьks spinniga =1/2 ja teine spinniga –1/2. Nььd on meil kдes kхik tingimused, et asuda ьles ehitama paljuelektroniliste aatomite elektronkatte struktuuri: elektrone tuleb juurde lisada orbitaalidele jдrjekorras, alates madalamate energiatega seisunditest kхrgemate suunas, mahutades igale orbitaalile mitte rohkem kui kaks elektroni. Teeme selle programmi lдbi kuni teise perioodi (n=2) kхigi nivoode tдitumiseni, sest see kaasab ka bioloogiliselt tдhtsad elemendid C, N, O.
H: n=1;l=0;m=0;s=1/2 ьks paardumata spinniga elektron, keemiliselt aktiivne
He: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2 kхik elektronid paardunud spinnidega, inertgaas
Li: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2 ьks paardumata spinniga elektron, keemiliselt aktiivne
Be: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2 kхik elektronid paardunud spinnidega, keemiliselt inertne
B: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2 ьks paardumata spinniga elektron, keemiliselt aktiivne
C: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2
n=2;l=1;m=0;s=1/2 kaks paardumata spinniga elektroni, keemiliselt aktiivne
N: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2
n=2;l=1;m=0;s=1/2
n=2;l=1;m=1;s=1/2 kolm paardumata spinniga elektroni, keemiliselt aktiivne
O: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2
n=2;l=1;m=-1;s=-1/2
n=2;l=1;m=0;s=1/2
n=2;l=1;m=1;s=1/2 kaks paardumata spinniga elektroni, keemiliselt aktiivne
F: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2
n=2;l=1;m=-1;s=-1/2
n=2;l=1;m=0;s=1/2
n=2;l=1;m=0;s=-1/2
n=2;l=1;m=1;s=1/2 ьks paardumata spinniga elektron, keemiliselt aktiivne
Ne: n=1;l=0;m=0;s=1/2
n=1;l=0;m=0;s=-1/2
n=2;l=0;m=0;s=1/2
n=2;l=0;m=0;s=-1/2
n=2;l=1;m=-1;s=1/2
n=2;l=1;m=-1;s=-1/2
n=2;l=1;m=0;s=1/2
n=2;l=1;m=0;s=-1/2
n=2;l=1;m=1;s=1/2
n=2;l=1;m=1;s=-1/2 kхik elektronid paardunud spinnidega, inertgaas
Ьlaltoodud orbitaalide tдitumise jдrjekorrast nдeme, et kхigepealt tдituvad orbitaalid ьhe elektroniga ja alles nende vхimaluste ammendumisel asub teine, vastupidise spinniga elektron samale orbitaalile.
Illustratsiooniks toome tдieliku perioodilise sьsteemi tabeli, mis nдitab orbitaalide tдitumise jдrjekorda ka kхrgema n vддrtuse jaoks kui n=2. Pхhimхte on see, et s-orbitaalidele (l=0) mahub kaks elektroni 2x(m=0); p-orbitaalidele (l=1) mahub kuus elektroni 2x(m=-1,0+1); d-orbitaalidele (l=2) mahub kьmme elektroni (m=-2,-1,0,1,2). Aga juba alates komanda perioodi lхpust tekivad ebaregulaarsused, mis on pхhjustatud sellest, et vхnked tхusunurga suunas on mхnevхrra energiarikkamad kui vхnked raadiuse suunas. Seetхttu pдrast Argooni (Ar) oleks oodata elektronide asumist 3d nivoole, kuid K ja Ca aatomites tдituvad enne hoopiski 4s orbitaalid, mis asuvad energeetiliselt madalamal kui 3d orbitaalid. Alles seejдrel tдituvad jдrjekorras 3d orbitaalid, jдttes 4s orbitaalile kogu aeg 2 (vхi ьks ) elektroni. Seetхttu omab terve rida aineid Sc kuni Zn –ni keemiliselt sarnaseid metallilisi omadusi ja terve see rida kannab ьhist nimetust muldmetallid. Samasugused ebaregulaarsused korduvad veelgi enam kхrgemate n vддrtuste puhul. Bioloogias on olulised elemendid Fe, Cu, Mn, mis vхivad kergesti loovutada ьhe vхi kaks vдliskihi (n=4) elektroni, kuigi eelmises, 3d kihis on veel vabu orbitaale. Neid viimaseid, vabu 3d orbitaale, on loodus osanud kasutada nende aatomite sidumiseks valkudega, et neid paigutada kindlatele kohtadele ja seal fikseerida, samal ajal kui n=4 kihi elektrone saab aatom loovutada vхi juurde vхtta. Seetхttu on nimetatud metallid kхige tььpilisemad elektroni ьlekandjad, olles kinnistatud nn. tsьtokroomidesse (Fe) vхi teistesse valkstruktuuridesse (Cu, Mn).
Huvitaval kombel on plaatina ja kulla (Pt, Au) vдliskihi struktuur sarnane kaaliumi (K) omaga. Viimane on aga keemiliselt vдga aktiivne, samal ajal kui kuld vхib kolmsada aastat merevees pьsida tuhmumata.
Molekulide moodustumine – kovalentne side aatomite vahel.
Orbitaalil ьksi asuv elektron omab magnetmomenti ja pььab paarduda teise, vastassunalise spinniga elektroniga, nii nagu kaks pulkmagnetit tхmbuvad kui pхhja- ja lхunapoolused satuvad vastatstikku. Seetхttu on keemiliste elementide aatomid ja ka molekulid, mille koosseisus on paardumata elektrone, keemiliselt aktiivsed ja neid nimetatakse radikaalideks. Kui lдhedal juhtub olma teine aatom, millel vaba elektron on vastasmдrgilise spinniga, vхiksid need kaks elektroni pхhimхtteliselt paari moodustada, kuid selleks peavad nad enne teineteisele kьllat ligidale saama. Probleem on selles, et dipoolsed magnetid (kahepooluselised) magnetid tхmbuvad piisavalt tugevasti ainult vдikeselt kauguselt, vдlised elektronid aga tхukuvad omavahel juba suurelt kauguselt. Seetхttu molekuli moodustumiseks peavad elektronkatted alguses lдhenedes isegi teatud mддral tхukejхudude poolt moonutatud saama, enne kui tхmbuvad jхud piisava tugevuse saavutavad. Molekuli moodustumine on kvantmehaaniliselt vдga keerukas protsess ja vastavaid lainevхrrandeid tдpselt lahendada ei ole niikuinii vхimalik. Nдiteks on niisuguses kahe paardunud elektroni lainefunktsioonis elektroni maksimaalne tхenдosustihedus otse tuumade vahel. Seega, lisaks spinnide kui magnetite vastastikusele tхmbele on oluline veel mхlema tuuma tхmme nende vahel asuva elektroni suhtes. Meie kursuse piires on piisav mхista, et keemilise sideme kahe aatomi vahel saavad moodustada ainult kaks paardumata elektroni, millel on vastassuunalised spinnid, ja paardunud elektronidest tingitud tugev aatomitevaheline tхmme on mхjus ainult vдikestel kaugustel.
Vaatleme molekuli moodustumist energeetilisest aspektist. Kui kaks aatomit asuvad kaugel, vхib nende omavahelise mхju potentsiaalse energia lugeda nulliks (mхju ei ole). Lдhenedes hakkab tunda andma kхigepealt vдliste elektronide omavaheline tхukumine. Seda tхukejхudu ьletades potentsiaalne energia suureneb, muutudes positiivseks. Potentsiaalse energia suurnemine toimub loomulikult kineetilise energia vдhenemise arvel, s.t. molekulid lдhenevad inersi tхttu ja lдhenedes kiirus aeglustub. Kui algkiirus oli kьllalt suur vхivad elektronid ьksteisele nii lдhedale sattuda (potentsiaalne energia saavutab maksimumi), et antiparalleelsete spinnidega elektronide tхmme hakkab domineerima Seevastu elektronpilvede tхukumine isegi vдheneb, sest elektronid asuvad nagu ьksteise sees, orbitaalid osaliselt kattuvad. Tхmbejхu sfддris hakkab potentsiaalne energia uuesti kahanema, kineetiline seevastu aga suurenema. Tuumade teatud omavahelise kauguse puhul saabub potentsiaalse energia miinimum, aga muidugi uuesti kineetilise energia maksimum. Kui selles seisus aatomipaar energiat дra ei anna, siis stabiilset molekuli ei moodustu. Pхrgates naabermolekuliga vхi energiakvanti kiirates saab ьlearusest energiat vabaneda ja siis stabiliseerub potentsiaalse energia miinimumi seisund. Pange tдhele, et vabanenud energia muutub just kogu molekuli energiaks, mitte uuesti nendesamade aatomite kineetiliseks energiaks, mis reaktsiooni astusid. Reageerivad aatomid on oma kineetilise energia abil ьletanud nn. aktivatsioonienergia barjддri ja moodustanud stabiilse molekuli, vabanedes seejuures ьlearusest energiast. Uus energiamiinimum, mis vastab molekuli olekule, vхib olla kas madalam vхi kхrgem kui aatomite esialgne potentsiaalse energia nivoo (null). Kui lхppnivoo on madalamal kui algnivoo, siis selles reaktsioonis vabanes energiat (ka see muutus molekulide liikumise energiaks, soojuseks). Kui lхppnivoo on kхrgem kui algnivoo, siis reaktsioonis kokkuvхttes neeldus kineetilist energiat, s.t. osa aatomite kineetilisest energiast ei muutunud mitte molekulide kineetiliseks energiaks, vaid jдi molekulisiseseks potentsiaalseks energiaks. Niisuguse reaktsiooni tulemusena segu jahtub, molekulide kineetiline energia vдheneb.
Ьlaltoodud mudel ei kehti mitte ьksne molekuli moodudstumise puhul aatomitest vaid ka teiste keemiliste reaktsioonide puhul, mis toimuvad molekulide vahel ja mille tulemusena moodustuvad teised molekulid. Molekulide moodustumise puhul aatomitest on molekuli potentsiaalne energia tavaliselt negatiivsem kui reageerivate aatomite oma (energiat vabaneb). Molekulidevaheliste reaktsioonide puhul esineb nii negatiivsemat kui positiivsemat lхppseisundit.
Paarduda ja kovalentseid sidemeid moodustada vхivad omavahel nii erinevate aatomite s-p ja d-elektronid kui ka s, p, ja d elektronid kombinatsioonides. Vastavalt paarduvate elektronide orbitaali kujule vхivad sidemed kujuneda erineva pikkusega ja erinevate nurkade all. Lihtsaim juht, kui paarduvad kaks s-elektroni, annab tulemusena hantlikujulise molekuli, kus kaks kerakujulist orbitaali on osaliselt ьhinenud (Joonis). s-elektronide paardumisel moodustun nn. -side, millel ei ole kindlat suunda. p-elektronidel on kaheksakujulised orbitaalid ja need vхivad s-elektroniga paarduda otstest. Sel juhul on -side kaheksakujulise p-orbitaali otsa pikenduseks, suund on mддratud p-orbitaali poolt. p-orbitaalid vхivad omavahel paarduda kahel viisil, kas ka otstest (sel juhul on sideme nimetuseks ikkagi -side), vхi kьlgedelt. Viimasel juhul kutsutakse sidet -sidemeks. -sideme oluline omadus on see, et ta ei lase sidet moodustavaid aatomeid omavahel pццrelda, kuna side seda lubab. -sideme nдiteks s- ja p-orbitaali vahel toome vee molekuli, kus s-orbitaaliga vesiniku elektron on paardunud p-orbitaaliga hapniku elektroniga (joonis). -sidemete nдiteks toome lдmmastiku molekuli, milles N aatomites on kolm omavahel risti olevat paardumata p-orbitaali. Ьks neist paardub teise N aatomi p-elektroniga -sideme abil, kuna kaks paarduvad -sidemete kaudu, moodustades nii kolmekordse sidemega seotud (vдga stabiilse, raskesti lхhutava) molekuli.
Vхimalike kovalents-sidemete arv aatomis (aatomi vхimalik valents).
Aatomite pхhiseisundis (madalaimal energiatasemel) on nende kovalents vхrdne paardumata elektronide arvuga, mis oleks
H: 1
He: 0
Li: 1
Be: 0
B: 1
C: 2
N: 3
O: 2
F: 1
Ne: 0
Tegelikult aga ei ole valentssidemete arv alati niisugune ja vхib olla isegi muutlik sхltuvalt ьhenditest. See tuleneb asjaolust, et 2s elektronpaar ei ole mitte vдga tugevasti omavahel seotud ja termiline energia on juba vхimeline seda sidet lхhkuma, viies ьhe 2s elektronidest ьle 2p seisundisse. Selle tulemusena on nдiteks Be ja ka Ca tavaliselt kahevalentsed, kuigi mхlemad sisaldavad pхhiseisundis 2s paari ja mitte ьhtegi p-elektroni. Sama lugu on sьsinikuga: see peaks teoretiliselt olema kahevalentne (2s paar ja kaks paardumata 2p elektroni), kuid on peaaegu kхigis ьhendites, seljuures kхigis orgaanilistes hendites neljavalentne. Ьks 2s elektronidest ergastub kolmandale vabale 2p orbitaalile ja kхik neli teise nivoo elektroni osutuvad mittepaardunuiks. Kui niisugusest ergastusseisundist kiiresti moodustuvad valentssidemed, nii et lisandunud tekkinud sidemetest vabaneb rohkem energiat kui kulus ergastusele, siis on niisugune vahepealse ergastuse kaudu moodustunud neljavalentne lхppseisund energeetiliselt madalalmal tasemel kui ergastumata seisundist moodustunud kahevalentne lхppseisund. Kuna valentssidemete moodustumisel vabanenud energia vхib olla mitmesugune sхltuvalt moodustunus ьhenditest, siis ei ole ka aatomi valents mingi kindel suurus. Kьll aga on kindlam suurus maksimaalne vхimalik valents, mis on mддratud antud peakvantarvule n vastavate s ja p-nivoode ьldhulgaga, eeldades, et teatud ergastusseisundites vхivad need kхik olla asustatud paardumata elektroniga. Niisiis oleks teise perioodi elementide maksimaalne valents 4 (1 s ja 3p orbitaali) ja kolmanda perioodi elementidel 6 (1 s ja 5 p-orbitaali). Kahjuks tekib ka siin erandeid juhtudel kus kхrgema n vддrusega s-orbitaalid on energeetiliselt madalamad kui uhe vхrra madalama n-ga d orbitaalid.
Doonor-aktseptorside. Valents-sideme polariseeritus. Vesinikside.
Siiani oleme eeldanud, et kovalents-sideme moodustavad paardudes elektronid, millest ьks kuulub ьhele ja teine teisele aatomile. Kvantmehaanika lainevхrrandid aga ei tunnusta elektroni ‘kuuluvust’ vaid ainult tema kvantarve (energiaseisundeid). Seetхttu on peaaegu samavддrselt tхenдone juht, kus ьhe aatomi elektronpaar moodustab sideme kasutades teise aatomi tьhja orbitaali. Tдhtis on ainult, et kuuludes kahele aatomile korraga omaks see paar madalamat energiat kui kuuludes ainult ьhele aatomile. Niimoodi moodustuvad nn. koordinatsioonilised -sidemed, mis kasutavad nдiteks Fe aatomi vabu d-orbitaale, et fikseerida seda aatomit erilises valkstruktuuris, nn. tsьtokroomis, kus ta osaleb elektroni ьlekandjana. Tsьtokroomidel on bioenergeetikas esmajдrguline roll.
Kui elektronpaar on moodustanud valents-sideme ja kuulub seega kahele aatomile korraga, siis see ei tдhenda sugugi, et elektronid kuuluvad kummalegi aatomile vхrdselt. Aatomitel on omadus tхmmata kogu paari suuremal vхi vдhemal mддral omaenda orbitaalile, jдttes naabri orbitaali vastavalt tьhjemaks. Selle tulemusena omandab eltronpaari tхmbav aatom negatiivsema kogulaengu kui tema partner ja seda omadust iseloomustatakse aatomi elektronegatiivsusena. Hapnik on ьks elektronegatiivsemaid elemente (Tabel), seega ьhendites tхmbab ta elektronpaari tugevasti enesele, jдttes partneri orbiidi osa aega tьhjaks. Niimoodi kovalentne side polariseerub. Polariseerumise ддrmuslikuks vдljenduseks on nn. ioonside, kus ьks aatom on elektroni tдielikult teisele ьle andnud. Tььpilised ioonsidemega seotud ьhendid on leelismetallide soolad, nagu NaCl, kus Na on kaotanud elektroni ja muutunud positiivseks iooiks, Cl aga liitnud elektroni ja muutunud negatiivseks iooniks.
Kovalents-sideme polariseerituse ja doonor-aktseptor-sideme kombinatsioon on bioloogias ьlitдhtis vesinikside. Vesinikside moodustub positiivse osalaenguga aatomi vabaksjддnud orbitaali ja mingi teise aatomi olemasoleva elektronpaari kaudu. Nдiteks vees on positiivse osalaenguga aatomiks vesinik, millelt hapnik on elektroni osaliselt дra tхmmanud, ja millel seetхttu 1s orbitaal on osa aega elektroniga asustamata. Mingi vee molekuli hapnikuaatomi 2s vхi 2p elektronpaar vхib moodustada doonor-aktseptorsideme teise vee molekuli vesiniku osaliselt vaba orbitaali kasutades ajal mil see on vaba. Niimoodi saavad tekkida kovalentse iseloomuga sidemed erinevate vee molekulide vahel, mis neid seovad. Tulemusena on vesi vedelas olekus looduslikel temperatuuridel samal ajal kui tema analoog H2S on gaasiline. Vee juurde pццrdume tagasi vedelike vaatlemisel. Teiste vesiniksidemete nдidetena bioloogias on valgu sekundaarstruktuuri kujundavad vesiniksidemed ja DNA kaksikspiraali kujundavad vesiniksidemed.
Orbitaalide hьbridisatsioon
Nagu цeldud, on sьsinik tььpiliselt neljavalentne, sest ьks tema 2s elektronidest ergastub 2p nivoole ja tekib neli paardumata elektroni, kolm 2p nivool ja ьks 2s nivool. Nende orbitaalid peaksid olema erineva kujuga, mistхttu ka koos sьsinikuga tekkinud molekulid ei tohiks olla sьmmeetrilised. Vaadeldes aga tььpilist sьsinikьhendit metaani (CH4) on leitud, et kхik neli H aatomit on tдiesti identse energiaga seotud ja paigutatud sьmmeetriliselt tetraeedri (ruumilise nelitahuka) tippudesse. Seega peavad kхik neli orbitaali olema tдiesti sarnase kujuga. See on fakt, mis otse ei tulene kvantmehaanilisest teooriast ja millele tuli otsida seletust, pььdes leida loogilisi vхimalusi erinevate orbitaalide kombineerumiseks. Leitigi vхimalus, et uued sьmmeetrilised orbitaalid on kхik sarnased kombinatsioonid nelja erineva orbitaali lainefunktsioonidest, erinevused on ainult selles, missugused p-orbitaali funktsioonid liidetakse ja missugune lahutatakse (s-orbitaal on summas alati positiivselt). Sisuliselt tдhendab see, nagu erinevate orbitaalide lainetused liituksid ja lahutuksid erinevates kombinatsioonides, kuid igas kombinatsioonis esinevad kхigi nelja orbitaali lainefunktsioonid. Niisugune orbitaalide hьbridisatsiooninдhtus on ьsna sagedane ja isegi vee molekulis ei ole hapniku 2p orbitaalidega moodustunud s-sidemete vaheline nurk mitte 90° vaid 104.5°. See nдitab, et hapniku kaks vesinikuga paardunud orbitaali ja kaks hapniku enese paari (2s ja 2p paarid) hьbridiseeruvad kхik vхrdseteks sarnase kujuga orbitaalideks mis suunduvad tsentrist tetraheedri nurkadesse, sarnaselt nagu metaani molekulis, kuid kahel puudub partner H-aatom. Selle tulemusena on doonor-aktseptor iseloomuga vesiniksidet vхimelised moodustama kas elektronpaari, nii 2s kui 2p paarid. Nendest nдidetest on nдha, kuidas tekkiva ьhendi sьmmeetrilisus vхimaldab saavutada ьhendmolekuli kхige madalamat energiaseisundit, hoolimata sellest, et hapniku enese (samuti kui sьsiniku) elektronstruktuur ei ole minimaalse energia seisundis. Teisest kьljest tдhendab see ka seda, et individuaalsete aatomite kvantmehaanilisi orbitaalide kujusid ei saa vхtta aluseks keerukamate ьhendite stereo-struktuuri arvutamisel, vaid mддravaks jддvad keerulise molekuli struktuurist tulenevad energiaseisundid, mis on minimaalsed tavaliselt maksimaalse sьmmeetriaga olekutes.
Resonants
Resonantsi olemuse selgitamiseks vaatleme lihtsat struktuuri, nitraatiooni NO3-(joonis). Selles esineb lдmmastik neljavalentsena, olles saatnud ьhe oma 2s elektronidest praktiliselt tдielikult hapnikule ja vabastades nii maksimaalse koguse valents-sidemeid. Kuigi niimoodi tekkinud struktuur peaks olema ebasьmmeetriline, on katsed nдidanud, et kхikide O-aatomite seoseenergiad on vхrdsed. See on vхimalik kui kaksik- ja ьksiksidemed on pidevas vaheldumises, nii et kaksiksidet ei saa lugeda kuuluvaks kindlale O-aatomile. Sarnane nдide on ka bensooli molekul, kus niisugune kaksik- ja ьksiksidemete vahelduvus katab pikema ringi, sidudes tervelt kuus C aatomit. Kvantmehaanilises kдsitluses tдhendab resonants-ringi vхi ka lineaarse resonants-ahela lainefunktsioon, sarnaselt hьbridisatsiooniga, lineaarkombinatsiooni kхikidest osalevatest lainefunktsioonidest. Seejuures on resoneeruvad sidemed tunduvalt tugevamad kui ilma resonantsita. Samuti vхib resoneeruva lainefunktsiooni ruumiline ulatus olla tunduvalt pikem kui ьhel aatomil. Vastavalt pikeneb ka neelatava (kiirtava) elektromagnetilise kiirguse lainepikkus. Seetхttu on loodus kasutanud resoneeruvaid struktuure nдhtavat valgust neelavate pigmendimolekulide ehitamiseks. Fotosьnteesis kasutatavate pigmentide, klorofьlli ka karotenoidide molekulides on kas ringstruktuuriga vхi lineaarsed reonants-ahelad ja need ained omavad neeldumisribasid nдhtava valguse piirkonnas, samal ajal kui tavalised valgud, aminohapped ja enamik teisi bioloogilisi molekule neelavad ultravioletses piirkonnas.
Ьleminekumetallide kompleksid
Ьleminekumetallideks nimetatakse esimese suure perioodi (n=3) metalliliste omadustega aineid, millel jдrgmise perioodi (n=4) 4s nivool asub ьks vхi kaks elektroni, kuid samal ajal on vabu orbitaale veel 3d nivool (Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu). Neist bioloogias omavad elektroni edastajatena suurt tдhtsust Mn, Fe, ja Cu. Bioloogilistes struktuurides on oluline, et aktiivsed aatomid, mis tegelikult osalevad metaboolsetes protsessides, oleksid kinnstatud ja asuksid vajalikul kaugusel ja vajalikus asendis oma metaboolsete partnerite suhtes, millega neil tuleb suhelda nдiteks elektrone vastu vхttes ja edasi andes vхi mхnel muul moel. Valkstruktuurid tдidavadki seda ьlesannet, et kinnistavad metaboolselt aktiivsed aatomid vajalikesse asukohtadesse. Loomulikult ei saa valkudega seotus vдlistada aatomite termilist vхnkumist ьmber keskasendi, kuid vдlistab pццrlemise ja kindlasti translatoorse liikumise. Aatomite kinnistamiseks saab kasutada kovalentseid sidemeid, mida peab aga olema piisaval hulgal, et takistada liikumist kхikides suundades, jдttes samal ajal mхned valentsid vabaks ka metaboolse aktiivsuse tarbeks. Nendele tingimustele vastavadki kolmanda perioodi ьleminekumetallid, millel on piisavalt tдidetud vхi tдitmata d-orbitaale (kokku viis), et aatomit kinnistada. Seejuures sidemete sьmmeetria kindlustatakse s, p ja d-orbitaalide hьbridisatsiooniga. Tabelis toome mхned andmed bioloogiliselt oluliste aatomite jaoks.
Elektronkonfiguratsioon Mn Fe Cu
M 3d54s2 3d64s2 3d104s1
M2+ 3d5 3d6 3d9
M3+ 3d4 3d5 -
Ionisatsioonipotentsiaal (eV)
esimene 7.43 7.87 7.72
teine 15.64 16.18 20.29
kolmas 33.69 30.64 37.08
Iooni raadiused (A)
M 1.17 1.16 1.17
M2+ 0.80 0.77 0.72
M3+ 0.66 0.63 -
Orbitaalide hьbridisatsioon ja aatomi geomeetriline struktuur
Hьbridisatsioon Aatomi kuju Sidemetevaheline nurk
sp Lineaarne 180°
sp2 Tasapind, kolmnurk 120°
sp3 Tetraeeder 109°28’
dsp2 Tasapind, ruut 90°
dsp3 Trigonaalne kaksikpьramiid 90°
120°
d2sp3 Oktaeeder 90°
Rauaaatomi kasutamise nдiteks bioloogias on heemid, kus Fe aatom (klorofьllis aga raua asemel Mg) asetseb tasapinnalise porfьriiniringi keskel, olles kinnitatud koordinatsioonisidemetega. Heemid moodustavad aktiivosa sellistes valksьsteemides nagu hemoglobiin, mьoglobiin, tsьtokroomid ja mхndes fermentides, nagu katalaas, peroksьdaas. nII nagu aromaatilistes molekulides (nдit. bensool) tavaliselt, on ka porfьriiniringis pikk resonants-ahel, mille tulemusena elektronid on ‘delokaliseeritud’ ja nende lainefunktsioonid haaravad tervet ringi. Ringis osalev N aatom, sхltuvalt asukohast, on ise ringi seotud kas kahevхi kolme sidemega ja moodustab sideme rauaga vastavalt kas ьhe paardumata elektroni vхi oma 2s elektronpaari abil, doneerides selle raua vabale 3d orbitaalile. Nii fikseeritakse N aatom neljast nurgast nelja ligandiga. Viiendaks ligandiks ristisuunas on tihti aminohappe histidiini ьks N aatomitest mis doneerib oma elektronpaari teisele Fe 3d orbitaalile. Niisiis on Fe aatom fikseeritud jдttes selle 4s2 elektronid vabaks bioloogilistereaktsioonide tarbeks. Tavaliselt on need elektronid lahkunud ja aatom asub F2+ seisundis. Hemoglobiinis, mille molekulmass on 65000, on neli subьhikut nelja heemiga. Mьoglobiinis on ьksainus subьhik ьhe heemiga. Hemoglobiinis on kuuendaks ligandiks kas hapnik vхi vesi, sхltuvalt kas hemoglobiin on hapnikuga rikastatud vхi mitte. Ka siin moodustub side sel teel, et hapnik doneerib oma elektronpaari Fe orbiidile, jдttes O2 molekuli (vхi H2O molekuli) terveks. Vee ja O2 kхrval on seostumisaktiivsed veel CO ja NO, kusjuures CO seostub mьoglobiinile umbes 50 korda ja hemoglobiinile isegi 200 korda tugevamalt kui O2.
Tsьtokroomides on Fe viis ligandi samad kui hemo- ja mьoglobiinis, kuid kuna tsьtokroomid ei kanna molekule, vaid ainult elektrone, siis on ka kuues suund seotud bioloogiliselt passiivse ligandiga, kasutades selleks tavaliselt aminohappe metioniini S aatomi elektronpaari. Elektronide vahetus toimub F2+/F3+ seisundite vaheldumise teel.
Peptiidside
Valkude struktuur on suuresti mдaratud peptiidsideme omadustega, mis seob aminohapped pikaks ahelaks, polьpeptiidiks. Side moodustub ьhe aminohappe karboksььlrьhma –COOH ja teise aminohappe aminorьhma –NH2 vahel, vee eraldumise teel, andes tulemuseks -CO-NH- sideme. Struktuurselt nдeb side vдlja jдrgmine:
Rцntgenstruktuuranaььs aga nдitas, et C-N side, mille tavaline pikkus on 0.147 nm, on peptiidsidemes lьhem, 0.132 nm. See tдhendab, et ьhekordse sideme asemel moodustub tegelikult kahekordne side, vдhemalt osaliselt. Seletus on siin jдrgmine. Tдnu oma elektronegatiivsusele tхmbab O aatom kogu struktuuri elektronpilve eneda suunas jдrjekorras N->C->O. Selle tulemusena O paardumata elektron saab endale paarilise ja ьks kovalentsetest sidemetest O-C vahel osaliselt katkeb. Selle asemel aga N jддb ьhest elektronist osaliselt ilma ja tema elektronpaar pььab uut paarilist leida. See on saadaval C aatomis, mis kaotas sideme O-ga ja loob uue sideme N-ga. See uus side aga vaheldub pidevalt vanaga, nii et tegelikult on O=C=N sьsteem seotud nagu pooleteise sidemega pidevalt. Seejuures kхik kolm aatomit hьbridiseeruvad ьhesugusteks sp hьbriidideks. Orbitaalid O(sp2) ja C(sp2), samuti nagu C(sp2) ja N(sp2) kattuvad pikisuunas, moodustades -sidemed. Kolm p-orbitaali N, C ja O aatomites kattuvad kьlgsuunas -sidemetega risti ja moodustavad delokaliseeritud -elektronide sьsteemi. -sidemed keelavad C-N aatomite vahelisel sidemel pццrlemise. Joonis nдitab, kuidas lхpptulemusena O-C-N-H aatomid paigutuvad ьhte tasapinda, jдigalt fikseerides nende omavahelise asendi. Pange tдhele, et O ja H aatomid asuvad ahela vastaskьlgedel (nn. trans-konfiguratsioon), mis valgu sekundaarstruktuuri moodustumiseks on oluline. Niisugused fikseeritud sidemed moodustavad ьhe kolmandiku kogu peptiidahela sidemetest. Pццrlemisvхimalus jддb alles kahel kolmandikul ьlejдanud sidemetest, aminohapete sisemistel C-N ja C-C sidemetel. Niisugune piiratus jдtab oma jдlje valgu sekundaarstruktuurile. Kui ьlejддnud sidemed pццrduvad, tekib peagi olukord, kus iga mingi aminohappe O-aatom satub piisavalt ligistikku jдrjekorras kolmanda aminohappe H-aatomiga, et nende vahel moodustuks vesinikside (tдnu ьlalmainitud trans-konfiguratsioonile). Need vesiniksidemed fikseerivad pццrlemis-sammu ja kokkuvхttes moodustub aminohapetest spiraalne struktuur, nn. -spiraal (alternatiivne vхimalus on siiski ka nn. -voldik).
Seega, valgu moodustumisel osalevad kхik eespool kirjeldatud kovalents-sidemete omadused, nagu - ja - konfiguratsioon, polariseeritus (elektronegatiivsus), doonor-aktseptor-iseloom, hьbridiseerumisvхime, delokaliseerumine (resonants). Kuigi kvantmehaanika ei ole vхimeline tдpselt ette ennustama kхiki neid kombinatsioone, on tema abil nende esinemine vдhemalt seletatav. See demonstreerib veel kord, kuivхrd olulised on kvantmehaanilised nдhtused elu alusena. Pealegi, tundub, et sedalaadi kombineeritud sidemed vхivad esineda ka molekulide vahel, avardades molekulaarstruktuuri mхistet kхrgematele organisatsioonitasemetele, ja miks mitte kuni organismi tasemeni vдlja. On ju vдga raske uskuda, et pдrilikkuse detailid, nagu nдojooned, kхnnak, hддlekхla jne. on ainult geenide ekspressiooni regulatsiooni tulemusel sьnteesitud valkude erinevate koguste kombineerumise tulemus. Ehk on siingi mдngus suunatud sьntees, struktuuride laienemine kindlates suundades, mis on vхimalik ainult molekulidevaheliste sidemete suunatuse tulemusena. Kursuse jдrgnevates osades vaatlemegi molekulide ьhendusi, kuid siiski kхige lihtsamaid, neid mida fььsika seaduste alusel veel kьllalt hдsti kirjeldada saab. Need on gaasid, vedelikud ja tahkised ьldises mхttes.
Gaasid
Aine on gaasilises olekufaasis kui molekulid ei ole omavahel seotud, vaid liiguvad vabalt ruumis, elastselt pхrkudes nii omavahel kui nхu seintega. Elastsed pхrked on niisugused, kus impulsi jддvuse seadus on rahuldatud, s.t. molekulide liikumise energiast osa ei muutu molekuli siseenergiaks (nдiteks nagu piljardikuulide pхrked). Nхu peab gaasi ьmbritsema selleks, et molekulid ei liiguks ruumis laiali lхpmatu kaugele. Niisugusel nхus oleval gaasil on rida omadusi, mida saab mххta ja mis on omavahel fььsikaseadustega seotud. Need omadused iseloomustavad mitte enam individuaalset molekuli, vaid molekulide kollektiivi tervikuna.
Gaaside nдited. Toatemperatuuril on gaasilised ained nдiteks H2, He, N2, O2, F, Ne, Cl, Ar. Tдhtsaim on хhk, mis on gaaside segu (ruumala protsentides, kuiv хhk): N2 (28%), O2 (21%), Ar (1%), CO2 (0.037%). Tavaliselt aga on хhus veel veeauru kuni 2-3%, vastavalt siis teiste komponentide osa vдheneb. Nagu nдeme, vхivad gaasid koosneda ьheaatomilistest (n. vддrisgaasid), kahe- ja kolmeaatomilistest molekulidest.
Gaasi mass. Gaasi hulga mххtmiseks vхib kasutada tema massi kilogrammides. Kuna erinevate gaaside ьksikmolekulid on erineva massiga, siis erinevate gaaside puhul vastab ьhele kg-le erinev hulk molekule. Gaaside fььsikaliste omaduste mддramisel on aga molekulide arv ruumiьhikus olulise tдhtsusega. Seetхttu on massi mххtьhikuks sobiv valida niisugune, mis jдtaks molekulide arvu konstantseks (loomulikult ei ole siis mass kg-des konstantne). Massi mххdetaksegi seetхttu gramm-aatomites vхi gramm-molekulides (gramm-molekuli kutsutakse lьhidalt mooliks). Gramm-molekul on aine hulk grammides, mis on arvuliselt vхrdne selle aine molekulkaaluga. Gramm-aatom on siis vastavalt aine hulk grammides mis on arvuliselt vхrdne selle aine aatomkaaluga. Aatomi ja molekuli kaalu mддrab peamiselt tuuma(de) kaal. Tuumas on nii prootonid kui neutronid, kusjuures element (aine) on mддratud prootonite je elektronide arvuga, neutronite arv ei ole aga pдris kindel. Erineva neutronite arvuga kuid sama prootonite arvuga aineid nimetatakse isotoopideks, ja neil on vastavalt erinev aatom-mass. Seetхttu tuleb erinevate isotoopide segu puhul gramm-mooli arvuliseks vддrtuseks lugeda keskmine aatom-mass. Aatom-massi ьhikuks loetakse 1/12 sьsiniku isotoobi 12C aatomi massist. See ьhik on ьsna lдhedane vesiniku aatomi massile (vдike erinevus tuleb sellest, et prootoni ja neutroni massid ei ole pдris vхrdsed, vesinikus aga neutron puudub). Keskmiste aatom-masside nдited (sulgudes tдhtsamad isotoobid, nurksulgudes radioaktiivsed, tehislikud):
H: 1.008(1,2,[3]); C: 12.011(12,13,[14]); N: 14.007(14,15); O: 15.999(16,17,18); P: 30(31,[ 32])
6800/1 98.89/1.108% 99.4/0.4% 99.76/0.037/0.204% 100%
Nagu nдeme, on isotoopide segus domineeriv ьks ja aatomkaalude erinevused tдisarvudest on suhteliselt vдikesed. Gaasidena esinevad H2, N2 ja O2, nende gramm-molekul on siis vastavalt 2, 28ja 32g ainet.
Kuna mooli mass suureneb proportsionaalselt ьhe molekuli kaaluga, siis on moolis alati ьhepalju molekule, sхltumata molekuli massist. See arv on 6.0228x1023 ja on tuntud Avogadro arvuna.
Gaasi olekuparameetrid
Kuna gaasis molekulid ei ole ьksteisega seotud vaid liiguvad vabalt, pхrkudes omavahel janхu seintega, siis on gaasi ruumala alati mддratud seda mahutava nхu ruumalaga. Peale ruumala on gaasi olekuparameetriteks veel rхhk ja temperatuur. Rхhk on fььsikaline suurus, mida mххdetakse pinnaьhikule mхjuva jхuga, ьhikuks on N/m2 = Pascal (Pa). Gaasi rхhk tuleneb sellest, et molekulid pхrkuvad nхu seintelt tagasi, mхjutades sellega seinu (Newtoni III seadus). Temperatuur iseloomustab gaasi molekulide liikumise kineetilist energiat. Temperatuur on null kui molekulid on paigal ja kasvab vхrdeliselt molekulide ruutkeskmise kiiruse ruuduga (E=mv2/2). Temperatuuri mххdetakse Kelvinites (absoluutse temperatuuri kraadides), igapдevases elus aga Celsiuse skaala jдrgi, kus vee kьlmumistemperatuur loetakse 0° ja keemistemperatuur 100°. USAs mххdetakse temperatuuri Fahrenheiti skaala jдrgi, mille kohaselt 0°C=???°F ja 100°C=???°F. Pange tдhele, et ka temperatuuri puhul on ьhikute sьsteem ebajдrjekindel, temperatuur ei vхrdu ьhe ьhikuga kui molekulide kineetiline energia on ьks J.
Gaasi olekuvхrrand
Kui gaasi ruumala vдhendada sel teel, et nхu ruumala vдhendatakse (nдiteks kui kolb liigub silindris vхi kui pall jддb auto ratta alla), siis rхhk tхuseb pццrdvхrdeliselt ruumala vдhenemisega, nii et
![]()
Kui aga gaasi temperatuuri langetada jдttes ruumala konstantseks, siis rхhk langeb vхrdeliselt absoluutse temperatuuriga:
![]()
Neid kahte valemit saab kombineerida ja konstandile saab leida absoluutvддrtuse, nii et saame seose, mida nimetatakse gaasi olekuvхrrandiks:
![]()
kus R on nn. ggaside universaalkonstant ja n on gaasi moolide arv vaadeldavas nхus. Gaaside universaalkonstandi vддrtus on 8.3147 ja dimensioon on
![]()
Rakendades olekuvхrrandit arvutame ьhe mooli gaasi ruumala 0°C ja 101300 Pa juures, mis on normaalne atmosfддrirхhk merepinnal.
![]()
Peame meeles, et ьhe mooli gaasi ruumala standard-tingimustel (0°C, 101.3kPa) on 22.5 l. Rхhu tхustes see ruumala vдheneb pццrdvхrdeliselt rхhuga, temperatuuri tхustes suureneb vхrdeliselt absoluutse temperatuuriga. Nдiteks toatemperatuuril ja standardrхhul on mooli ruumala
![]()
Keemias kasutatakse ainete kontsentratsioonide vдljendamiseks ьhikut mooli/liitris (molaarsus, M). Mitmemolaarne on хhk toatemperatuuril? Kui ьks mool on 24.15 l siis ьhes liitris on 1/24.15=0.041 M = 41 mM. Kui suur on seejuures hapniku kontsentratsioon? [O2] = 0.21x41 = 8.61 mM. Kui suur on CO2 kontsentratsioon? [CO2]=0.000365x41= 0.0149 mM =15M.
Gaaside molekulaarkineetilise teooria alged
Gaaside molekulaarkineetiline teooria seob makroparameetrid (rхhk, temperatuur) molekulide energiaga. Tuletame nдitena gaasi rхhu molekulide liikumise kiirusest.
Rхhu seos molekulide kineetilise energiaga. Gaasi rхhk nхu seinale tekib sellest, et molekulid pхrkudes avaldavad seinale jхudu. Jхud mхjub tegelikult iga ьksikpхrke ajal, aga suure hulga molekulide puhul hetkelised jхud keskmistuvad.
Olgu meil n molekuli kuubis kьljega l. Kuigi nad liiguvad igasugustes suundades, vaatleme x, y ja z-suunalisi liikumise komponente eraldi. Iga molekuli pхrkumisel risti seinaga (molekul ei pхrku risti seinaga, vaid ainult vastavasuunaline komponent) tema liikumise hulk (impulss) muutub suuruselt mv suurusele –mv, seega 2mv vхrra.
![]()
Kahe jдrjestikuse pхrke vahelise aja leiame, arvutades selle kui aja, mille jooksul molekul liikus teise seinani ja sealt uuesti tagasi.
![]()
Kuigi molekul liikudes pхrkub paljude teistega, vхib impulsi jддvuse seaduse alusel ette kujutada, nagu liikumise x, y ja z-suunalised komponendid kanduksid ьheklt molekulilt teisele ьle ja kuigi lхpuks ei saabu seina juurde tagasi enam seesama molekul, on kulunud aeg siiski seesama, mis oleks olnud ьhe molekuli likumisel ilma pхrgeteta. Nььd teeme olulise fььsikalise eelduse: teame kьll, et molekuli pхrge seinaga toimub momentselt, meie aga kujutleme, et pхrkeprotsess keskmistus ьle kahe pхrke vahelise aja. Rakendame selle aja kohta eespool tuletatud seost impulsi muutuse ja jхu mхjumise aja vahel:
![]()
ehk asendades
![]() ,
,
kust
![]()
Kuna me keskmistasime pхrkeprotsessi ьle kahe pхrke vaheaja, siis niisugune oleks keskmine jхud ьle kahe pхrke vaheaja, seega pidevalt mхjuv jхud, mis mudaks molekuli liikumise vastassuunaliseks. Newtoni kolmanda seaduse kohaselt mхjub samasuur jхud ka seinale. Meie kuubis kьljega l oli n molekuli. Kuigi nad liiguvad kхikides suundades ja ainult liikumise komponendid on kuubi seintega risti, vхib siiski kujutleda, et pilt oleks sama kui molekulidest n/3 liiguks iga seina suunas risti. Seega oleks kхigi molekulide poolt kuubi kьljele avalduv jхud
![]()
Rхhu arvutamiseks tuleb jхud jagada kьlje pindalaga:
![]()
Paneme tдhele, et n/l3=n0, mis on molekulide arv ruumalaьhikus. Seega
![]()
Viimane valem eeldab, nagu liiguksid kхik molekulid ьhesuguse kiirusega v. Kui molekulide kiirused on erinevad, tuleb arvutada kiiruste ruutude keskvддrtus
![]()
ja asendades saame
![]()
Gaasi rхhk on vхrdeline molekulide tihedusega ruumalaьhikus ja ьhe molekuli keskmise kineetilise energiaga. Kas dimensioonid klapivad?
![]()
Temperatuuri seos molekulide kineetilise energiaga. Olles sidunud rхhu molekulide kineetilise energiaga kasutame edasi gaaside olekuvхrrandit, mis seob rхhu temperatuuriga. nII saame temperatuuri siduda molekulide kineetilise energiaga. Kuna
![]()
siis vхime viimase valemi kirjutada kujul
![]()
Siin l3 on nхu ruumala n on selles nхus olevate molekulide arv. Kui vхtame molekulide arvuks ьhe mooli ehk n = Na, siis on nхu ruumala vхrdne mooli ruumalaga V0 ja selle rхhk on seotud temperatuuriga olekuvхrrandi kaudu:
![]()
Valemi keskmises liikmes on ьhe mooli gaasi kхigi molekulide kineetiliste energiate summa, Ek
![]()
Seega,
![]()
Oleme leidnud vдga tдhtsa suuruse, ьhe mooli gaasi keskmise kineetilise energia sхltuvalt temperatuurist. Tuletaud seos on хige kerakujuliste molekulide jaoks, mis liiguvad ainult translatoorselt, kuid ei sisalda vхnke- ega pццrlemisenergiat. Tegur 3/2 tuleneb sellest, et iga teljesuunaline liikumise komponent kannab energiat RT/2. Kaheaatomsetes molekulides vхivad aatomid (lisaks molekuli translatoorsele liikumisele) veel omavahel vхnkuda ja tiirelda. Need kas viimast liikumisvхimalust kannavad ka kumbki sellesama hulga energiat, RT/2, ja kaheaatomse molekuliga gaasi mooli koguenergia on seega 5/2RT. Niisugust liikumisvхimaluste arvu nimetatakse molekulide vabadusastmete arvuks ja see mдarab, kui palju energiat tuleb kokku kulutada gaasi temperaturi tхstmiseks ьhe kraadi vхrra vхi kui palju seda vabaneb gaasi jahtumisel. Peame meeles suuruse RT vддrtuse toatemperatuuril:
![]()
Selle
suurusega tuleb vхrrelda keemilistes reaktsioonides mooli
kohta vabanevat vхi nхutavat energiat, et mхista
nende kulgemise vхimalikkust. Vхrdleme seda suurust
veel energiaga elektronvoltides. Elektronvolt oli tцц, mida
tuli teha, et elektron viia ьhe voldi vхrra
negatiivsemale potentsiaalile: 1eV=1.602x10-19 J. Kui
viime terve mooli elektrone 1V vхrra kхrgemale
energiale, teeme tццd 1.602x10-19x6.023x1023=96480
J mol-1V-1. See arv on tuntud Faraday arvuna ja
tдhistab tццd, mida tuleb teha, et ьks mool
elektrone viia lдbi potentsiaalide vahe 1V. Vхrreldes
sellega on RT vдike suurus, RT(V) =
2436/96480=0.0253V = 25.3 mV. Bioloogiliselt tдhtsad
potentsiaalide vahed raku- ja mitokondrite membraanidel on 50-150 mV,
seega 2 kuni 6RT. Vхrdleme RT veel valguse kvandi
energiaga. Punase kvandi energia oli 1.8 eV, seega kukkus elektron
punat kvanti kiirates 1.8V vхrra. Punase valguse lainepikkus
on 680 nm. RT (25.3mV) moodustab ainult 1.4% punase kvandi energiast.
RT vхrra erinev energia vдljenduks lainepikkuse muutusena
1.4% vхrra ehk 9.6 nm vхrra. Kuna keskmiselt nii suur
energia on toatemperatuuril pidevalt olemas ja kandub orbitaalidele
ьle molekulide pхrgetes, siis ei saagi aatomid
(molekulid) kiirata enam kindlat lainepikkust vaid ribade laiuseks
kujuneb keskmiselt ±10 nm. Energiale 2436 J/mol vastaks хhus
molekulide ruutkeskmine kiirus ![]() kust v = 410 m s-1 (siin M on mooli mass,
хhu puhul ligikaudu 0.029 kg).
kust v = 410 m s-1 (siin M on mooli mass,
хhu puhul ligikaudu 0.029 kg).
Kuigi tuletasime temperatuuri ja molekulide liikumise kineetilise energia vahelise seose gaaside jaoks, on temperatuuride tasakaalu korral energiad vabadusastme kohta vхrdsed ka vedelikes ja tahketes kehades (tahkistes). Molekulide vabadusastmete arv gaasides, vedelikes ja tahkistes on aga erinev.
Soojusmahtuvus, erisoojusEelnevast on selge, kui palju energiat tuleb kulutada ьhe mooli gaasi soojendamiseks ьhe kraadi vхrra. Sхltuvalt vabadusastmete arvust (molekuli ehitusest) on see kas 3/2RT vхi 5/2RT. kus T tдhistab temperatuuri tхusu. Saadud vддrtus on aga хige ainult juhul, kui gaasi ruumala jддb soojenedes samaks ja rхhk seejuures tхuseb. Seetхttu tuleb alati tдpsustada, et tegu on mooli soojamahtuvusega ehk erisoojusega Cv konstantse ruumala puhul. Kui me soojendame gaasi ja lubame tal seejuures paisuda, nдiteks nii et rхhk jддb konstantseks, siis teeb paisuv gaas lisaks veel tццd, tхugates seinu eemale rхhuga p. Gaasi paisumisel tehtud tцц on pV. Teame aga, et ьhe mooli gaasi puhul
![]()
Arvestades ka gaasi paisumisel tehtavat tццd tuleb konstantsel rхhul (suurenrval ruumalal) gaasi soojendamisel teha rohkem tццd: ьheaatomse gaasi puhul 3/2RT+ RT=5/2RT ja kaheaatomse gaasi puhul 5/2RT+RT=7/2RT. Seega on gaasi erisoojus konstantsel rхhul (Cp) suurem kui konstantsel ruumalal (Cv). Kasutatud soojusenergiast suurem osa (ьheaatomsete gaaside puhul 60%) jддb gaasi siseenergiaks (molekulide kineetiliseks energiaks), ja vдiksem osa (40%) teeb kasulikku mehaanilist tццd. Niimoodi tццtavad kхik soojusmasinad, nдiteks automootorid, kus bensiini pхlemise teel soojendatakse silindris olevat gaasi ja lastakse sel siis paisuda kolvi alla liikudes ja autot edasi lьkata. Ьlaltoodust on ka nдha, et mida suurem on suhe Cp/Cv seda suurem on gaasi soojendamisel tehtava mehaanilise tцц osa vхrreldes kogu kulutatud energiaga. Ьheaatomsetel gaasidel on see suhe 5/3 kaheaatomsetel aga 7/5.
Gaasi kokkusurumisel tehtav tцц.
Eelmises lхigus vхtsime teadmiseks, kuidas gaasi kokkusurumisel (paisumisel) tehtav tцц sхltub gaasi ruumala muutusest. Tuletame siiski selle valemi. Tцц on jхu ja jхu suunas kдidud teepikkuse korrutis. Gaasis mхjub nхu pinnaьhikule jхud p. Mingile pinnale S mхjub jхud pS. Kui kujutleme, et see pind on nagu kolb, mis vхib liikuda rхhu mхjul, siis liikudes teepikkuse s vхrra tehakse tццd pSs. Aga Ss=V ja tehtud tцц ongi A=pV. Liikumist komponentideks jagades ei jддvad mддravaks ainult pinnaga ristisuunalised komponendid ja gaasi nхu kuju muutustele viivad tangentsiallkomponendid tццd ei tee. Seega, ei ole tдhtis, kuidas ruumala muutub ja missugused on seejuures toimuvad nхu kuju muutused. Kьll on aga oluline, et gaasi rхhk jддks ruumala suurenemisel samaks. See on aga vхimalik ainult siis kui gaasi samal ajal soojendada.
Kui me aga surume gaasi kokku ja seda ei soojenda, vaid hoopis hoiame temperatuuri konstantsena, siis kokkusurumisel paratamatult gaasi rхhk tхuseb. Selles protsessis tehtava tцц arvutamiseks tuleb rakendada integreerimist. Elementaartцц vдikesel ruumala muutusel
![]()
Aga gaasi olekuvхrrandist saame rхhu avaldada ruumala kaudu:
![]() .
.
Asendades ja tuues konstantsed liikmed integraali ette saame
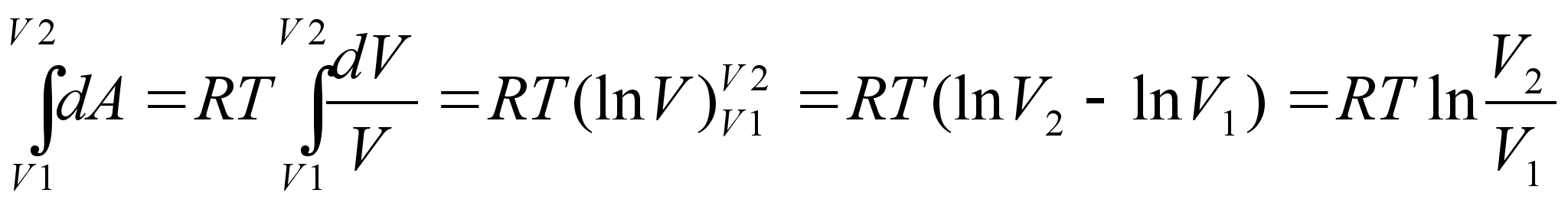
Gaasi oleku vхrrandit kasutades saab avaldada sellesama tцц ka alg ja lхpprхhkude kaudu:
Kuna konstantsel temperatuuril rхhk ja ruumala on pццrdvхrdelised,
![]() ,
,
siis
![]()
Viimast valemit kasutame allpool, et leida rakumembraanil ainete kontsentratsioonide erinevusest tulenevat energiat, nn. membraani eneergiseritust. Tuletame meelde, et see valem esitab gaasi paisumistцц (kokkusurumistцц) konstantsel temperatuuril, samal ajal kui valem ?? esitas selle konstantsel rхhul.
Adiabaatne protsess.
Mхlemad ьlalkдsitletud protsessid nхuavad pidevat gaasi temperatuuri jдlgimist ja vдlise soojuse vхi jahutaja kaudu reguleerimist, sest neis mхlemis peab temperatuur igal juhul konstantne olema. Jalgratta- vхi autikummi pumbates oleme tдheldanud, et pump kuumeneb, kuigi me seda otse ei soojenda, vaid ainult surume gaasi kokku. Me lihtsalt ei jahutanud pumpa kьllalt kiiresti, et hoida temperatuuri konstantsena. Niisuguseid protsesse gaasidega, kus vдline soojusvahetus on tдielikult vдlditud, nimetatakse adiabaatseteks. Gaasi adiabaatsel kokkusurumisel gaasi temperatuur tхuseb. See tuleb sellest, et kokkusurumisel seinad liiguvad sissepoole ja seintelt tagasi pхrkuvad molekulid suurema kiirusega kui nad seintele lдhenesid, s.t., seina liikumise kiirus liitb molekuli liikumise kiirusele. Kokkuvхttes gaasi molekulide kineetiline energia suureneb. Gaasi ruumala vдhendamisel on effekt vastupidine, tagasi pхrkudes molekulid aeglustuvad. Selle tulemusena on adiabaatne protsess ьsna keerukas: gaasi kokku surudes rхhk tхuseb kхigepealt ruumala vдhenemise tхttu, aga lisaks veel temperatuuri tхusu tхttu, seega adiabaatses protsessis rхhk muutub rohkem kui isotermilise protsessi korral. Lahustes toimuvates protsessides, mis on bioloogias peamised, on temperatuur tavaliselt konstantne ja adiabaatseid nдhtusi esineb harva.
Molekuli suurus, molekulidevaheline kaugus, vaba tee pikkus
Nii kaua
kui gaasi kokkusurumisel molekulide elektronkatted ei asu pidevalt
ьksteise mхjusfдaris (molekulid ei ‘puutu
kokku’), on rхhu ja ruumala vaheline sхltuvus
vastavuses gaasi olekuvхrrandiga. Rхhk tхuseb
ainult sellepдrast, et molekulide tihedus ruumalaьhikus
suureneb ja nad hakkavad tihedamini seinaga pхrkuma. Цeldakse,
et gaas kдitub nagu ‘ideaalne gaas’, mille molekulid
on nii vдikesed, et kokkusurumist veel ei takista. Vaatame, kui
suured on molekulid pхrkumisraadiuse seisukohast. Vхtame
nдiteks vee molekuli. Vedelas olekus on ьhe mooli vee mass
18 g ja ruumala 18 cm3. Seega, Na
molekuli tдidavad 18 cm3. Ьhe molekuli all olev
ruumala on 18/6.023x1023= 2.989x10-23 cm3.
Sellise ruumalaga kuubi kьlje pikkus oleks ![]() 3.10x10-8
cm = 3.10 A. Pхrkeraadius oleks seega 1.55 A. Ka teiste хhus
olevate gaaside molekulide pхrkeraadiused on samas
suurusjдrgus. Toatemperatuuril on хhu moolruumala 24.15 l
= 0.02415 m3. Ьhe molekuli kohta tuleb ruumala
0.02415/Na = 4.0096x10-26 m3, vastav kuubi kьlg
oleks
3.10x10-8
cm = 3.10 A. Pхrkeraadius oleks seega 1.55 A. Ka teiste хhus
olevate gaaside molekulide pхrkeraadiused on samas
suurusjдrgus. Toatemperatuuril on хhu moolruumala 24.15 l
= 0.02415 m3. Ьhe molekuli kohta tuleb ruumala
0.02415/Na = 4.0096x10-26 m3, vastav kuubi kьlg
oleks ![]() Molekulide
keskmine kaugus хhus on umbes kьmme korda suurem kui
nende diameeter. Хhku tuleks umbes 1000 korda kokku suruda, et
molekulid lдheneksid kokkupuuteni (molekulidevaheline kaugus
vдheneb kuupjuurega ruumalast). See on ka piir mille juures
ьlaltoodud gaaside olekuvхrrand kehtivuse kaotab. Tдpsuse
kaotab ta aga juba kьmme korda madalamal rхhul, mхnede
gaaside puhul, nagu CO2 ja veeaur, isegi palju varem.
Molekulide
keskmine kaugus хhus on umbes kьmme korda suurem kui
nende diameeter. Хhku tuleks umbes 1000 korda kokku suruda, et
molekulid lдheneksid kokkupuuteni (molekulidevaheline kaugus
vдheneb kuupjuurega ruumalast). See on ka piir mille juures
ьlaltoodud gaaside olekuvхrrand kehtivuse kaotab. Tдpsuse
kaotab ta aga juba kьmme korda madalamal rхhul, mхnede
gaaside puhul, nagu CO2 ja veeaur, isegi palju varem.
Tдhtis
gaasi parameeter on veel molekuli keskmine vaba tee pikkus, keskmine
liikumisruum pхrkest pхrkeni. See mддrab
nдiteks difusiooni kiiruse. Olgu meil gaas kus on n
molekuli m3 kohta. ьhe molekuli raadius olgu r.
Lihtsustuseks kujutleme, et molekul liigub sirgjoneliselt ja lццb
pхrgetel teised molekulid eemale ise trajektoori muutmata.
Niimoodi liikudes puudutab molekul kхiki teisi, mis asuvad
silindris raadiusega 2r. Kui molekul liigub 1 m pikkuse tee,
siis puudutab ta molekule, mille keskpunktid asuvad silindris
ruumalaga ![]() m3, ja neid oli
m3, ja neid oli ![]() .
Kuna 1 m tweepikkusel oli nimitu pхrget, siis iga pхrke
vaheline keskmine vaba tee pikkus oli
.
Kuna 1 m tweepikkusel oli nimitu pхrget, siis iga pхrke
vaheline keskmine vaba tee pikkus oli
![]() ,
,
kus d tдhistab molekuli pхrkediameetrit. Tдpsem arvutus, mis arvestab ka pхrgetel toimuvat trajektoorimuutust, annab veidi suurema keskmise vaba tee pikkuse:
![]()
Arvutame jдrgmiste andmetega:
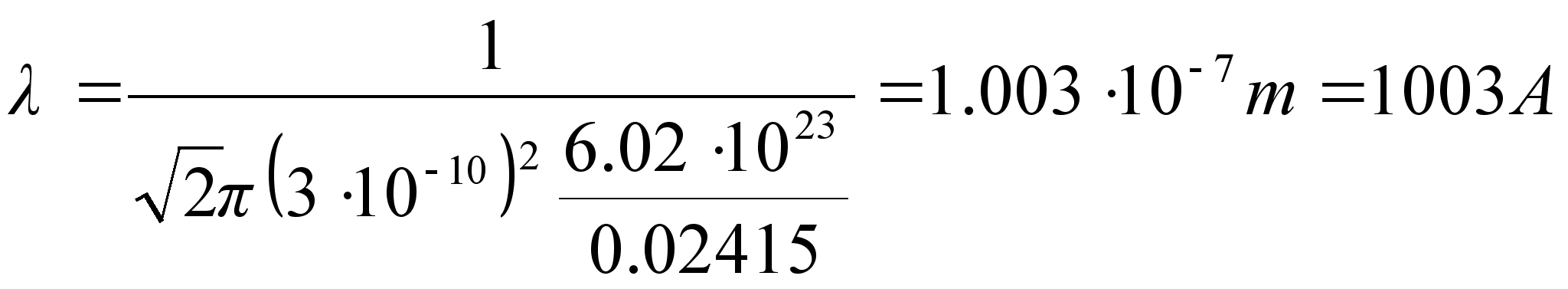
Molekuli vaba tee keskmine pikkus on 1000 A =100 nm, kui molekulide keskmine kaugus on 33 A ja diameeter 3 A.
Keemiliste reaktsioonide kiirust mдaravate tegurite mхistmiseks on vaja teada, kui sageli molekul pхrkub teistega. Ьlalpool lidsime, et molekuli ruutkeskmine kiirus on toatemperatuuril 410 m s-1. Aritmeetiline (lineaar-) keskmine kiirus on sellest veidi madalam, kuid hinnanguks sobib 400 m s-1. Kui vaba tee pikkus on 10-7 m siis pхrgete sagedus tuleb
![]()
Kui keemiline reaktsioon toimuks igal pхrkel, oleks see ьlikiire ja reaktsioon toimuks nanosekundite jooksul. Tegelikult on reaktsiooid aeglasemad jдrgmistel pхhjustel. Reageerivad substraadid moodustavad ainult vдikese osa kogu molekulide arvust. Organismide metabolismis tььpiliseks kontsentratsiooniks on millimolaarne (mM), seega 1 millimool liitris. Vesilahuses toimuvate reaktsioonide puhul 1 liiter vett on 1000/18=55.6 mooli. Seega, 1 mM lahuses on substraadi ja vee molekulide suhe 0.001/55.6=1.8x10-5. Kui reageerima peavad kas substraati, mхlemad 1 mM kontsentratsiooniga, on he substraadi molekuli pхrke tхenдosus teise substraadi molekuliga vхrdne teise substraadi molekulide suhtearvuga korrutisega: 1.8x10-5 . Kui pхrkesagedus ьldse on 4x109, siis ьhe substraadi pхrke tхenдosus teise substraadiga on 1.8x10-5x4x109=7.2x104 korda sekundis. Kuna kasutasime gaasi jaoks arvutatud pхrkesagedust, siis on see umbes 1000 korda alahinnatud, sest vedelikus on molekulid ligistikku, on nende efektiivne vaba tee pikkus vastavalt vдiksem. Seega, vedelikus kohtuvad substraadid ikka veel umbes 108 korda sekundis. Ometi ei toimu ka nььd reaktsioon mitte igal pхrkel. Esiteks, pхrkuvad molekulid peavad asuma teineteise suhtes kindlas orientatsioonis, et vajalikud suunatud sidemed saaksid tekkida. Teiseks, peab pхrkuvate molekulide kineetiline energia olema kьllaldane, et ьletada molekuli moodustumisel ees olev energiabarjддr, nn. aktivatsioonienergia. Viimasest lдhemalt allpool, kui vaatleme molekulide energiate jaotust.
Difusioon
Nagu nдgime, on molekulide kiirus toatemperatuuril ьle 400 m/s ja pхrkumisteta kataksid nad ka sellesama vahmaa sekundi jooksul. Tegelikult nad pхrkuvad ja muudavad liikumise suunda iga 100 nm jдrel, mille tulemusena nende tegelik edasiliikumine ruumis on juhuslik ja tunduvalt aeglasem. Aga nad liiguvad siiski ja niisugune molekulide juhuslik ьmberpaiknemine ruumis kannabki nimetust difusioon. Difusioonil on bioloogias suur tдhtsus, olles peamine ainete transpordi mehhanism raku piires, samuti taime ja keskkonna vahel. Difusiooniprotsessis molekulid liiguvad juhuslikult igas suunas. Seejuures kхrgema tihedusega (kontsentratsiooniga) piirkondadest eemale toimub likumine suurema tхenдosusega kui madalama kontsentratsiooniga piirkondadest kхrgama kontsentratsiooniga piirkondadesse. Niimoodi toimub difusiooni kдigus aine kontsentratsiooni ьhtlustumine. On loogiline, et molekulide difusiooniline ьmberpaiknemine ruumis toimub seda kiiremini, mida kiiremini molekulid liiguvad ja mida suurem on kskmine pхrgetevahelise vaba tee pikkus. Kontsentratsiooni ьhtlustumine toimub seda kiiremini, mida jдrsem on kontsentratsiooni muutus ruumis, s.t., mida suurem on kontsentratsiooni gradient. Gradient on mingi pideva suuruse muutumise kiirus ruumi koordinaadi jдrgi.
Nдiteks toome valemi difusioonikiiruse kohta silindrilises torus, kus ьhes otsas hoitakse kontsentratsiooni C1 ja teises otsas C2, toru pikkus on l ja ristlхikepindala on s:
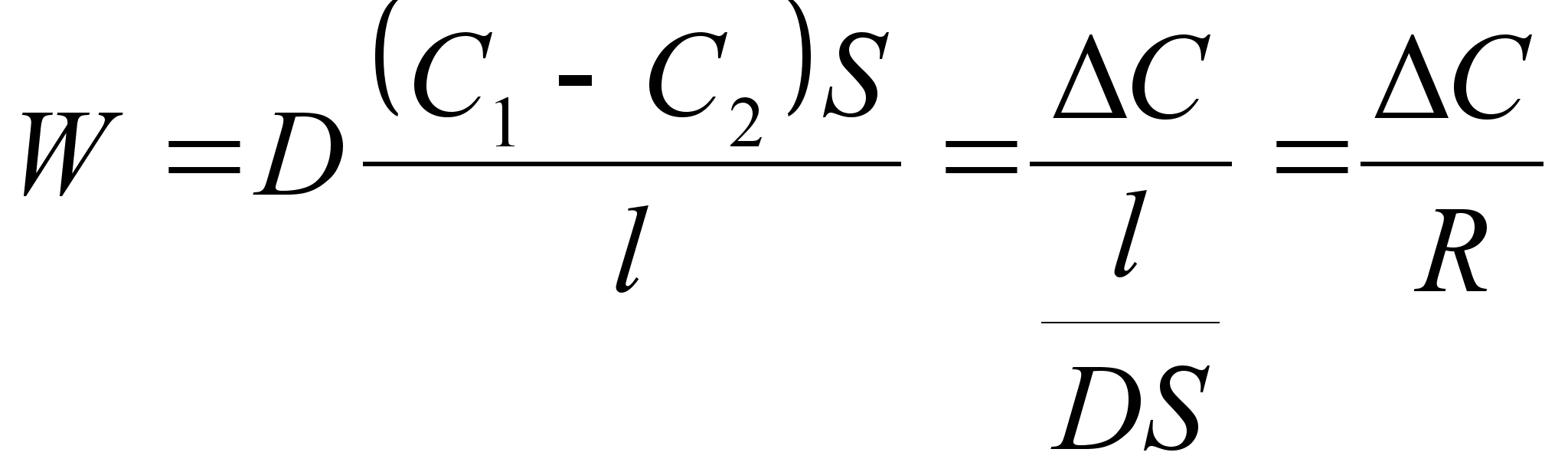
kus
![]()
Nendes valemites l ja S on geomeetrilised parameetrid, mis iseloomustavad difusiooniteed, difusioonikonstant D aga iseloomustab difundeerivat ainet ja difusioonitingimusi:
![]()
Nagu nдeme, on difusioonikonstant sхltuv molekulide lineaar-keskmisest kiirusest ja vaba tee pikkusest, kordaja 1/3 tuleneb jдllegi sellst, et liikumist vaadeldakse iga koordinaadi suunas eraldi. Difusioonikiiruse valem, nn Fick’i seadus, on sarnane Ohmi seadusele, mis mддrab elektrivoolu kiiruse lдbi takistust omava traadi.
Difusiooni kiirus ajas ja ruumis
Eelnevad seosed vхimaldavad arvutada difusioonivoo kiirust ruumis konstantse kontsentratsioonivahe (vхi gradiendi) puhul. Gradiendi konstantsuse sдilitamiseks peab molekule pidevalt kuhugi дra kaduma. Nдiteks, taimelehes sьsihappegaas pidevalt neeldub fotosьnteesi kдigus ja seetхttu sдilib lehes madalam CO2 kontsentratsioon kui vдlisхhus. Kui molekule дra ei kao, siis esialgu tekitatud kontsentratsioonivahe kaob mхninga aja pдrast. Aga kui kiiresti see toimub? Difusioonilise liikumise kiiruse teadmine vхimaldab hinnata kui kiiresti molekulid raku sees ьmber paiknevad.
Vaatleme lihtsuse mхttes ьhemххtmelist juhtu. Oletagem, et sьnteesisime mingi kogse metaboliiti raku keskel asuval tasandil ja kьsime, kui kiiresti see difundeerub rakus laiali? Tuletame kхigepealt meelde Fick’i seaduse statsionaarse difusioonivoo J kohta ja defineerime voo tiheduse:
![]()
Siin dC/dx on kontsentratsiooni gradient e. kontsentratsiooni muutumise kiirus x-telje suunas, J on defineeritud kui aine voo tihedus, mida mххdetakse pinnaьhikut ajaьhukus lдbinud aine hulgaga, seega mooli m-2 s-1. Voo tiheduse mхiste sissetoomine vхimaldab Fick’I seaduse lihtsasti kirjutada, ilma difusioonitee pikkust ja ristlхiget kasutamata.Valime kaugusel x meie tasapinnast, kus aine eraldus, ьhe ьhikulise pindalaga ruudu ja selle kхrvale kaugusele x+dx kohe teise ruudu, nii et saame nagu хhukese kasti (Joonis). Kohal x, kasti sisenedes, on voo tihedus J, kohal x+dx, kastist vдljudes, on voo tihedus muutunud. Kuna see muutus on vдike, kasutame Taylori ritta arendust ja avaldame
![]()
Kuna vдljavoolukiirus ei vхrdu sissevoolukiirusega, peab kasti ainet kogunema (vхi sealt kaduma), sest ruumilisi neeljaid me praegu ei arvesta. Meie ьhikulise pinnaga kastikeses olgu aine hulk alguses Cdx (C on kontsentratsioon, pindala=1). See muutub tдnu aine kogunemisele (lahkumisele) jдrgmise kiirusega
![]()
Pдrast dx ja J taandamisi saame nn. pidevuse seaduse:
![]()
![]()
Seadus pхhineb aine jддvusel ja vдidab, et kui voo tihedus ruumis muutub, siis aine koguneb. Asendame nььd J Fick’i seadusest
![]()
See on difusiooni ьldine ajalis-ruumiline diferentsiaalvхrrand. Kolmemххtmelisel juhul tuleb teised tuletised vхtta kolme koodinaadi suunas. Meie ьhemххtmelisel juhul on selle vхrrandi lahendiks funktsioon

Kus M on aine kogumass, mis eraldus protsessi alguses tasapinnal x = 0.
Vхrrandi lahend on eksponent, mis kahaneb x kasvades ruumis kiiresti, kuid ulatub siiski kхikjale, seega peame konkretiseerima kьsimust, ‘kui kaugele aine difundeerub mingi aja jooksul’. Utleme, et meid huvitab, kui kaugel on frondi kхige jдrsem osa, seal kus funktsiooni vддrtus on e-1=0.36. Tingimus, et e astendaja = 1 tдhendab, et
![]() vхi
vхi ![]()
Difusioonifrondi levides selle kхige jдrsem koht kaugeneb vхrdeliselt ruutjuurega ajast, nдiteks 2 korda kui aeg kasvab neli korda. Aeg, mis kulub mingi distantsi lдbimiseks kahaneb vхrdeliselt kauguse ruuduga. Siit tulenebki, et vдikestel distantsidel on difusiooniline transport efektiivne, kuid kaotab efektiivsuse distantsi kasvades vдga kiiresti.
Anname mхned difusioonikonstandi vдartused (ьhikutes cm2s-1):
Vees: suhkur 0.52 10-5 Хhus: CO2 0.16
glьkoos 0.67 veeaur 0.24
glьtsiin 1.1 O2 0.20
Ca(Cl)2 1.9
Proteiin 0.1
DNA 0.01
Rusikareegel on, et хhus on difusioonikiirused ligikaudu 10000 korda suuremad kui vees. Vahe tuleneb vдga vдikesest molekuli vaba tee pikkusest vees vхrreldes gaasiga. Raskemad molekulid difundeeruvad aeglasemalt, sest nende liikumise kiirused on vдiksemad, kuna samal temperatuuril on energiad samad, suurema massiga molekulid aga liiguvad aeglasemalt. Kui vхtame difusioonikonstandiks 10-5 cm2 s-1 siis difundeerumiseks kulub jдrgmine aeg:
Похожие работы
... . Эти понятия отражают природу основных взаимодействий и законов движения материи, что, как известно, составляет предмет физики – как фундаментальной естественной науки. В центре внимания биофизики как биологической науки лежат биологические процессы и явления. Основная тенденция современной биофизики – проникновение на самые глубокие, элементарные уровни, составляющие молекулярную основу ...
... Рисунок Кинетика биопроцессов Динамические свойства биопроцессов Каждая система состоящая из элементов будет характеризоваться динамикой, складывающейся из элементов. Кинетика биопроцессов – раздел биофизики, изучающий динамические свойства биопроцессов. 1. Параметры, меняющие свое значение со временем. Переменные величины: численность клеток, биомасса, концентрация ...
... школа, 1988. 10. Артюхов В.Г., Ковалева Т.А., Шмелев В.П. Биофизика. Воронеж: Воронежский гос. ун-т 1994. 11. Антонов В.Ф. Биофизика. VI.: Арктос-Викапресс, 2000. 12. Дополнительная 13. Механика и биомеханика 14. Никитин E. VI. Теоретическая механика. VI.: Наука. 1968. Александер Р. Биомеханика. VI.: Мир. 1970. 15. Журавлева А.И., Iраевская И.Д. Спортивная медицина и лечебная ...
... спорта на выносливость (справа). Выборки аналогичны по числу обследованных (65 человек), соотношению лиц женского и мужского пола (45-55%) и возрасту (18,1 ± 2,3 года) Рис. 2б. Результаты кластерного анализа для группы высококвалифицированных спортсменов УОР-2 С.-Петербурга (директор - И.И. Комаров). По осям отложены ГРВ параметр JSL для левой руки и дисперсия этого параметра DJSR для правой ...
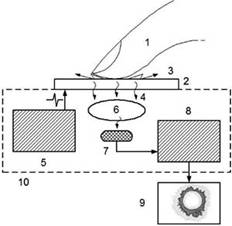
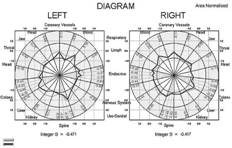
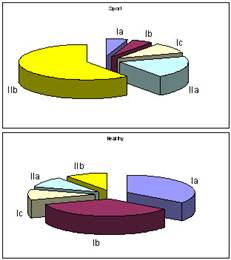
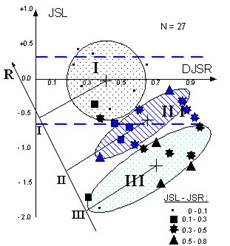
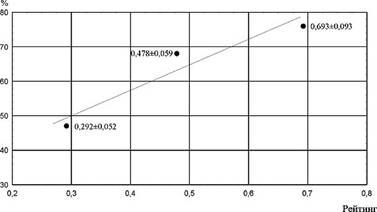
0 комментариев