Навигация
Содержание.
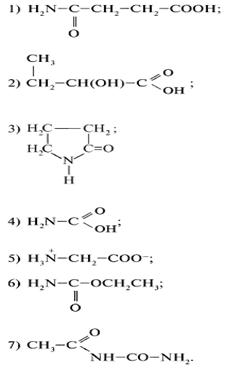
1. Классификация аминокислот.
2. Синтезы ![]() ,
, ![]() ,
, ![]() - аминокислот.
- аминокислот.
3. Свойства аминокислот: амфотерность, реакция по аминогруппе и карбоксилу.
4. ![]() - аминокислоты, их роль в природе.
- аминокислоты, их роль в природе.
5. Синтез пептидов.
Белковые вещества:
1. Классификация.
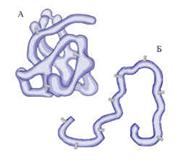
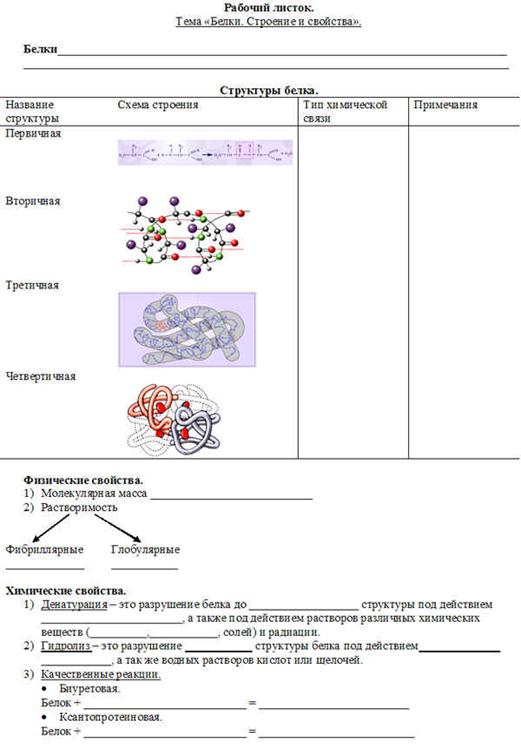
2. Строение. Первичная структура, понятие о вторичной, третичной и четвертичной структурах.
3. Понятие о ферментах.
Классификация аминокислот.
Аминокислотами называются органические кислоты, содержащие одну или несколько аминогрупп. В зависимости от природы кислотной функции аминокислоты подразделяют на аминокарбоновые, например H2N(CH2)5COOH, аминосульфоновые, например H2N(CH2)2SO3H, аминофосфоновые, H2NCH[P(O)(OH)2]2, аминоарсиновые, например, H2NC6H4AsO3H2.
Согласно правилам ИЮПАК название аминокислот производят от названия соответствующей кислоты; взаимное расположение в углеродной цепи карбоксильной и аминной групп обозначают обычно цифрами, в некоторых случаях - греческими буквами. Однако, как правило, пользуются тривиальными названиями аминокислот. ( см. таблицу 1.) .
В зависимости от положения аминогруппы по отношению к карбоксилу различают ![]() ,
, ![]() и
и ![]() - аминокислоты:
- аминокислоты:
|
|
|
Все
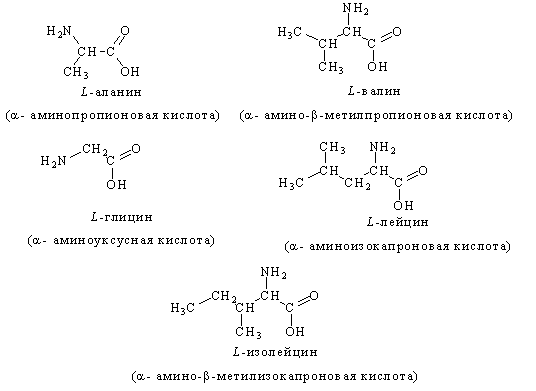
![]() - аминокислоты, кроме аминоуксусной (глицина), имеют асимметрический
- аминокислоты, кроме аминоуксусной (глицина), имеют асимметрический ![]() - углеродный атом и существуют в виде двух энантиомеров. За редким исключением, природные
- углеродный атом и существуют в виде двух энантиомеров. За редким исключением, природные ![]() -аминокислоты относятся к L- ряду (S-конфигурация) и имеют следующее пространственное строение:
-аминокислоты относятся к L- ряду (S-конфигурация) и имеют следующее пространственное строение:
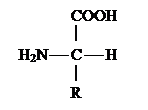 По физическим и ряду химических свойств аминокислоты резко отличаются от соответствующих кислот и оснований. Они лучше растворяются в воде, чем в органических растворителях; хорошо кристаллизуются; имеют высокую плотность и исключительно высокие температуры плавления. Эти свойства указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твёрдом состоянии и в растворе (в широком интервале pH) находятся в цвиттер-ионной форме (т.е. как внутренние соли). Взаимное влияние групп особенно ярко проявляется у
По физическим и ряду химических свойств аминокислоты резко отличаются от соответствующих кислот и оснований. Они лучше растворяются в воде, чем в органических растворителях; хорошо кристаллизуются; имеют высокую плотность и исключительно высокие температуры плавления. Эти свойства указывают на взаимодействие аминных и кислотных групп, вследствие чего аминокислоты в твёрдом состоянии и в растворе (в широком интервале pH) находятся в цвиттер-ионной форме (т.е. как внутренние соли). Взаимное влияние групп особенно ярко проявляется у ![]() -аминокислот, где обе группы находятся в непосредственной близости.
-аминокислот, где обе группы находятся в непосредственной близости.
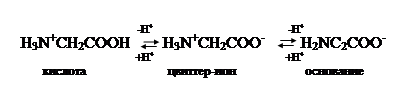
Цвиттер-ионная структура аминокислот подтверждается их большим дипольным моментом (не менее 50×10-30 Кл × м), а также полосой поглощения в ИК- спектре твердой аминокислоты или её раствора.
Таблица 1. Важнейшие аминокислоты.| Тривиальное название | Сокр.название ос- татка ами нок-ты | Формула | Температура плавления, 0С. | Растворимость в воде при 250С, г/100г. |
| Моноаминомонокарбоновые кислоты | ||||
| Гликокол или глицин | Gly | H2NCH2COOH | 262 | 25 |
| Аланин | Ala | H2NCH(CH3) COOH | 297 | 16,6 |
| Валин | Val | H2NCHCOOH ï CH(CH3)2 | 315 | 8,85 |
| Лейцин | Leu | H2NCHCOOH ï CH2CH(CH3)2 | 337 | 2,2 |
| Изолейцин | He | H2NCHCOOH ï CH3 ─ CH ─ C2H5 | 284 | 4,12 |
| Фенилаланин | Phe | H2NCHCOOH ï CH2C6H5 | 283 (разл.) | ― |
| Моноаминодикарбоновые кислоты и их амиды | ||||
| Аспарагиновая кислота | Asp(D) | H2NCHCOOH ï CH2COOH | 270 | 0,5 |
| Аспарагин | Asn(N) | H2NCHCOOH ï CH2CONH2 | 236 | 2,5 |
| Глутаминовая кислота | Glu(E) | H2NCHCOOH ï CH2CH2COOH | 249 | 0,84 |
| Глутамин | Gln(Q) | H2NCHCOOH ï CH2CH2CONH2 | 185 | 4,2 |
| Диаминомонокарбоновые кислоты | ||||
| Орнитин(+) | Orn | H2NCHCOOH ï CH2CH2CH2 NH2 | 140 | ― |
| Лизин | Lys(K) | H2NCHCOOH ï CH2CH2CH2 CH2NH2 | 224 | Хорошо растворим |
| Аминокислоты | ||||
| Аргинин | Arg® | H2NCHCOOH ï CH2 ï CH2CH2 NH ─ C ─ NH2 ║ NH | 238 | 15 |
| Гидроксиаминокислоты | ||||
| Серин | Ser(S) | H2NCHCOOH ï CH2OH | 228 | 5 |
| Треонин | Tre(T) | H2NCHCOOH ï CH2 (OH)CH3 | 253 | 20,5 |
| Тирозин | Tyr(Y) | H2NCHCOOH ï CH2C6H4OH-n | 344 | ― |
| Тиоаминокислоты | ||||
| Метионин | Met(M) | H2NCHCOOH ï CH2CH2SCH3 | 283 | 3,5 |
| Цистин | (Cys)2 |
2 | 260 | 0,011 |
| Цистеин | Cys© | H2NCHCOOH ï CH2SH | 178 | Хорошо растворим |
| Гетероциклические аминокислоты | ||||
|
| Try(W) | H2NCHCOOH ï H2C NH | 382 | 1,14 |
|
| Pro(P) | H2C CH2 ï ï H2C CHCOOH NH | 299 | 16,2 |
|
| Opr | HOHC CH2 ï ï H2C CHCOOH NH | 270 | 36,1 |
|
| His(H) | NH2CHCOOH ï H2C ―C ―― CH ï ï N NH CH | 277 | 4,3 |
Синтезы
![]() -аминокислоты получают галогенированием карбоновых кислот или эфиров в
-аминокислоты получают галогенированием карбоновых кислот или эфиров в ![]() -положение с последующей заменой галогена на аминогруппу при обработке амином, аммиаком или фталимидом калия (по Габриэлю).
-положение с последующей заменой галогена на аминогруппу при обработке амином, аммиаком или фталимидом калия (по Габриэлю).
|
По Штрекеру – Зелинскому ![]() -аминокислоты получают из альдегидов:
-аминокислоты получают из альдегидов:
|
Этот метод позволяет также получать нитрилы и амиды соответствующих
|
В этой реакции вместо альдегидов могут быть использованы кетоны, а вместо диалкилфосфитов- диалкилтиофосфиты, кислые эфиры алкилфосфонистых кислот RP(OH)OR и диарилфосфиноксиды Ar2HPO.
Альдегиды и кетоны или их более активные производные – кетали служат для синтеза ![]() - аминокислот с увеличением числа углеродных атомов на две единицы. Для этого их конденсируют с циклическими производными аминоуксусной кислоты – азалактонами, гидантоинами, тиогидантоинами, 2,5-пиперазиндионами или с её медными или кобальтовыми хелатами, например:
- аминокислот с увеличением числа углеродных атомов на две единицы. Для этого их конденсируют с циклическими производными аминоуксусной кислоты – азалактонами, гидантоинами, тиогидантоинами, 2,5-пиперазиндионами или с её медными или кобальтовыми хелатами, например:
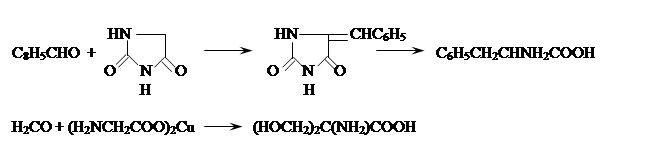
Удобные предшественники ![]() -аминокислот - аминомалоновый эфир и нитроуксусный эфир. К их
-аминокислот - аминомалоновый эфир и нитроуксусный эфир. К их ![]() -углеродным атомам можно предварительно ввести желаемые радикалы методами алкилирования
или конденсации.
-углеродным атомам можно предварительно ввести желаемые радикалы методами алкилирования
или конденсации. ![]() -кетокислоты превращают в
-кетокислоты превращают в ![]() -аминокислоты
гидрированием в присутствии NH3 или гидрированием их оксимов, гидразонов и фенилгидразонов.
-аминокислоты
гидрированием в присутствии NH3 или гидрированием их оксимов, гидразонов и фенилгидразонов.

![]()
Можно получать ![]() -аминокислоты также непосредственно из
-аминокислоты также непосредственно из ![]() -кетонокислот, действуя на них аммиаком и водородом над никелевым катализатором:
-кетонокислот, действуя на них аммиаком и водородом над никелевым катализатором:
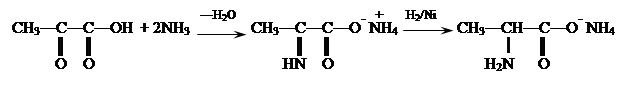
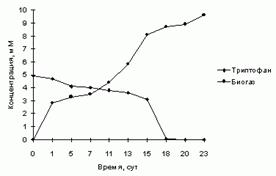
Некоторые L-![]() -аминокислоты ввиду сложности синтеза и разделения оптических изомеров получают микробиологическим способом (лизин, триптофан, треонин) или выделяют из гидролизатов природных белковых продуктов (пролин, цистин, аргинин, гистидин).
-аминокислоты ввиду сложности синтеза и разделения оптических изомеров получают микробиологическим способом (лизин, триптофан, треонин) или выделяют из гидролизатов природных белковых продуктов (пролин, цистин, аргинин, гистидин).
![]() - аминосульфоновые кислоты получают при обработке аммиаком продуктов присоединения NaHSO3 к альдегидам:
- аминосульфоновые кислоты получают при обработке аммиаком продуктов присоединения NaHSO3 к альдегидам:
RCHO + NaHSO3 ® RCH(OH)SO3Na ® RCH(NH2)SO3Na
|
В.М.Родионов предложил метод, в котором совмещаются в одной операции получение ![]() ,
,![]() -непредельной кислоты конденсацией альдегида с малоновой кислотой и присоединение аммиака:
-непредельной кислоты конденсацией альдегида с малоновой кислотой и присоединение аммиака:
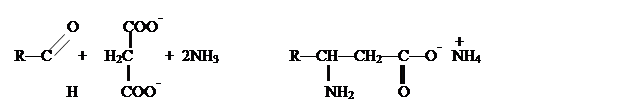
![]()
|
![]() -аминокислоты получают гидролизом соответствующих лактамов, которые образуются в результате перегруппировки Бекмана из оксимов циклических кетонов под действием H2SO4.
-аминокислоты получают гидролизом соответствующих лактамов, которые образуются в результате перегруппировки Бекмана из оксимов циклических кетонов под действием H2SO4. ![]() -аминоэтановую и
-аминоэтановую и ![]() -аминоундекановую кислоты синтезируют из
-аминоундекановую кислоты синтезируют из ![]() ,
,![]() ,
,![]() ,
,![]() -тетрахлоралканов путем их гидролиза конц. H2SO4 до -хлоралкановых кислот с последующим аммонолизом:
-тетрахлоралканов путем их гидролиза конц. H2SO4 до -хлоралкановых кислот с последующим аммонолизом:
Cℓ(CH2CH2)nCCℓ3 → Cℓ(CH2CH2)nCOOH → H2N(CH2CH2)nCOOH
Исходные тетрахлоралканы получают теломеризацией этилена с CCℓ4.
Бекмановская перегруппировка оксимов циклических кетонов. Наибольшей практический интерес представляет перегруппировка оксима циклогексанона:
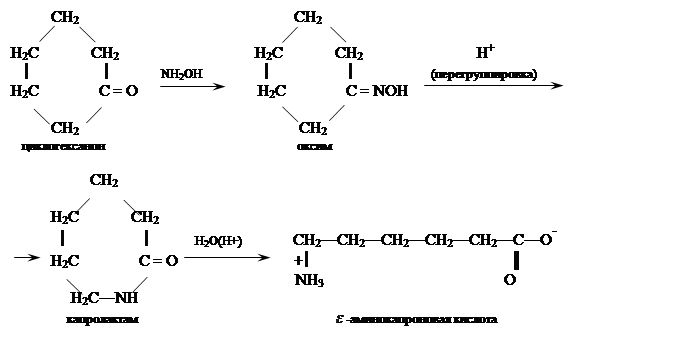
Получаемый этим путем капролактам полимеризуют в высокомолекулярный поликапромид
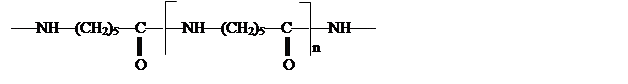
![]()
![]()
из которого изготовляют капроновое волокно.
Свойства аминокислот: амфотерность, реакция по аминогруппе и карбоксилу.
Похожие работы
... частью содержится в цитоплазме клеток. Содержание РНК, как правило, в 5-10 раз больше, чем ДНК. Соотношение РНК/ДНК в клетках тем выше, чем интенсивнее в них синтез белка. Нуклеиновые кислоты обладают сильно выраженными кислотными свойствами и при физиологических значениях рН несут высокий отрицательный заряд. В связи с этим в клетках организмов они легко взаимодействуют с различными катионами и ...
... - могут. Такие комбинированные продукты питания, которые содержат взаимодополняющие (комплементарные) белки, входят в состав традиционной кухни всех народов мира [5,6]. ГЛАВА 3. ЭКОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ИЗУЧЕНИЯ ТЕМЫ «АМИНОКИСЛОТЫ» Человеческое тело не может запасать белки, поэтому сбалансированное белковое питание требуется человеку каждый день. Взрослому человеку весом 82 кг требуется 79 г ...
... приближается к 100%. Очень высока степень усвоения и других продуктов животного происхождения: молока (75—80%), мяса (70—75%), рыбы (70—80%) и т. д., Многие растительные продукты, особенно злаковые, содержат белки пониженной биологической ценности: в кукурузе, например, обнаружен значительный дефицит лизина и триптофана, в пшенице — лизина и треонина. В большинстве растительных материалов ...
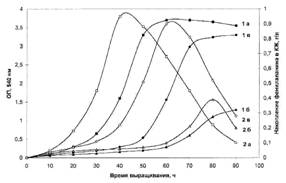
... . Так, в Phe детектировалось 80,5 % метки, в Ala - 95 %, в Gly - 90% (см. табл. 6). Во всех экспериментах степени включения дейтерия и изотопа углерода 13С в метаболически связанных аминокислотах обнаружили определённую коррелляцию. Так, степени изотопного обогащения валина и лейцина (семейство пирувата), фснилаланина и тирозина (семейство ароматических аминокислот} совпадают (табл. 6). Степени ...

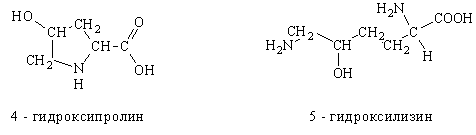

0 комментариев