Навигация
I. Строение молекулы метана.
Молекулярная формула метана CH4.
Так как атом углерода имеет большую электроотрицательность (2,5), чем водород (2,1), то в молекуле метана происходит незначительное смещение общих электронных пар в сторону атома углерода.
Однако такая формула не отражает пространственного строения молекулы. Чтобы это показать, необходимо вспомнить о формулах электронных облаков и размещении электронов по энергетическим уровням и подуровням. Например, строение атома углерода изображают следующей схемой:
| 2P | ||||||
| ) ) | 2S | ↑ | ↑ | |||
| С +6 2 4 | S | ↑↓ | ||||
| ) ) | ↑↓ | 1S2 2S2 2P2 |
Так как на втором энергетическом уровне р-подуровне имеется свободная орбиталь, то на нее может перейти один из 2S2 – электронов:
| ) ) | ||||||
| С +6 2 4 | ↓ | ↓ | ↓ | |||
| ) ) | ↓ | |||||
| S Sp | ↑↓ |
В результате все четыре наружных электрона второго энергетического уровня в атоме углерода окажутся неспаренными, и атом углерода в возбужденном состоянии становится четырехвалентным.
Чтобы понять, как происходит образование химических связей в молекуле метана перекрыванием электронных облаков и почему молекула метана имеет тетраэдрическое строение, нужно знать то, что эти облака после гибридизации распространяется в пространстве так, что их оси оказываются направленными к вершинам тетраэдры. При образовании молекул метана вершины этих гибридных облаков перекрываются с облаками электронов атомов водорода.
Так как в этом случае в гибридизации участвует один S-электрон и три p-электрона, то такой ее вид называется SP3- гибридизацией.
Химическая формула и строение молекул этилена.
Молекулярная формула этилена C2H4.
Если между двумя взаимно связанными атомами углерода разместить четыре атома водорода, то структурную формулу этилена следовало бы изобразить так:
H H
| |
H – C – C – H
| |
Однако свободных связей в молекуле не должно быть. Поэтому в структурной формуле этилена изображают двойную связь:
H H
| |
H – C = C – H
Следовательно, в отличие от предельных углеводородов, в молекулах которых между атомами углерода имеется ординарная связь, в молекулах углеводородов ряда этилена между атомами углерода имеется одна двойная связь.
В молекуле этилена подвергаются гибридизации одно S- и два p – электронных облака атомов углерода. Таким образом каждый атом углерода имеет по три (всего шесть) гибридных электронных облака и по одному (всего два) негибридному p – облаку. Два из гибридных электронных облаков атомов углерода взаимно перекрываются и образуют между атомами углерода δ (сигма) – связь. Остальные четыре гибридных электронных облака атомов углерода перекрываются в той же плоскости с четыремя S – электронными облаками атомов водорода и также образуют четыре δ – связи. Негибридные два p-облака атомов углерода взаимно перекрываются в плоскости, которая расположена перпендикулярно плоскости δ – связи, т.е. образуется одна П-связь. Следовательно, в молекуле этилена между атомами имеется одна δ и одна П – связь. В углеродных соединениях П – связь значительно слабее, чем δ – связь. Под воздействием респектов П – связь легко разрывается.
Легко понять, что в молекулах предельных углеводов атомы углерода могут свободно вращаться вокруг δ – связи. Если же между атомами углерода существует не только δ – связь, но и П – связь, то такое вращение без разрыва последней невозможно.
II.
1.Изомерия цепи атомов углерода в различных органических соединениях
Впервые с этим видом изомерии мы встретились при изучении предельных углеводородов. Например, молекулярной формуле C5H12 соответствуют три вещества:
CH3 – CH2 - CH2 - CH2 - CH3
Пентан
| CH3 | |
| | | |
| CH3 – CH – CH2 – CH3 | CH3 – C - CH3 |
| | | | |
| CH3 | CH3 |
| 2-метилбутан | 2,2 диметилпропан |
Этот вид изомерии встречается не только у предельных углеводородов, но и у других классов органических соединений. Так, например, в зависимости от строения углеродной цепи одной и той же молекулярной формуле С4Н90Н соответствуют два спирта:
| CH3 | |
| 4 3 2 1 | 3 2| 1 |
| CH3 - CH2 - CH2 - CH2 - ОH | CH3 - CH – CH2 - ОH |
| 1-бутанол | 2-метил-1-пропанол |
Другой пример. Одной и той же молекулярной формуле C4H9O2в зависимости от строения углеродной цепи соответствуют две аминокислоты:
| O | CH3 O |
| 4 3 2 1// | 3 2| 1// |
| CH3 – CH2 – CH – C | CH3 – C – C |
| | | | \ |
| NH2 | NH2 OH |
| 2-аминобутановая кислота | 2-амино-2-метил-пропановая кислота |
Похожие работы
... ВС...?!! Бесспорным фаворитом теории валентности стал метод МО ЛКАО, идеально приспособленный к алгоритмам современной вычислительной математики и компьютерной техники. Сейчас уже совершенно ясно, что теория ЛКАО МО была настоящей идейной революцией. В её основу положено одноэлектронное приближение. Молекулярный ион водорода был первой и простейшей системой, на примере которой было понято и ...
... . ХИМИЯ ДРАГОЦЕННОГО ДАРА ПРИРОДЫ Октябрь 1917 года был переломным в биографии Н.Д. Зелинского не только как гражданина, но и как ученого. В 1917 году Николай Дмитриевич смог вернуться в Московский университет. Лаборатория Зелинского с первых дней активно подключилась к выполнению исследований, связанных с нуждами страны. В 1918 – 1919 года он разработал метод получения ...
... менее в более упорядоченное состояние. В самоорганизации всегда возникает нечто новое, чего раньше не было. Самоорганизация - это междисциплинарная область знания, ведущий принцип всего современного естествознания, применение ко многим предметам, наукам. В процессе усложнения систем различают два взаимодополняющих механизма: объединение частей и разделение (фракционирование) систем. Механизмы, ...
... подразумевают упорядоченную связь и взаимодействие между элементами системы, благодаря которой и возникают новые целостные свойства. В такой химической системе, как молекула, именно специфический характер взаимодействия составляющих ее атомов определяет свойства молекулы. 3.2 «Триумфальное шествие органического синтеза» Возникновение структурной теории позволило химикам впервые обрести ...

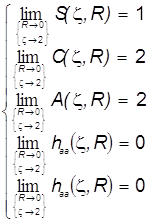
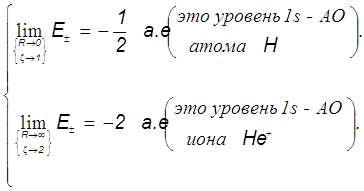
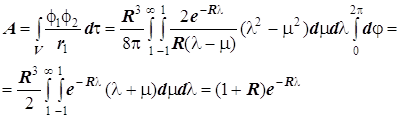
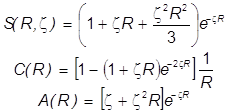


0 комментариев