Лекция: Большое каноническое распределение Гиббса.
План:
1. Функция распределения системы, ограниченной воображаемыми стенками.
2. Большой канонический формализм.
3. Термодинамическая интерпретация распределений Гиббса.
1.Рассмотрим построение термодинамического формализма, связанного с выделением термодинамической системы с помощью воображаемых стенок (![]() ). Несмотря на то, что определение химического потенциала представляется весьма сложной задачей (эта величина непосредственно не измеряется, а вычисляется на основе косвенных измерений, причем, достаточно сложным образом), отказ от точной фиксации числа частиц существенно упрощает рассмотрение ряда задач.
). Несмотря на то, что определение химического потенциала представляется весьма сложной задачей (эта величина непосредственно не измеряется, а вычисляется на основе косвенных измерений, причем, достаточно сложным образом), отказ от точной фиксации числа частиц существенно упрощает рассмотрение ряда задач.
Очевидно, что рассмотренная ранее фиксация числа частиц N с точностью до 1 шт. носит идеализированный характер и по большому счету представляет формальный прием, облегчающий анализ. В действительности же не только не только энергия, но и число частиц оказываются размыты о числу частиц ![]() около среднего значения
около среднего значения ![]() . Как и для разброса
. Как и для разброса ![]() , разброс
, разброс ![]() захватывает сравнительно большое число частиц (
захватывает сравнительно большое число частиц (![]() ).
).
Полагая далее, что система выделена с помощью воображаемых стенок и число N не может быть включено в число переменных состояния системы, воспользуемся сопряженной к ![]() величиной – химическим потенциалом
величиной – химическим потенциалом ![]() . Поскольку величина внутренней энергии
. Поскольку величина внутренней энергии ![]() также зависит от числа частиц ее необходимо заменить на величину
также зависит от числа частиц ее необходимо заменить на величину ![]() (см. тему №3)
(см. тему №3)
Тогда II-е начало термодинамики для квазистатических процессов, имеющее вид:
![]() (7.1а)
(7.1а)
преобразуется к виду:
![]() (7.1б)
(7.1б)
Найдем функцию распределения ![]() по микроскопическим состояниям термодинамической системы. Очевидно, эта функция должна удовлетворять ряду требований:
по микроскопическим состояниям термодинамической системы. Очевидно, эта функция должна удовлетворять ряду требований:
1. Распределение ![]() должно определять вероятность обнаружить систему в состоянии с заданными значениями N и n. Здесь N – число частиц в системе (с точностью до 1 штуки),
должно определять вероятность обнаружить систему в состоянии с заданными значениями N и n. Здесь N – число частиц в системе (с точностью до 1 штуки), ![]() - набор квантовых чисел, определяющих микроскопическое состояние системы N тел.
- набор квантовых чисел, определяющих микроскопическое состояние системы N тел.
2. Желательно, чтобы в качестве макроскопических переменных, описывающих состояние термодинамической системы, использовались величины (![]() ).
).
3. Полученное распределение должно быть сосредоточенным около значения ![]() по числу частиц N и около значения
по числу частиц N и около значения ![]() по энергии.
по энергии.
Сформулированное требование позволяет использовать закономерности и допущения, положенные в основу микроканонического и канонического распределений.
Очевидно, величина ![]() при фиксированном
при фиксированном ![]() представляет среднее значение микроскопических характеристик
представляет среднее значение микроскопических характеристик ![]() . Тогда, учитывая сформулированную выше аксиому о равновероятности микросостояний, соответствующих заданному макросостоянию, выражение для распределения по микроскопическим состояниям
. Тогда, учитывая сформулированную выше аксиому о равновероятности микросостояний, соответствующих заданному макросостоянию, выражение для распределения по микроскопическим состояниям ![]() , можно записать, по аналогии с микроскопическим распределением Гиббса (5.12):
, можно записать, по аналогии с микроскопическим распределением Гиббса (5.12):
![]() . (7.2)
. (7.2)
Здесь ![]() - сосредоточенная около нуля квазикронекоровская функция (
- сосредоточенная около нуля квазикронекоровская функция (![]() ),
), ![]() - нормировочная сумма (аналог статистического веса):
- нормировочная сумма (аналог статистического веса):
![]() (7.3)
(7.3)
Как известно, основная асимптотика статистического веса Г при ![]() не зависит от выбора типа стенок, ограничивающих термодинамическую систему. То есть она не зависит от выбора набора макроскопических параметров : (
не зависит от выбора типа стенок, ограничивающих термодинамическую систему. То есть она не зависит от выбора набора макроскопических параметров : (![]() ), (
), (![]() ), (
), (![]() ) и т.д., фиксирующих равновесное состояние системы. Тогда введенная величина
) и т.д., фиксирующих равновесное состояние системы. Тогда введенная величина ![]() и связанная с ней
и связанная с ней ![]() по сути являются статистическим весом Г и энергией S термодинамической системы
по сути являются статистическим весом Г и энергией S термодинамической системы
Учитывая (6.8), представляющей явное выражение функции ![]() , перепишем (7.2) в виде:
, перепишем (7.2) в виде:
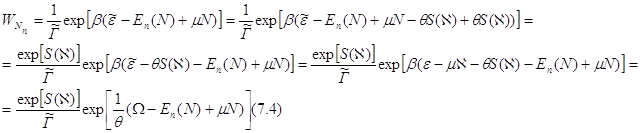
При записи (7.4) было использовано выражение (3.21) для термодинамического потенциала “омега” ![]() .
.
Найдем выражение для нормировочной суммы ![]() , подставляя в (7.3) выражение (6.8) для функции
, подставляя в (7.3) выражение (6.8) для функции ![]() :
:
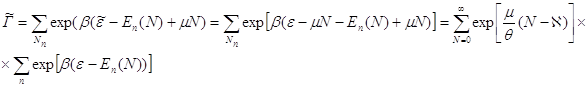
Поскольку, согласно (5.11) ![]()
получим:
![]() (7.5)
(7.5)
Для дальнейшего анализа разложим энтропию ![]() в степенной ряд по отношению числа частиц N от среднего термодинамического значения
в степенной ряд по отношению числа частиц N от среднего термодинамического значения ![]() , ограничиваясь членами второго порядка. При этом учтем:
, ограничиваясь членами второго порядка. При этом учтем: ![]() (см. ф-лу (3.28)). Тогда получим:
(см. ф-лу (3.28)). Тогда получим:
![]()
Подставляя полученный результат в (7.5), находим:
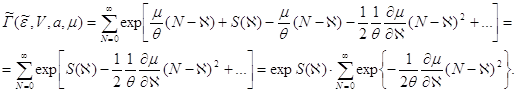
Учитывая большое число частиц N и, пологая ![]() , перейдем от суммирования в последнем выражении к интегралу. Получаем:
, перейдем от суммирования в последнем выражении к интегралу. Получаем:
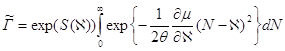 (7.6)
(7.6)
Вычислим интеграл в полученном равенстве:
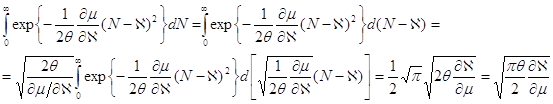
Подставляя полученный результат в (7.6), получаем:
![]()
Тогда вычисляя в обеих частях последнего равенства предел при ![]() и отбрасывая в правой части сомножители, растущие медленнее, чем
и отбрасывая в правой части сомножители, растущие медленнее, чем ![]() , получаем:
, получаем:
![]() (7.6)
(7.6)
Подставляя (7.6) в (7.4), находим:
![]() (7.7)
(7.7)
Выражение (7.7) получило название большого канонического распределения Гиббса. Включая в себя каноническое распределение (6.15) как частный случай, это распределение также содержит распределение по числу частиц. Если ![]() , то (7.7) принимает вид (6.15).
, то (7.7) принимает вид (6.15).
Нормировочная сумма:
![]() (7.8)
(7.8)
получила название большой статистической сумы. Эта величина связана с термодинамическим потенциалом ![]() посредством соотношения:
посредством соотношения:
![]() (7.9)
(7.9)
При необходимости, используя аппарат макроскопической термодинамики можно осуществить в (7.8) переход к другим переменным. Покажем, что на примере перехода от (![]() ) и (
) и (![]() ). Из (7.1) следует:
). Из (7.1) следует:
![]() или
или ![]() и т.д.
и т.д.
Полученные равенства можно рассматривать как термодинамические уравнения относительно химического потенциала, решением которых будет выражение ![]() . А учитывая (3.21):
. А учитывая (3.21): ![]() , можно исключить и переменную
, можно исключить и переменную ![]() , выражая ее в виде
, выражая ее в виде ![]() . Тогда для энтропии и, соответственно статистического веса, можно записать:
. Тогда для энтропии и, соответственно статистического веса, можно записать:
![]() (7.10)
(7.10)
Аналогичным образом осуществляется пересчет и для других переменных состояния и параметров термодинамической системы.
Как и в рассмотренном ранее каноническом распределении, для большого канонического распределения можно показать, что ![]() является чрезвычайно сосредоточенным распределением как по числу частиц N, так и по энергии Е.
является чрезвычайно сосредоточенным распределением как по числу частиц N, так и по энергии Е.
Воспользуемся аналогией с выполненным в предыдущей теме расчетом ширины канонического распределения по энергии. Тогда ширина распределения по N рассчитывается на основе дисперсии ![]() и оказывается равной
и оказывается равной
![]() (7.11)
(7.11)
Здесь ![]() - макроскопические усреднения концентрации частиц.
- макроскопические усреднения концентрации частиц.
Тогда для относительной флуктуации ![]() числа частиц, получаем:
числа частиц, получаем:
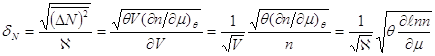 (7.12)
(7.12)
Таким образом, допустимые большим каноническим распределением состояния с числом частиц N сосредоточены в узком интервале значений вблизи точки ![]() . Ширина этого интервала в предельном статистическом случае стремится к нулю по закону
. Ширина этого интервала в предельном статистическом случае стремится к нулю по закону ![]() . Несложно получить и вид распределения по числу частиц. Выполняя ту же последовательность действий, что и в предыдущей теме для получения распределения по энергии
. Несложно получить и вид распределения по числу частиц. Выполняя ту же последовательность действий, что и в предыдущей теме для получения распределения по энергии ![]() , приходим к следующему распределению:
, приходим к следующему распределению:
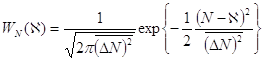 (7.13)
(7.13)
Легко видеть, что (7.13) с математической точки зрения представляет распределение Гаусса с математическим ожиданием ![]() и дисперсией
и дисперсией ![]() .
.
Кроме того, большое математическое распределение может быть использовано для определения дисперсии энергии ![]() . Используя соотношение
. Используя соотношение ![]() , проводя непосредственные вычислении и учитывая (6.19), в итоге получим:
, проводя непосредственные вычислении и учитывая (6.19), в итоге получим:
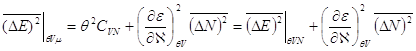 (7.14)
(7.14)
2.Введеный в предыдущем вопросе большой канонический формализм Гиббса представляет собой замкнутый аппарат равновесной статистической механики.
Запишем алгоритм проведения конкретных расчетов с использованием большого канонического распределения:
1. Ищется решение уравнения Шредингера для каждого значения N в пределах ![]() :
:
![]() (7.15)
(7.15)
2. Осуществляется вычисление в главной по V (или по ![]() ) асимптотике большой кинетической суммы:
) асимптотике большой кинетической суммы:
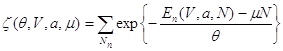 (7.16)
(7.16)
Зная явный вид выражения (7.16), могут быть вычислены термодинамический потенциал “омега” и все термодинамические характеристики системы:
![]()
![]()
![]() и т.д.
и т.д.
Заметим, что все термодинамические характеристики задаются в переменных (![]() ).
).
Кроме того, может быть найдено большое каноническое распределение
![]()
Это распределение позволяет рассчитать средние значения любых динамических величин, дисперсии флуктуации (при фиксированных ![]() ) и т.д.
) и т.д.
В случае необходимости, которая, как правило, возникает, производится пересчет полученных результатов от переменных (![]() ) к переменным (
) к переменным (![]() ), который производится на термодинамическом уровне. Уравнение
), который производится на термодинамическом уровне. Уравнение
![]()
разрешается относительно ![]() .
.
Это позволяет исключить ![]() из результатов, полученных в пункте 2. Например,
из результатов, полученных в пункте 2. Например,
![]()
Заметим, что процедура пересчета результатов в других переменных может быть осуществлено и при вычислении статистических сумм.
3.Подведем итог полученным результатам в соответствии с различными способами выделения термодинамической системы из окружения. То есть фактически приведем общую структуру равновесной статистической механики, которая нами была построена, применительно к различным способам термодинамического описания систем многих частиц:
1) Система с адиабатическими стенками. В этом случае фиксируются параметры (![]() ). Функция распределения Wn, определяющая структуру смешанного состояния, выражается при помощи микроканонического распределения Гиббса:
). Функция распределения Wn, определяющая структуру смешанного состояния, выражается при помощи микроканонического распределения Гиббса:
![]() ,
,
а аналитический вес
![]()
связан с макроскопической характеристикой – энтропией:
![]() ,
,
которая является термодинамическим потенциалом для переменных состояния (![]() ).
).
Такое представление имеет преимущественно общетеоретический интерес, поскольку на его основе четко просматриваются основные постулаты и ограничения. На основе которых осуществляется построение статистической механики.
2) Система в термостате, ![]() - состояние задается параметрами (
- состояние задается параметрами (![]() ). Функция распределения Wn задается каноническим распределением Гиббса:
). Функция распределения Wn задается каноническим распределением Гиббса:
![]()
Статистическая сумма
![]()
связана с макроскопическим параметром – свободной энергией
![]() ,
,
являющейся термодинамическим потенциалом в переменных (![]() ).
).
3) Система, выделенная с помощью воображаемых стенок. Выбранный способ описания очень удобен и широко используется, особенно в статистической механике классических систем. В этом случае фиксированными оказываются параметры (![]() ), а число частиц N оказывается микроскопическим параметром. В этом случае функция распределения
), а число частиц N оказывается микроскопическим параметром. В этом случае функция распределения ![]() вводится с помощью большого канонического распределения Гиббса:
вводится с помощью большого канонического распределения Гиббса:
![]()
Для выбранного способа описания связь с макроскопическими характеристиками системы осуществляется посредством большой статистической суммы:
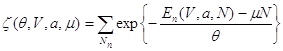
Соответствующим термодинамическим потенциалом является потенциал ![]() :
:
![]() ,
,
который и является термодинамическим потенциалом для системы с воображаемыми стенками.
Этот способ описания также широко используется. Наиболее удобным оказалось использование этого способа в квантовой статистической механике. Относительное неудобство большого канонического формализма связано с часто возникающей необходимостью пересчета результатов к более удобным параметрам (![]() ).
).
4) Система под поршнем. В этом случае фиксируются параметры (![]() ), а объем V рассматривается в качестве микроскопического параметра. Тогда функция распределения
), а объем V рассматривается в качестве микроскопического параметра. Тогда функция распределения ![]() , задающая структуру смешанного состояния, имеет вид:
, задающая структуру смешанного состояния, имеет вид:
![]()
Здесь ![]() - “гибсовская” статистическая сумма, равная:
- “гибсовская” статистическая сумма, равная:
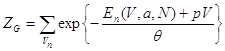
и связанная с термодинамическим потенциалом Гиббса:
![]() ,
,
характеризующим систему, заданную в переменных (![]() ).
).
Этот подход также оказывается удобным при рассмотрении некоторых частных задач.
В случае необходимости состояние термодинамической системы может быть описано и с помощью другого набора параметров. Тогда необходимо ввести соответствующие функции распределения и статистические суммы, связав последние с соответствующим термодинамическим потенциалом. Выбор конкретного способа описания не влияет на окончательный результат, однако способен существенно упростить или усложнить процесс исследования термодинамической системы. Это относится как к точным, так и к приближенным методам.
Похожие работы
... 4. Каноническое распределение по уровням. Набором квантовых состояний – уровней определяется любого коллектива целиком определяется его полная статистическая сумма состояний и его свободная энергия (4.1) Канонический ансамбль состояний описывает реальную изотермическую систему при постоянной температуре. Коллектив - система может быть макроскопическим, и должен состоять из огромного числа ...
... с кислородом, восстановлением - отнятие кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций было распространено на реакции, в которых кислород не участвует. В неорганической химии окислительно-восстановительные реакции (ОВР) формально могут рассматриваться как перемещение электронов от атома одного реагента (восстановителя) к атому другого ( ...
... определенный с точностью до постоянного компонента объем слоя 6N-мерного фазового пространства (p,q), заключенного между энергетическими гиперповерхностями и . Несмотря на эквивалентность всех формализмов равновесной статистической механики, наибольшее распространение в классической теории получило каноническое распределение Гиббса и статистический интеграл . Это связано с удобством ...
... вклад энергии стабилизации радикала CH3CH2C· H2Y, образующегося в результате присоединения метильного радикала к мономеру CH2=CHY, в энтальпию этой реакции. Таблица 1. Энтальпия, энтропия и энергия Гиббса присоединения атомов и радикалов X·к этилену. X· -DH, кДж моль-1 -DS, Дж моль-1 К-1 -DG (298 K), кДж моль-1 H· 150 84 125 Cl· 82 88 56 C· H3 100 ...


0 комментариев