Навигация
Антиоксидантная система плазмы крови в норме и при патологии
ФЕДЕРАЛЬНОЕ АГЕНСТВО ПО ОБРАЗОВАНИЮ
СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ
Институт фундаментальной биологии и биотехнологии
Кафедра биохимии и физиологии человека и животных
О.А. Голубев
Студент 3 курса
Антиоксидантная система плазмы крови в норме и при патологии
(Курсовая работа)
Научные руководители:
канд. биол. наук
Титова Н.М. ____________
док. мед. наук
Черданцев Д.В.____________
Красноярск 2008
Содержание
Глава 1. Обзор литературы.. 5
1.1. Активные формы кислорода и оксидативная модификация макромолекул: польза, вред и защита. 5
1.2. Характеристика антиоксидантной системы организма. 7
1.2.1. Неферментативная антиоксидантная система………………………...8
1.2.2. Ферментативная антиоксидантная система…………………………..
1.3. Антиоксиданты плазмы крови. 17
Глава 2. Материалы и методы.. 21
2.1. Объект исследования. 21
2.2. Методика определения церулоплазмина……………………………….21
2.3 Статистическая обработка результатов. 22
Глава 3. Результаты исследований и их обсуждение…………………………23
ВЫВОДЫ.. 25
ЛИТЕРАТУРА.. 26
Приложение. 28
Введение
Человек в покое вдыхает около 280 мл О2 /мин, или не менее 400 л/сут, что соответствует 18 молям О2 . Основное количество О2 (95-98%) расходуется на выработку энергии и окислительный катаболизм субстратов. Относительно небольшая часть (2-5%) переходит в активные формы кислорода (АФК) [1, 2] и затем частично используется для оксидативной модификации (ОМ) макромолекул. Это означает, что в АФК переходит ~ 0,4-0,9 моля О2 . При отсутствии метаболизма средняя концентрация АФК в организме достигла бы 6-14 мМ. Однако реальный уровень в тканях равен 10- 8 М, то есть в 106 раз меньше [2].
Возникают вопросы: 1) какое значение имеют АФК и ОМ макромолекул – это просто утечка с главного пути использования О2 или важные процессы, но тогда они полезны или вредны; 2) как осуществляется мощный метаболизм АФК и активных окисленных молекул и почему это нужно?
Целью данной работы было изучение изменения активности церулоплазмина плазмы крови у больных эндемическим зобом для выяснения возможной взаимосвязи антиоксидантной функции данного энзима с болезнью.
В задачи работы входило:
1) анализ литературы по изучаемому вопросу;
2) отработка методики определения содержания церулоплазмина;
3) изучение содержания церулоплазмина в плазме крови людей, больных эндемическим зобом.
Данная работа выполнялась на базе кафедры биохимии и физиологии человека и животных Института фундаментальной биологии и биотехнологии Сибирского федерального университета и кафедры хирургических болезней №2 с курсом сердечно-сосудистой хирургии им. А.М. Дыхно Красноярской государственной медицинской академии и является частью комплексных исследований состояния АОС в норме и при различных патологических состояниях.
ГЛАВА 1. ОБЗОР ЛИТЕРАТУРЫ 1.1. Активные формы кислорода и оксидативная модификация макромолекул: польза, вред и защита Кроме полного четырехэлектронного восстановления молекулы О2 до воды в дыхательной цепи митохондрий в аэробных клетках всегда происходит и неполное – одно-трехэлектронное восстановление с последовательным образованием различных АФК, к которым относятся свободный радикал-анион супероксид, перекись водорода Н2О2 и наиболее активный радикал – гидроксил НОJ (реакции (1)): Донорами электрона могут быть Fe2 +, Сu+ или семихиноны, а для второй и третьей реакций – также и :H2O2 + Fe2 + HO- + HOJ + Fe3 +
Термин «АФК» шире, чем «свободные радикалы кислорода» (НОJ), так как кроме последних включает также молекулы Н2О2 , синглетный кислород О2 , озон О3 и гипохлорит HOCl.
АФК генерируются во всех частях клетки. Наибольший вклад вносит дыхательная цепь митохондрий, особенно при низкой концентрации АДФ. Важна роль и системы цитохрома Р-450, локализованной в эндоплазматической сети. Участвуют ядерная мембрана и другие части клетки, при этом АФК часто возникают не только спонтанно, но и ферментативно (НАДФН-оксидаза дыхательного взрыва в плазматической мембране и ксантиноксидаза в гиалоплазме). Концентрации АФК в тканях невысоки: Н2О2 – 10- 8 М, – 10-11 М, НОJ < 10-11 М. АФК вызывают образование органических гидропероксидов ROOH – ДНК, белков, липидов, а также малых молекул [1, 3]. ROOH образуются и в реакции с обычным молекулярным О2 при участии ферментов диоксигеназ (реакция (4)) или циклооксигеназ:
RH + O2 ROOH
ROOH по своей структуре подобны Н2О2 (R-O–O-H и Н-О-О-Н) и химически тоже активны, при последующем метаболизме они переходят в спирты, альдегиды, эпоксиды и другие окисленные соединения. Образование ROOH называют перекисным окислением (пероксидацией), а совокупность описанных реакций (рис. 1) теперь именуют ОМ молекул.
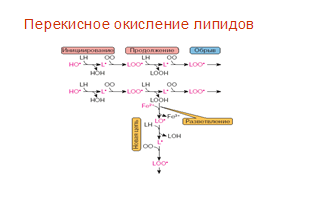
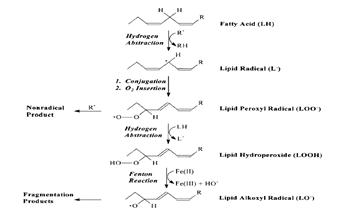
АФК вызывают в липидах (L), в основном в остатках полиненасыщенных жирных кислот, цепные реакции с накоплением липидных радикалов LJ, пероксилов LOOJ, гидропероксидов LOOH и алкоксилов LOJ:
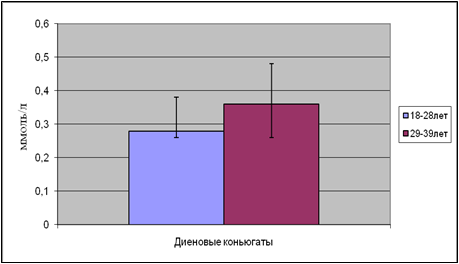
Первые три реакции – это инициация и продолжение цепи, а реакция LOOH c Fe2+ создает ее разветвление. Далее образуются диеновые конъюгаты, а затем минорные метаболиты: малоновый диальдегид, этан, пентан и др. [1, 3]. На протяжении многих лет перекисное окисление липидов (ПОЛ) считали преимущественно спонтанным (неферментативным) и неспецифическим самоускоряющимся процессом и ему придавали ведущее значение в ОМ и ее последствиях. Однако затем стало ясно, что: 1) огромное значение имеют и ферментативные реакции типа (4), катализируемые липоксигеназами [4] и циклооксигеназами – первыми ферментами путей, приводящих к образованию специфических регуляторов – эйкозаноидов [5-7]; 2) в организме главными продуктами ПОЛ являются 4-гидроксиалкенали типа С5Н9-СНОН-СН=СН-СНО, то есть снова специфические вещества; 3) большое значение имеет ОМ и других макромолекул – ДНК и белков, усиленно изучаемая в 90-е годы [8, 9].
АФК вызывают ОМ нуклеотидов и нуклеиновых кислот, особенно ДНК. Это приводит к гидропероксидам ROOH (так, из _емма_ образуется 5-СН2ООН-урацил), а затем к гидроксипроизводным ROH или R(OH)2 , основными из которых являются 8-ОН-2'-дезоксигуанозин и тимингликоль (их определение в тканях и моче используют как индексы ОМ ДНК) [8]. ОМ белков также вызывает образование в организме ROOH, а затем ROH (o- и m-тирозины), R(OH)2 (ДОФА), карбонилов и других окисленных производных; образуются и димеры (дитирозины); происходит также аутооксидативное гликозилирование белков [9].
1.2. ХАРАКТЕРИСТИКА АНТИОКСИДАНТНОЙ СИСТЕМЫ ОРГАНИЗМААнтиоксидантная система (АОС) включает:
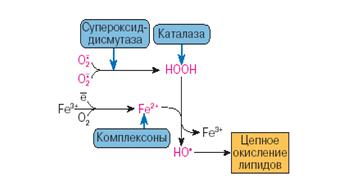
1. Энзиматические перехватчики, такие как супероксиддисмутазу (СОД), дисмутирующую О2- до Н2О2, каталазу и глутатионпероксидазу (ГПО), которые конвертируют Н2О2 до воды. ГПО и глутатион-S-трансфераза (ГSТ) участвуют в детоксикации гидропероксидов жирных кислот;
2. Гидрофильные скэвенджеры радикалов – восстановленный глутатион (ГSН), аскорбат, урат, тиолы (цистеин, эрготионеин);
3. Липофильные перехватчики радикалов – токоферолы, флавоноиды, каротиноиды, убихиноны, билирубин.;
4. Ферменты, осуществляющие восстановление окисленных низкомолекулярных биоантиоксидантов (глутатионредуктаза) или участвующие в поддержании в функционально активном состоянии белковых тиолов (тиоредоксинредуктаза);
5. Ферменты ,участвующие в поддержании внутриклеточного стационарного уровня восстановительных эквивалентов (глюкозо-6-фосфатдегидрогеназа, катализирующая образование НАДФН в пентозофосфатном пути окисления глюкозы);
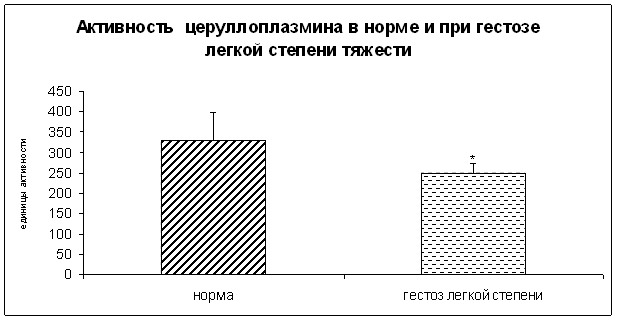
6. Антиоксидантные белки (церулоплазмин, альбумин, ферритин, трансферрин, лактоферрин и др.), участвующие в хранении, транспорте или обезвреживании ионов металлов переменной валентности.
Клеточная АОС представлена семейством супероксиддисмутаз, глутатионпероксидаз и глутатион-S-трансфераз, а также глутатионредуктазой, найденных в цитоплазме, митохондриях и ядре. Каталаза локализована в пероксисомах и цитоплазме, а в такой высокодифференцированной и специализированной клетке, как эритроцит, существует в растворимой (в цитоплазме) и мембраносвязанной формах.
Состав низомолекулярных антиоксидантов достаточно обширен: восстановленный глутатион и аскорбиновая кислота находятся в водной фазе клетки, защищая компоненты цитозоля и матрикса митохондрий, токоферолы и каротиноиды – плазматическую и внутриклеточные мембраны.
АФК постоянно генерируются в водной фазе плазмы крови и других биологических жидкостей. О2- и Н2О2 могут образовываться ферментами активированных фагоцитирующих клеток, в продукцию О2- вовлечен и сосудистый энодотелий. Активированные нейтрофилы, кроме того, при участии миелопероксидазы генерируют внеклеточный гипохлорит [ ].
Похожие работы
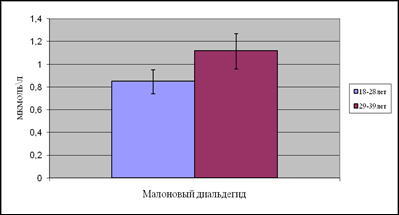
... находится на невысоком уровне, но при стрессовых ситуациях происходит усиленная активация процессов ПОЛ под действием АФК, что приводит к патологическому состоянию. 3.1. Содержание продуктов перекисного окисления липидов в плазме крови небеременных женщин. В данной работе было определено содержание диеновых коньюгатов и малонового диальдегида у небеременных женщин (N=31), которые составили ...
... Біології. Київ. – 2007. (Здобувач брала безпосередню участь дослідженні, аналізі експериментальних даних, написанні та оформленні тез). АНОТАЦІЯ Люта М.Я. Морфофункціональні та біохімічні особливості системи еритрону за умов цукрового діабету 1-го типу. – Рукопис. Дисертація на здобуття наукового ступеня кандидата біологічних наук за спеціальністю 03.00.11 – цитологія, клітинна біологія, ...
... узловым зобом. //Материалы V Российского Форума «Мать и Дитя», Москва,2003, 44–45 20. Габелова К.А., Арутюнян А.В., Зубжицкая Л.Б. Фиксированные иммунные комплексы и NO-синтетазная активность плаценты при гестозе // Вестн. Росс. Ассоц. акуш.-гин. – 2000. – №1. – С. 22-24. 21. Гармашева Н.Л., Константинова Н.Н. Патофизиологические основы охраны внутриутробного развития человека. Л.,1985.,159 ...
... среду [Менщикова, 2008]. 3.2. Анализ содержание GSH и активность глутатионзависимых ферментов в эритроцитах крови практически здоровых людей, проживающих в различных по уровню загрязнения районах г.Красноярска Город Красноярск административно разделен на 7 районов, различаемых по уровню техногенной нагрузки, которая определяется структурой промышленности и энергетики, исходного и ...
0 комментариев