Навигация
Второй способ изложен в [17]
2. Второй способ изложен в [17]
Для систем испарения:
m xi =(m-dm)( xi -dxi) + yi dm 1.25
m xi = m xi -m dxi- xi dm + dm dxi + yi dm
после отбрасывания бесконечно малых второго порядка имеем:
m dxi=( yi -xi)dm
![]() ; dt= dln m<0
; dt= dln m<0
Если же идет конденсация dm молей пара в жидкость, имеем:
yi dm + m xi = (m+dm)( xi +dxi) 1.26
или
yi dm + m xi = m xi + m dxi +xi dm + dm dxi
dm (yi - xi) = m dxi 1.27
![]() ; dt= dln m>0 1.28
; dt= dln m>0 1.28
Обоими методами мы получили один и тот же результат, а именно: если рассматривается изменение состояния жидкой фазы, используется нода, а не ренода.
Теперь рассмотрим изменение концентрации компонента i в паровой фазе, в зависимости от того, приходит ли dm молей состава xi из паровой фазы. Здесь также существует два метода вывода уравнений:
1. Для систем испарения:
xi dm= d(m yi) 1.29
xi dm= yi dm + m dyi 1.30
dm (xi- yi) = m dyi 1.31
или ![]() 1.32
1.32
2. Для систем конденсации:
m yi =(m-dm)( yi -dyi) + xi dm 1.33
m yi = m yi -m dyi- yi dm + dm dyi + xi dm
после отбрасывания бесконечно малых второго порядка имеем
m dyi=(xi -yi)dm 1.34
или ![]() , dt= dln m<0 1.35
, dt= dln m<0 1.35
Для систем смешения (с dt>0)
m yi + xi dm = (m+dm)( yi +dyi) 1.36
m yi + xi dm = m yi + m dyi-+ yi dm + dm dyi 1.37
dm (xi- yi ) = m dyi 1.38
![]() , dt= dln m>0 1.39
, dt= dln m>0 1.39
Второй метод более громоздок. Каждый вывод предусматривает dt>0 или dt<0.
Первый метод более универсален и лаконичен. Основной вывод заключается в том, что при исследовании изменения концентраций за счет добавления или удаления из данной фазы dm молей состава другой фазы, для жидкой фазы используется нода, а для паровой фазы - ренода. Это правило действует в случае балансовых соотношений.
1.7. Общие фазовые эффекты.
Общие фазовые эффекты отражают изменение химических потенциалов компонентов при изменении их концентрации за счет фазового обмена [1]. Рассмотрим m молей жидкой фазы и допустим, что пришло (или ушло) в нее dm молей состава паровой фазы. Как и прежде dt= dln m. Тогда при постоянном давлении и температуре имеет место:
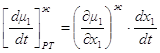 1.40
1.40
 1.41
1.41
но ![]() и
и ![]()
используя эти соотношения, из 1.40 и 1.41 получим:
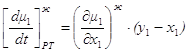 1.42
1.42
 1.43
1.43
Обозначив
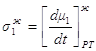 1.44
1.44
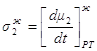 1.45
1.45
получим
 1.46
1.46
 1.47
1.47
Таким образом, при
y1>x1 , dt>0 dx1>0 ![]()
![]()
y2<x2 , dt>0 dx2<0 ![]()
Обычно говорят, что если фазовый эффект ![]() положителен, то компонент i «высаливается» из жидкой фазы, а если он отрицателен, то компонент i «всаливается» в жидкую фазу. Это означает, что при организации открытого равновесного испарения количество компонента 1 будет уменьшаться в жидкой фазе, а количество компонента 2 увеличиваться. Последнее понятно, так как уходящий пар будет обогащен легколетучим (первым) компонентом и обеднен тяжелолетучим (вторым) компонентом. Обратим внимание на тот факт, что в случае dt<0 (испарения при постоянных Р и Т) компоненты 1 и 2 меняются местами.
положителен, то компонент i «высаливается» из жидкой фазы, а если он отрицателен, то компонент i «всаливается» в жидкую фазу. Это означает, что при организации открытого равновесного испарения количество компонента 1 будет уменьшаться в жидкой фазе, а количество компонента 2 увеличиваться. Последнее понятно, так как уходящий пар будет обогащен легколетучим (первым) компонентом и обеднен тяжелолетучим (вторым) компонентом. Обратим внимание на тот факт, что в случае dt<0 (испарения при постоянных Р и Т) компоненты 1 и 2 меняются местами.
Перейдем к фазовым эффектам в паровой фазе.
Здесь
 1.48
1.48
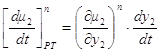 1.49
1.49
Но при приходе (или уходе) из паровой фазы dm молей состава жидкой фазы
![]()
![]()
Следовательно, из 1.48 и 1.49 окончательно получаем
 1.50
1.50
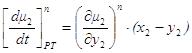 1.51
1.51
Следовательно, при
x1< y1, dt>0, dy1<0, ![]()
![]()
x2> y2, dt>0, dy2>0, ![]()
Таким образом, если ![]() положителен, то компонент i «высаливается» из паровой фазы. Таким компонентом является компонент 2, т.е. тяжелолетучий компонент. Если
положителен, то компонент i «высаливается» из паровой фазы. Таким компонентом является компонент 2, т.е. тяжелолетучий компонент. Если ![]() отрицателен, то компонент i «всаливается» в паровую фазу. Таким компонентом является первый компонент. Таким образом, если организовать процесс открытой равновесной конденсации, будет уходить из пара тяжелолетучий компонент, а количество легколетучего будет увеличиваться. Обобщая, получим, что компонент, который «высаливается» из жидкой фазы, «всаливается» в паровую фазу. А компонент, который «всаливается» в жидкую фазу, «высаливается» из паровой фазы.
отрицателен, то компонент i «всаливается» в паровую фазу. Таким компонентом является первый компонент. Таким образом, если организовать процесс открытой равновесной конденсации, будет уходить из пара тяжелолетучий компонент, а количество легколетучего будет увеличиваться. Обобщая, получим, что компонент, который «высаливается» из жидкой фазы, «всаливается» в паровую фазу. А компонент, который «всаливается» в жидкую фазу, «высаливается» из паровой фазы.
Запишем уравнение фазовых эффектов в жидкой фазе.
Так как сумма dx1+dx2=0, следовательно, dx1= -dx2 , а также у1-х1= -(у2-х2), получаем:
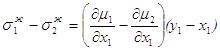
но ![]()
![]() 1.52
1.52
Аналогично можно получить
![]() 1.53
1.53
Таким образом, были получены общие фазовые эффекты. В случае азеотропных смесей при y1 = x1 очевидно σ1 – σ2 = 0, при этом σ1 = 0 и σ2 = 0. Таким образом, в случае азеотропных смесей общие фазовые эффекты равны нулю, в отличие от зеотропных смесей, где они отличаются от нуля.
1.8. Цель работы
Получение и анализ новой формы уравнения Ван-дер-Ваальса на примере азеотропных смесей с использованием общих и частных фазовых эффектов.
2. Частные фазовые эффекты и вывод уравнения Ван-дер-Ваальса.
2.1. Вывод основных уравнений для частных фазовых эффектов жидкой и паровой фаз при постоянной температуре и давлении.
Проведем вывод, используя диаграммы зеотропных смесей. На рис. 2.1 представлена зависимость V – x, y из [18]
Любой материальный баланс линеен, в том смысле, что участвующие в нем два потока разных составов лежат на одной прямой с потоком, из которого они образованы.
В случае, когда температура постоянна, а давление является функцией состава, вектор ![]() направлен вдоль прямой, образующей которой служит вектор коннода (или реконнода). Таким образом, эти векторы, один из которых бесконечно мал, лежат на одной прямой. Если снести эти векторы на отрезок (концентрационный симплекс), то получим вектор ноду
направлен вдоль прямой, образующей которой служит вектор коннода (или реконнода). Таким образом, эти векторы, один из которых бесконечно мал, лежат на одной прямой. Если снести эти векторы на отрезок (концентрационный симплекс), то получим вектор ноду ![]() и вектор смещения состава
и вектор смещения состава ![]() , эти векторы и должны лежать на одной прямой. Смещение состава может быть вызвано или уходом из m молей жидкости dm молей пара, или приходом dm молей пара в жидкость. Договоримся, в первом случае dm имеет знак минус, а во втором знак плюс. Если рассмотреть проекции вектора ноды на ось х1, y1, то получим: для легколетучего компонента y1>x1. Таким образом, в случае ухода dm молей пара из жидкости векторы
, эти векторы и должны лежать на одной прямой. Смещение состава может быть вызвано или уходом из m молей жидкости dm молей пара, или приходом dm молей пара в жидкость. Договоримся, в первом случае dm имеет знак минус, а во втором знак плюс. Если рассмотреть проекции вектора ноды на ось х1, y1, то получим: для легколетучего компонента y1>x1. Таким образом, в случае ухода dm молей пара из жидкости векторы ![]() и
и ![]() будут направлены противоположно друг другу. Геометрически эти векторы выглядят так (рис 2.2):
будут направлены противоположно друг другу. Геометрически эти векторы выглядят так (рис 2.2):
Приход или уход dm молей из жидкости приводит к изменению, как её состава, так и её количества. С одной стороны бесконечно малое количество ушедшего или пришедшего в жидкость вещества (компонента i) равно d(mxi).
С другой стороны это же количество можно выразить как yi dm.
Очевидно
d(mxi)= yi dm
xi dm + m dxi= yi dm 2.1
m dxi=( yi - xi) dm
![]() , где dt=dlnm
, где dt=dlnm
Очевидно, если dt>0, то dlnm>0 и вещество приходит в жидкую фазу, если dt<0, то dlnm<0 и вещество уходит из жидкой фазы. Физический смысл здесь ясен: если dt>0 количество жидкости увеличивается, а если dt<0 - уменьшается. Если индекс i равен 1, т.е. компонент легколетучий, имеем:
y1> x1 dt<0 , то dх1<0 или
y1> x1 dt>0 , то dх1>0
Таким образом, для легколетучего компонента, согласно физическому смыслу, если уходит dm молей состава пара, то уменьшается концентрация компонента 1 в жидкости, а если приходит, то увеличивается.
Если же i=2
y2< x2 dt<0 , то dх2>0
y2< x2 dt>0 , то dх2<0
Для тяжелолетучего компонента, если уходит dm молей состава пара, то концентрация компонента 2 увеличивается в жидкости, а если приходит, то уменьшается.
Вместе с тем, вектор ![]() направлен противоположно вектору ноде
направлен противоположно вектору ноде ![]() , если dm молей уходит из жидкости и имеет тоже направление, если dm молей приходит в жидкую фазу. Это видно из уравнения 2.2
, если dm молей уходит из жидкости и имеет тоже направление, если dm молей приходит в жидкую фазу. Это видно из уравнения 2.2
![]() 2.2
2.2
В обоих случаях векторы колинеарны, т.е. лежат на одной прямой, а их направления определяются знаком dt, как скалярного множителя (бесконечно малого).
Возвращаясь к диаграмме (рис.2.1), в случае постоянной температуры и переменного давления, вектор ![]() лежит на одной прямой с вектором, который имеет координаты
лежит на одной прямой с вектором, который имеет координаты ![]() , что и показано на рисунке. Если же рассматривается этот же состав х1, имеющий объем Vж, то при постоянных давлении и температуры, направление вектора
, что и показано на рисунке. Если же рассматривается этот же состав х1, имеющий объем Vж, то при постоянных давлении и температуры, направление вектора ![]() должно совпадать с направлением изотермо-изобары жидкой фазы. Следовательно, этот вектор не колинеарен вектору
должно совпадать с направлением изотермо-изобары жидкой фазы. Следовательно, этот вектор не колинеарен вектору ![]() . Образно говоря, движущая сила этого смещения состава, другая. Эта движущая сила должна лежать на касательной к изотермо-изобаре жидкости, т.е. проекция на ось абсцисс х, у остается при этом неизменной, а изменяется проекция на ось ординат V. Таким образом, векторы
. Образно говоря, движущая сила этого смещения состава, другая. Эта движущая сила должна лежать на касательной к изотермо-изобаре жидкости, т.е. проекция на ось абсцисс х, у остается при этом неизменной, а изменяется проекция на ось ординат V. Таким образом, векторы ![]() и
и ![]() имеют разное направление, т.е. смещены друг относительно друга на угол β.
имеют разное направление, т.е. смещены друг относительно друга на угол β.
Таким образом, величина, определяющая вектор![]() находится по определенной методике:
находится по определенной методике:
1. Проводим касательную к изотермо-изобаре жидкости в точке с координатами х1, Vж.
2. Пересечение этой прямой с прямой у1=const, дает вторую точку вектора (А).
3. Следовательно, вектор равен (см. рис. 2.1)

Начальной точкой этого вектора является точка с координатами х1, Vж. Конечной точкой является точка А. В самом деле, если рассматривается коннода жидкость-пар (рис.2.3), то её координаты равны ![]()
Полученные результаты находятся в полном соответствии с физико-химическим смыслом. В самом деле, при dt<0 часть веществ уходит из жидкой фазы при постоянном давлении и температуре, следовательно, объем жидкой фазы уменьшается. При приходе dm молей в жидкую фазу объем жидкой фазы, в общем, увеличивается.
Таим образом, для азеотропных смесей частные фазовые эффекты жидкой фазы противоположны по знаку частным фазовым эффектам паровой фазы. В отличие от общих они не равны нулю в азеотропных точках.
2.2.Вывод уравнений Ван-дер-Ваальса для жидкой и паровой фаз.
Уравнение Ван-дер-Ваальса является представлением разности нулевых потенциалов Гиббса в координатах g-потенциала [14].
Напомним, что для жидкой фазы нулевой потенциал для бинарной смеси обычно записывается в форме [14]
Sж dT –Vж dР+ x1 dμ1 + x2 dμ2=0 2.7
g-потенциал, соответственно, равен
dgж= -Sж dT +Vж dР+ μ1dх1+ μ2 dх2 2.8
Аналогично для паровой фазы имеем
Sп dT –Vп dР+ у1 dμ1 + у2 dμ2=0 2.9
dgп= -Sп dT +Vп dР+ μ1dу1+ μ2 dу2 2.10
В работе [14] дан вывод нулевого потенциала. Приведем его полностью. Для случая бинарной смеси уравнение внутренней энергии имеет вид:
U= TS-PV+ μ1x1+ μ2x2 2.11
После дифференцирования получаем
dU= TdS + SdT – PdV – VdP + μ1 dx1 + x1dμ1 + μ2 dx2 + x2dμ2 2.12
Но так как
dU= TdS - PdV+ μ1 dx1 + μ2 dx2 2.13
то очевидно
SdT-VdP+ x1dμ1+ x2dμ2 =0 2.14 Если применять почленно преобразование Лежандра, то, учитывая, что при этом меняется в каждом случае знак, получим
-SdT+VdP- x1dμ1- x2dμ2 =0 2.15
Автор [14] не видит разницы между уравнениями в форме 2.14 и 2.15, поэтому приводит уравнение 2.15, очевидно считая, что если правая часть равна нулю, то обе формы идентичны.
Как уже говорилось, нулевой потенциал есть скалярное произведение вектора
< S, V, x1, x2 >
на вектор < dT, dP, dμ1, dμ2 >
Учитывая, что это скалярное произведение равно нулю, векторы-сомножители ортогональны друг другу.
Так как, вектор < dT, dP, dμ1, dμ2 > есть вектор параметров, которые могут изменяться независимо, очевидно вектор < S, V, x1, x2 > может быть представлен двояко < S, -V, x1, x2 > или <- S, V, -x1, - x2 >
![]() Оба представления получаются равнозначными, так как эти векторы ортогональны. Проиллюстрируем это при условии Р=соnst. В этом случае имеем
Оба представления получаются равнозначными, так как эти векторы ортогональны. Проиллюстрируем это при условии Р=соnst. В этом случае имеем
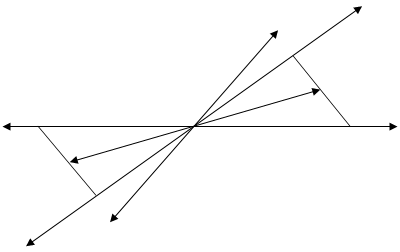 < S, x1, x2 > и <- S, -x1, - x2 > S
< S, x1, x2 > и <- S, -x1, - x2 > S
S х1 х2 х1
х
-х2 х2
-х
-S -х1 -х2
-х1
- S
Рис.2.10. Взаимное расположение вектора состава
То есть, в случае перемены знаков произведение знака не меняет, если давление постоянно.
Выведем уравнение Ван-дер-Ваальса для жидкой фазы. Исходим из того, что в этом случае начальная точка вектора конноды при Р=соnst будет точка, соответствующая свойствам жидкой фазы. В связи с этим правилом запишем уравнения 2.14 для паровой и жидкой фаз при Р=соnst:
Sп dT + у1 dμ1 + у2 dμ2=0 2.16
Sж dT + x1 dμ1 + x2 dμ2=0 2.17
Отнимем от первого уравнение второе и получим:
(Sп- Sж) dT + (у1- х1)dμ1 +(у2- x2)dμ2=0 2.18
Таким образом, мы, получим произведение конноды жидкость-пар < Sп- Sж, у1- х1, у2- x2> на вектор параметров < dT, dμ1, dμ2 >, которые в условиях термодинамического равновесия одинаковы, как в жидкой, так и в паровой фазах.
Так как х1+х2=1 и у1+у2=1, то очевидно
у1- х1+ у2- x2=0
т.е. у2- x2= -(у1- х1) 2.19
Следовательно, с учетом 2.19
(Sп- Sж) dT + (у1- х1) (dμ1-dμ2)=0 2.20
В уравнении 2.20 dT и d(μ1-μ2) полные дифференциалы.
Для перехода к координатам функции g необходимо выразить d(μ1-μ2), как функции х1 и Т (Р=соnst)
d(μ1-μ2) =![]()
![]() 2.21
2.21
Подставляя в уравнение 2.20 значение d(μ1-μ2) из 2.21, получим
![]() 2.22
2.22
![]() можно представить в виде
можно представить в виде ![]() . В самом деле,
. В самом деле, ![]() ,
, ![]() . Но
. Но ![]() согласно соотношению Максвелла (смешанные производные не зависят от порядка дифференцирования).
согласно соотношению Максвелла (смешанные производные не зависят от порядка дифференцирования).
В связи с этим  2.23
2.23
 2.24
2.24
Таким образом, с учетом 2.23 и 2.24 окончательно получим
- 2.25
2.25
Аналогично можно получить для жидкой фазы уравнение при постоянной температуре и переменном давлении
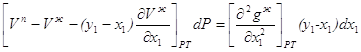 2.26
2.26
Учитывая, что нода для двухкомпонентной смеси определяется разностью концентраций одного из компонентов, уравнения 2.25 и 2.26 можно записать в форме
![]() 2.27
2.27
и
![]() 2.28
2.28
Отметим, что так как в азеотропных смесях коннода вертикальна, нода вырождается в точку.
Похожие работы
... С целью увеличения выхода и упрощения технологии процесса за счет исключения стадии щелочной промывки из процесса осушки 1,3-диоксолана и повышения экологической чистоты технологии разделения азеотропной смеси 1,3-диоксолан-вода, проводят экстрактивную ректификацию с использованием в качестве экстрагента этиленгликоль. Предлагаемое изобретение может быть использовано для получения 1,3-диоксолана, ...
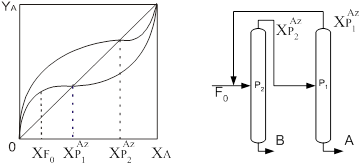
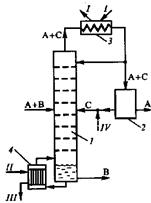
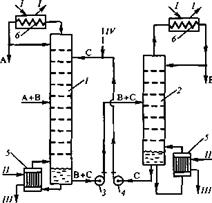
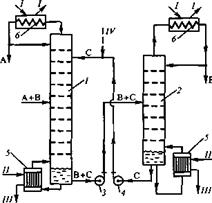
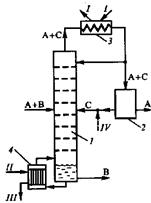
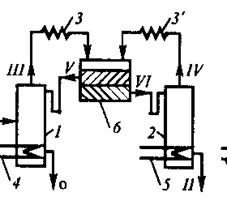
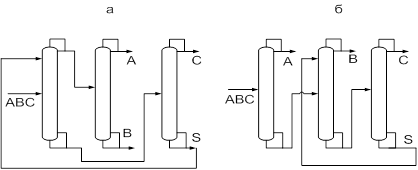
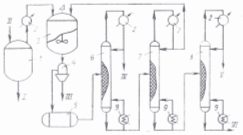
... смеси на четыре продукта [17]. I – IV — продукты. 2. ПОСТАНОВКА ЗАДАЧИ ИССЛЕДОВАНИЯ. Целью настоящей работы является определение оптимальных рабочих параметров процесса экстрактивной ректификации смеси ацетон-хлороформ азеотропного состава в сложной колонне с боковой укрепляющей секцией. К таким параметрам относятся температура и расход разделяющего агента, тарелки подачи исходной смеси и ...
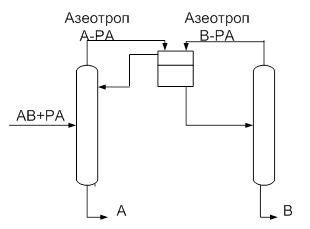
... резкое изменение температуры, обусловленное скачкообразным изменением концентрации РА. [12] Постановка задачи Целью данной работы является поиск оптимальной схемы экстрактивной ректификации смеси бензол-циклогексан-этилбензол-н-пропилбензол, содержащей один бинарный азеотроп. Для этого необходимо выполнить: · параметрическую оптимизацию традиционных схем экстрактивной ректификации; · ...
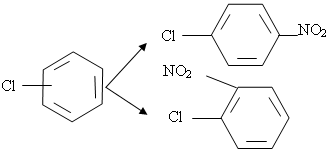
... 8,6961 6,6957 9,9694 - Энергозатраты по схемам ГДЖ/ч 10,0379 15,3918 9,9624 7. Выводы В результате проделанной работы решена задача разделения промышленной смеси продуктов синтеза хлорбензола. В качестве модели наиболее адекватно описывающей парожидкостное равновесие смеси была выбрана модель UNIFAC. Были синтезированы две схемы, состоящие из двух простых двухсекционных колонн ...

0 комментариев