Навигация
1.2.2 Классификация анионов
Аналитические классификации анионов основаны на их окислительно-восстановительных свойствах, способности образовывать с катионами малорастворимые соединения, а также на реакциях взаимодействия некоторых с кислотами, сопровождающихся выделением газообразных продуктов. В отличие от катионов, единой общепринятой классификации анионов, учитывающей все эти свойства, не существует.
Классификация анионов, основанная на реакциях осаждения
| Группа | Анионы | Групповой признак | Групповой реагент |
| I | SO42-, SO32-, S2O32-, CO32-, C2O42-, PO43-, SiO32-, Cr2O72-, CrO42-, F-, B2O72-, AsO33-, AsO43- | Соли бария и серебра не растворимы в воде, но растворимы в HCl и HNO3 (за исключением BaSO4) | BaCl2 в нейтральной или слабощелочной среде |
| II | S2-, Cl-, Br-, I-, SCN-, CN-, IO3-, BrO3- | Соли бария растворимы, а соли серебра не растворяются в воде и разбавленной HNO3 (кроме BrO3-) | AgNO3 в азотнокислой среде |
| III | NO3-, NO2-, CH3COO-, MnO4- | Соли бария и серебра растворимы в воде | Отсутствует |
Классификация анионов, основанная на их окислительно-восстановительных свойствах
| Группа | Анионы | Групповой признак | Групповой реагент |
| I | NO2-, Cr2O72-, AsO43-, BrO3- | Окислители: выделение свободного йода | KI + H2SO4 |
| NO3-, Cr2O72-, NO2-, MnO4- | Окислители: выделение MnCl62- бурого цвета | MnCl2 + HCl(к) | |
| II | SO32-, S2-, S2O32-, NO2-, C2O42-, Cl-, Br-, I-, SCN-, CN-, AsO33- | Восстановители: обесцвечивание раствора перманганата калия с образованием Mn2+ | KMnO4 + H2SO4 |
| SO32-, S2-, S2O32-, AsO33- | Восстановители: восстановление I2 до I2-, исчезновение синей окраски иодкрахмального комплекса | I2 в KI, подкислён. H2SO4 | |
| III | SO42-, CO32-, PO43-, SiO32-, B2O72-, CH3COO- | Индифферентные | Отсутствует |
Глава 2. Качественный анализ
2.1 Обнаружение катионов
Анализ смеси, состоящей из трёх неизвестных катионов, начали с проведения предварительных испытаний.
Изучили внешний вид исследуемой смеси. Она состояла из тёмно-зелёных, бесцветных и белых кристаллов. Тёмно-зелёные кристаллы указывают на возможное присутствие катионов хрома. Отсутствие розовых, синих и буро-жёлтых кристаллов говорит об отсутствии соответственно ионов Co2+, Cu2+ и Fe3+.
Измельчили смесь в фарфоровой ступке. Приготовили водную вытяжку: для этого часть исследуемой смеси растворили в воде при нагревании и тщательном перемешивании. При этом небольшое количество вещества осталось в осадке, что свидетельствует о наличии малорастворимого соединения. Также отсутствие в водной вытяжке студенистого осадка указывает на отсутствие в смеси легко гидролизующихся солей Sb3+ и Bi3+.
Провели дробный анализ. Проверили наличие ионов Cr3+: для этого к исследуемому раствору добавили 2М раствор NaOH и 3% Н2О2 и нагрели. Изменение зелёной окраски раствора (цвет аквакомплексов [Cr(H2O)6]3+) на жёлтую (цвет хромат-ионов CrO42-) говорит о присутствии в исследуемой смеси ионов Cr3+.
2[Cr(H2O)6]3+ + 3Н2О2 = 2CrO42- + 6SO42- + 14H+
Проверили наличие ионов Fe2+: к исследуемому раствору прилили раствор красной кровяной соли K3[Fe(CN)6]. Синий осадок не выпал, значит, отсутствуют ионы Fe2+.
Проверили наличие ионов Ni2+ : к анализируемому раствору прилили NH4OH (без избытка), амиловый спирт и диметилглиоксим (реактив Чугаева). Отсутствие малиновой окраски в слое органического растворителя говорит об отсутствии ионов Ni2+.
Проверили содержание в исследуемом растворе ионов аммония NH4+: к раствору прилили избыток щёлочи для растворения выпавших гидроокисей тяжёлых металлов и добавили избыток реактива Несслера (смесь раствора тетраиодомеркурата(II) калия K2[HgI4] с 2н КОН). Образовался красно-бурый осадок иодида меркураммония:
NH4+ + 2[HgI4]2- + 2ОН- = [OHg2NH2]I↓ + 7I- + 3H2O
Cостав осадка описывается формулой:
Провели систематический анализ. К исследуемому раствору добавили этиловый спирт и 2н HCl. Отсутствие осадка свидетельствует об отсутствии катионов I аналитической группы.
К анализируемой водной вытяжке прилили этиловый спирт и 2н H2SO4. осадок не выпал, значит, отсутствуют катионы II аналитической группы.
К исследуемому раствору добавили перекись водорода и 6н NaOH до полного осаждения, затем избыток щёлочи и нагрели при тщательном перемешивании стеклянной палочкой. Прокипятили на водяной бане для удаления избытка перекиси водорода. При этом катионы III аналитической группы остались в растворе, а катионы IV – V группы должны были выпасть в осадок, но этого не произошло, значит, в исследуемом растворе нет катионов IV – V группы.
Находящиеся в полученном растворе ионы CrO42- мешают открытию остальных катионов III аналитической группы, потому для открытия ионов Al3+ провели удаление этих ионов: к раствору добавили сухую соль NH4Cl и прокипятили до полного удаления аммиака (проба со влажной лакмусовой бумажкой). При этом в осадок выпали гидроксиды возможно содержащихся в растворе Al3+ и Sn2+, а в растворе остались ионы CrO42- и,возможно, ионы ZnO22-. Осадок отделили центрифугированием, промыли дистиллированной водой, растворили в 2н HCl и проверили наличие в этом растворе ионов Al3+ : к раствору прилили 2н NH4OH до рН = 10-11 и ализарин (1,2 – диоксиантрахинон). Выпал красный осадок «алюминиевого лака», значит, в исследуемом растворе содержались ионы Al3+.
Al(OH)3 + → + H2O
Дальнейший систематический анализ катионов не имеет смысла, так как открыты все находящиеся в анализируемом растворе катионы.
Похожие работы
... красного окрашивания раствора не наблюдаем, следовательно анион NO2-действительно в данной смеси отсутствует. Качественные реакции на анионы третьей аналитической группы Подтвердим присутствие в анализируемом веществе аниона NO3-. Проведем следующую реакцию: к нескольким каплям раствора неизвестного вещества прибавим 2-3 капли дефениламина и 5 капель концентрированной серной кислоты. Наблюдается ...
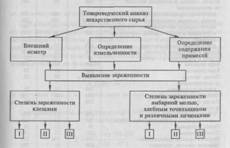
... и, конечно же, за многими другими, которые будут получены, — будущее. В этом направлении и работают многие НИИ и исследователи. Аспекты поиска новых лекарств, изыскание новых лекарственных веществ состоит из трех основных этапов: химический синтез, установление фармакологической активности и безвредности (токсичности). Такая стратегия поиска с большой затратой времени, реактивов, животных, труда ...
... (II) аммония. Cd2+-+ [Hg(SCN)4]2- -> Cd[Hg(SCN)4] ()бразование бесцветных продолговатых кристаллов тетрароданомеркурата кадмия Аналитически реакции катионов VI аналитической группы по кислотно-основной классификации: Cu2+, Hg2+, Cd2+, Co2+, Ni2+ Групповой реагент – NH4OH в избытке Хотя элементы расположены в разных груупах периодической системы Д.Ию Менделеева, все эти катионы ...
... Глава II. Методики исследования загрязнения окружающей среды и оценки ее качества Для выполнения задач и достижения цели были разработаны нами методики исследования комплексной эколого-геохимической оценки урболандшафтов Волгоградской агломерации, которая заключается в исследовании почв, растительности, оценки выбросов промышленных предприятий и влияния ОС на здоровье человека. 2.1 ...
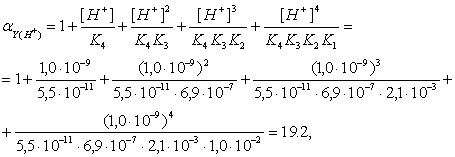
0 комментариев