Навигация
Анализы объектов на содержание хлорид-иона
3. Анализы объектов на содержание хлорид-иона
1 Определение массовой доли хлоридов в отложениях парового оборудования электростанций
Навеску отложений от 0,5 до 0,8 г, взвешенную на аналитических весах, помещают в химический стакан. Обрабатывают материал 20–30 см3 горячей дистиллированной воды, кислоты и отфильтровывают не растворившийся осадок на плотный беззольный фильтр, собирая фильтрат в мерную колбу вместимостью 100 или 250 см3. Осадок на фильтре промывают горячей дистиллированной водой, собирая промывные воды в ту же колбу. Промывание ведут до исчезновения в фильтрате положительной реакции на присутствие хлорид-иона (проба с AgNO3: несколько капель фильтрата смешивают с раствором, содержащим 1% AgNO3). Из мерной колбы, содержащей фильтрат отбирают пипеткой от 10 до 100 см3 жидкости в зависимости от предполагаемого содержания хлоридов в анализируемом материале.
Аликвоту осветлившегося раствора, отобранную пипеткой, помещают в коническую колбу, приливают 2 см3 концентрированной азотной кислоты и дистиллированной воды до общего объема примерно 100 см3. Затем вводят на кончике ножа несколько кристаллов нитропруссида натрия и три капли раствора метилоранжа. Кристаллы нитропруссида натрия растворяют и титруют окрашенную в оранжево-красный цвет жидкость раствором нитрата ртути II такой концентрации, чтобы каждый миллилитр раствора отвечал 1 мг хлор-иона. Титрование ведут до появления мути в жидкости, которая хорошо заметна при прибавлении одной капли ртутного раствора на фоне черной глянцевой бумаги. Массовую долю хлоридов (%) в пересчете на хлористый натрий получают по формуле:
 (.1)
(.1)
где А – расход титранта, т.е. раствора азотнокислой ртути, см3;
Т – содержание хлор-ионов, которому соответствует 1 см3 ртутного раствора, мг/см3;
58,443 и 35,453 – молекулярные веса хлористого натрия и хлор-иона.
П – объём аликвотной порции, отобранной для определения, см3;
G – навеска, г;
В-объем мерной колбы, в которую собран фильтрат после отделения кремнекислоты, см3.
2 Определение ионов хлора в нефтяном буровом растворе
Данный тест предназначен для измерения суммарной концентрации растворимых хлоридов в буровом растворе. Источниками ионов хлора в растворе служат хлористый натрий, хлористый кальций и хлористый калий. Для получения правильных результатов титрования фильтрат должен иметь слегка щелочную реакцию – рН ≈ 8,3. В процессе титрования одновременно протекают две химические реакции.
1. Аg+ + Сl-→AgCl
2. 2Аg+ + СгО42-→ Аg2СгO4
Результатом первой реакции (образование хлористого серебра) служит появление белых вкраплений или молочное окрашивание раствора. Образование красного хромата серебра начинается лишь после того, как все ионы хлора оказываются связанными в хлористое серебро. После этого нитрат серебра вступает в реакцию с индикаторным раствором хромата калия, в результате чего образуется хромат серебра. Таким образом, для нормального протекания обеих реакций фильтрат должен иметь слабощелочную реакцию, (рН = 8.3). При высоком рН происходит выпадение осадка окиси серебра.
Оборудование
Шприц со стеклянным наконечником, 5 мл; мерный стакан, 400 мл, стеклянный; магнитная мешалка с «микромешалками»
Реактивы:
Дистиллированная вода, раствор хромата калия, индикаторный раствор фенолфталеина, раствор серной кислоты 0,1 N, раствор нитрата серебра, растворитель Arcosolv PNP.
Методика определения
Для начала определите щелочность цельного бурового раствора:
1. Внесите 100 мл растворителя Arcosolv PNP в 400-мл мерный стакан.
2. Наберите в 5-мл шприц не менее 3 мл цельного бурового раствора и введите 2 мл в мерный стакан.
3. Взбалтывайте смесь круговыми движениями до достижения однородности.
4. Добавьте 200 мл дистиллированной воды. Добавьте 15 капель индикаторного раствора фенолфталеина.
5. Перемешивая смесь магнитной мешалкой, медленно титруйте 0,1N серной кислотой до начала исчезновения розовой окраски. Продолжайте перемешивать смесь в течение еще одной минуты и, если розовая окраска не появится вновь, прекратите перемешивание. Иногда бывает необходимо прекратить перемешивание, чтобы обеспечить разделение обеих фаз и возможность более четкого визуального определения цвета водной фазы.
6. Оставьте образец на 5 минут, и если розовая окраска не появится вновь, то это будет свидетельствовать о достижении конечной точки титрования. В случае возобновления розовой окраски проведите повторное титрование серной кислотой. Если розовая окраска окончательно не исчезает, оттитруйте смесь в третий раз, однако в случае возобновления окраски после третьего титрования следует прекратить дальнейшие попытки и принять полученный результат за конечную точку.
7. Закончив определение щелочности, обеспечьте наличие кислой реакции (рН < 7) у смеси, которую предполагается титровать на содержание хлоридов, путем добавления 10–20 капель 0,1 Н серной кислоты.
8. Добавьте 3,0 мл индикаторного раствора хромата калия.
9. Перемешивая смесь с помощью магнитной мешалки, медленно титруйте ее 0.282N раствором нитрата серебра до появления оранжево-розовой окраски, сохраняющейся на протяжении как минимум одной минуты. Иногда бывает необходимо прекратить перемешивание, чтобы обеспечить разделение обеих фаз и возможность более четкого визуального определения цвета водной фазы. 10. Расчет содержания хлоридов в цельном буровом растворе основывается на суммарном количестве миллилитров 0.282N нитрата серебра, потребовавшемся для достижения конечной точки титрования.
Расчет содержания хлоридов осуществляется по формуле:
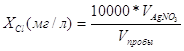 (.2)
(.2)
Похожие работы
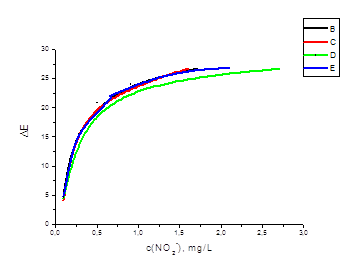
... NO2- для разных шкал Приготовить четыре стандартных шкалы с разным шагом ных четыре шкалы для блюдателей воре, что позволяет применять для их определения спектроскопию крок шкали, загальне колідля визуального тест-определения нитрит-иона, расположив окрашенные таблетки ППУ на белом фоне в порядке возрастания концентрации нитрит-ионов для каждой шкалы. Большому числу независимых наблюдателей ( ...
... «минерализация природных вод» и на основе аргентометрического и титриметрического методов химического анализа провести количественное определение анионов Cl-, SO42-, НCO3-, CO32- и на основе полученных экспериментальных данных сделать вывод о степени минерализации вод рек Раковка и Комаровка. Глава I. Вода на Земле, ее происхождение и состав I.1. ...
... необходимой для анализа пробы согласно следующей таблице: вид осадка содержание сульфат-ионов в водной вытяжке, мл/100 мл процентное содержание сульфат-ионов в почвенном образце, г/100 г почвы требуемый объем вытяжки для количественного определения сульфат-ионов, мл большой осадок, быстро оседающий на дно более 59 десятые доли 5 сразу появляющееся замутнение в пробирке 10 ...
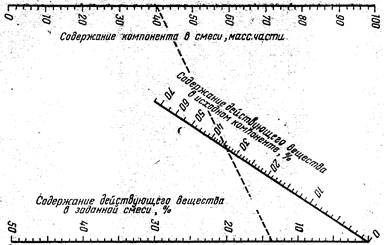
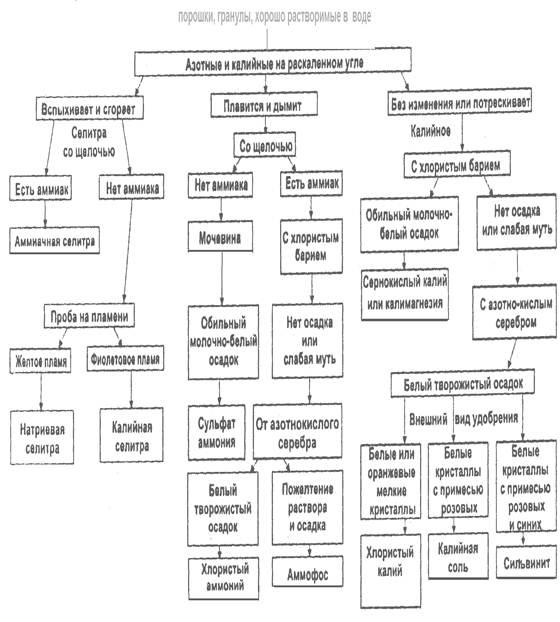
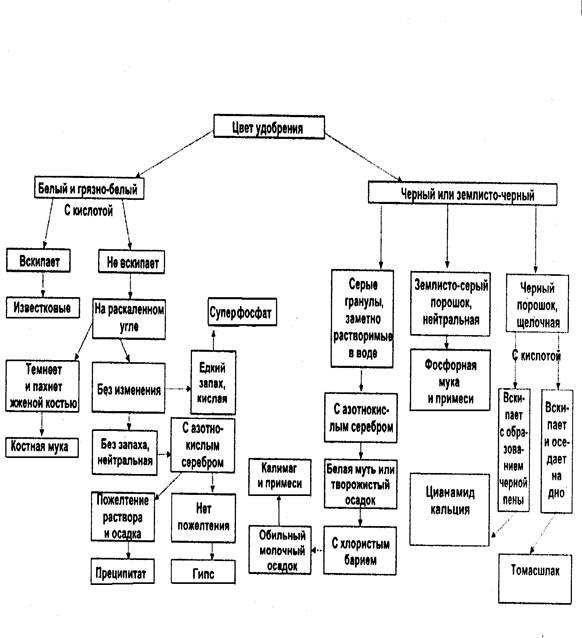
... ее образуются желто-красные осадки гидразонов, склонные к быстрой кристаллизации. Таким же путем легко обнаружить и биурет в карбамиде. Количественные определения минеральных удобрений Все количественные определения минеральных удобрений производятся согласно ГОСТ 21560.4-02. В промышленных минеральных удобрениях принято рассчитывать следующие количественные показатели: 1. ...
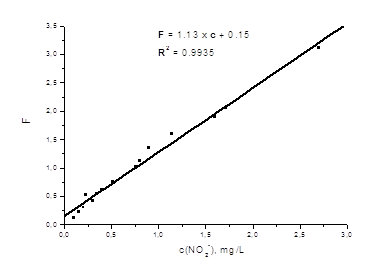
0 комментариев