Навигация
Биохимия сахарного диабета
Министерство здравоохранения Украины
Запорожский государственный медицинский университет
Кафедра биологической химии и лабораторной диагностики
Реферат
на тему:
«Биохимия сахарного диабета»
Выполнила:
студентка 2 курса 14 группы
медицинского факультета
Чмуль Карина Олеговна
г. Запорожье, 2007 г.
План
Ø Инсулинзависимый сахарный диабет
Ø Клеточный иммунитет
Ø Иммунный ответ на эндогенные и эндоцитированные белки
Ø Интерлейкин-1
Ø Модель аутоиммунной гибели -клеток
Ø дефицит инсулина
Ø Коматозные состояния (острые осложнения) при диабете
Ø Гликирование белков - одна из главных причин поздних осложнений сахарного диабета
Ø Диабетические ангиопатии
Ø Диабетические макроангиопатии.
Ø Микроангиопатии.
Инсулинзависимый сахарный диабет
1. При ИЗСД происходит разрушение -клеток в результате аутоиммунной реакции
Гипергликемия и другие первичные симптомы ИЗСД обусловлены дефицитом инсулина, который в свою очередь вызван уменьшением количества -клеток (а также островков Лангерганса) в поджелудочной железе. Множество экспериментальных и клинических исследований указывает на то, что разрушение островков происходит в результате клеточной аутоиммунной реакции.
При манифестации (т.е. первом клиническом проявлении) ИЗСД почти всегда обнаруживается воспалительная реакция в поджелудочной железе - инсулит. Панкреатический инфильтрат при ИЗСД содержит Т-лимфоциты, В-лимфоциты, натуральные киллеры и макрофаги. При этом инфильтрат образуется только в тех островках, в которых есть -клетки. В островках, продуцирующих глюкагон, соматостатин, но не содержащих -клеток, нет и инфильтрата. Такая локальность, точечность реакции указывает на то, что причиной ее являются компоненты и свойства, присущие только -клеткам. Как показывают многие наблюдения, специфичность повреждения -клеток может быть следствием клеточной аутоиммунной реакции.
Клеточный иммунитет. Основными молекулами, обеспечивающими клеточный иммунитет, являются Т-рецепторы и белки главного комплекса гистосовместимости (белки ГКГ). Эти два семейства молекул принадлежат к суперсемейству иммуноглобулинов, в которое входит также семейство иммуноглобулинов (антител), давших название всему суперсемейству. В отличие от антител, которые находятся в жидкостях организма в растворенном состоянии, Т-рецепторы и белки ГКГ - это интегральные белки клеточных мембран.
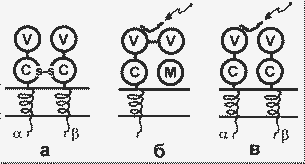
Т-рецепторы имеются на поверхности Т-лимфоцитов, а белки ГКГ - на поверхности практически всех клеток. Т-рецепторы представляют собой гетеродимеры , содержащие межцепочечную дисульфидную связь. Каждая цепь содержит глобулярные вариабильный и константный домены, экспонированные на наружной поверхности мембраны, а также трансмембранный домен и короткий цитоплазматический домен:
|
Строение Т-рецепторов (а) и белков ГКГ классов I (б) и II (в). Стрелки указывают на пептиды - лиганды белков ГКГ; М - 2-микроглобулин |
Т-рецептор составляет часть многомолекулярного белкового комплекса, включающего в общей сложности 7- 9 пронизывающих мембрану пептидных цепей. Этот комплекс формируется в цитозоле и затем включается в мембрану. Существует множество клонов Т-лимфоцитов, различающихся по структуре вариабильного домена, т.е. множество Т-рецепторов с разной специфичностью к лигандам. Разнообразие Т-рецепторов возникает так же, как и разнообразие антител, т.е. в результате соматической рекомбинации генов. Лигандами для Т-рецепторов служат короткие пептиды (10 - 20 аминокислотных остатков), которые образуются из чужеродных белков в результате протеолитической фрагментации. При этом для узнавания рецепторами необходимо, чтобы такие пептиды были соединены с белками ГКГ.
Известны два класса белков ГКГ, несколько различающихся по структуре и функциям. Белки класса I содержат две нековалентно связанные пептидные цепи - легкую и тяжелую. Тяжелая цепь своей большой N-концевой частью экспонирована на наружной поверхности клеточной мембраны, далее следуют небольшие трансмембранный и цитоплазматический домены. Легкая цепь представлена 2-микроглобулином (2m). Внеклеточная часть тяжелой цепи содержит три глобулярных домена: 1 и 2 - вариабильные домены, 3 - константный домен, сходный по структуре с пептидом 2m.
Белки ГКГ класса II - это гомодимеры; на поверхности клетки экспонированы вариабельный и константный глобулярные домены обеих цепей.
Белки ГКГ класса I имеются практически во всех клетках организма человека, а класса II - только в макрофагах, В-лимфоцитах и некоторых специализированных эпителиальных клетках. В геноме человека имеется лишь несколько генов (генных локусов) белков ГКГ (гены HLA). Однако в популяциях человека известно большое количество аллельных вариантов этих белков - варианты белков класса I и варианты белков класса II; отдельные индивиды могут наследовать лишь один (гомозиготы) или два (гетерозиготы) из этих вариантов, причем вероятность наследования разными индивидами одинаковых вариантов ничтожна. Т.о. между людьми существуют индивидуальные различия по белкам ГКГ. Именно с этим связана трансплантационная несовместимость индивидов.
Белки ГКГ являются рецепторами небольших пептидов (длиной в 10 - 20 аминокислотных остатков). Центр связывания этих пептидов образуют вариабельные домены белков ГКГ. Пептиды-лиганды могут образоваться в результате протеолитической фрагментации как собственных белков организма, так и чужеродных белков; в последнем случае пептиды-лиганды служат антигенами, вызывают иммунную реакцию с участием Т-лимфоцитов. К пептидам, образовавшимся из собственных нормальных (не мутантных) белков на ранних стадиях эмбрионального развития вырабатывается иммунологическая толерантность.
Комплекс белка ГКГ с пептидом служит лигандом Т-рецептора определенного клона Т-лимфоцитов. Т-лимфоцит своим Т-рецептором присоединяется к клетке, представившей на своей поверхности комплекс ГКГ/пептид, и если пептид в этом комплексе происходит не из собственного, а из чужеродного белка, Т-лимфоцит активируется, и включается механизм уничтожения клетки, несущей чужеродный пептид. Подчеркнем, что Т-рецептор связан не отдельно с белком ГКГ, и не отдельно с петидом-антигеном, а именно с комплексом этих молекул, которые вместе и в равной мере участвуют в образовании центра связывания для Т-рецепторов. Т.о. специфичность иммунного ответа есть результат вариабельности белков ГКГ, которые определяют и выбор пептида-антигена, и выбор Т-лимфоцита соответствующего клона.
Т-лимфоциты в организме человека представлены тремя типами: цитотоксические Т-лимфоциты (Т-киллеры), имеющие механизм уничтожения клеток, и два типа лимфоцитов, выполняющих регуляторные функции - Т-хелперы и Т-супрессоры. Т-хелперы, присоединившие антиген, стимулируют остальные компоненты иммунной системы: специфичные к данному антигену другие Т-лимфоциты, а также и В-лимфоциты. Т-супрессоры, наоборот, подавляют активность этих клеток. Т-хелперы, вероятно, играют главную роль в инициации иммунного ответа. В частности, пролиферация и окончательная дифференцировка В-лимфоцитов, узнавших чужеродный антиген, требует активации Т-лимфоцитами.
Таблица 2. Иммунный ответ на эндогенные и эндоцитированные белки
|
|
Чужеродные белки могут появиться в клетке двумя путями: 1) образоваться в самой клетке (вирусные белки, мутантные белки); 2) проникнуть путем эндоцитоза в клетки макрофагов и некоторых других фагоцитирующих клеток (любые белки, появляющиеся в жидкостях организма). Ответ клеточного иммунитета в этих случаях будет несколько различным (табл. 2).
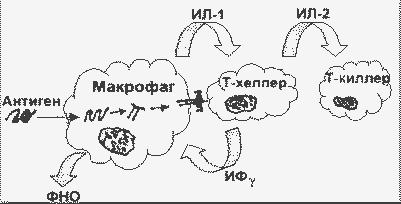
На рисунке приведена схема инициации клеточного иммунного ответа на эндоцитированный чужеродный белок:
|
Инициация клеточного иммунного ответа |
Антиген (Аг), обычно растворимый белок , часто гликопротеин, эндоцитируется антигенпредставляющими клетками (АПК; например, тканевыми макрофагами или В-лимфоцитами). В эндоцитозе участвует рецептор антигена на поверхности АПК. Комплекс Аг-рецептор интернализуется, в эндосоме происходит частичный протеолиз с образованием пептидов длиной в 10 - 20 аминокислотных остатков, пептиды соединяются с белками класса II главного комплекса гистосовместимости. Затем эндосома сливается с плазматической мембраной, и комплекс антигенный пептид/класс II-ГКГ экспонируется на поверхности клетки. Экспонированный комплекс может быть распознан Т-хелперами специфического клона, несущими подходящий Т-рецептор.
Когда Аг узнается Т-хелпером, он (Т-хелпер) активируется прежде всего в отношении транскрипции ряда цитокиновых генов. Продукция цитокинов (см. ниже) вызывает хемотаксис лейкоцитов к месту, где происходят эти события, активацию эндотелиальных клеток, пролиферацию и дифференцировку рекрутированных лейкоцитов, апоптоз и много других биологических активностей.
Похожие работы
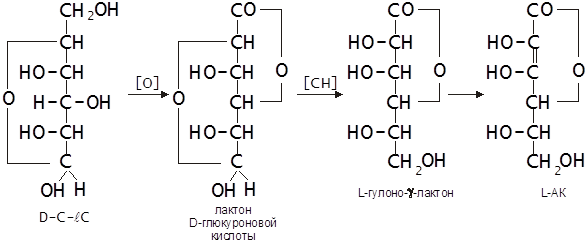
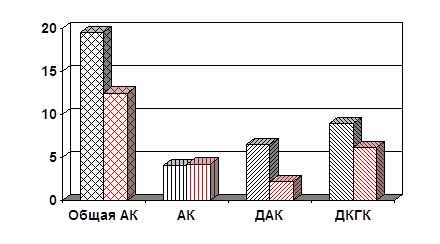
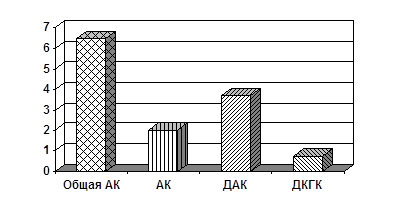
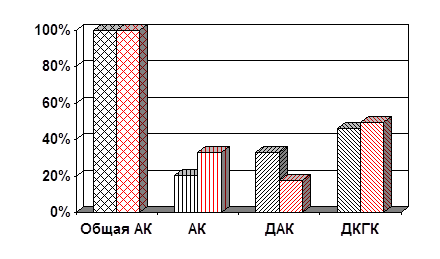
... в течение пятнадцати минут при 3000 об/мин. Супернатант отсасывали, процедуру повторяли 3 раза. Это делалось для более плотной упаковки эритроцитов. 2.2. Метод раздельного определения аскорбиновой, дегидроаскорбиновой и дикетогулоновой кислот в эритроцитах Для количественных определений АК, ДАК и ДКГК использовали метод J.H. Roe, C.A. Kuether (1943) в модификации В.В. Соколовского, Л.В. ...
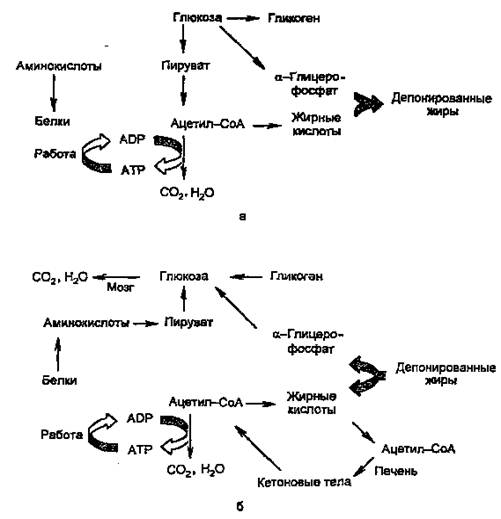
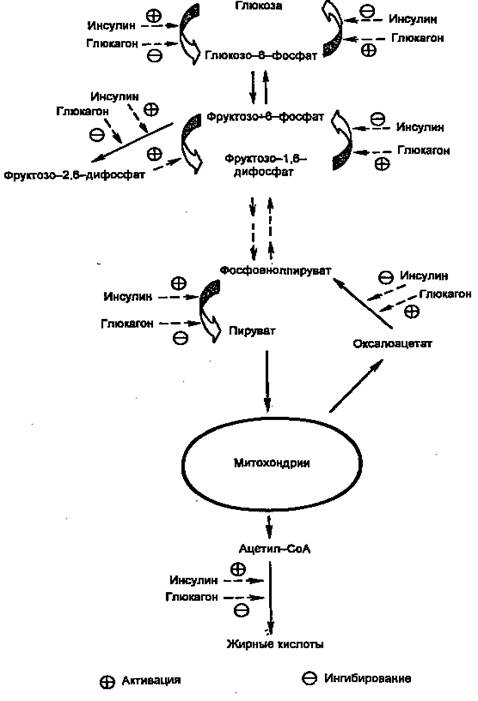
... с различной чувствительностью к глюкозе. Это еще один элемент глюкозосенсорного механизма: при высокой концентрации глюкозы увеличивается число клеток, секретирующих инсулин. НАРУШЕНИя метаболизма углеводов и липидов при сахарном диабете При сахарном диабете инсулин-глюкагоновый индекс снижен. Это связано не только с уменьшением секреции инсулина, но и с увеличением секреции глюкагона ( ...
... липопротеинов (ЛПОНП), что способствует возникновению атеросклероза. 6. Бета-липопротеины по Бурнштейну - 93 ед, норма-до 55 ед, повышено. Гиперлипопротеинемия. Преобладание атерогенных фракций липопротеинов7 При сахарном диабете усиливаются процессы гликозилирования. Гликозилирование ЛНП приводит к повышению их отрицательного заряда, а это в свою очередь к потере способности связываться со ...
... Ф. и др. Потенциальный клинико-лабораторный тест в диабетологии. // Клинико-лабораторная диагностика. 1997. № 5. С. 27-28. 11. Гольдберг Е. Д. , Ещенко В. А. , Бовт В. Д. Сахарный диабет. Томск, 1993. С 85-91. 12. Грязнова И. М. , Второва В. Г. Сахарный диабет и беременность. М. : Медицина, 1985. С. 156-160. 13. Давиденкова Е. Ф. , Либерман И. С. Гентика сахарного диабета. Л. : Медицина, 1988. ...

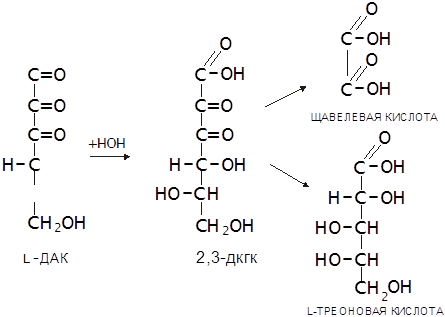
0 комментариев