Навигация
6. Полисульфиды.
Растворы щелочных металлов способны растворять значительные количества серы, и при этом образуются окрашенные в цвета от желтого до коричнево-красного полисульфиды, т.е. соединения общей формулы M2Sn, где n обычно имеет значения от 2 до 5, но в некоторых случаях может принимать и еще большие значения. Известные полисульфиды щелочных металлов представлены в таблице 5.
Полисульфиды щелочных металлов образуются также при стоянии растворов щелочных сульфидов на воздухе вследствие медленного окисления гидросульфид-ионов кислородом воздуха:
2HS- + ½ O2 = H2O + S2- (17)
Полисульфиды щелочных металлов получают также сплавлением сульфидов щелочных металлов с серой. Кроме того, их можно получить, сплавляя гидроокиси или карбонаты щелочных металлов с серой. Однако в последнем случае получающиеся полисульфиды бывают загрязнены одновременно образующимся тиосульфатом, а при доступе воздуха и сульфатом.
Кроме полисульфидов щелочных металлов, известны также полисульфиды щелочноземельных металлов. Самыми устойчивыми являются, по –видимому, полисульфиды с четырьмя атомами серы.
В таблице 5 представлены известные полисульфиды щелочных меаллов.
Таблица 5
Известные полисульфиды щелочных металлов
| Na2S2 | K2S2 | Rb2S2 | Cs2S2 |
| - | K2S3 | Rb2S3 | Cs2S3 |
| Na2S4 | K2S4 | Rb2S4 | Cs2S4 |
| Na2S5 | K2S5 | Rb2S5 | Cs2S5 |
| - | K2S6 | Rb2S6 | Cs2S6 |
Гидролитическое расщепление полисульфидов происходит в значительно меньшей степени, чем обычных сульфидов. Например, в отличие от нормального сульфида аммония (NH4)2S полисульфиды аммония при обычных температурах устойчивы. Кислоты разлагают полисульфиды с отщеплением серы:
Na2S2 + 2HCI = 2NaCI + H2S + S (18)
7. Промышленное применение сульфидов
В таблице 6 представлены промышленные области применения сульфидов.
Таблица 6 Промышленное применение сульфидов
| № п/п | Формула | Применение | |
| 1 | 2 | 3 |
|
| 1 | Ag2S | · Обеспечивает «темнение под старину» новых серебряных изделий; |
|
| 2 | As2S3 | · в чистом виде «королевская желтая» краска; · краска-«опермент»- в неочищенном состоянии; |
|
| 3 | As4S4 | · живопись; · изготовление фейерверков; |
|
| 4 | Bi2S3 | · главный исходный материад для получения висмута; |
|
| 5 | CaS | · пестицидный препарат для борьбы с мучнистой росой; |
|
| 6 | CdS | · зеленый люминофор в цветных кинескопах; |
|
| 7 | Cu2S | · хороший проводник; · для изготовления художественных красок; |
|
| 8 | CuS | · главный исходный материад для получения для получения меди; · для изготовления художественных красок; |
|
| 9 | FeS | · в лабораторных условиях для получения сероводорода; |
|
| 10 | FeS2 | · главный исходный материад для получения серной кислоты; · в качестве детекторов в радиотехнике; |
|
| 11 | HgS | · для получения ртути; · для изготовления художественных красок; |
|
| 1 | 2 | 3 |
|
| 12 | K2S | · в медицинских целях; · посульфиды калия применяют для сульфидирования стальных, чугунных, медных и серебряных изделий (окрашивание) |
|
| 13 | MoS2 | · сухая смазка и присадка к моторным маслам; |
|
| 16 | Na2S | · восстановитель для органических соединений; · при дублении кож; |
|
| 17 | NiS | · используется для получения никеля; |
|
| 18 | P4S3 | · используется для изготовления спичек, загорающихся при трении о любую поверхность; · используется как вещество для нагревательных бань; |
|
| 19 | PbS | · для получения свинца; |
|
| 20 | Sb2S3 | · исходный материал для получения сурьмы; · в пиротехнике; · для изготовления спичек; · для изготовления рубинового стекла; |
|
| 21 | Sb2S5 | · используют в медицине (ветеринарии); · для вулканизации каучука; |
|
| 22 | SnS2 | · «сусальное золото» - золото для мозаичных работ; · «оловянная бронза» - для бронзирования; |
|
| 23 | SrS | · люминофорный материал (голубовато-зеленое свечение) |
|
| 24 | ZnS | · люминофорный материал (зеленое свечение); · для получения цинка; · в смеси с BaSO4 – белая краска; |
|
Похожие работы
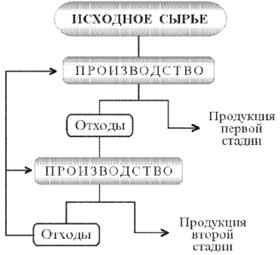
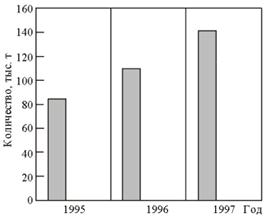
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...
... . Практика свидетельствует, что любая деятельность потенциально опасна. Это аксиома о потенциальной опасности деятельности. Каждое производство характеризуется своим комплексом опасных и вредных факторов, источниками которых являются оборудование и технологические процессы. Современное машиностроительное предприятие, как правило, включает литейные и кузнечно-прессовые, термические, сварочные и ...
... к сети зануления или заземления. Выравнивание потенциалов применяется как дополнительный технический способ защиты при наличии зануления или заземления в помещениях с повышенной опасностью или особо опасных. Применение выравнивания потенциалов обязательно в животноводческих помещениях. Устройство выравнивания потенциалов осуществляется по проекту. 5. Режим защиты персонала при работе на ...
... близки к исчерпанию. Поэтому обеспечить как потребности экономики, так и требования по охране природы можно лишь путем перехода к ресурсосберегающим технологиям в лесном комплексе мирового хозяйства. 4. Распределение природных ресурсов между странами Природные ресурсы распределены крайне неравномерно между странами. Только 20-25 стран располагают более 5% мировых запасов какого-либо одного вида ...
0 комментариев