Навигация
Химия и технология производства 2–нафтола щелочным плавлением
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
«СИБИРСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ»
Факультет химических технологий
Кафедра ОХ и ХТОВ
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
Химия и технология производства 2 – нафтола щелочным плавлением
(ХТОВ. 000000.016ПЗ)
Руководитель:
Б.Б. Кочетков
_______________Е.В. Роот
(подпись)
_______________________
(оценка, дата)
Разработал:
Студент группы 64-7:
Троцюк А.В.
_________________
(подпись)
__________________________
(дата)
ЗАДАНИЕ НА КУРСОВУЮ РАБОТУ
вариант 16
Студенту группы 64-7 Троцюк Анне Васильевне
Тема курсовой работы: Химия и технология производства 2 – нафтола щелочным плавлением.
Задание выдано
________________________________Руководитель Кочетков Б.Б.
Реферат
В данной курсовой работе была произведена оценка и выбрана наиболее выгодная схема получения β - нафтола, подобрано аппаратурное оформление и технологическая схема для его получения.
Курсовая работа содержит 37 страниц, 3 таблицы, 4 рисунка.
Содержание
Введение
1 Назначение и характеристика выпускаемой продукции
2 Технологическая часть
2.1 Кинетика и механизм реакции
2.2 Технология щелочного плавления
2.3 Получение β – нафтола
2.3.1 Щелочное плавление β – соли
2.3.2 Подкисление раствора нафтолята
2.3.3 Очистка 2 – нафтола
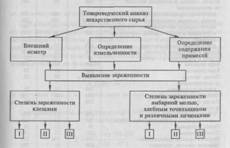
3 Контроль процесса щелочного плавления и методы определения гидроксисоединений
4 Аппаратура для обработки продуктов щелочного плавления
5 Безопасность и экологичность работы
Заключение
Список использованных источников
Приложение А
Приложение А.1
Приложение А.2
Приложение Б
Приложение В
Введение
Щелочное плавление - процесс взаимодействия металлических солей сульфокислот со щелочами, приводящих к замещению сульфогруппы гидроксильной группой. Данный метод является одним из основных для получения ароматических гидроксильных соединений, которые очень важны в производстве многих продуктов тонкого органического синтеза. Исходным органическим сырьем в процессах щелочного плавления являются металлические (главным образом натриевые) соли сульфокислот (бензолсульфонат натрия, нафталин сульфонат натрия, натриевые соли нафталинаминосульфокислот, антрахононсульфокислот и т.д.), применяемые в виде растворов, паст и сухих веществ. Неорганическим сырьем, участвующим в этих процессах, являются щелочи (едкий натр, едкое кали, окись кальция и др.), применяемые в виде растворов и расплавов.
1 Назначение и характеристика выпускаемой продукции
2-нафтолы (β-нафтолы)-бесцветные кристаллы со слабым фенольным запахом; хорошо растворимы в этаноле, диэтиловом эфире, хлороформе, бензоле, плохо - в воде.
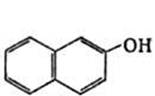
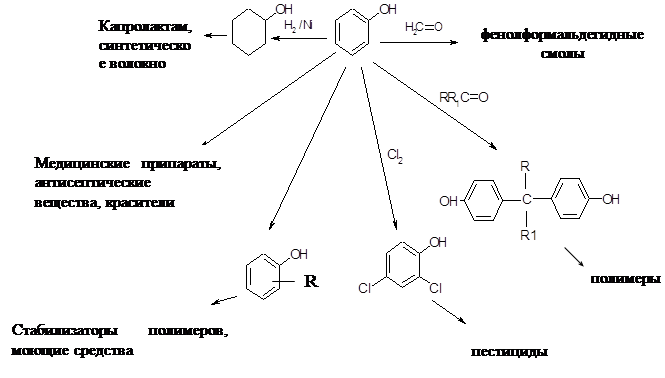
β – нафтол применяется при производстве органических красителей, в парфюмерной промышленности, в медицине.
β – нафтол полупродукт органического синтеза, имеет молекулярную массу М=144,17 г/моль;
плотность p=1,217;
температура кипения t кип=2860С;
температура плавления t пл=1220С;
Растворим в воде (0,074) и в органических растворителях: хлороформе, бензоле, этаноле.
2 Технологическая часть
2.1 Кинетика и механизм реакции Замена сульфогруппы гидроксигруппой в ароматических соединениях методом щелочного плавления является одним из основных методов получения ароматических гидроксисоединений — важного класса органических соединений, используемых в производстве многих продуктов тонкого органического синтеза, в том числе в производстве органических красителей.Впервые в 1864 г. Дюзаром и почти одновременно и независимо Вюрцем и Кекуле было осуществлено превращение бензолсульфокислоты в фенол. Эта реакция, в которой один заместитель в ароматическом ядре замещается другим, происходит с разрывом связи С—S и образованием новой связи С—О. Реакции замещения сульфогруппы гидроксигруппой протекают в жестких условиях, при высокой температуре (150—340 °С), часто при действии расплавленной щелочи(NaOH или КОН) с небольшим содержанием воды.
В качестве реагентов для превращения сульфогруппы в гидроксигруппу применяют гидроксид натрия NaOH, гидроксид калия КОН и гидроксид кальция Са(ОН)2 (в ряду антрахинона). Наиболее часто используют NaOH, который более дешев, хотя и менее реакционноспособен, чем КОН. В некоторых случаях используют смесь NaOH и КОН, имеющую более низкую температуру плавления, чем каждый реагент в отдельности (т. пл. NaOH 328 °С, т. пл. КОН 360 °С), что позволяет вести процесс при более низких температурах.
Замещение сульфогруппы в ароматических соединениях гидроксигруппой протекает при действии щелочей на соли сульфокислот (уравнение 1).
ArSO3Na + 2NaOH ® ArONa + Na2SO3 + H2O (1)
Однако в действительности реакция протекает более сложно, чем показано в уравнении (1). При изучении кинетики реакций щелочного плавления бензолсульфокислоты и некоторых нафталинсульфокислот с водными растворами NaOH было найдено, что для большинства сульфокислот реакции имеют второй порядок, а для бензолсульфокислоты, 6-гидрокси- и 7-гидроксинафталин-2-сульфокислот — порядок близок к трем, т. е. наблюда ется первый порядок по сульфокислоте и второй — по щелочи. Эти данные указывают, что реакция протекает в две стадии (схема 2). На первой стадии
-+он- +он-
ArSO3- ¾¾¾®[HOArSO3]2-¾¾® ArO- +SO32-+ Н2О (2)
происходит присоединение гидроксид-иона к аниону аренсульфокислоты с образованием дианиона, который далее (вторая стадия) реагирует со вторым гидроксид-ионом, образуя феноксид-ион, сульфит-ион и воду. Эта схема была предложена Н. Н. Ворожцовым ст. еще в 30-е годы XX века.
В соответствии с общими положениями ароматического нуклеофилыюго замещения и данными, полученными при изучении кинетики этой реакции, в настоящее время механизм щелочного плавления может быть представлен уравнением (3). Считают, что при действии второго гидроксид-иона происходит отрыв протона от гидроксильной группы s-комплекса. Электронодонорное влияние образующегося заместителя О- способствует последующему отщеплению иона SO32-
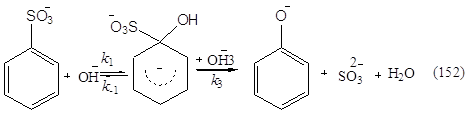 (3)
(3)
Применив, принцип стационарности и определив концентрацию продукта присоединения первого гидроксид-иона (s-комплекса) (уравнение 4) получим для скорости реакции щелочного плавления уравнение (5).
[HOArSO32-] = k1[ArSO3-][ОН-]/ k -1 + k2 [НО-] (4)
v = k1k2 [ArSO3-][НО-]2/k -1 + k2 [НО-] (5)
Если в соответствии с общей схемой щелочного плавления (смотри схему 3) первая стадия (присоединение гидроксид-иона к аниону сульфокислоты) будет медленной стадией, т.е. k1<k2, то скорость реакции щелочного плавления будет определяться уравнением (6), а порядок реакции будет равен 2.
v = k1 [ArSO3-] [НО-] (6)
Если действие второго гидроксид-иона и отрыв сульфит-аниона будут проходить медленно, т. е. k1>k2, и определять скорость всего процесса, то реакция будет описываться уравнением (7) и иметь порядок, равный 3.
v = Kk2 [ArSO3-] [НО-]2 (7)
где K = k1/k-1.
Понижение электронной плотности в реакционном центре, облегчающее нуклеофильную атаку гидроксид-ионом вызывается в основном только индуктивным эффектом ионизированной сульфогруппы. Поэтому реакция имеет высокую энергию активации (143—197 кДж/моль) и протекает в жестких условиях (300—340 °С). Протекание реакции при высокой температуре объясняется тем, что в ходе реакции происходит взаимодействие двух отрицательных ионов — ArSO3- и НО-. Структура промежуточно образующихся s-комплексов объясняет стабильность к щелочному плавлению, например, 4-гидроксибензол-1-сульфокислоты (п-фенолсульфокислоты) и невозможность получения из нее гидрохинона. В этом случае во взаимодействие с гидроксид-ионом должен был бы вступать дианион 4-гидроксибензол-1-сульфо-кислоты, в котором у атома углерода, связанного с сульфогруппой, дополнительно повышается электронная плотность из-за мезомерного влияния ионизированной группы ОН.
Таким образом, введение в молекулу ароматической сульфокислоты электронодонорного заместителя затрудняет реакцию щелочного плавления, и, наоборот, электроноакцепторные заместители облегчают реакцию.
Изучение щелочного плавления [14C] бензолсульфокислоты показало, что гидроксильная группа вступает в то же положение, где находилась сульфогруппа. При щелочном плавлении п-толуолсульфокислоты образуется только п-крезол. При действии на соль бензолсульфокислсмы гидроксидов натрия и калия, обогащенных 18О, было обнаружено, что атом кислорода гидроксида переходит в образующиеся феноксид и воду. Все это является подтверждением рассмотренного выше механизма щелочного плавления.
Согласно имеющимся данным, реакция замещения сульфогруппы гидроксигруппой протекает по механизму ароматического нуклеофильного замещения (присоединения — отщепления), а реакция, протекающая по «ариновому» механизму, практически отсутствует.
2.2 Технология щелочного плавления
Щелочное плавление можно осуществлять тремя способами: при атмосферном давлении, так называемая открытая плавка; 2) при повышенном давлении в автоклавах; 3) с использованием гидроксида кальция (извести), так называемый известковый плав.
Для щелочного плавления при атмосферном давлении применяют гидроксид натрия как в твердом состоянии, так и в виде 12%-ного или 70—73%-ного растворов. При использовании растворов NaOH их упаривают до концентрации: 80—85%; при применении твердого NaOH к его расплаву добавляют до 10% воды. Все это позволяет получить плав, подвижный при 270— 290 °С, и создать благоприятные условия для ведения реакции.
Для успешного проведения реакции используемая соль сульфокислоты должна содержать минимальное количество минеральных_солей (хлорид и сульфат натрия). В противном случае наблюдаются неполная растворимость соли сульфокислоты в расплавленной щелочи, появление в плаве комков (комкование), что приводит к снижению подвижности плава и возможности местных перегревов; при высоких температурах (выше 300 °С) это может вызвать подгорание плава или даже горение всей массы. При хорошем размешивании небольшое содержание минеральных солей (до 10% > обычно не отражается на процессе). Соль сульфокислоты не должна иметь кислую реакцию, так как это приводит к дополнительному расходу NaOH на нейтрализацию, а следовательно, и к увеличению содержания минеральных солей.
Теоретически для щелочного плавления необходимо 2 моль NaOH (на 1 моль сульфокислоты), практически используют избыток щелочи (2,1 - 2,4 моль, и отдельных случаях 3—4 моль),
Общий метод проведения щелочного плавления состоит в следующем: в хорошо подвижный, жидкий плав NaOH при 275—280 °С вносят постепенно (порциями) при размешивании соль сульфокислоты в виде сухого измельченного порошка или насыщенного водного раствора. Вода постепенно испаряется, но подвижная реакционная масса легко размешивается. К тому же количество воды в массе пополняется вследствие её образования в ходе реакции. Выделяющиеся пары воды также способствуют перемешиванию массы. После окончания загрузки соли сульфокислоты реакционную массу при размешивании нагревают, повышая температуру до необходимой (300—340 °С). Готовый плав содержит феноксид натрия, сульфит натрия, а также небольшое количество свободной щелочи. Контроль за процессом щелочного плавления осуществляют, определяя содержание в плаве свободного NaOH,
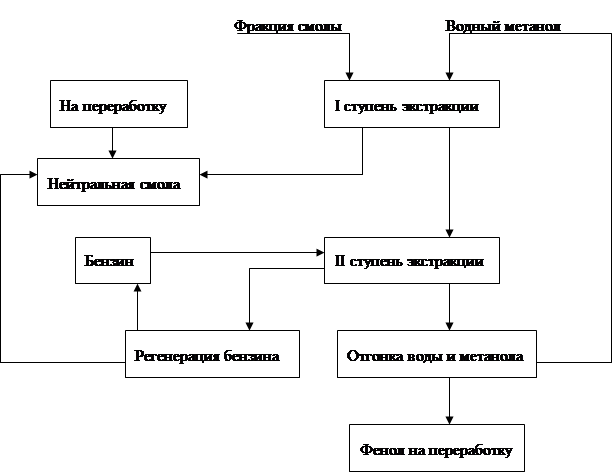
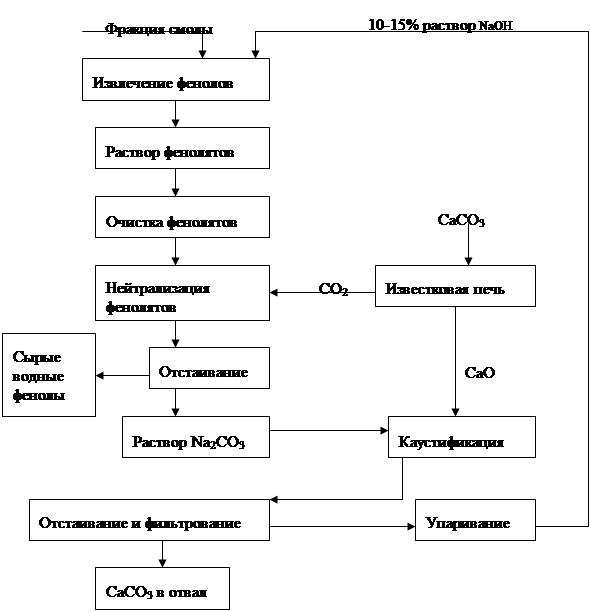
После окончания реакции плав выливают в воду — так называемое гашение плава. В полученном растворе выделяется в осадок сульфит натрия, который отфильтровывают, а из фильтрата при подкислении выделяют свободное гидроксисоединение, которое направляют на очистку.
Щелочную плавку при атмосферном давлении проводят в аппаратах, изготовленных из чугуна с присадкой никеля и хрома и снабженных мешалкой и нижним штуцером для выгрузки реакционной массы (рисунок 4). В крышке плавильного котла имеется люк для вентиляционной трубы, отверстия для загрузки сульфоната, отбора проб плава во время процесса, штуцеры для загрузки жидкого NaOH и установки термопары. Котел монтируют в кладке печи и обогревают топочными газами. Применяются также чугунные котлы, в стенках которых имеются стальные змеевики, по которым циркулирует перегретая вода. В отдельных случаях используют электрообогрев плавильных котлов ( Приложение В).
Щелочная плавка под давлением проводится в вертикальных стальных автоклавах. В этом случае используют водные растворы щелочи и соли ароматической сульфокислоты.
Щелочное плавление антрахинонсульфокислот с применением гидроксида кальция (извести) проводится в автоклавах под давлением. Условия щелочного плавления, т. е. концентрация щелочи, температура и продолжительность плавки, зависят от природы исходной соли сульфокислоты.
Относительная легкость проведения процесса сплавления со щелочами зависит в значительной степени от большей или меньшей подвижности сульфогруппы в том или ином соединении и характеризуется температурой, при которой скорость замещения сульфогруппы гидроксигруппой становится наибольшей. Так, в бензолсульфокислоте и ее гомологах сульфогруппа сравнительно мало подвижна и поэтому плавка протекает в жестких условиях (300—340 °С). В нафталин-1-сульфокислотах сульфогруппа более подвижна, и щелочное плавление в этих случаях ведут при более низких температурах (160—250 °С).
При проведении щелочного плавления аминосульфокислот необходимо учитывать возможность побочных реакций — гидролиз аминогруппы с выделением аммиака и замещение аминогруппы гидроксигруппой. К нитросульфокислотам метод щелочного плавления не применяется. В этом случае при высоких температурах возможно протекание окислительно-восстановительных процессов из-за наличия в молекуле нитрогруппы.
Как указано ранее, введение электроноакцепторной группы приводит к увеличению подвижности сульфогруппы, а введение электронодонорной группы — к уменьшению ее подвижности, поэтому в полисульфокислотах сульфогруппа более подвижна, чем в моносульфокислотах (8). Введение в молекулу нафталинсульфокислоты второй сульфогруппы, как, например, в соединении (9), значительно (в 10—20 раз) увеличивает скорость замещения сульфогруппы. Гидроксинафталинсульфокислоты (10), образующиеся в реакции щелочного плавления, реагируют значительно медленнее не только дисульфокислот, но и соответствующих моносульфокислот.
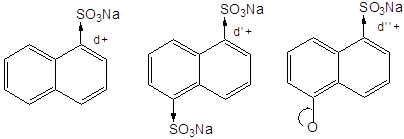
| (8) | (9) d’+ > d+ | (10) d’+ < d+ |
Так, в нафталин- 1,5-дисульфокислоте (158) за счет электроно-акцепторного действия сульфогруппы уменьшена электронная плотность у атома углерода, у которого находится вторая сульфогруппа, что облегчает взаимодействие с гидроксид-ионом. Ионизированная гидроксигруппа, наоборот, увеличивает электронную плотность в ароматическом кольце, что затрудняет присоединение гидроксид-иона к атому углерода кольца. Вследствие этого подбором условий щелочной плавки в нафталинполисуль-фокислотах можно заместить только одну гидроксигруппу. При плавлении, например, нафталин-1,5- и нафталин-2,7-дисульфокислот в качестве основных продуктов реакции можно получить соответственно 6-гидроксинафталин-1-сульфокислоту (азуриновую кислоту) и 7-гидроксинафталин-2-сульфокислоту. Таким образом, регулируя температуру проведения реакции, а также концентрацию щелочи можно управлять ходом реакции щелочного плавления.
Введение достаточного количества воды в плав позволяет поддерживать реакционную массу в жидком состоянии при относительно низких температурах. Однако добавление воды в реакционную массу хотя не меняет основного направления реакции щелочного плавления, но резко снижает ее скорость. Поэтому водные растворы щелочи более удобно применять для частичной замены сульфогруппы в полисульфокислотах. Так получают из нафтплин-1,5-дисульфокислоты 5-гидроксинафталин-1-сульфокислоту (схема 11).
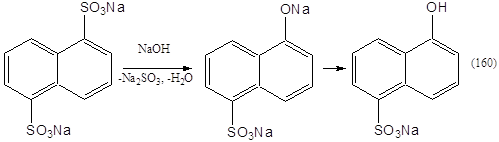
Методом щелочного плавления в автоклаве с высокими выходами можно получать гидроксисоединения (например, фенол, b-нафтол) из моносульфокислот. Процесс проводят в жестких условиях (>300°С, 10 МПа). Получение фенола может быть осуществлено непрерывным способом; в этом случае водный раствор щелочи и соль бензолсульфокислоты под давлением при 350—370 °С пропускают через аппарат трубчатого типа.
Аппараты для щелочного плавления
В зависимости от метода в процессах щелочного плавления перерабатываются жидкие или твердые (сыпучие) вещества.
Консистенция реакционной массы в этих процессах различна, в зависимости от характера обрабатываемых веществ и условий процессов. В процессах щелочного плавления при атмосферном давлении реакционная масса может представлять собой жидкость или суспензию различной консистенции достаточно подвижную, вязкую или тестообразную массу в зависимости от свойств, сплавляемых веществ. Так, при плавлении бензолсульфоната натрия образуется жидкая подвижная реакционная масса, которую можно размешивать мешалкой любого типа. В процессе плавления β - нафталинсульфоната натрия получается довольно вязкая жидкая реакционная масса, размешивание которой возможно лишь мощными лопастными или якорными мешалками.
В процессе сплавления с сульфидирующими агентами (растворы сернистого натрия или полисульфидов натрия) реакционная масса имеет консистенцию достаточно подвижной жидкости или суспензии, с небольшим содержанием твердых частиц. В этих случаях для размешивания пригодны мешалки любого типа. Процессы сульфидирования, проводимые под давлением, также приводят к образованию достаточно подвижной реакционной массы. При сульфидированин методом запекания, которое проводится с участием молекулярной серы, как и в процессах щелочного плавления, проводимого методом запекания, получаются твердые продукты реакции или жидкие, но настолько вязкие, что размешивание реакционной массы иногда становится невозможным. Следует отметить, что в процессах щелочного плавления не требуется Интенсивное перемешивание; так как в данном случае оно не является фактором, способствующим взаимодействию ингредиентов. Перемешивание используется в этих процессах для некоторого улучшения условий их проведения, т. е. для очистки стенок аппарата от налипающей на них массы и суспендирования незначительного количества твердых взвешенных частиц, что позволяет предотвратить местные перегревы и пригорание реакционной массы. Поэтому реакционную аппаратуру в ряде случаев снабжают мешалками, обеспечивающими неэнергичное перемешивание массы.
Температура процессов щелочного плавления колеблется в пределах 150—450° и в реакционной массе часто присутствует значительное количество воды. Это обусловливает возможность проведения указанных процессов различными методами. В процессе, проводимом при атмосферном давлении, из реакционной массы испаряется значительное количество воды; следовательно, требуемая температура в аппарате может быть достигнута лишь после окончания испарения, т. е. в результате подвода больших количеств тепла. Если же процесс проводится под давлением, требуемая температура достигается гораздо быстрее и с меньшей затратой тепла.
Необходимо подчеркнуть, что методы щелочного плавления под давлением имеют ряд существенных достоинств. Щелочное плавление малоконцентрированных растворов под давлением протекает более гладко вследствие большей подвижности реакционной массы и с большим выходом, поскольку в закрытых аппаратах продукты плавления не окисляются на поверхности реакционной массы, соприкасающейся с воздухом. Процессы щелочного плавления протекают с выделением довольно большого количества тепла, однако если они проводятся при атмосферном давлении, необходимо не охлаждение, а нагревание реакционной массы для испарения воды, требующего большого расхода тепла.
Рассматриваемые процессы при достаточно высокой температуре протекают с очень большой скоростью. Время, необходимое для завершения процесса, практически зависит от скорости подвода к реакционной массе тепла, которое расходуется на испарение воды и нагревание ингредиентов до требуемой температуры. Поэтому аппаратура должна иметь развитую поверхность нагрева и конструировать эти аппараты следует с учетом возможности максимальной интенсификации теплообмена. С этой точки зрения процессы под давлением (переработка безводных ингредиентов) имеют большие преимущества по сравнению с прочими методами щелочного плавления, потому что при щелочном плавлении под давлением не происходит испарения воды и, следовательно, расход тепла при проведении процесса минимален.
Реакционная масса, перерабатываемая в аппаратах для щелочного плавления, имеет щелочной характер. К. воздействию щелочных сред устойчивы сталь и чугун, особенно легированные. Вследствие высокой температуры процессов щелочного плавления износ чугунных и стальных аппаратов увеличивается. Присадка хрома повышает жаростойкость и прочность чугунных отливок, присадка никеля увеличивает их щелочеустойчивость.
Реакционная масса, образующаяся в процессах сульфидирования, по химическим свойствам соответствует растворам щелочи, сернистого натрия или полисульфидов натрия. Органические соединения, содержащиеся в реакционной массе, при выборе материала аппаратуры можно не принимать во внимание, так как воздействие их на металлические детали аппаратов весьма незначительно. Как показывает опыт действующих заводов, аппараты из черных металлов в большинстве случаев достаточно стойки к действию растворов щелочей, сульфидов и полисульфидов натрия и могут служить в течение 2—7 лет при условии более частой замены некоторых быстроизнашивающихся деталей.
Более сильному коррозионному воздействию подвергаются части аппаратов, непосредственно соприкасающиеся с газовой фазой. Газовая фаза реакционной массы содержит SО2. В этих условиях наиболее быстро разрушаются те части аппаратуры, которые также соприкасаются с газовой фазой.
Резюмируя изложенное, можно сделать вывод, что для процессов щелочного плавления наиболее пригодны реакционные аппараты следующих типов:
1) аппараты, работающие при атмосферном давлений, в виде котлов с мешалками соответствующей конструкции (эти аппараты называются в технике плавильными и варочными котлами);
2) аппараты, работающие при атмосферном давлении и применяемые при обработке твердых ингредиентов;
3) аппараты, работающие под давлением.
Выбор мешалок и их характеристика
Аппараты с перемешивающими устройствами применяют для самых различных процессов. Однако, несмотря на разнообразие технологических целей, для которых применяется перемешивание, большинство из них сводится к улучшению тепло- и маcсообмена, получению равномерных смесей нескольких жидкостей, жидкости и твердого тела, жидкости и газа. Основная задача перемешивания – равномерное распределение вещества или температуры в перемешиваемом объеме. Иногда перемешивание служит для эмульгирования одной жидкости в другую или диспергирования твердой фазы, а иногда для создания высоких скоростей среды около теплообменных поверхностей с целью интенсификации теплообмена.
В нашем случае используют фаолитовую мешалку, стальной вал которой защищен фаолитом т.е. мешалка с антикоррозионном защитой.
Похожие работы
... и, конечно же, за многими другими, которые будут получены, — будущее. В этом направлении и работают многие НИИ и исследователи. Аспекты поиска новых лекарств, изыскание новых лекарственных веществ состоит из трех основных этапов: химический синтез, установление фармакологической активности и безвредности (токсичности). Такая стратегия поиска с большой затратой времени, реактивов, животных, труда ...
... и отработка методов превращения последних в крезолы. Классическим методом синтеза фенолов является щелочное плавление сульфокислот ароматических углеводородов Этот метод до сих пор используют для получения фенола и β- нафтола из бензола и нафталина соответственно. Oн, по-видимому, наиболее перспективен для производства п-крезола из толуола и в этом варианте реализован в ряде стран. ...
... оксида углерода: Диоксид урана, полученный термической диссоциацией оксалата уранила, пирофорен, легко взаимодействует с газообразным фтористым водородом т плавиковой кислотой. Получение оксидов урана из аммонийуранилтрикарбоната Аммонийуранилтрикарбонат разлагается на воздухе при температуре 700 – 900°С с образованием закиси-окиси урана: В этом же интервале температур, но в ...
... , анализ которых не может быть осуществлен в условиях аптеки, производится «под наблюдением», т. е. в присутствии провизора-аналитика или провизора-технолога. Концентраты, полуфабрикаты и внутриаптечная заготовка готовятся в асептических условиях и обязательно подвергаются полному химическому контролю. Они хранятся в соответствии с их физико-химическими свойствами и установленными сроками годности ...
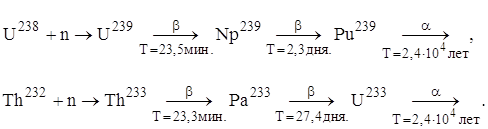
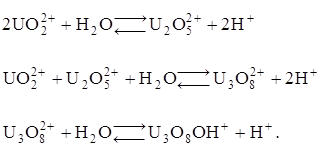
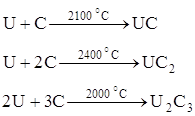

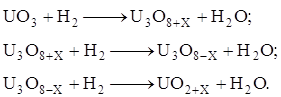
0 комментариев