Навигация
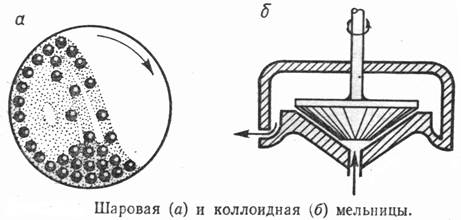
Методы получения дисперсных систем
9. Определить изменение изобарно-изотермического потенциала реакции N2(г) + 2Н2О(ж) = NH4NO2 (ж) и дать заключение о направлении ее протекания при стандартных условиях, если ![]() для Н2О(ж) равна – 237,4 кДж/моль, а для NH4NO2(ж) равна – 115,8 кДж/моль.
для Н2О(ж) равна – 237,4 кДж/моль, а для NH4NO2(ж) равна – 115,8 кДж/моль.
Решение:
![]()
![]() Изменение изобарно-изотермического потенциала меньше 0, следовательно, процесс может протекать самопроизвольно в сторону прямой реакции.
Изменение изобарно-изотермического потенциала меньше 0, следовательно, процесс может протекать самопроизвольно в сторону прямой реакции.
14. Определить молекулярность и порядок химической реакции на конкретных примерах.
Молекулярность реакции определяется минимальным числом молекул, одновременно участвующих в элементарном акте данной реакции. Молекулярность и порядок реакции численно совпадают только для простейших реакций. Для сложных процессов эти характеристики реакции будут отличаться (порядок реакции меньше ее молекулярности). Следовательно, формальное понятие о порядке реакции в большинстве случаев не отражает ее сложного механизма, т.е. наличия нескольких промежуточных элементарных реакций (стадий). Однако знание экспериментального порядка реакции позволяет судить о ее предполагаемом механизме путем сопоставления расчетных и экспериментально наблюдаемых значений величины n. Когда порядок реакции, найденный экспериментально, не соответствует числу моль реагентов, участвующих в реакции, то это говорит о том, что реакция не является элементарным процессом, а протекает по сложному механизму. Для сложного механизма скорость суммарной реакции определяется скоростью наиболее медленной стадии многоступенчатого процесса. Таким образом, если реакция протекает в одну стадию, то порядок ее равен молекулярности; если реакция протекает в несколько стадий, то порядок каждой из стадий реакции равен молекулярности только этой стадии. Следовательно, экспериментальное определение порядка реакции может служить методом изучения ее механизма.
Если для осуществления элементарного акта необходима всего одна частица (молекула), то такая реакция называется мономолекулярной.
Для элементарного процесса с одновременным участием двух частиц реакция будет называться бимолекулярной и т.д.
Например:
![]()
Реакция мономолекулярна, порядок реакции равен 1/3.
С(т) + Н2О(г)![]() СО(г) + Н2 (г)
СО(г) + Н2 (г)
Реакция бимолекулярна, порядок реакции равен 2/2= 1.
![]()
Реакция тримолекулярна, порядок реакции равен 2/3 (из трех молекул реагирующих веществ получают две молекулы продукта реакции).
29. Изменение свободной энергии, сопровождающее химическую реакцию, ее связь с константой равновесия. Расчет теплового эффекта реакции.
Изменение свободной энергии Гиббса![]() , или изменение изобарно-изотермического потенциала - это та максимальная часть энергии системы, которая в данных условиях может превратиться в полезную работу. При
, или изменение изобарно-изотермического потенциала - это та максимальная часть энергии системы, которая в данных условиях может превратиться в полезную работу. При ![]() реакция протекает самопроизвольно.
реакция протекает самопроизвольно.
В соответствии с законом действующих масс для произвольной реакции
а A + b B = c C + d D (1)
уравнение скорости прямой реакции можно записать:
![]() , (2)
, (2)
а для скорости обратной реакции
![]() . (3)
. (3)
По мере протекания реакции (1.33) слева направо концентрации веществ А и В будут уменьшаться и скорость прямой реакции будет падать. С другой стороны, по мере накопления продуктов реакции C и D скорость реакции справа налево будет расти. Наступает момент, когда скорости υ 1 и υ 2 становятся одинаковыми, концентрации всех веществ остаются неизменными, следовательно,
![]() , (4)
, (4)
Откуда Kc = k1 / k2 = ![]() .
.
Постоянная величина Кс, равная отношению констант скоростей прямой и обратной реакций, количественно описывает состояние равновесия через равновесные концентрации исходных веществ и продуктов их взаимодействия (в степени их стехиометрических коэффициентов) и называется константой равновесия. Константа равновесия является постоянной только для данной температуры, т.е. Кс = f (Т). Константу равновесия химической реакции принято выражать отношением, в числителе которого стоит произведение равновесных молярных концентраций продуктов реакции, а в знаменателе – произведение концентраций исходных веществ.
Если компоненты реакции представляют собой смесь идеальных газов, то константа равновесия (Кр) выражается через парциальные давления компонентов:
Kp = ![]() . (5)
. (5)
Или ![]() . (6)
. (6)
Из уравнения (6) следует, что Кр = Кс при условии, если реакция идет без изменения числа моль в газовой фазе, т.е. когда (с + d) = (a + b).
Если реакция (1) протекает самопроизвольно при постоянных Р и Т или V и Т, то значения G и этой реакции можно получить из уравнения:
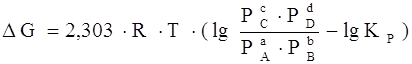 , (7)
, (7)
где Р А, Р В, Р С, РD – парциальные давления исходных веществ и продуктов реакции.
Уравнение (7) называются уравнениями изотермы химической реакции Вант-Гоффа. Это соотношение позволяет рассчитать значения G и F реакции, определить ее направление при различных концентрациях исходных веществ.
Необходимо отметить, что как для газовых систем, так и для растворов, при участии в реакции твердых тел (т.е. для гетерогенных систем) концентрация твердой фазы не входит в выражение для константы равновесия, поскольку эта концентрация практически постоянна. Так, для реакции
2 СО (г) = СО 2 (г) + С (т)
константа равновесия записывается в виде
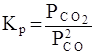 .
.
Зависимость константы равновесия от температуры (для температуры Т2 относительно температуры Т1) выражается следующим уравнением Вант-Гоффа:
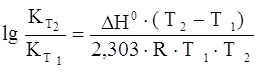 , (8)
, (8)
гдеН0 – тепловой эффект реакции.
Похожие работы
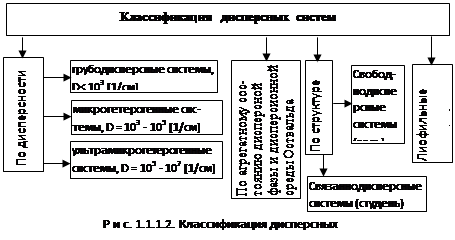
... 103 [1/см] (рис. 1.1.1.3); б) микрогетерогенные системы, для них D = 103 - 105 [1/см]; в) ультрамикрогетерогенные системы, для них D = 105 - 107 [1/см]. 2. По агрегатному состоянию дисперсной фазы и дисперсионной среды. Эта классификация была предложена Оствальдом (см. табл. 1.1.1.1). 3. По структуре дисперсные системы различают: 1) свободные дисперсные системы, когда ...
... , чтобы подчеркнуть, что дисперсной средой является жидкость. Если дисперсной средой является вода, то такие золи называют гидрозолями, а если органическая жидкость – органозолями. Дисперсные системы могут быть свободнодисперсными и связнодисперсными в зависимости от отсутствия или наличия взаимодействия между частицами дисперсной фазы. К свободнодисперсным системам относятся аэрозоли, ...
... , и мел осядет на дно стакана, жидкость станет прозрачной. Под действием силы тяжести частицы твердого вещества седиментируют. Это aw кое доказательство того, что наша система получилась Грубодисперсной. Получить дисперсную систему карбонат кальция-вода можно химическим способом: пропусканием углекислого газа через известковую воду (раствор гидроксид кальция). При этом раствор мутнеет. Полученная ...
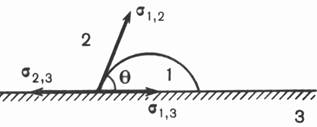
... фазы от молекул другой фазы. Адгезия сопровождается уменьшением поверхностной энергии (при совмещении разных фаз энергия Гиббса системы уменьшается на величину работы адгезии): Wc = - DG. Для общего описания дисперсных систем обычно используют понятие дисперсность, характерезующее степень измельченности дисперсной фазы. Дисперсность выражается ...



0 комментариев