Навигация
Разделяя переменные, получаем
4.3.8.4. Разделяя переменные, получаем
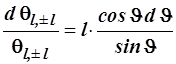 (4.115)
(4.115)
Учтём что ![]() ,
,
![]() (4.116)
(4.116)
Интегрирование уравнения (4.116) даёт
![]() (4.117)
(4.117)
где![]() – постоянная интегрирования, определяемая из условия нормировки. Окончательно получаем формулу для функции
– постоянная интегрирования, определяемая из условия нормировки. Окончательно получаем формулу для функции
![]() (4.118)
(4.118)
4.3.8.5.Формула (4.118) дает лишь предельные выражения волновых функций ![]() , отвечающие максимальному и минимальному значениям квантового числа m, а именно
, отвечающие максимальному и минимальному значениям квантового числа m, а именно ![]() и
и ![]() , или что то же самое
, или что то же самое ![]() . Все волновые функции, соответствующие промежуточным значениям
. Все волновые функции, соответствующие промежуточным значениям ![]() очень просто получаются последовательным действием операторов
очень просто получаются последовательным действием операторов ![]() с точностью до нормировочных множителей, которые могут быть рассчитаны в каждом конкретном случае
с точностью до нормировочных множителей, которые могут быть рассчитаны в каждом конкретном случае
4.3.8.6.Отметим, что мы не ставим перед собой и перед читателем задачу вывода общей формулы сферических волновых функций. Это связано, с одной стороны, с тем, что она обязательно покажется слишком перегруженной индексами и коэффициентами, к которым удобнее привыкать постепенно. С другой стороны, для практических целей редко требуются функции с большими значениями квантового числа l. В химическом обиходе встречается состояния с l = 0, 1, 2, 3, поэтому ограничимся этими значениями, (их символы см. в табл. 4.5 ).
4.3.8.7. Итак, нас будут интересовать s–, p–, d–, f– орбитали жесткого ротатора. Запишем соответствующие исходные функции ![]() и
и ![]() , с точностью до постоянного множителя:
, с точностью до постоянного множителя:
для s-состояния ![]() и
и 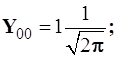
для p- состояния ![]() и
и ![]()
для d- состояния ![]() и
и ![]()
для f- состояния ![]() и
и ![]()
4.3.8.8.Орбиталь s –типа – лишь одна и волновая пункция ![]() требует только нормировки. Поскольку сомножитель
требует только нормировки. Поскольку сомножитель 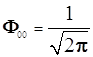 уже нормирован, достаточно пронормировать функцию
уже нормирован, достаточно пронормировать функцию ![]() . Выделяя из элемента конфигурационного пространства
. Выделяя из элемента конфигурационного пространства ![]() (см. рис 4.3) все сомножители, определенные на переменной
(см. рис 4.3) все сомножители, определенные на переменной ![]() , получаем
, получаем
![]()
и, соответственно, нормировочное соотношение имеет вид
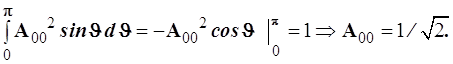 (4.119)
(4.119)
Во всех дальнейших преобразованиях следующих двух разделов будем опускать постоянные численные коэффициенты перед волновыми функциями, получающимися в результате операций сдвигов состояний над исходными функциями ![]() – степенями синусоиды
– степенями синусоиды ![]() .
.
4.3.8.9. Квантовое число l=1 порождает три р-функции с m=1, 0, -1 т.е. орбитали с ![]() Двум из них с
Двум из них с ![]() отвечает
отвечает ![]() Нормировочный множитель находим из соотношения
Нормировочный множитель находим из соотношения
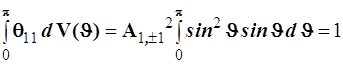 .
.
Откуда следует: ![]() (4.120)
(4.120)
Функцию ![]() , необходимую для полного набора р-орбиталей, можно найти, сдвигая
, необходимую для полного набора р-орбиталей, можно найти, сдвигая ![]() вниз или
вниз или ![]() вверх на одно состояние
вверх на одно состояние
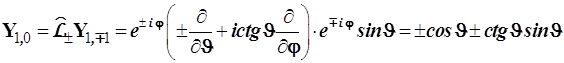
Определим нормировочный множитель ![]() для
для ![]()
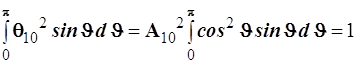
Интегрируя с помощью подстановки ![]() и, следовательно полагая,
и, следовательно полагая, ![]() получаем
получаем
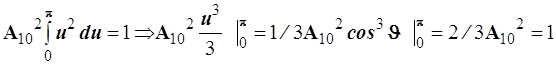 , т.е.
, т.е. ![]()
4.3.8.10. Далее получим последовательно d-орбитали, отвечающие набору ![]() . Соответственно
. Соответственно
![]()
![]() (4.121)
(4.121)
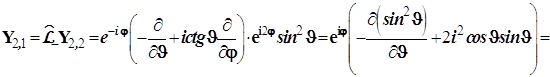
![]() (4.121)
(4.121)
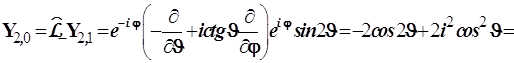
![]() (4.122)
(4.122)
Отсюда получаются d-функции
![]() ;
; ![]() ;
;
![]() .
.
Величины ![]() ;
;![]() ;
;![]() представлены в таблице 4.6.
представлены в таблице 4.6.
Похожие работы
т вследствие уменьшения момента инерции при сохранении момента вращения. Тут мы и убеждаемся наглядно, что чем меньше момент инерции, тем выше угловая скорость и, как следствие, короче период вращения, обратно пропорциональный ей. 3. Что такое радиоактивность (естественная и искусственная)? Как использование явлений радиоактивности позволило осуществить мечту алхимиков? Радиоактивность (от ...
... физиологическом механизме внимания также и вегетативных центров. Основные виды внимания При изучении внимания необходимо различать два основных уровня или вида его и ряд его свойств или сторон. Основными видами внимания являются непроизвольное и так называемое произвольное внимание. Непроизвольное внимание связано с рефлекторными установками. Оно устанавливается и поддерживается независимо ...
... этими двумя ветвями так велико, что его невозможно объяснить ошибками в оценке энергии Eg или потерей подпороговых g квантов, или статистическими флуктуациями. Результаты Поперечные импульсы для обоих взаимодействий (с большим и малым PT) были рассчитаны методом факториальных моментов. Из-за удобства и подобных свойств между поперечным импульсом и псевдоскоростью в вычислениях ,была ...
... полуцелые. Существуют правила отбора квантовых чисел атома: ΔL = ± 1,ΔS = 0,ΔJ = 0, ± 1 Магнитный момент атома Как уже говорилось ранее, орбитальный и магнитный моменты электрона связаны гиромагнитным отношением: . Экспериментально было доказано, что для механического и магнитного орбитальных моментов атома выполняется аналогичное соотношение . Подставляя , где L – ...


0 комментариев