Навигация
Смешанные фосфаты лития и переходных металлов
1.2. Смешанные фосфаты лития и переходных металлов
Двойные фосфаты, имеющие общую формулу LiMPO4 (где M = Mn, Fe, Co, Ni), изоструктурны оливину - силикату магния и железа (Mg,Fe)2SiO4.
Таблица 1Параметры решетки и разрядные характеристики соединений LiMPO4 [6- 9]
| M | a, Å | b, Å | c, Å | U, В | Емкость, А*час/кг |
| Mn | 10,45 | 6,11 | 4,75 | 4,1 | 140 |
| Fe | 10,31 | 6,00 | 4,69 | 4,3 | 148 |
| Co | 10,20 | 5,92 | 4,68 | 4,8 | 86 |
| Ni | 10,20 | 5,92 | 4,68 |
Фосфаты LiMPO4, где M = Mn, Co, Ni получены в ходе взаимодействия карбоната лития, оксида металла (MO или MnO2) и дигидрофосфата аммония - (NH4)2HPO4 при температуре 350 °C, которую затем повышали до 780 °C и выдерживали 18 часов на воздухе [6]. LiFePO4 получен аналогично, но в инертной атмосфере [10].
1.3. Смешанные фторидофосфаты щелочных и переходных металлов
Просмотр реферативных журналов, баз данных PDF-2 и ICSD обнаружил только три фазы формульного типа A+2MPO4F, из них с литием только одна: Li2NiPO4F [11]. Известны также Na2MnPO4F [12], Na2MgPO4F [13], Na4,6FeP2O8,6F0,4 [14, 15, 16, 17].
Структура Li2NiPO4F (рис. 1) определена рентгенографически на монокристалле [11]. Она относится к ромбической сингонии (пространственная группа Pnma, параметры a = 10.473(3) Å, b = 6.2887(8) Å, c = 10.846(1) Å, Z=8). В структуре можно выделить рутиловые цепи из октаэдров NiO4F2, соединенных ребрами, вытянутые вдоль оси y. Эти цепи соединены в двух остальных измерениях тетраэдрами PO4. В пустотах каркаса размещаются катионы лития. Половина их находится в уплощенных тетраэдрах из четырех атомов кислорода, четверть – в квадратных пирамидах из 4 O + 1 F и еще одна четверть в сильно асимметричной координации, где трудно сделать однозначный выбор между КЧ 4,5,6. Достаточно короткие (до 3,21 Å) расстояния Li-Li соединяют все позиции лития в двумерную сеть в плоскости y0z (рис. 2). Это позволяет ожидать достаточно высокую подвижность ионов лития в каркасе и возможность их извлечения с окислением никеля и сохранением исходного каркаса:
Li2Ni2+PO4F ® LiNi3+PO4F + Li+ + e ® Ni4+PO4F + 2 Li+ + 2 e
Но сведений о таких свойствах Li2NiPO4F в литературе не обнаружено. Можно было бы ожидать существование аналогичных фаз, содержащих на месте никеля другие катионы близкого размера с переменной степенью окисления (табл. 2), но никаких сведений о них в литературе также не обнаружено.
Таблица 2
Эффективные кристаллохимические радиусы [18] некоторых двухзарядных катионов в октаэдрической координации в высокоспиновом состоянии
| M | Mn2+ | Fe2+ | Co2+ | Ni2+ |
| VIR, Å | 0,97 | 0,92 | 0,885 | 0,83 |
В данной работе поставлена задача получения новых фаз состава Li2MPO4F, где M = Mn, Fe, Co, и исследования возможности окислительного извлечения лития из них и из ранее известного никелевого соединения. Предполагалось, что за счет удвоенного содержания лития можно будет повысить емкость электродного материала по сравнению с фазами типа оливина (табл. 3).
Таблица 3Теоретические удельные емкости некоторых известных и предполагаемых материалов положительного электрода литий-ионного аккумулятора
| Восстановленная форма | Окисленная форма | Емкость, А*час/кг |
| LiMO2 (M = Co, Ni) | Li0.5MO2 | 140 |
| LiMPO4 (M = Mn, Fe, Co, Ni) | MPO4 | 170 |
| Li2MPO4F (M = Mn, Fe, Co, Ni) | LiMPO4F | 144 |
| MPO4F | 288 |
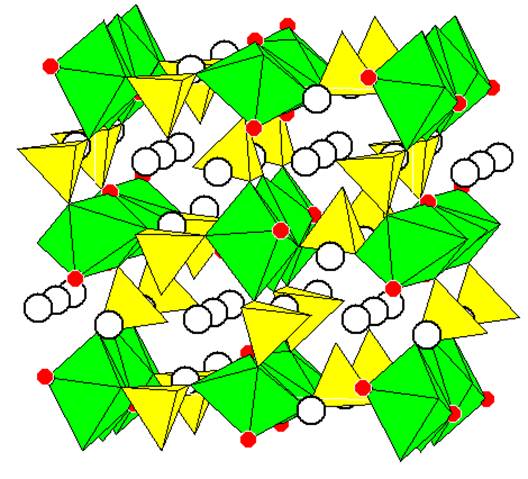
Полиэдрическое изображение кристаллической структуры Li2NiPO4F [10]
Зеленым цветом показаны октаэдры вокруг катионов никеля, желтым – тетраэдры PO4, красным – ионы фтора (в остальных вершинах – кислород), светлыми кружками показаны ионы лития.
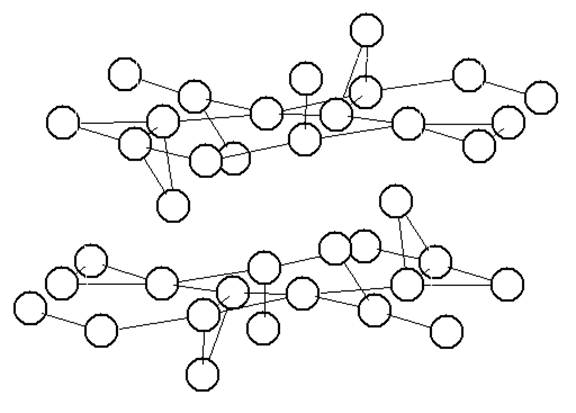
Система позиций лития в структуре Li2NiPO4F. Соединены позиции, отстоящие друг от друга не более чем на 3,21 Å.
0 комментариев