Навигация
X 1 = 0; ® X3+2-3X=0; ® X1,2,3= -2; +1; +1; ® E1,2,3=+2
1 X 1 = 0; ® X3+2-3X=0; ® X1,2,3= -2; +1; +1; ® E1,2,3=+2
1 X два решения одинаковы – уровень дважды вырожден
Молекулярные орбитали дважды-вырожденного уровня треугольного цикла. Базисные АО =2p(C)
j1=(p1+p2+p3)/31/2 невырожденный уровень AСвязывающий основной
j2=(p1+p2-2p3)/61/2
j3=(p1-p2)/21/2 дважды вырожденный уровень EРазрыхляющий
О номенклатуре МО. Символика МО:
-Порядковый номер уровня (энергетическое квантовое число)
-Символы вырожденности a,b,e,t
-Символ разрыхления
-Символы чётности g,u
-Символы симметрии относительно плоскости .
Молекулярные ионы H3+; D3+; H3*; D3* (Томсен, Герцберг) построены подобно C3H3. Замена базиса: =2pz(C) ®=1s(H) даёт аналогичные МО циклов C3H3 ®H3.
![]() j1=(s1+s2+s3)/31/2 невырожденный уровень A Связывающий основной j2=(s1+s2-2s3)/61/2
j1=(s1+s2+s3)/31/2 невырожденный уровень A Связывающий основной j2=(s1+s2-2s3)/61/2
j3=(s1-s2)/21/2 дважды вырожденный уровень E Разрыхляющий
Уровни H3+ ab initio-базис 6-31G**(большой базис) E EМО
E (1A2’) = 33.238800 эВ
E (2E’) = 19.651634 эВ
E (2A1’) = 7.573212 эВ
E (1E’) = - 4.786128 эВ
E (1A1’) = -33.239368 эВ
Задача может быть решена и чисто симметрийным способом. Но в нашем курсе это не доступно. Основное: Треугольный цикл является удобной заготовкой для построения более сложных молекул с треугольной симметрией. Эквивалентные атомы (лиганды) рассматриваются в таких случаях совместно, а вид их коллективных орбиталей тот же, что и у изолированного цикла
![]() jA =(s1+s2+s3)/31/2 невырожденный уровень A
jA =(s1+s2+s3)/31/2 невырожденный уровень A
![]() jE’ =(s1+s2-2s3)/61/2 дважды вырожденному уровню E
jE’ =(s1+s2-2s3)/61/2 дважды вырожденному уровню E
jE” =(s1-s2)/21/2 соответствуют 2 орбитали
Пример (кратко о бутадиене):
Корни ВД и уровни -МО: X1,2,3,4= ± (1 ± 51/2)/2.
(E1,4, E2,3)=(±=±).
Матрица нормированных составов МО построена всего из двух чисел:
(0.3717; 0.6015)
Профильные диаграммы амплитуд МО.
Уровни. Конфигурация. Числа заполнения.
Минимальное понятие о топологии молекулярной структуры: центры-атомы, рёбра-связи. Индексы электронной структуры:
Атомные: Заселённости АО парциальные и полные.
Для связей: Заселённости связей (порядки связей) парциальные и полные. Полные порядки пи-связи равны (2´2´ab; 2´(a2-b2);)=(0.894; 0.263) » (0.9; 0.3) Хюккелевские порядки связей. Порядок связи и длина (корреляия).
| |CC|, Ao | pp | Молекула | Примечание |
| 1.54 | 0 | Этан | |
| 1.45 | 0.5 | Графит | Экстрапол. по – C< |
| 1.397 | 2/3 | Бензол | |
| 1.33 | 1 | Этен | |
| 1.22 | 2 | Этин |
Свободные валентности
Индекс свободной валентности (у бутадиена): F1,4=31/2-0.9»0.8; F2,3=31/2-0.9-0.3»0.5.
Альтернантные УВ и две теоремы об АУВ: 1) Уровни. 2) Заселённости АО. Сопряжение и Ароматичность. Алкены. Арены. Алкины. Длина связи CC.
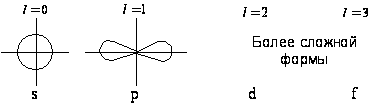
Двухатомные гомоядерные молекулы. Гибридизация орбиталей: -модельный случай у плоского ротатора. Кривая зависимости ПИ(Z) для 2s-2p АО и гибридизация (s±p)-АО у атомов элементов 2-го периода. Пиктограммы гибридных АО.
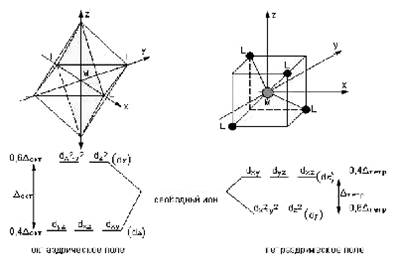
Две корреляционные схемы уровней АО-МО у элементов 2-го периода
(атомы и 2-х атомные молекулы).
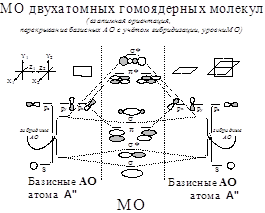
Схема А: Вариант с гибридизацией АО,
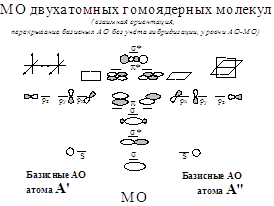
Схема Б: Вариант без гибридизации АО.
Последовательности уровней МО:
Схема А:1g<1u<2g<2u<1u<3g<1g<3u
Схема Б: 1g<1u<2g<2u<3g<1u<1g<3u
Конфигурации и параметры 2-х атомных молекул и молекулярных ионов.
Дистанции E(2s)-E(2p) у элементов 2-го Периода Системы Менделеева
|
| H | Li | Be | B | C | N | O | F | Ne |
| Z | 1 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 1-й ПИ, эВ | 13.62 | 5.377 | 9.281 | 8.28 | 11.23 | 14.48 | 13.57 | 17.37 | 21.509 |
| ЭС, эВ | 0.747 | 0.82 | -0.19 | 0.38 | 2.1;1.12 | 0.05 | 1.465 | 3.58;3.50 | - |
| E2s2p, эВ | теор. | 1.85 | 3.36 | 5.76 | 8.77 | 12.39 | 16.53 | 21.54 |
|
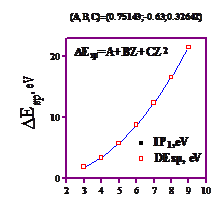
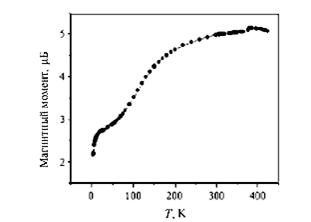
График этой зависимости имеет вид гладкой функции.
Она очень неплохо аппроксимируется параболой: E=A+BZ+CZ2
|
| ||||
| ||||
ПРОБЛЕМЫ: Связь и разрыхление. Длины связей. Энергии связи. Силовые постоянные собственных колебаний. Устойчивость конфигураций. Баланс «связь-разрыхление» и кратность связи по Герцбергу: PГ=(1/2)´ (n-n*).
Свойства гомоядерных двухатомных молекул элементов 2-го периода Системы Менделеева
|
| PГ | R0, Ао | D, эВ | D, кДж/моль | Терм | k´10-5, дн/см | k´10-2, н/м | |
| H2+ | (1g)1 | 1/2 | 1.058 | 2.798 | 268.19 | 2g+ | 1.56 | 1.56 |
| H2 | (1g)2 | 1 | 0.742 | 4.4746 | 432 | 1g+ | 5.60 | 5.60 |
| He2+ | (1g) 2(1u)1 | 1/2 | 1.080 | 2.5 | 241 | 3g+ | 3.13 | 3.13 |
| He2 | (1g)2(1u)2 | 0 | - | - | 1g+ | - | - | |
| Li2 | [He2](2g) 2 | 1 | 2.673 | 1.14 | 110 | 1g+ | 0.25 | 0.25 |
| Be2 | [He2](2g) 2(2u)2 | 0 | - | - | 1g+ | - | - | |
| B2 | [Be2] (1u) 2 | 1 | 1.589 | 3.0±0.5 | 289.5 | 3g- | 3.60 | 3.60 |
| C2 | [Be2] (1u)3(3g)1 | 2 | 1.242 | 6.36 | 613.8 | 3u | 9.55 | 9.55 |
| N2+ | [Be2] (1u)4(3g)1 | 5/2 | 1.116 | 8.86 | 855 | 2g+ | 20.1 | 20.1 |
| N2 | [Be2] (1u)4(3g)2 | 3 | 1.094 | 9.902 | 955.6 | 1g+ | 23.1 | 23.1 |
| O2+ | [Be2] (3g)2(1u)4(1g)1 | 5/2 | 1.1227 | 6.77 | 653.3 | 2g | 16.6 | 16.6 |
| O2 | [Be2] (3g)2(1u)4(1g)2 | 2 | 1.2074 | 5.213 | 503 | 3g- | 11.8 | 11.8 |
| F2 | [Be2] (1u)4(3g)2(1g)4 | 1 | 1.435 | 1.34 | 129.3 | 1g+ | 4.45 | 4.45 |
Изоэлектронность химических структур. Принцип изоэлектронности качественный.
Его можно сформулировать в виде : «Изоэлектронные структуры обладают близкими электронными свойствами. Их спектры МО подобны».
Физические свойства веществ, образованных изоэлектронными частицами могут заметно различаться Изоэлектронные двухатомные гетероядерные молекулы.
Роль электроотрицательности и гибридизации. 10-электронные оболочки и конфигурации. Молекула CO.
Уровни МО и конфигурация.
Уровни МО молекулы СО в различных приближениях метода МО ЛКАО
| МО | Ab initio, эВ | PM3, эВ | MNDO, эВ | CNDO, эВ |
|
| 1 | -562.513672 |
|
|
|
|
| 2 | -309.039368 |
|
|
|
|
| 3 | -41.615940 | -40.028755 | -44. 932140 | -43.969006 |
|
| 4 | -21.708000 | -20.684595 | -20.990582 | -24.385288 |
|
| 1 | -17.394398 | -16.153131 | -15.736658 | -20.043474 |
|
| 5n | -14.849416 | -13.027870 | -13.426928 | -17.534723 |
|
| 2 | 4.576420 | 1.000063 | 1.155621 | 4.463773 |
|
| 6 | 11.192607 | 6.081843 | 6.802823 | 12.847558 |
|
| 3 | 19.956134 |
|
|
|
|
| 7 | 21.060755 |
|
|
|
|
Свойства изоэлектронных молекул
|
| BF | N2 | CO | NO+ |
| CN- | ·NO |
| D, эВ | 8.03 | 9.90 | 11.14 | 11.52 | ® (N+, O) |
| 6.643 |
|
|
|
|
| 10.72 | ® (N, O+) |
|
|
| R0, Ao | 1.26 | 1.116 | 1.1282 |
|
|
| 1.151 |
| , D |
|
| -0.112 |
|
|
|
|
|
|
|
|
|
|
|
| (*) |
(*) димер N2O2 не существует, хотя у молекулы ·NO имеется неспаренный электрон, но он находится на разрыхляющей МО.
Физические свойства
1 дебай = 10-18 см ед.Q в
СГСЕ= (1/3) ´ 10-29 Кл´м (в СИ)
|
Похожие работы
... с кислородом, восстановлением - отнятие кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций было распространено на реакции, в которых кислород не участвует. В неорганической химии окислительно-восстановительные реакции (ОВР) формально могут рассматриваться как перемещение электронов от атома одного реагента (восстановителя) к атому другого ( ...
... окисления +2. Железо образует достаточно большое количество комплексных соединений. Наиболее характерным для железа (II) и железа (III) является координационное число (КЧ) = 6 (реже 4 и 5). Способность к комплексообразованию более характерна для железа в С/О = +3. Рассмотрим некоторые комплексы железа и методы их получения. 1.3.1 Гексацианоферраты(II, III) Для железа (II) очень устойчивы ...
... (например, АЭС), с сельским хозяйством, с обезвреживанием промышленных отходов, охраной природы и др. История неорг. химии тесно связана с общей историей химии, а вместе с ней – с историей естествознания и историей человеческой цивилизации. Этапными для развития неорг. химии явились работы И. Берцелиуса, который в 1814 опубликовал таблицу атомных масс. А. Авогадро и Ж. Гей-Люссак открыли ...
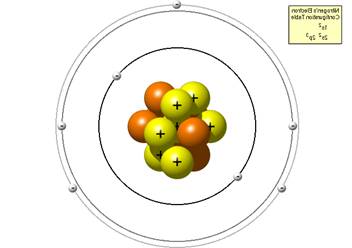
... увеличением порядкого номера. Эти элементы имеют 5 валентных электронов на наружном слое атома. Однако способность к присоединению электронов у них выражена значительно слабее, чем у элементов 7 и 6 группы [12,14]. Свойства азота. Изотопы, атом, молекула Строение ядра и электронных оболочек. В природе существуют два стабильных изотопа азота: с массовым числом 14 ( содержит 7 протонов и 7 ...
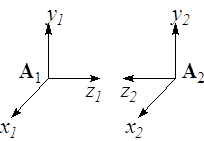

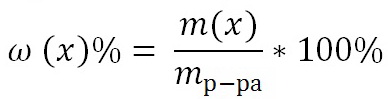


0 комментариев