Содержание
Введение
Катаболизм гема: образование желчных пигментов
Поглощение билирубина печенью
Конъюгация билирубина
Секреция билирубина в желчь
Метаболизм билирубина в кишечнике
Гипебилирубинемии
Неконъюгированная гипербилирубинемия Конъюгированная гипербилирубинемия Билирубиновая энцефалопатия Уробилиноген в мочеСПИСОК ЛИТЕРАТУРЫ
Введение
Сведения по биохимии порфиринов и гема являются основой, необходимой для понимания различных функций гемопротеинов в организме (транспорт кислорода, транспорт электронов, метаболизм лекарственных соединений и т.д.). Порфирии – это группа заболеваний, обусловленных нарушениями биосинтеза различных порфиринов. Эти заболевания встречаются сравнительно редко, но практикующие врачи должны о них знать; больные порфирией могут обратиться к дерматологам, гепатологам и психиаторам; сравнительно часто встречается желтуха, обусловленная повышением содержания в плазме крови билирубина. Это повышение может быть вызвано либо чрезмерным образованием билирубина, либо нарушением его экскреции; оно наблюдается при многих заболеваниях, от вирусного гепатита до рака поджелудочной железы.
КАТАБОЛИЗМ ГЕМА: ОБРАЗОВАНИЕ ЖЕЛЧНЫХ ПИГМЕНТОВ
При физиологических условиях в организме взрослого человека разрушается 1—2108 эритроцитов в час. Таким образом, в течение суток у человека массой 70 кг обновляется приблизительно 6 г гемоглобина. При разрушении гемоглобина его белковая часть (глобин) может быть использована как таковая или после гидролиза в форме составляющих ее аминокислот; железо гема включается в общий пул железа и также снова используется. Вместе с тем свободная от железа порфириновая часть гема обязательно деградирует; это в основном происходит в ретикулоэндотелиальных клетках печени, селезенки и костного мозга. Катаболизм гема, освобожденного из любых гемовых белков, осуществляется в микросомальной фракции ретикулоэндотелиальных клеток сложной ферментной системой – гем-оксигеназой. К моменту поступления гема из гемовых белков в гем-оксигеназную систему железо обычно окисляется в ферри-форму (гем превращается в гемин); гемин может легко связываться с альбумином с образованием метгемальбумина. Гем-оксигеназная система индуцируется субстратом. Она локализована около микросомальной системы транспорта электронов. Гемин восстанавливается в ферро-форму с помощью NADPH; далее при участии NADPH кислород присоединяется к а-метенильному мостику между пиррольными кольцами I и II. Ферро-форма железа снова окисляется в ферри-форму. При последующем присоединении кислорода происходит освобождение ферри-иона, выделение молекулы оксида углерода (II) и образование в результате раскрытия тетрапиррольного кольца эквимолярного количества биливердина IX - a. В этой реакции сам гем участвует в роли катализатора.
У птиц и земноводных зеленый пигмент биливердин IX - a экскретируется из организма; у млекопитающих растворимый фермент биливердинредуктаза катализирует восстановление метенильного мостика между пирролами III и IV в метиленовую группу, в результате образуется желтый пигмент билирубин IX - a. По расчету из 1 г гемоглобина образуется 35 мг билирубина. Суточное образование билирубина у взрослого человека составляет приблизительно 250—350 мг.
Химическое превращение гема в билирубин ретикулоэндотелиальными клетками можно наблюдать in vivo: в гематоме обусловленный гемом пурпурный цвет медленно переходит в желтый цвет билирубина.
Дальнейшей метаболизм билирубина в основном происходит в печени. Он складывается из трех процессов: 1) поглощение билирубина паренхимальными клетками печени; 2) конъюгация билирубина в гладком эндоплазматическом ретикулуме и 3) секреция билирубина из эндоплазматического ретикулума в желчь. Рассмотрим каждый из процессов в отдельности.
Поглощение билирубина печенью
Билирубин слаборастворим в плазме и воде; в плазме он специфически связывается с альбумином. Каждая молекула альбумина имеет, по-видимому, два центра связывания билирубина — высоко- и низкоаффинный. В 100 мл плазмы может содержаться 25 мг билирубина, прочно связанного с альбумином по его высокоаффинному центру. «Избыточный» билирубин связывается с альбумином менее прочно; он легко отделяется от альбумина, диффундируя в ткани. Ряд соединений — антибиотики и некоторые другие лекарственные вещества — конкурируют с билирубином за высокоаффинный центр альбумина. Эти соединения могут вытеснять билирубин из комплекса с альбумином и проявляют значительное клиническое действие.
В печени происходит переход билирубина от альбумина на синусоидальную поверхность гепатоцитов при участии насыщаемой системы переноса, в функционировании которой участвует некий переносчик. Эта система облегченного транспорта имеет очень большую емкость и даже при патологических условиях не лимитирует скорость метаболизма билирубина. Поскольку система облегченного транспорта обеспечивает установление равновесия билирубина по обе стороны синусоидальной мембраны гепатоцита, поглощение билирубина зависит от его потребления в последующих метаболических процессах.
Конъюгация билирубина
В печени к билирубину присоединяются полярные группы и он переходит в водорастворимую форму, которая секретируется в желчь. Процесс, обеспечивающий повышение растворимости в воде (т. е. повышение полярности) билирубина, называется конъюгацией. Этот процесс, по крайней мере на начальных стадиях, протекает в гладком эндоплазматическом ретикулуме и осуществляется специальным набором ферментов. У млекопитающих билирубин секретируется в желчь преимущественно в форме билирубиндиглюкуронида (рис. 1).
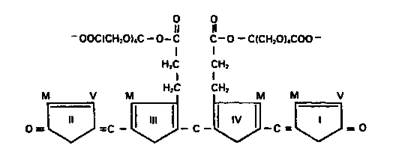
Рисунок 1 - Структура билирубиндиклюкуронида (конъюгированный «прямой» билирубин).
Глюкуроновая кислота присоединяется эфирной связью к двум группам пропионовой кислоты с образованием ацилглюкуронида (М – метильная группа, V – винильная)
Сначала происходит образование билирубинмоноглюкуронида, которое катализируется UDP-глюкуронилтрансферазой — ферментом, присутствующим в гладком эндоплазматическом ретикулуме и состоящим, вероятно, из нескольких компонентов. Катализируемая реакция представлена на рис. 2.
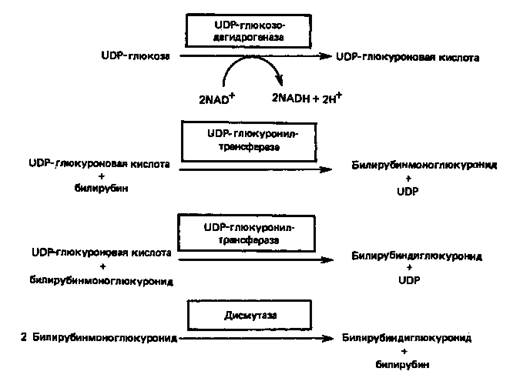
Рисунок 2 - Конъюгирование билирубина с глюкуроновой кислотой
Донором глюкуроната является UDP-глюкуроновая кислота, образующаяся из UDP-глюкозы.
Она протекает главным образом в печени, а также в почках и слизистой кишечника. При нарушении метаболизма билирубина его конъюгаты находятся в сыворотке преимущественно в форме моноглюку-ронидов.
Образование диглюкуронида билирубина может происходить в канальцах мембраны гепатоцитов при участии UDP-глюкуронилтрансферазы, подобной рассмотренной выше (рис. 1) или другого фермента дисмутазы, которая катализирует превращение двух молекул билирубинмоноглюкуронида в молекулу билирубиндиглю-куронида и молекулу свободного билирубина (рис. 2). Система конъюгации билирубина будет рассматриваться ниже в связи с наследственными нарушениями ее работы.
Активность UDP-глюкуронилтрансферазы может индуцироваться рядом используемых в клинике лекарств, в частности фенобарбиталом.
Есть данные, что еще в древности Митридат систематически принимал небольшие дозы ядов, чтобы избежать острого отравления. "Эффект Митридата" основан на индукции определенных защитных систем: фенобарбитал индуцирует систему цитохрома Р-450, глутатион- и УДФ-глюкуронилтрансферазы и эпоксидгидролазы; дибунол (бутилокситолуол) и бутилоксианизол - эти же трансферазы и ферменты синтеза глутатиона; противораковые лекарства - Р-гликопротеин и синтез глутатиона; металлы вызывают накопление обоих видов связывающих их SH-веществ. В результате возрастает устойчивость клеток и организма к ядам и лекарствам. Так, снотворное действие фенобарбитала постепенно все больше снижается. Курсовое введение фенобарбитала у новорожденных увеличивает связывание и, следовательно, обезвреживание свободного билирубина при наследственном дефекте этой системы или гемолитической желтухе.
Секреция билирубина в желчь
Секреция конъюгированного билирубина в желчь идет против весьма высокого градиента концентрации и должна осуществляться с помощью механизма активного транспорта. Активный транспорт является, вероятно, скорость-лимитирующей стадией всего процесса метаболизма билирубина в печени. Транспорт конъюгированного билирубина из печени в желчь индуцируется теми же лекарствами, которые способны индуцировать конъюгацию билирубина. Таким образом, системы конъюгации билирубина и его вывода из гепатоцитов работают как единый функционально координируемый механизм.
При физиологических условиях практически весь секретируемый в желчь билирубин (свыше 97%) находится в конъюгированной форме. Только после светотерапии заметные количества неконъюгированного билирубина могут быть обнаружены в желчи.
В печени имеются многочисленные системы секреции в желчь природных и синтетических лекарственных соединений после их метаболизма. Некоторые из этих систем используются также билиру-биндиглюкуронидами.
МЕТАБОЛИЗМ БИЛИРУБИНА В КИШЕЧНИКЕ
После того как билирубин достигает области подвздошной и толстой кишок, глюкурониды гидролизуются специфическими бактериальными ферментами (р-глюкуронидазами); далее кишечная микрофлора восстанавливает пигмент с образованием группы бесцветных тетрапиррольных соединений, называемых уробилиногенами.
В подвздошной и толстой кишках небольшая часть уробилиногенов снова всасывается и попадает в печень, т.е. осуществляется внутрипеченочный уробилиногеновый цикл. При патологических состояниях, например при накоплении избыточных количеств желчных пигментов или при заболеваниях печени, нарушающих работу внутрипеченочного цикла, уробилиноген может экскретироваться с мочой.
В норме большая часть бесцветных уробилиногенов, образующихся в толстой кишке под действием кишечной микрофлоры, окисляется в уробилины (окрашенные соединения) и удаляется с фекалиями (рис. 2). Наблюдаемое потемнение последних на воздухе является следствием окисления оставшихся уробилиногенов в уробилины.
ГИПЕРБИЛИРУБИНЕМИИ
В тех случаях, когда содержание билирубина в крови превышает 1 мг/100 мл (17,1 мкмольл -1), говорят о состоянии гипербилирубинемии. Гипербилирубинемия может быть следствием образования билирубина в большем количестве, чем то, которое нормальная печень может экскретировать, или же следствием повреждений печени, нарушающих экскрецию билирубина в нормальных количествах. Помимо повреждений самой печени к развитию гипербилирубинемии приводит закупорка желчевыводящих протоков печени, препятствующая выделению билирубина. Во всех этих ситуациях билирубин накапливается в крови и по достижении определенных концентраций диффундирует в ткани, окрашивая их в желтый цвет. Это состояние называют желтухой. При клиническом обследовании больных желтухой ценную информацию дает определение содержания билирубина в сыворотке. Метод количественного анализа билирубина в сыворотке был впервые предложен Ван ден Бергом на основе разработанного Эрлихом метода определения содержания билирубина в моче. Реакция Эрлиха основана на использовании диазосульфаниловой кислоты (диазореа-гент Эрлиха), образующей при соединении с билирубином красновато-пурпурное азосоединение. В первоначальной методике Эрлиха использовался метанол, в котором растворим и билирубин, и диазореагент. Ван ден Берг при анализе желчи пациента на содержание желчного пигмента случайно не добавил метанол и с удивлением обнаружил, что окрашивание идет «прямым» путем и без метанола. Впоследствии эту форму билирубина, которая способна вступать в реакцию без добавления метанола, назвали формой, определяемой в «прямой реакции». Такую же прямую реакцию затем обнаружили в сыворотке больных желтухой, вызванной закупоркой желчных протоков. Однако для обнаружения билирубина в нормальной сыворотке все-таки необходимо добавлять метанол; то же относится к анализу на избыточное содержание билирубина в сыворотке при гемолитической желтухе, не связанной с закупоркой желчных протоков. Ту форма билирубина, которая дает реакцию только после добавления метанола, назвали формой, определяемой в «непрямой реакции».
В настоящее время известно, что «непрямой» билирубин— это «свободный» (неконъюгированный) билирубин, транспортируемый в печень из ретикулоэндотелиальных тканей, где он образуется в результате распада гемопорфиринов. Поскольку эта форма билирубина нерастворима в воде, для ее взаимодействия с диазореагентом необходимо добавление метанола. В печени происходит конъюгирование билирубина с глюкуроновой кислотой, после чего конъюгат – билирубинглюкуронид может секретироваться в желчь. Конъюгированный билирубин растворим в воде и может непосредственно реагировать с диазореагентом; следовательно, «прямой билирубин» Ван ден Берга – это на самом деле конъюгат билирубина (билирубинглюкуронид). В зависимости от того, какой тип билирубина присутствует в плазме – неконъюгированный или конъюгированный, гипербилирубинемия классифицируется как постгепатитная (неконъюги-рованная) и регургитационная (конъюгированная) соответственно.
В центральную нервную систему через гематоэнцефалический барьер может проникать только неконъюгированный билирубин; поэтому энцефалопатия, возникающая вследствие гипербилирубинемии (ядерная желтуха), может быть вызвана только постгепатитной билирубинемией. С другой стороны, с мочой может экскретироваться только конъюгированный билирубин. Соответственно этому холеурическая желтуха наблюдается только при регургитационнй гипербилирубинемии, тогда как ахолеурическая желтуха – только при избытке неконъюгированного билирубина.
Неконъюгированная гипербилирубинемия
Даже при значительном гемолизе неконъюгированная гипербилирубинемия обычно весьма незначительна (менее 4 мг/100 мл, менее 68,4 мкмоль/л) вследствие большой способности печени в отношении конъюгирования билирубина. Если, однако, конъюгирование билирубина в печени оказывается неполноценным вследствие приобретенных или наследственных причин, может наблюдаться весьма выраженная неконъюгированная гипербилирубинемия.
Наиболее распространенной формой неконъюгированной гипербилирубинемии является «физиологическая желтуха», наблюдающаяся как временное состояние у новорожденных. Причиной этой гипербилирубинемии является ускоренный гемолиз и незрелое состояние печеночной системы поглощения, конъюгации и секреции билирубина. При этом не только понижается активность UDP-глюкуронил-трансферазы, но и, вероятно, оказывается недостаточным синтез субстрата этого фермента — UDP-глюкуроновой кислоты. Поскольку накапливающийся билирубин находится в неконъюгированной форме, он может преодолевать гаматоэнцефалический барьер, когда его концентрация в плазме превысит уровень насыщения высокоаффинных участков альбумина (20 – 25 мг/100 мл). Это может привести к гипербилирубинемической токсической энцефалопатии(ядерной желтухе). Поскольку известно, что система конъюгирования билирубина является индуцируемой, оказалось эффективным введение новорожденным с физиологической желтухой фенобарбитала. Кроме того, удалению неконъюгированного билирубина печенью может способствовать воздействие видимого света (механизм неизвестен); в этом случае часть билирубина превращается в производные, которые удаляются с мочой.
А. Синдром Криглера – Найяра типа I; врожденная негемолитическая желтуха. Синдром Криглера – Найяра типа I – метаболическое нарушение конъюгации билирубина. Болезнь может быть охарактеризована как тяжелая врожденная желтуха, возникающая вследствие наследуемого отсутствия в печеночной ткани активности билирубин-UDP-глюкуронилтрансферазы. Болезнь обычно приводит к фатальному исходу в первые 15 месяцев жизни, но отмечены случаи, когда болезнь проявлялась лишь в юношеском возрасте. Больным назначали светотерапию, которая приводила к некоторому снижению содержания билирубина в плазме. Фенобарбитал и другие лекарственные препараты, индуцирующие метаболизм билирубина в нормальной печени, в случае синдрома Криглера – Найяра типа I не оказывали влияния на образование билирубинглюкуронидов. При отсутствии лечения содержание билирубина в сыворотке обычно превышает 20 мг/100 мл.
Б. Синдром Криглера – Найяра типа II. Это редкое наследуемое заболевание, по-видимому, обусловлено менее серьезными дефектами в системе конъюгирования билирубина и характеризуется более доброкачественным течением. Концентрация билирубина в сыворотке обычно не превышает 20 мг/100 мл, весь накапливающийся билирубин относится к неконъюгированному типу. Как ни удивительно, но желчь этих больных содержит билирубинкглюкуронид; отсюда возникло предположение, что генетическое нарушение может затрагивать печеночную UDP-глюкуронилтрансферазу, которая катализирует присоединение второй глюкуронильной группы к билирубинмоноглюкурониду.
Было показано, что больные с этим синдромом поддаются лечению большими дозами фенобарбитала. Вызванное приемом лекарства снижение гипербилирубинемии, по-видимому, обусловлено индукцией всей системы метаболизма билирубина, а не только стимуляцией конъюгирования билирубина.
В нескольких случаях у предполагаемых гетерозигот с этим нарушением отмечена легкая неконъюгированная гипербилирубинемия, неотличимая от той, которая наблюдается при болезни Гильберта (см. ниже). Вполне возможно, что аутосомно-рецессивный синдром Криглера—Найяра типа II соответствует гомозиготному состоянию для дефекта, который при гетерозиготном состоянии проявляется в виде легкой хронической гипербилирубинемии Гильберта.
В. Болезнь Гильберта. Это заболевание представляет собой гетерогенную группу нарушений, многие из которых, как теперь известно, являются следствием компенсированного гемолиза, сопряженного с неконъюгированной гипербилирубинемией. Имеются, по-видимому, также нарушения, обусловленные ненормальным снижением поглощения билирубина паренхиматозными клетками печени. Пониженной у этих больных оказалась и активность в печени билирубин-UDP-глюкуронилтрансферазы.
Доброкачественные нарушения, известные под общим названием «болезни Гильберта», имеют, по-видимому, аутосомно-доминантный характер наследования.
Г. Токсическая гипербилирубинемия. Неконъюгированная гипер-билирубинемия может быть результатом дисфункции печени, наступающей вследствие токсического действия ряда веществ (хлороформа, арсфенаминов, четыреххлористого углерода, ацета-минофена), а также наблюдаемой при вирусном гепатите, циррозе и отравлении грибами рода Amanita. Большинство этих приобретенных нарушений является следствием повреждения паренхиматозных клеток печени; часто наблюдается также закупорка системы желчных протоков печени, приводящая к конъюгированной гипербилирубинемии.
Конъюгированная гипербилирубинемия
Поскольку конъюгированный билирубин растворим в воде, он обнаруживается в моче большинства больных конъюгированной гипербилирубинемией; поэтому болезнь часто называют холеурической желтухой.
А. Хроническая идиопатическая желтуха (синдром Дубина – Джонсона). Это аутосомно-рецессивное нарушение проявляется в виде конъюгированной гипербилирубинемии у детей и у взрослых. Причиной этой гипербилиру бинемии является, вероятно, нарушение печеночной секреции конъюгированного билирубина в желчь. Однако нарушение секреции конъюги-рованных веществ не ограничивается билирубином, оно касается секреции ряда других конъюгированных соединений, в частности эстрогенов и индикаторных веществ, например красителя сульфобромфталеина. Нарушение секреции конъюгированного сульфобромфталеина приводит к тому, что он снова возвращается в плазму, в которой наблюдается вторичное повышение его концентрации. Данное явление патогномонично для синдрома Дубина – Джонсона. При использовании для анализа других соединений, например индоцианина зеленого или бенгальского розового, секреция которых не требует конъюгации, вторичного повышения концентрации этих соединений в плазме больных не наблюдается. Таким образом, нарушение в данном случае связано с секреторным процессом, который в норме касается только конъюгированных соединений, включая конъюгированные билирубины. Интересно отметить, что у пациентов с синдромом Дубина — Джонсона гепатоциты центральных печеночных долек содержат необычный и пока еще неидентифицированный пигмент.
Закупорка желчных протоков. Конъюгированная гипербилирубинемия возникает также при закупорке печеночных или общего желчного протоков. В этом случае, как полагают, желчный пигмент, поступающий из крови в клетки печени, не может экскретироваться. В результате конъюгированный билирубин поступает в печеночные вены и лимфатические сосуды.
Термин холестатическая желтуха используют для всех форм желтухи, связанных с внепеченочной закупоркой, а также для ряда форм паренхиматозной желтухи, которые характеризуются конъюгированной гипербилирубинемией.
Билирубиновая энцефалопатия
Наибольший интерес вызывает вопрос нейротоксичности билирубина и возникновения билирубиновой энцефалопатии. Первое патоморфологическое описание желтушного окрашивания ядерных масс мозга новорожденных детей, у которых желтуха появилась сразу после рождения, сделано в 1875 году. В процессе изучения данной патологии выдвигались различные гипотезы о механизмах повреждающего действия билирубина на мозг новорожденных, влекущее за собой возникновение билирубиновой энцефалопатии. Отложения кристаллов практически нерастворимого в водных средах билирубина при данном заболевании обнаруживают не только в головном мозгу (палеокортекс, базальные ядра, субталамические ядра, продолговатый мозг, мозжечок), но и в стенке дыхательных путей, стенке желудочно-кишечного тракта, селезенке, почках, надпочечниках, семенных железах, костном мозгу. Это позволяет рассматривать билирубиновую энцефалопатию как проявление общей билирубиновой интоксикации организма. Здесь уместно было бы предположить, что нарушение собственно барьерной функции ГЭБ может являться следствием повреждения мембранных структур астроцитов и эндотелиоцитов билирубином, который относится к токсическим продуктам метаболизма. Спорным является вопрос о роли печени в нарушении проницаемости ГЭБ при гемолитической болезни. Наличие отчетливых морфологических изменений при нарушении детоксирующей роли печени впервые отметил Zammora (отек, вакуолизация, конечные разветвления астроцитарных отростков при экспериментальном выключении печени крыс из кровотока). Причиной билирубиновой интоксикации может быть дефект микросомальной ферментной системы гепатоцитов, катализирующей конъюгацию билирубина, а также конъюгацию различных иных субстанций алифатического, ароматического и/или стероидного ряда, способных тоже оказывать токсическое действие на организм. В результате многочисленных исследований было установлено, что связанный с сывороточным альбумином билирубин в клетки мозга не проникает, однако следует отметить, что каждая молекула альбумина может связать две молекулы непрямого билирубина, но первую очень прочной связью, а вторую рыхло. Непрямой билирубин в кислой форме находится в рыхлой связи с альбумином и токсичен для мозга.
В последние годы в некоторых работах было предложено определять соотношение билирубин/альбумин вместо определения концентрации билирубина и альбумина отдельно. Тем самым предполагалось достигнуть лучших результатов в прогнозировании и предотвращении билирубиновой энцефалопатии путем оптимизации показаний для заменного переливания крови. Однако существенных результатов эти исследования не дали. Общеизвестно, что существуют факторы, способствующие нарушению связывающей билирубин способности альбумина, а также вещества-лиганды, конкурирующие за места прочного связывания на альбумине (асфиксия, ацидоз, неэстерифицированные жирные кислоты, лекарственные вещества и т.д.).
Гипоксия предрасполагает к развитию билирубиновой энцефалопатии в первую очередь из-за угнетения активности системы глюкоронил-трасферазы. Известно, что митохондрии мозга, равно как и других органов и тканей, содержат билирубиноксидантную систему, окисляющую в присутствии кислорода билирубин. В связи с тем, что процесс гипоксии вызывает повреждение митохондрий и инактивацию оксидаз, может нарушиться механизм окисления билирубина, попадающего в капиллярные субстанции. Этот механизм в норме "срабатывает" у новорожденных в случае достаточной ферментативной активности, тогда как гипоксия нарушает этот процесс. Сочетание желтухи с гипоксией особенно опасно из-за повышенной чувствительности нервных клеток к гипоксии, когда недостаток кислорода вызывает локальный тканевый ацидоз, который может существовать еще некоторое время после коррекции рН крови. Наибольшее значение в патогенезе билирубиновой энцефалопатии имеет проницаемость ГЭБ, который является сложной регуляторной поверхностью, четко контролирующей прохождение веществ через стенку сосудов мозга в клетки мозга. Патоморфологи диагностируют ядерную желтуху не ранее 36 часов после рождения. Таким образом, изменения ЦНС, возникшие в первые 36 часов жизни, могут быть обратимыми. При ядерной желтухе в первую очередь прокрашиваются базальные ганглии: хвостатое ядро, скорлупа, бледный шар. Могут повреждаться также кора мозга, мозжечок, подбугровая область, аммонов рог, ядра продолговатого мозга и мозжечка. Интенсивное поражение ядер дна 4-го желудочка может быть причиной смерти новорожденного. На дне 4-го желудочка чаще прокрашиваются боковые отделы в области кохлеарных и вестибулярных ядер. Значительно реже желтушность находят в зрительном бугре и других отделах мозга. Особенно редуцированы пирамидные клетки 3-го слоя коры, двигательной области спинного мозга и стволовой части головного мозга. После 6-7-го дня жизни ребенка интенсивность острых изменений нейронов снижается, выявляются поля опустошения во многих отделах мозга с последующим развитием глиоза. Нарушается формирование мозга и всего организма ребенка. В клинической картине билирубиновой энцефалопатии наблюдается следующая триада симптомов: гиперкинетическая форма ДЦП, дефект слуха и умственная недостаточность. К сопутствующим проявлениям заболевания относятся ограничение взора вверх, желтушное окрашивание и дефект зубной эмали, дизартрия.
Уробилиноген в моче
В норме уробилиноген присутствует в моче лишь в следовых количествах (в среднем суточная порция содержит 0,64 мг уробилиногена; повышение до 4 мг все еще рассматривается как не выходящее за пределы нормы). При полной закупорке желчного протока уробилиноген в моче отсутствует, поскольку билирубин не может попасть в кишечник, где он превратился бы в уробилиноген. В этом случае присутствие в моче билирубина и отсутствие уробилиногена свидетельствуют о наличии обтурационной (механической) желтухи либо внутрипеченочной, либо внепеченочной. При гемолитической желтухе увеличение образования билирубина приводит к повышенному синтезу уробилиногена, который появляется в моче в больших количествах. Билирубин в моче больных гемолитической желтухой обычно не обнаруживается; таким образом, повышенное содержание в моче уробилиногена и отсутствие билирубина свидетельствуют о гемолитической желтухе. Обусловленное различными причинами усиление деградации кровяных клеток (например, при пернициозной анемии) также приводит к повышенному содержанию в моче уробилиногена. Кроме того, при попадании инфекции в желчные канальцы содержание уробилиногена в моче может повышаться и в отсутствие нарушений функции печени за счет восстановительной активности инфицирующих бактерий.
Схема, приведенная на рис. 4, суммирует данные о транспорте били-рубина и уробилиногена из печени в кишечник и почки в нормальных условиях, а также при гемолитической желтухе, гепатите или желтухе, обусловленной закупоркой желчных протоков.
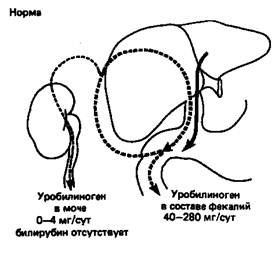
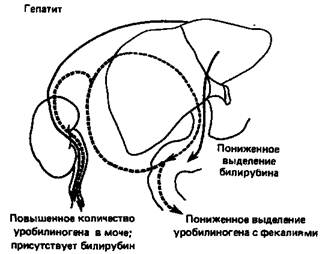
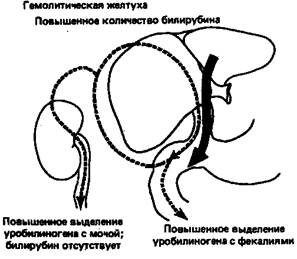
Рисунок 4 - Билирубин-уробилиногеновый цикл
Сплошные стрелки показывают движение билирубиндиклюкуронида, штриховые стрелки — движение уробилиногена.
СПИСОК ЛИТЕРАТУРЫ
1. Марри Р., Греннер Д., Мейерс П., Родуэл В. Биохимия человека. – M., Мир, 1993. –Т 1, 384 с.
2. Berk P. D. et al. Disorders of bilirubin metabolism. In: Metabolic Control and Disease, 8th ed., Bondy P. K., Rosenberg L.E. (eds), Saunders, 1980.
3. Ляхович В.В., Цырлов И.Б. Индукция ферментов метаболизма ксенобиотиков. Новосибирск: Наука, 1981. 240 с.
4. Арчаков А.И. Микросомальное окисление. М.: Наука, 1975. 327 с.
5. Саприн А.Н. // Успехи биол. химии. 1991. Т. 32. С. 146-175.
6. Колесниченко Л.С., Кулинский В.И. // Успехи соврем. биологии. 1989. Т. 107, вып. 2. С. 179-194.
Похожие работы
... в результате расщепления поступающих с пищей белков и последующее окисление этих аминокислот в клетке с образованием СО2, и Н2О, что сопровождается высвобождением энергии. Процессы анаболизма и катаболизма находятся в организме в состоянии динамического равновесия. Преобладание анаболических процессов над катаболическими приводит к росту, накоплению массы тканей, а преобладание катаболических ...
... – высокоаэробных.[6,2000] Показано, что ряд дегидрогеназ используют только НАД или НАДФ, другие могут катализировать окислительно-восстановительные реакции в присутствии любого из них. В процессе биологического окисления НАД и НАДФ выполняют роль промежуточных переносчиков электронов и протонов между окисляемым субстратом и флавиновыми ферментами. Основными источниками никотиновой кислоты и ее ...
... изолейцин, валин) и повышением содержания ароматических аминокислот (тирозин, фениламин и метионин).Понижение содержания аминокислот с разветвленными ?аминокислотами(цепями) приводит при хронических заболеваниях печени к наблюдаемой гиперинсулинемии.Гиперинсулинемия обусловлена повышенным распадом аминокислот с разветвленными цепями на переферии, в мускулатуре и жировой ткани (84) и, следовательно ...
... активности клеток в кроветворных органах и тканях. Приобретенная аутоагрессивная гемолитическая анемия: в селезенке происходит разрушение и растворение (лизис) эритроцитов. Биохимия и патобиохимия печени. Рассмотрим основные представления о биохимических процессах, протекающих в печени. На пути между кишечником и внутренней средой организма – системой крови и лимфы – находится печень. В ...
0 комментариев