Навигация
Количественное определение
7. Количественное определение
При количественном определении фенолгликозидов применяют химические (титриметрические) и инструментальные (спектрофотометрические и хроматографические) методы анализа.
Нормативно-техническая документация предусматривает количественное определение арбутина в листьях толокнянки и брусники. Метод определения основан на иодометрическом титровании гидрохинона, полученного после извлечения и гидролиза арбутина [16].
Разработан спектрофотометрический метод определения салидрозида в экстрактек корневищ с корнями родиолы розовой, который можно использовать для количественного определения салидрозида в растительном материале [1].
Исходя из строения фенольных гликозидов и их УФ спектров, возможно количественное хромато-спектрофотометрическое определение всех представителей этой группы [14].
И хотя сейчас всё более широкое применение получают инструментальные методы установления колличественного содержания фенолгликозидов [16], ещё применяется и включён в НТД [16] титриметрический метод количественного определения.
Рассмотрим подробнее методы количественного определения фенолгликозидов в ЛРС.
7.1 Титриметрический метод количественного определения фенолгликозидов [16]
Около 0.5 гр (точная навеска) сырья, измельченного и просеянного через сито с диаметром отверстий 1 мм, помещают в колбу вместимостью 100 мл, заливают 50 мл воды и нагревают с обратным холодильником поддерживая слабое кипение, в течение 30 мин. Горячее извлечение фильтруют в мерную колбу вместимостью 100 мл через бумажный фильтр, избегая попадания частиц сырья на фильтр. В колбу с сырьем повторно прибавляют 25 мл воды и кипятят в течение 20 мин. Горячее извлечение вместе с сырьем переносят на тот же фильтр и остаток на фильтре дважды промывают горячей водой порциями по 10 мл. К фильтрату прибавляют 3 мл раствора свинца (II) ацетата основного, перемешивают, охлаждают и доводят водой до объема 100,0 мл. Колбу помещают в водяную баню и выдерживают до полной коагуляции осадка. Горячую жидкость полностью отфильтровывают в колбу через бумажный фильтр, прикрывая воронку часовым стеклом. Охлаждают, к фильтрату прибавляют 1 мл кислоты серной, колбу взвешивают с точностью до 0,01 г и кипятят с обратным холодильником в течение 1,5 ч, поддерживая равномерное и слабое кипение. Охлаждают до комнатной температуры, взвешивают, доводят массу колбы до первоначальной водой, и полностью отфильтровывают через бумажный фильтр в колбу вместимостью 250 мл. К фильтрату прибавляют 0,1 г порошка цинка и встряхивают в течение 5 мин.
Жидкость нейтрализуют натрия гидрокарбонатом (около 1—2 г) по красной лакмусовой бумаге, прибавляют еще 2 г натрия гидрокарбоната и после его растворения фильтруют через бумажный фильтр.
50,0 мл фильтрата переносят в плоскодонную колбу вместимостью 500 мл, прибавляют 200 мл воды и немедленно титруют из микро- или полумикробюретки 0,1 М раствором йода до появления синего окрашивания, не исчезающего в течение 1 мин, используя в качестве индикатора раствор крахмала, свободный от йодидов.
1мл 0.1н раствора йода соответствует 0.01361 арбутина. Процентное содержание арбутина в растительном материале х в пересчете на абсолютно сухое сырье вычисляют по формуле:
Х= V0.01361∙2∙100∙100 / m (100-w)
где V - объем 0.1н раствора йода, израсходованного на титрование, мл;
m- масса навески сырья, гр; w - потеря в массе сырья при высушивании, %
Содержание арбутина в сырье регламентируется НТД.
Известно, что в зеленых листьях бадана толстолистного содержится арбутина 20%, в листьях брусники- 10-16%.
Способ выделения арбутина из листьев бадана включает: двух- кратную экстракцию сырья кипящей водой, фильтрацию и сепарирование извлечения, осаждение полифенолов раствором ацетата свинца, отделение осадка, упаривание фильтрата до сухого остатка, двух- кратную эктракцию сухого остатка 96%-ным этанолом, упаривание этанольного экстракта и обработка маслянистого остатка смесью хлороформ- этанол, кристаллизация арбутина из этой смеси. Выход арбутина-4%. Способ позволяет получить получить химически чистый арбутин без примесей, что подтвердается данными УФ-, ИК, ПМР-спектров. УФ- спектр арбутина имеет максимальное поглощение при 285 нм, в ИК- спектре имеются для характерные для арбутина полосы поглощения при 817, 831, 1513, 1447.
7.2 Инструментальные методы
Среди инструментальных методов определения можно выделить фотоэлектроколориметрический и спетрофотометрический. Рассмотрим эти методы на примере колличественного определения арбутина.
В основе определения арбутина фотоэлектроколориметрическим методом лежит реакция образования азокрасителя после его взаимодействия с диазотированным сульфаниламидом (например, сульфацил-натрий) [14].
Количественное содержание определяется по калибровочному графику. Осаждение полифенолов проводится раствором свинца ацетата основного. Потери арбутина при данном способе определения составляют около 1,5%. Это объясняется тем, что очистка извлечения от сопутствующих полифенольных соединений раствором свинца ацетата основного приводит к соосаждению арбутина [14].
Спектрофотометрический метод для определения арбутина основан на измерении оптической плотности в видимой области спектра после получения антипиринового красителя. В качестве реактивов, например, используют 2% водный раствор 4-аминоантипирина, аммиак и 2% водный раствор калия феррицианида. Окрашенный продукт извлекают хлороформом и измеряют оптическую плотность окрашенного продукта на спектрофотометре при длине волны 455 нм. [14, 15].
Похожие работы
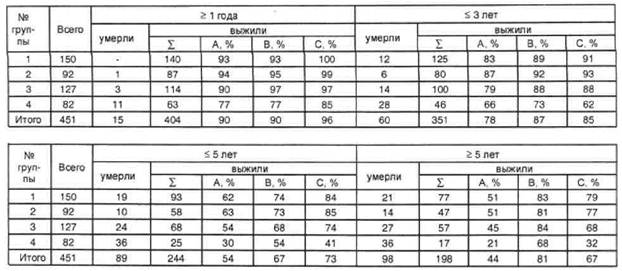
... комплексы с сухим экстрактом специальных фитосборов целевого назначения – фитохитодез. Галеновые формы указанных фитопрепаратов приготавливались в строгом соответствии с требованиями государственной фармакопеи с использованием лекарственных растений, включенных в государственный реестр. В настоящее время обработаны данные КБФ по 2235-и больным, из них онкологических – 451. Впервые мы имеем ...
... 1-2 раза переворачивают. При сушке с искусственным обогревом температура не должна превышать 40-50°С. Химический состав. Флавоноиды (производные флавонола) (до 3%), среди которых преобладают гликозиды кверцетина - авикулярин, кверцитрин и гиперозид. К сопутствующим веществам относятся витамин К, аскорбиновая кислота, дубильные вещества, каротиноиды, фенолкарбоновые кислоты, соединения кремниевой ...
0 комментариев